中国组织工程研究 ›› 2019, Vol. 23 ›› Issue (27): 4375-4380.doi: 10.3969/j.issn.2095-4344.1388
• 组织构建实验造模 experimental modeling in tissue construction • 上一篇 下一篇
补肾活血汤干预骨质疏松症并骨关节炎模型兔软骨细胞NF-KBp65蛋白的表达
张 波1,张开伟2,马文娟3,沈冯君2,陈海霞1
- (1贵州中医药大学,贵州省贵阳市 550000;2贵阳中医学院第一附属医院,贵州省贵阳市 550000;3贵州省金沙县中医院,贵州省毕节市 551800)
Effect of Bushen Huoxue Decoction on the expression level of nuclear factor-KBp65 protein in chondrocytes of rabbit models of osteoporosis and osteoarthritis
Zhang Bo1, Zhang Kaiwei2, Ma Wenjuan3, Shen Fengjun2, Chen Haixia1
- (1Guiyang University of Traditional Chinese Medicine, Guiyang 550000, Guizhou Province, China; 2the First Affiliated Hospital of Guiyang University of Traditional Chinese Medicine, Guiyang 550000, Guizhou Province, China; 3Jinsha County Hospital of Traditional Chinese Medicine of Guizhou Province, Bijie 551800, Guizhou Province, China)
摘要:
文章快速阅读:
.jpg) 文题释义:
信号通路(NF-KB):广泛存在于细胞基质内的一种核转录因子,在未受刺激的细胞中,Kappa B 抑制蛋白结合在NF-KB的核定位序列上,从而将NF-KB阻滞在细胞质,使其不能进入细胞核发挥转录调控作用,但受到各种因子如白细胞介素1、白细胞介素6、肿瘤坏死因子α等刺激后,Kappa B抑制蛋白被降解,NF-KB被激活后F转移到细胞核内结合到其靶基因的启动子上,通过启动靶基因的转录,进而调控细胞的生长和炎症反应。
阿仑膦酸钠:适用于治疗绝经后妇女的骨质疏松症,以预防髋部和脊柱骨折(椎骨压缩性骨折),也适用于男性骨质疏松症以增加骨量。动物研究发现,在细胞水平,阿仑膦酸钠对骨吸收部位特别是破骨细胞作用的部位有亲嗜性。正常情况下,破骨细胞黏附于骨表面但并不粗糙,而粗糙的边缘则是骨吸收活跃的标志。阿仑膦酸钠不影响破骨细胞的聚集或黏附,但它确实能够抑制破骨细胞的活性。
文题释义:
信号通路(NF-KB):广泛存在于细胞基质内的一种核转录因子,在未受刺激的细胞中,Kappa B 抑制蛋白结合在NF-KB的核定位序列上,从而将NF-KB阻滞在细胞质,使其不能进入细胞核发挥转录调控作用,但受到各种因子如白细胞介素1、白细胞介素6、肿瘤坏死因子α等刺激后,Kappa B抑制蛋白被降解,NF-KB被激活后F转移到细胞核内结合到其靶基因的启动子上,通过启动靶基因的转录,进而调控细胞的生长和炎症反应。
阿仑膦酸钠:适用于治疗绝经后妇女的骨质疏松症,以预防髋部和脊柱骨折(椎骨压缩性骨折),也适用于男性骨质疏松症以增加骨量。动物研究发现,在细胞水平,阿仑膦酸钠对骨吸收部位特别是破骨细胞作用的部位有亲嗜性。正常情况下,破骨细胞黏附于骨表面但并不粗糙,而粗糙的边缘则是骨吸收活跃的标志。阿仑膦酸钠不影响破骨细胞的聚集或黏附,但它确实能够抑制破骨细胞的活性。
.jpg) 文题释义:
信号通路(NF-KB):广泛存在于细胞基质内的一种核转录因子,在未受刺激的细胞中,Kappa B 抑制蛋白结合在NF-KB的核定位序列上,从而将NF-KB阻滞在细胞质,使其不能进入细胞核发挥转录调控作用,但受到各种因子如白细胞介素1、白细胞介素6、肿瘤坏死因子α等刺激后,Kappa B抑制蛋白被降解,NF-KB被激活后F转移到细胞核内结合到其靶基因的启动子上,通过启动靶基因的转录,进而调控细胞的生长和炎症反应。
阿仑膦酸钠:适用于治疗绝经后妇女的骨质疏松症,以预防髋部和脊柱骨折(椎骨压缩性骨折),也适用于男性骨质疏松症以增加骨量。动物研究发现,在细胞水平,阿仑膦酸钠对骨吸收部位特别是破骨细胞作用的部位有亲嗜性。正常情况下,破骨细胞黏附于骨表面但并不粗糙,而粗糙的边缘则是骨吸收活跃的标志。阿仑膦酸钠不影响破骨细胞的聚集或黏附,但它确实能够抑制破骨细胞的活性。
文题释义:
信号通路(NF-KB):广泛存在于细胞基质内的一种核转录因子,在未受刺激的细胞中,Kappa B 抑制蛋白结合在NF-KB的核定位序列上,从而将NF-KB阻滞在细胞质,使其不能进入细胞核发挥转录调控作用,但受到各种因子如白细胞介素1、白细胞介素6、肿瘤坏死因子α等刺激后,Kappa B抑制蛋白被降解,NF-KB被激活后F转移到细胞核内结合到其靶基因的启动子上,通过启动靶基因的转录,进而调控细胞的生长和炎症反应。
阿仑膦酸钠:适用于治疗绝经后妇女的骨质疏松症,以预防髋部和脊柱骨折(椎骨压缩性骨折),也适用于男性骨质疏松症以增加骨量。动物研究发现,在细胞水平,阿仑膦酸钠对骨吸收部位特别是破骨细胞作用的部位有亲嗜性。正常情况下,破骨细胞黏附于骨表面但并不粗糙,而粗糙的边缘则是骨吸收活跃的标志。阿仑膦酸钠不影响破骨细胞的聚集或黏附,但它确实能够抑制破骨细胞的活性。摘要
背景:临床研究发现肾虚血淤是骨性关节炎、骨质疏松症共同病因、病机,运用补肾活血法治疗该类病变疗效肯定。
目的:进一步验证补肾活血汤对兔软骨细胞NF-KBp65蛋白表达的影响。
方法:雌性新西兰大白兔37只,由贵阳医学院动物实验中心提供,实验方案经贵阳医学院动物实验伦理委员会批准(批准号:2015-024)。随机选取30只大白兔编号后随机均分为3组,分别建立骨质疏松模型、骨关节炎模型、骨质疏松+骨关节炎模型。剩余7只用于制备7种含药血清(分别为正常组、低剂量补肾活血汤组、中剂量补肾活血汤组、高剂量补肾活血汤组、盐酸氨基葡萄糖组、阿仑膦酸钠组、盐酸氨基葡萄糖+阿仑磷酸钠组)。采用Western-blot检测7组药物对3组模型兔软骨细胞NF-KBp65蛋白表达的影响。
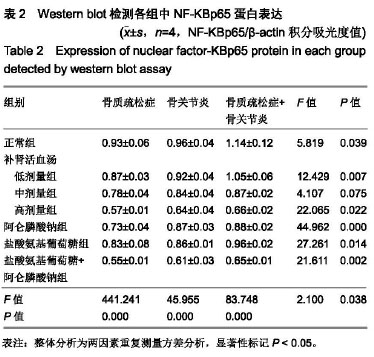
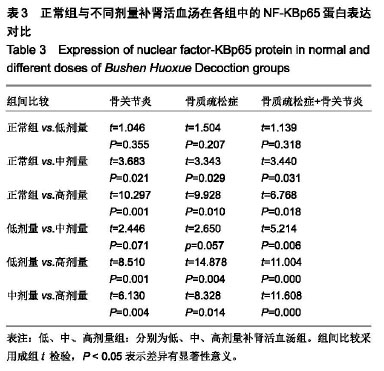
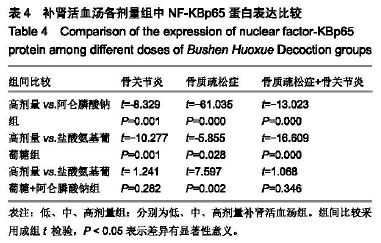
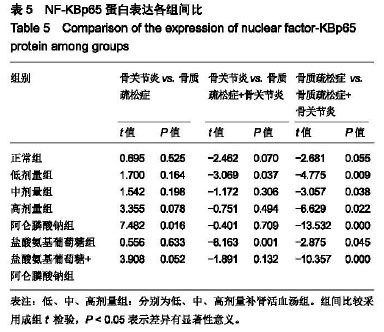
结果与结论:①中、高剂量组有下调细胞中NF-KBp65蛋白的作用,与正常组对比差异有显著性(P < 0.05),其中以高剂量组作用最为明显,与低、中剂量组对比差异有显著性意义(P < 0.05);②高剂量组下调NF-KBp65蛋白表达的作用较阿仑膦酸钠组和盐酸氨基葡萄糖组明显(P < 0.05);③高剂量组与盐酸氨基葡萄糖+阿仑膦酸钠组在骨质疏松症组对比差异有显著性意义(t=7.597,P < 0.05),但在骨关节炎组及骨关节炎+骨质疏松症组中则差异无显著性意义(P > 0.05),说明高剂量组下调NF-KBp65蛋白表达的作用优于阿仑膦酸钠组及盐酸氨基葡萄糖组,与盐酸氨基葡萄糖+阿仑膦酸钠组大体相当;④结果表明,补肾活血汤能下调NF-KBp65蛋白表达,从而减轻或抑制骨质疏松症和骨关节炎的炎症反应,间接或直接起到保护或修复软骨细胞的作用。
中图分类号:

.jpg)
.jpg)
.jpg) 文题释义:
信号通路(NF-KB):广泛存在于细胞基质内的一种核转录因子,在未受刺激的细胞中,Kappa B 抑制蛋白结合在NF-KB的核定位序列上,从而将NF-KB阻滞在细胞质,使其不能进入细胞核发挥转录调控作用,但受到各种因子如白细胞介素1、白细胞介素6、肿瘤坏死因子α等刺激后,Kappa B抑制蛋白被降解,NF-KB被激活后F转移到细胞核内结合到其靶基因的启动子上,通过启动靶基因的转录,进而调控细胞的生长和炎症反应。
阿仑膦酸钠:适用于治疗绝经后妇女的骨质疏松症,以预防髋部和脊柱骨折(椎骨压缩性骨折),也适用于男性骨质疏松症以增加骨量。动物研究发现,在细胞水平,阿仑膦酸钠对骨吸收部位特别是破骨细胞作用的部位有亲嗜性。正常情况下,破骨细胞黏附于骨表面但并不粗糙,而粗糙的边缘则是骨吸收活跃的标志。阿仑膦酸钠不影响破骨细胞的聚集或黏附,但它确实能够抑制破骨细胞的活性。
文题释义:
信号通路(NF-KB):广泛存在于细胞基质内的一种核转录因子,在未受刺激的细胞中,Kappa B 抑制蛋白结合在NF-KB的核定位序列上,从而将NF-KB阻滞在细胞质,使其不能进入细胞核发挥转录调控作用,但受到各种因子如白细胞介素1、白细胞介素6、肿瘤坏死因子α等刺激后,Kappa B抑制蛋白被降解,NF-KB被激活后F转移到细胞核内结合到其靶基因的启动子上,通过启动靶基因的转录,进而调控细胞的生长和炎症反应。
阿仑膦酸钠:适用于治疗绝经后妇女的骨质疏松症,以预防髋部和脊柱骨折(椎骨压缩性骨折),也适用于男性骨质疏松症以增加骨量。动物研究发现,在细胞水平,阿仑膦酸钠对骨吸收部位特别是破骨细胞作用的部位有亲嗜性。正常情况下,破骨细胞黏附于骨表面但并不粗糙,而粗糙的边缘则是骨吸收活跃的标志。阿仑膦酸钠不影响破骨细胞的聚集或黏附,但它确实能够抑制破骨细胞的活性。