2.1 脂肪干细胞的特性及诱导培养基 脂肪干细胞来源广泛,取材方便,扩增迅速,具有干细胞特性及多项分化潜能,能抑制淋巴细胞增殖而具有弱免疫原性,可分化形成软骨细胞、骨细胞及脂肪细胞等,其表达脂肪源性细胞相关基因(PPAR-γ和CEBPα)及干细胞相关基因(sox2)。研究证实纯化的CD90+脂肪干细胞高表达sox2同时PPAR-γ和CEBPα低表达,具有更高的成软骨分化能力,同时研究认为髌下脂肪垫来源脂肪干细胞具有更高的成软骨分化潜能[8]。然而许多研究结果显示不同的基础培养基对脂肪干细胞成软骨分化产生很大影响。高糖DMEM培养基可抑制细胞凋亡及有氧呼吸,胎牛血清含有多种细胞因子可能影响软骨分化,含色氨酸的培养基可能含有抑制有丝分裂的因子,需要高浓度胰岛素抑制其与IGF位点结合,维生素C有利于胶原形成时赖脯氨酸的羟基化进而促进三维结构的形成[9]。Estes等[10]研究表明常用的诱导细胞因子转化生长因子β1及转化生长因子β3质量浓度均为10 μg/L,骨形态发生蛋白6质量浓度为500 μg/L。
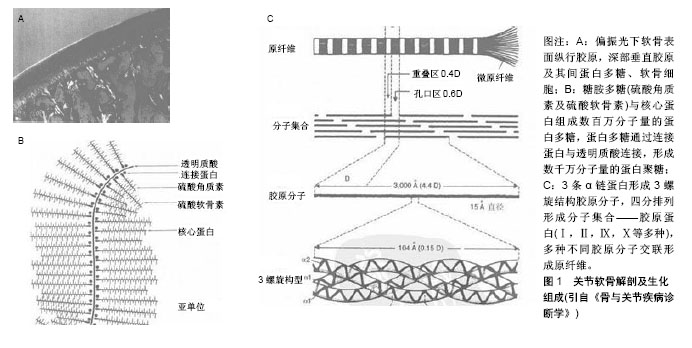
2.2 成软骨诱导效果的特异性基因及其产物 软骨由软骨细胞、胶原和蛋白多糖组成。胶原超过15种,主要为Ⅱ、Ⅵ、Ⅸ、Ⅺ型胶原,某些胶原局限于特定区域,Ⅱ型胶原占关节软骨干质量的50%以上。蛋白多糖主要由糖胺聚糖和透明质酸组成,其中硫酸软骨素和硫酸角质素是2个主要的糖胺聚糖。关节软骨解剖及生化组成,见图1。模拟关键细胞外基质成分的组装和空间结构是组织工程化软骨植入物发展的重要环节。关节软骨的主要营养来自滑膜液,关节软骨的代谢有内源性及外源性酶的参与,炎性、损伤等多种病理过程中外源性酶大量异常产生,造成关节软骨破坏及退化[4]。
2.2.1 标志软骨形成的基因及产物 Ⅱ型胶原产量高表明成软骨分化效果较好。然而,Ⅱ型胶原基因COL2A1及其产物Ⅱ型胶原在成软骨刺激培养的最初时期没有被观察到并不能暗示成软骨分化的失败[4]。聚集蛋白聚糖是软骨细胞的特异性标记物,基因表达及产物可用于评估软骨形成[11]。Ⅸ型胶原基因及其产物是软骨细胞长期稳定性的指标,Ⅸ型胶原以共价形式与Ⅱ型胶原相连,Ⅸ型胶原减少对软骨形成意义不大,但导致软骨早期退化性疾病风险增加[9]。Ⅸ型胶原在负重区含量高,增加Ⅸ型胶原的含量有助于形成稳固的软骨组织[9]。低氧诱导因子1α位于软骨转录因子SOX9上游,调控关节软骨细胞适应低氧环境,研究表明低氧环境更有利于软骨细胞外基质的产生[12];SOX9的表达说明软骨细胞诱导成功启动[13-14]。SOX9可以直接诱导Ⅱ型胶原、糖胺聚糖的产生。SOX9与L-SOX5、SOX6共同调节软骨形成及维持成熟软骨细胞表型。有实验证实SOX9处理脂肪干细胞,它的辅因子L-SOX5表达上调,SOX6也有轻度增加[15-16]。软骨细胞及脂肪干细胞均表达CD90,是成熟软骨细胞去分化的一个靶点。CD105是预测分化软骨细胞体内产生软骨的标志物[16]。
2.2.2 不利软骨形成或形成不完全的基因及产物 Ⅰ型胶原为肌腱细胞的主要细胞外基质,COL1A1及Ⅰ型胶原可以调节间叶细胞聚集,同时研究表明Ⅰ型胶原表达过多的细胞向纤维组织方向转变[16]。也有报道认为Ⅰ型胶原能使脂肪干细胞来源软骨细胞去分化。Ⅹ型胶原为肥大软骨细胞标记物[17-18],但有研究认为Ⅹ型胶原作为软骨肥大的评定指标尚有疑问[16]。Ⅹ型胶原发现在软骨成骨的过程中,因此适当的Ⅹ型胶原存在脂肪干细胞成软骨分化过程是合理的,但过多的Ⅹ型胶原表达表明细胞向成骨方向转变[10]。基质金属蛋白酶3编码可以降解纤维蛋白、层粘连蛋白、Ⅲ型、Ⅳ型、Ⅸ型、Ⅹ型胶原蛋白、软骨蛋白聚糖等细胞外基质成分。基质金属蛋白酶13可以明显降解Ⅱ型胶原[19]。碱性磷酸酶与分化后软骨细胞肥大有明显相关性[5]。研究表明肌动蛋白纤维与成软骨分化呈负相关[5]。脂肪干细胞具有多分化潜能,因此脂肪细胞、骨细胞、纤维细胞等特异性基因及其产物的表达均是成软骨不完全的表现,了解脂肪干细胞多向分化机制有助于研究其成软骨分化条件[20]。
2.3 影响脂肪干细胞成软骨分化的细胞因子及其相互作用
2.3.1 影响脂肪干细胞成软骨分化的细胞因子Diekman等[2]研究表明外源性地塞米松可以促进脂肪干细胞聚集蛋白聚糖表达,COL2A1的表达没有增加,可以下调COL1A1、COL10A1的表达。
(1)骨形态发生蛋白:属于转化生长因子超家族。骨形态发生蛋白与蛋白裂解、软骨重塑及血管生成调节有关,可诱导干细胞向软骨细胞分裂,促进软骨细胞有丝分裂,促进细胞外基质的产生[6]。然而Jungmann等[5]研究表明骨形态发生蛋白2可降低脂肪干细胞Ⅱ型胶原的表达,增加Ⅹ型胶原的表达。同时赵璨明等[21]总结发现骨形态发生蛋白2单独转染可促进脂肪干细胞成骨分化,但与胰岛素样生长因子1同时转染则促进脂肪干细胞成软骨分化。骨形态发生蛋白3与病理过程有关,急性关节损伤患者骨形态发生蛋白3升高,伴随着白细胞介素1β和肿瘤坏死因子α升高[2]。外源性骨形态发生蛋白6短时间接触可以促进聚集蛋白聚糖、Ⅱ型胶原、硫酸软骨素C-4-S的表达,促进COL1A1的表达,COL10A1表达少量增加,相比转化生长因子β1、地塞米松、成纤维细胞生长因子2等作用更强[2,18];3D环境中,高浓度的骨形态发生蛋白6可以促进软骨特异性成分COL2A1及AGC1表达,而抑制肥大软骨细胞标记COL10A1表 达[17-18]。Zaragosi等[22]进一步研究发现骨形态发生蛋白6转染的脂肪干细胞可以获得完全软骨细胞表型,硫酸软骨素及Ⅱ型胶原产生增加,同时Ⅰ型胶原及Ⅹ型胶原产生减少,其效果比同期实验的外源性骨形态发生蛋白6更明显。但有研究发现持续高浓度的骨形态发生蛋白6加入,使成纤维软骨表型表达增加[17];同时有研究发现在软骨细胞培养中骨形态发生蛋白6促进肥大相关表型COL10的表达[23];与其在脂肪干细胞成软骨分化中作用不同,具体机制不明。因此作者推测脂肪干细胞与软骨细胞存在不同的胞外基质调控机制,骨形态发生蛋白对脂肪干细胞促软骨分化的机制尚需更多实验去发现。
(2)转化生长因子家族:包括转化生长因子α、转化生长因子β,其中转化生长因子β包括转化生长因子β1-3,可促进软骨细胞产生Ⅱ型胶原及蛋白聚糖,同时可促进成软骨分化。转化生长因子β1单独应用在平面培养基中促进Ⅱ型胶原、黏多糖及SOX9表达作用很弱。与软骨细胞共培养时,上述产物明显增加。转化生长因子β1通过结合细胞表面受体发挥作用。促分化作用主要依靠2个细胞内途径:Smad信号转录因子,通过丝蛋白激酶激活蛋白激酶——跨膜Ser/Thr激酶受体[7]。Jin等[24]研究发现Ad5-hTGFβ2转染后脂肪干细胞在聚乳酸-羟基乙酸共聚物支架中成软骨分化能力增强,聚集蛋白聚糖及Ⅱ型胶原表达全程增加。用形成的软骨块移植于裸鼠,有明显软骨形成。转化生长因子β3在培养14 d时促进了蛋白聚糖的表达,21 d时则产生了抑制作用;但正常软骨细胞在这2个时间点蛋白聚糖没有产生明显改变[11,25],这可能与正常软骨细胞的成熟表型有关。Lu等[26]研究发现杆状病毒携带转化生长因子β3转染的脂肪干细胞成软骨能力增强,且胶原及蛋白聚糖形成增加。
Ⅰ型受体即激活素受体激酶5(activin receptor-like kinase-5,ALK-5)磷酸化可激活Smad通路[12]。查阅经典理论可知转化生长因子β通路参与的蛋白有Smad2、Smad3、Smad4、Smad7,其中Smad2、Smad3可以促进Ⅰ、Ⅱ型胶原的表达。TGFβ/Smad通路对软骨有双向调节作用:转化生长因子β过低则软骨修复作用减弱;转化生长因子β过高则软骨易纤维化。小G蛋白可以影响细胞大小及形态。小G蛋白是基因表达信号及信号通路信号,与细胞周期进程(凋亡、增殖和分化)有关。Rac1参与转化生长因子β通路,Rac1使Ⅱ型胶原表达增加,Ⅹ型胶原及肌动蛋白纤维减少[5];同时Rac1可以减少分化软骨细胞的直径及体积,增加细胞弹性,使脂肪干细胞分化细胞更接近于软骨细胞。
(3)软骨源性形态发生蛋白(CDMP):生长分化因子是重要的软骨细胞分化的生长因子,包括CDMP1、CDMP2、CDMP3。已有研究证实CDMP1可以诱导真皮成纤维细胞向软骨分化及基质分泌。二维培养研究中,生长分化因子5促进软骨细胞形态改变,Ⅱ型胶原、糖胺聚糖表达在14 d时达到高峰,而后降低。生长分化因子5以同源二聚体的形式与转化生长因子β超家族其他成员一样激活BMPR-Ⅰ、BMPR-Ⅱ和激活素受体Ⅱ,再通过Smad将信号传至核内,调节基因表达,因此推测生长分化因子5与转化生长因子β存在不同的激活受体,而存在相同的下游通路[27-29]。
(4)胰岛素样生长因子:可以促进软骨低聚基质蛋白基因的表达,其产物连接软骨基质纤维而促进软骨修 复[30]。胰岛素样生长因子分为胰岛素样生长因子1、2两种形式。胰岛素样生长因子1促软骨分化作用明确。胰岛素样生长因子1可促进Ⅱ型胶原、蛋白多糖的产生,同时抑制胞外基质的降解(可能与软骨低聚基质蛋白基因表达有关)[6,27],呈剂量-时间依赖关系,能明显缩短细胞周期G1时间,同时可以营养软骨细胞外基质[31]。张传辉等[12]总结发现胰岛素样生长因子1通过减少低氧诱导因子1α蛋白的降解,间接促进SOX9表达,促进成软骨分化及细胞外基质产生。
(5)碱性成纤维细胞生长因子:是重要的有丝分裂促进因子,可抑制幼稚软骨细胞分化,抑制肥大细胞形成。它促进Ⅱ型胶原及糖胺聚糖的产生,同时抑制Ⅰ型胶原的产生,该结果主要取决于碱性成纤维细胞生长因子浓度及细胞传代数,可能与其诱导碱性成纤维细胞生长因子受体、SOX9及N-黏钙素作用有关[13,32-33]。
2.3.2 影响脂肪干细胞成软骨分化细胞因子的相互作用 地塞米松位于骨形态发生蛋白6的上游[34],可以上调骨形态发生蛋白6的表达,同时与AGC1的上调及COL10A1的下调相关。研究证实培养最初1周内短时间的地塞米松加入,与骨形态发生蛋白产生协同促进作用,推测脂肪干细胞成软骨分化有骨形态发生蛋白或糖皮质激素串扰作用参与[2]。但Estes等[18]研究发现地塞米松加入含转化生长因子β的藻朊酸盐包埋脂肪干细胞中,抑制了转化生长因子β对促蛋白聚糖沉积的促进作用。
骨形态发生蛋白6可以诱导转化生长因子β受体的表达,骨形态发生蛋白6与转化生长因子β3组合应用促进了脂肪干细胞成软骨分化,同时骨形态发生蛋白2与激活素组合促进脂肪干细胞成软骨分化,据此推测骨形态发生蛋白与转化生长因子β诱导成软骨存在相互作用[19],此作用尚需要结合细胞通路及基因调控解释。骨形态发生蛋白2可以增强胰岛素样生长因子受体(IGF1-R)的结合力,同时可以抑制骨形态发生蛋白3的表达及活化[6]。该结果同样被Li等[35]的研究证实:骨形态发生蛋白2与胰岛素样生长因子1同时应用促进了软骨细胞分化及细胞外基质的沉积。该研究结果证实了既往脂肪干细胞成骨分化中碱性成纤维细胞生长因子对血管内皮生长因子正性调节,同时血管内皮生长因子可正性反馈促进骨形态发生蛋白2表达。研究发现胰岛素样生长因子1和碱性成纤维细胞生长因子联合应用效果明显优于单独使用胰岛素样生长因子1 [36]。转化生长因子β1、胰岛素样生长因子1和骨形态发生蛋白2联合应用有利于促进脂肪干细胞成软骨分化[37]。研究发现,转化生长因子β3和骨形态发生蛋白6联合应用明显促进脂肪干细胞成软骨分化,但加入胰岛素样生长因子2则发生了逆转[1]。10 μg/L转化生长因子β3、100 μg/L胰岛素样生长因子1和500 μg/L骨形态发生蛋白6合用促进了Ⅰ型胶原的表达。胰岛素样生长因子1和转化生长因子β3及骨形态发生蛋白6同时应用不及骨形态发生蛋白6单独应用时的软骨分化效果[3,18,38-39]。
研究表明某一细胞因子单独应用时促进脂肪干细胞软骨形成,但联合应用时可产生拮抗作用,甚至发生效果逆转,其表现需要进一步通过细胞通路来解释。也有研究发现Wnt1/Wnt-β-actin/TCF通路的灭活可促进脂肪干细胞成软骨分化,Ⅱ型胶原、聚集蛋白聚糖、sox9的表达[40]。
2.4 其他影响脂肪干细胞成软骨分化方法 细胞外基质被认为是一种支持结构,可以提供所需的物理、机械和化学信号功能,包括附着力、迁移、增殖以及分化。印迹基板模仿细胞外基质的二维环境,具有诱导形状特异性及分子表型特异性细胞的作用,软骨印记基板促进成软骨分化—Ⅱ型胶原表达增加、Ⅰ型胶原表达降低。由此推测普通聚苯乙烯组织培养板可以被分子印迹技术所替代[20]。
脂肪干细胞与耳廓软骨细胞混悬物注射于裸鼠体内,其Ⅱ型胶原及弹性蛋白表达明显增加。软骨细胞共培养显著促进了脂肪干细胞的成软骨分化,但研究并未提及可能涉及的机制[41]。
骨关节炎患者软骨细胞提取物促进髌下脂肪垫细胞成软骨分化,脂肪干细胞转变成软骨细胞样形态,蛋白多糖形成增加,Ⅱ型胶原产生增加,同时SOX9与L-SOX5、SOX6、Col2a1表达增加,暗示了骨关节炎软骨细胞提取物促进了脂肪干细胞形成成熟软骨细胞表型,其他研究也证实了这一点[9,16,42-43]。
静水压驱动三维支架诱导脂肪干细胞与胶原成软骨分化的实验表明静水压可促进脂肪干细胞成软骨分化,但其组织块变小,结合基质金属蛋白酶3及基质金属蛋白酶13高表达,暗示了静水压促进了软骨细胞外基质的降解[19]。脂肪干细胞激活压力敏感钙信号通路并调节sox-9的表达,促进转化生长因子β、激活蛋白复合物表达。随后细胞内钙增加激活二级信号的传导。动态压缩单独应用其诱导软骨形成的效果较胰岛素样生长因子转染组差。动态压缩与胰岛素样生长因子1转染同时应用增加了胰岛素样生长因子1的表达,增加了Ⅱ型胶原、聚集蛋白聚糖、SOX9的表达,不增加Ⅹ型胶原的表达,促进了细胞增殖及胶原和蛋白多糖的沉积[35]。
2.5 3D支架促进脂肪干细胞成软骨分化 软骨细胞所处关节微环境有助于其表型维持及调节软骨细胞代谢。软骨细胞外基质三维环境有助于诱导成软骨分化,同时细胞外基质可以负反馈调节软骨基质产生。
研究证实生物可降解乳酸-乙醇酸支架可促进软骨细胞成熟及表型维持,有望应用于体内临床研究[16]。Mahmoudifar等[44]发现非网眼聚乙醇支架结合静水压可促进脂肪干细胞成软骨分化。加入转化生长因子β1和胰岛素软骨分化增强,Ⅱ型胶原及糖胺聚糖比例增加,但仍不及软骨细胞组。Ⅱ型胶原透明质酸支架[45]、聚乙二醇聚丙炔共聚物蛋白支架[46]、尼平交联软骨来源基 质[47]、3D胶原海绵支架[48]、软骨脱细胞支架都表现出良好的促软骨分化能力[49]。许多三维生物支架应用于脂肪干细胞诱导实验中[50-52]。支架材料需要具有良好的力学性能、可控的降解速率、亲水性、细胞黏性、孔隙率等。结果表明支架可以促进脂肪干细胞成软骨分化,但仍存在诸如强度不足、软骨分化不全及去分化等缺点,见表1,2。

.jpg)


.jpg)