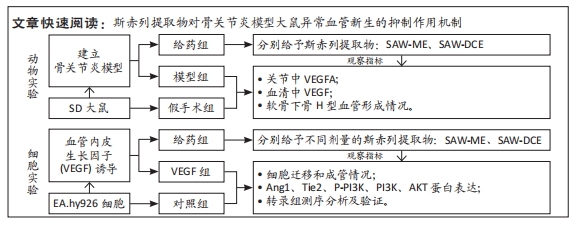
1.1 设计 对比观察实验及转录组学分析,组间比较采用单因素方差分析,并进行LSD或Tamhane’s法检验。
1.2 时间及地点 实验于2022 年3 月至2023 年3 月在云南中医药大学国家中医药管理局科研三级实验室中药药理实验室完成。
1.3 材料
1.3.1 实验动物 SPF级6周龄雌性SD大鼠40只,体质量180-200 g,购自湖南斯莱克景达实验动物有限公司,生产许可证号:SCXK(湘)2019-0004,饲养于云南中医药大学实验动物房,使用许可证号:SYXK(滇)K2022-0004,适应性喂养1周,标准饲料喂养,温度15-25 ℃,饮水自由。实验方案经云南中医药大学动物实验伦理委员会批准,批准号为R-062022099。
1.3.2 实验细胞 人脐静脉内皮细胞融合细胞:EA.hy926,购自昆明动物所。
1.3.3 主要试剂与仪器 血管内皮生长因子(vascular endothelial growth factor,VEGF)A Polyclonal antibody、Recombinant Human VEGF165、Ang1 Rabbit Polyclonal Antibody、Tie2 Rabbit Polyclonal antibody、PI3 Kinase p85 Alpha Monoclonal antibody、AKT Monoclonal antibody、Cy3-conjugated Affinipure Goat Anti- Rabbit IgG(H+L)、Fluorescein (FITC)-conjugated Affinipure Goat Anti-Rabbit IgG(H+L)、beta-actin抗体、超敏ECL化学发光检测试剂盒 (美国Proteintech公司);Phospho-PI3 Kinase p85 (Tyr458)/p55 (Tyr199) Antibody (美国Cell Signaling公司);Anti-Endomucin Rabbit pAb、Anti -CD31 Rabbit pAb (中国servicebio公司);ELISA试剂盒 (南京建成公司);RNA提取液、Servicebio RT First StrandcDNA Synthesis Kit、2×SYBR Green qPCR Master Mix (None ROX)引物 (中国servicebio公司);Matrigel Basement Membrane Matrix (美国BD Biocoat公司);Fetal Bovine Serum(澳大利亚Australia)、DMEM培养基、胰酶 (美国Gibco公司);荧光倒置显微镜 (德国蔡司公司);酶标仪 (瑞士Tecan公司);荧光定量PCR仪 (美国Bio-rad公司);无菌操作台、CO2培养箱 (美国Nalgene公司)。
1.4 实验方法
1.4.1 斯赤列提取物SAW-ME和SAW-DCE的制备 斯赤列样品采自云南省曲靖市马龙县,由云南中医药大学普春霞副教授鉴定为忍冬科接骨木属植物血满草 (Sambucus adnata Wall.)。① SAW-ME:斯赤列地上部分粗粉 (88 kg),甲醇浸提2次,每次48 h,过滤,得到浸提液,该浸提液用石油醚萃取后选取甲醇部分。②SAW-DCE:斯赤列地上部分粗粉(66.5 kg),体积分数95%乙醇浸提2次,每次48 h,过滤,回收乙醇,得浸膏,将总浸膏混悬于水中,依次用石油醚、二氯甲烷、乙酸乙酯提取,选取二氯甲烷部分。
1.4.2 动物分组及给药 随机将40只SD大鼠分为假手术组、模型组、SAW-ME组、SAW-DCE组,每组各10只。造模24 h后,假手术组和模型组灌胃给予生理盐水,SAW-ME组给予SAW-ME(600 mg/kg灌胃,为临床给药量的10倍);SAW-DCE组给予SAW-DCE(400 mg/kg灌胃,为临床给药量的5倍),每天1次,所有动物干预3周后取材。
1.4.3 大鼠骨关节炎模型的复制 除假手术组外,其余大鼠采用戊巴比妥钠(400 mg/kg)麻醉后剪去关节部位的毛,用碘伏对关节部位反复消毒,在大鼠关节外部皮肤切开约3 cm切口,剪开肌肉,屈膝,露出关节囊并切开,将髌骨外翻,显露交叉韧带,剪断前交叉韧带,进行抽屉实验,确保前交叉韧带完全剪断,生理盐水冲洗关节腔,缝合外部伤口,涂抹碘伏。假手术组大鼠切开关节外部皮肤和关节囊,髌骨外翻,缝合伤口,碘伏消毒。手术结束后,将大鼠放回鼠框,保温。术后肌肉注射青霉素8万单位/只,连续3 d。

1.4.4 膝关节石蜡标本的制作 造模后第22天,戊巴比妥钠麻醉后处死大鼠,取大鼠膝关节,经脱钙、脱水、透明、浸蜡、包埋等过程制成组织蜡块,最后使用转轮式石蜡切片机切片(厚度为5 μm),保存备用。
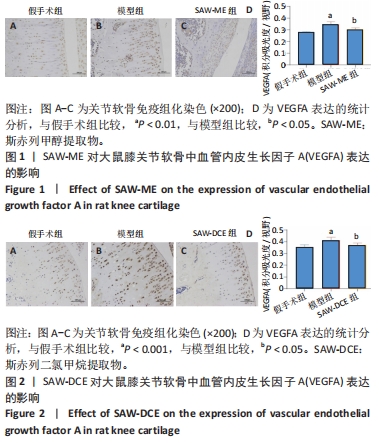
1.4.5 免疫组化染色 取出石蜡切片,经二甲苯、乙醇梯度处理,枸橼酸缓冲液修复,山羊血清室温封闭1.0-2.0 h,滴加50-100 μL按比例稀释的VEGFA一抗,4 ℃过夜,生物素标记二抗工作液,室温孵育2 h,DAB显色,苏木素染核,滴入中性树脂封固。显微镜下观察、拍照。
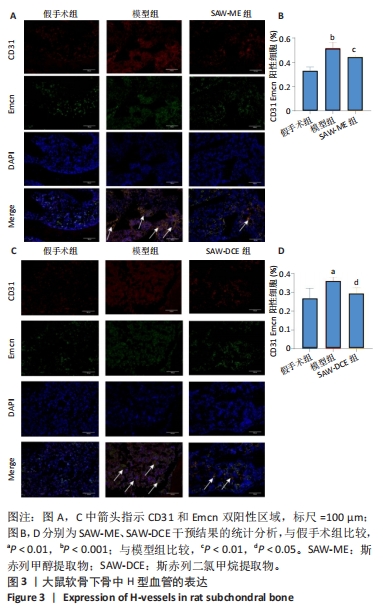
1.4.6 CD31/Emcn 免疫荧光双染色 取出石蜡切片,山羊血清封闭1.0-2.0 h,滴加CD31一抗(稀释比例1∶200),4 ℃过夜,滴加荧光Cy3二抗(稀释比例1∶200)孵育1.0-2.0 h,TSA室温孵育15 min。于TBST中洗涤,进行抗原修复。滴加Emcn一抗(稀释比例1∶600),4 ℃孵育过夜;滴加荧光FITC二抗(稀释比例1∶800),避光室温孵育1.0-2.0 h。
滴加DAPI染液,避光室温孵育10 min。加入自发荧光淬灭剂,孵育5 min,流水冲洗10 min,抗荧光淬灭封片剂封固,显微镜下观察、拍照。
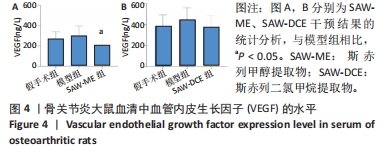
1.4.7 酶联免疫吸附测定 (ELISA) 腹主动脉取血,室温静置20-30 min,3 000 r/min,离心2次,每次10 min。收集上清,-80 ℃保存,备用。采用大鼠酶联免疫吸附测定试剂盒检测骨关节炎大鼠血清中VEGF的水平,具体步骤按试剂盒说明书操作。
1.4.8 细胞培养 采用DMEM培养基(添加青霉素-链霉素溶液、胎牛血清)培养人脐静脉内皮细胞融合细胞(EA.hy926),细胞培养1 d更换培养基,之后每2 d换1次培养基,细胞长满培养瓶底部80%-90%,胰酶消化,按1∶2的比例进行传代。
1.4.9 EA.hy926细胞分组培养 将EA.hy926细胞分为:对照组、VEGF组、SAW-ME组(VEGF+SAW-ME)、SAW-DCE组(VEGF+SAW-DCE)。对照组在正常培养液中培养24 h;VEGF组在培养液中加入20 ng/mL VEGF培养24 h;SAW-ME组分别给予20 ng/mL的VEGF和50,25,12.5 μg/mL的SAW-ME培养24 h;SAW-DCE组分别给予20 ng/mL的VEGF和5,2.5,1.25 μg/mL的SAW-DCE培养24 h。
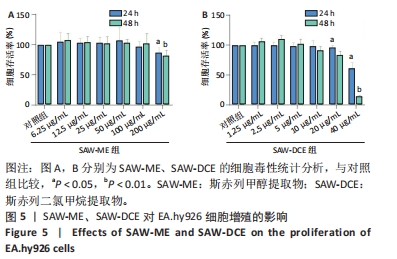
1.4.10 MTT检测 将EA.hy926细胞调整浓度至5×107 L-1,按每孔100 μL接种于96孔板中,实验细胞设为空白组(完全培养基)、对照组(完全培养基+细胞)、提取物组 (SAW-ME的质量浓度分别为200,100,50,25,12.5,6.25 μg/mL;SAW-DCE的质量浓度分别为40,20,10,5,2.5,1.25 μg/mL),每个不同浓度组设置6个复孔,培养24,48 h后,每孔避光加入20 μL MTS溶液,再放入培养箱孵育2 h后,在酶标仪吸光度490 nm处测定各孔吸光度值 (A值)。
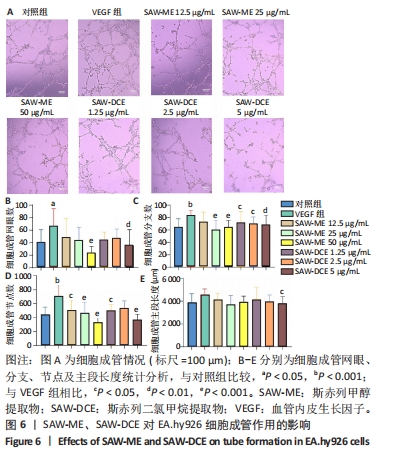
1.4.11 Matrigel基质胶法 将冷冻的 Matrigel 基质胶于 4 ℃过夜,解冻,取凝胶状基质胶50 μL/孔均匀涂布96孔板底部,于细胞培养箱中放置1 h使其凝固。取100 μL终浓度为4×108 L-1的EA.hy926细胞接种于底部覆盖基质胶的96孔板内,实验分为8组:对照组、VEGF组、SAW-ME 50 μg/mL组(VEGF+SAW-ME 50 μg/mL)、SAW-ME 25 μg/mL组(VEGF+SAW-ME 25 μg/mL)、SAW-ME 12.5 μg/mL组(VEGF+SAW-ME 12.5 μg/mL)、SAW-DCE 5 μg/mL组(VEGF+SAW-DCE 5 μg/mL)、SAW-DCE 2.5 μg/mL组(VEGF+SAW-DCE 2.5 μg/mL)、SAW-DCE 1.25 μg/mL组(VEGF+SAW-DCE 1.25 μg/mL);在细胞培养箱内培养6 h,显微镜下观察细胞成管的情况并拍照,用Image J软件进行分析统计。
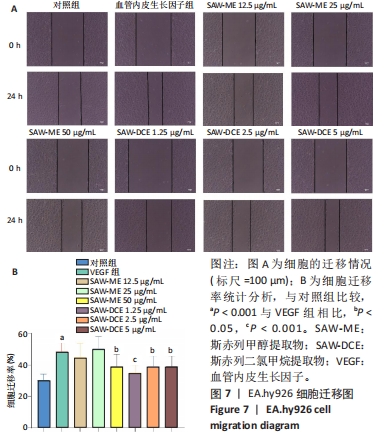
1.4.12 细胞迁移实验 将EA.hy926细胞以2×108 L-1浓度种于6孔板,每孔2 mL,细胞长满后去除培养基,用200 µL枪头,于每孔中心位置划一道划痕区域。分组情况同1.4.11,每组设置3个复孔。显微镜下观察细胞迁移情况,每孔选择3个不同视野拍照。记录2种提取物作用0,24 h后划痕愈合情况。
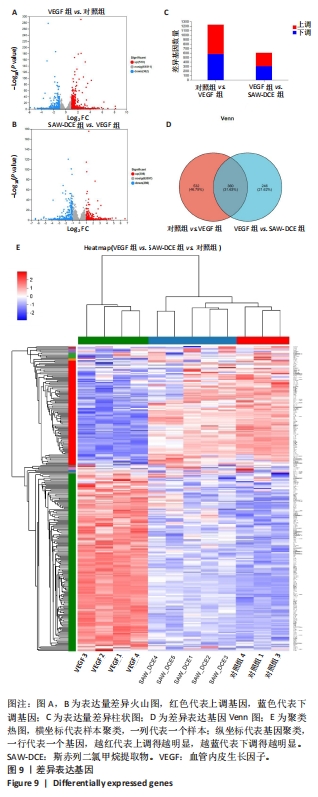
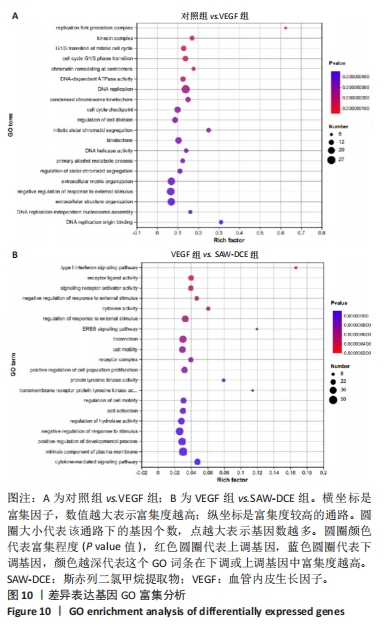
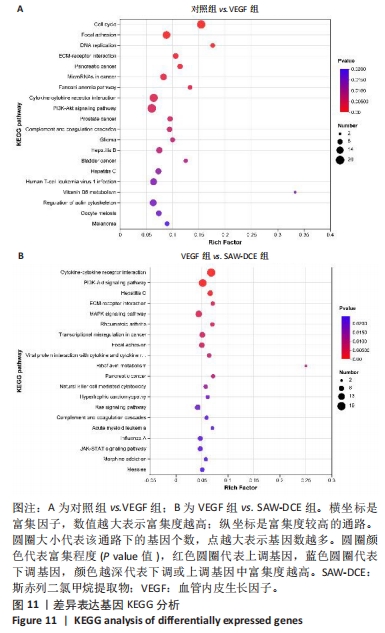
1.4.13 转录组学测序 EA.hy926细胞以2×108 L-1浓度种于6孔板,每孔2 mL,细胞长满后去除培养基,实验分为3组:对照组、VEGF组、SAW-DCE 5 μg/mL组(VEGF+SAW-DCE);每组设置6个复孔。使用TRIZOL从细胞中提取总RNA。对得到的RNA进行降解、纯度、浓度和完整性评价。通过高通量Illumina测序技术进行测序,以 P < 0.05和 log2FC 2作为差异表达基因的筛选标准,得到差异表达基因,对多个样本进行组别间基因的差异表达分析,筛选出组别间差异表达基因并进行功能分析。
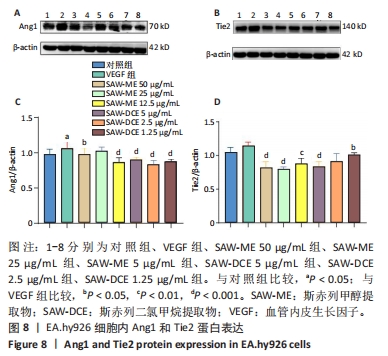
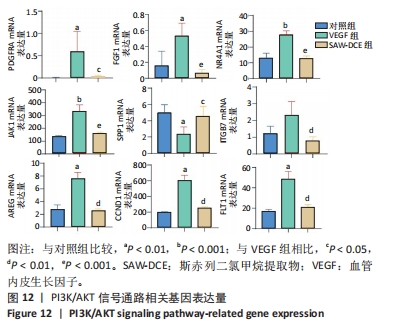
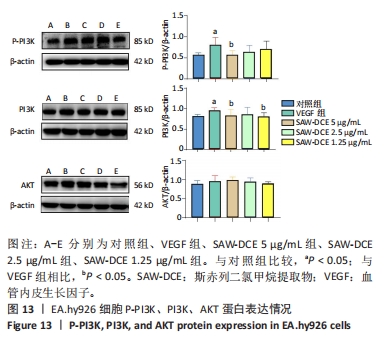
1.4.14 Western bolt检测 细胞种板密度及分组同1.4.13。细胞提取蛋白后,进行上样、电泳、转膜后加入牛奶封闭1 h,加Ang1、Tie2一抗,4 ℃孵育过夜,洗涤,加入相应的二抗孵育2 h(内参为beta-actin)。加入超敏ECL显影液,多功能分子凝胶成像系统进行拍照。用Image J对结果进行分析,并对转录组学分析结果筛选出与骨关节炎相关关键通路PI3K/AKT信号通路进行验证。
1.5 主要观察指标 ①SAW-ME、SAW-DCE对大鼠关节中VEGFA、血清中VEGF及H型血管的影响;②SAW-ME、SAW-DCE对细胞增殖的影响;③SAW-ME、SAW-DCE对细胞成管和迁移能力的影响;④EA.hy926细胞内Ang1、Tie2蛋白的变化;⑤转录组测序分析结果及验证。
1.6 统计学分析 实验所得结果以x±s表示,组间比较采用单因素方差分析法 (One-Way analysis of variance ANOVA),方差齐者采用LSD法检验,方差不齐者采用Tamhane’s法检验。文章统计学方法已经云南中医药大学生物统计学专家审核。