1.1 设计 随机对照动物实验和细胞学实验观察。
1.2 时间及地点 实验于2021年9月至2022年9月在复旦大学附属中山医院完成。
1.3 材料
1.3.1 实验动物 8周龄SPF级雌性C57BL/6J小鼠200只,体质量(20.0±1.5) g,购于上海斯莱克实验动物有限公司,许可证号:SYXK(沪)2022-0012。小鼠饲养条件为12 h光照,室内温度控制在(22±1) ℃,饲养需要的颗粒干饲料和饮用水均由动物实验中心提供。动物实验按照动物伦理委员会:Institutional Animal Care and Use Committee of SLAC(IACUC)批准方案(批准文号:20210725011)进行。
1.3.2 主要试剂 40 g/L多聚甲醛(Boster,中国);阿佛丁(Avertin,AbMole,美国);EDTA(江苏彤盛化学试剂有限公司);淫羊藿苷(Icariin,Selleck上海蓝木化工有限公司);抗酒石酸酸性磷酸酶(tartrate resistant acid phosphatase,TRAP) 染色检测试剂盒(Sigma,美国);ɑ-MEM培养基、胎牛血清 (FBS)、青霉素-链霉素(Gibco,美国);巨噬细胞集落刺激因子(macrophage colony-stimulating factor,M-CSF)、核因子κB受体活化因子配体(receptor activator of NF-kB ligand,RANKL,R&D Systems,美国);Cell Counting Kit-8 试剂盒 (CCK8,Dojindo,日本);CAⅡ抑制剂(Brinzolamide,Selleck上海蓝木化工有限公司);BCA 蛋白定量分析试剂盒(翊圣);凝胶电泳蛋白 Marker(Thermo Fisher,美国);NFATC1抗体(ab2796)、β-actin(ab8227);c-Fos抗体(ab208942)、CathepsinK抗体(ab207086)、CAⅡ抗体(ab191343)、TRPV1抗体(ab305299)均为abcam产品;HRP-羊抗兔二抗、HRP-羊抗小鼠二抗(Jackson ImmunoResearch,美国)。
1.3.3 主要仪器 正置显微镜、倒置显微镜、荧光显微镜(Olympus,日本);Micro-CT(Scanco Mecdica,瑞士);足底热刺痛仪、鼠尾光照测痛仪(上海欣软有限公司);化学发光/荧光图像分析系统(Tanon,中国);快速蛋白凝胶电泳仪(天根生化);超微量分光光度计(Biodrop 公司,英国);pH计(FE28 Five Easy,Mettler Toledo,瑞士)。
1.4 实验方法
1.4.1 动物实验
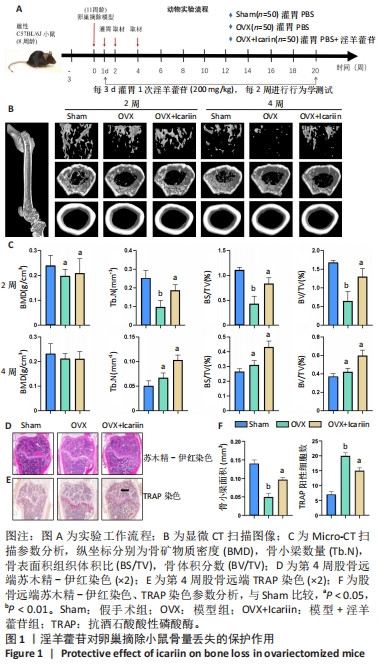
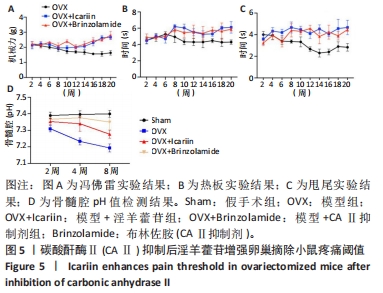
(1)卵巢摘除模型造模及淫羊藿苷给药治疗:将200只C57BL/6小鼠随机分为4组:假手术组(n=50)、卵巢摘除(ovariectomized,OVX)模型组(模型组,n=50),模型+淫羊藿苷治疗组(模型+淫羊藿苷组,n=50),模型+CAⅡ抑制剂(Brinzolamide)治疗组(模型+CAⅡ抑制剂组,n=50)。在麻醉(阿佛丁气麻,30 μL/g)状态下摘除小鼠双侧卵巢建立绝经后骨质疏松模型。假手术组小鼠暴露双侧卵巢后不摘除并缝合皮肤切口。模型+淫羊藿苷组小鼠在造模后第2天灌胃淫羊藿苷(200 mg/kg),将淫羊藿苷溶于磷酸缓冲盐溶液,每只灌胃100 μL,每3 d灌胃1次,各组小鼠分别持续灌胃至取材为止;模型+CAⅡ抑制剂组小鼠灌胃CAⅡ抑制剂200 mg/kg;假手术组和模型组每只小鼠灌胃100 μL磷酸缓冲盐溶液,每3 d灌胃1次。所有小鼠每2周进行1次疼痛行为学实验[冯弗雷(Von Frey)、热板和甩尾试验]并取材,观察10个时间点:造模后第2,4,6,8,10,12,14,16,18,20周,50只小鼠被平均分配在10个时间点,每个时间点5只小鼠。

(2)Micro-CT扫描及分析:在卵巢摘除术后第2,4周,CO2窒息处死小鼠,采集双侧股骨,采用Micro-CT扫描远端股骨,分辨率为100 kV,98 μA,10 μm。采用220的CT阈值,使用SkyScan DataViewer软件选择感兴趣区域(ROI)进行三维(3D)重建。通过测定骨体积分数(bone volume fraction,BV/TV)、BMD、骨小梁数(trabecular number,Tb.N)等参数来评价标本中的骨量及骨微结构。
(3)骨组织苏木精-伊红及TRAP染色:保留股骨并在15% EDTA中脱钙。对脱钙股骨进行切片,并用苏木精和伊红染色观察细胞,同时用TRAP染色观察破骨细胞活性。在显微镜下检查染色的切片,并使用3D扫描仪(Pannoramic MIDI)进行分析,评估骨结构、破骨细胞细胞形态及活性。
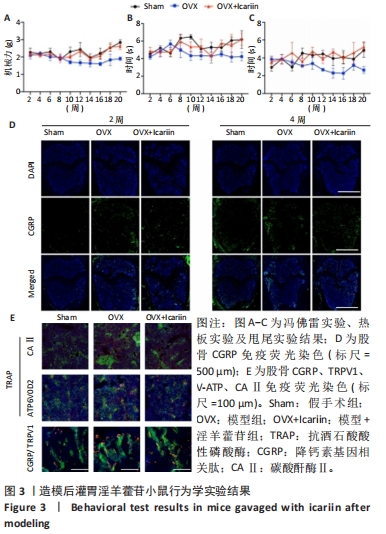
(4)骨组织免疫荧光染色:骨组织切片脱蜡复水,然后进行抗原修复。切片覆盖一层均匀的体积分数3%牛血清白蛋白,室温下封闭30 min。去除封闭液后,用荧光标记抗体(CGRP、TRPV1、CAⅡ)覆盖切片,确保均匀分布,放置于潮湿的避光箱中,4 ℃孵育过夜。随后用DAPI染色液对细胞核进行复染,室温下避光孵育10 min。为了长期保存荧光信号,切片用抗荧光猝灭剂封固。最后,使用倒置荧光显微镜观察切片并获取图像,观察破骨细胞数量和背根神经节神经元数量。
(5)冯弗雷测试:小鼠在行为室中驯化≥2 d后被放置在一个架高的有机玻璃笼子里(30 cm×9 cm×24 cm),笼底有金属网地板,可以接触到小鼠后爪足底表面。小鼠适应环境后(15-20 min),采用改良的Dixon上下法对同一后爪进行机械灵敏度测试,采用Von Frey丝刺激,刺激力分别为0.07,0.4,0.6,1,1.4,2,4,6 g,垂直放置至弯曲并保持两三秒。每只后爪连续测量2次,间隔≥5 min。撤爪或舔爪表示积极反应。无反应小鼠接受更高强度的Von Frey丝(最大弯曲力6 g)测试。在第1次异常反应之后,进行了另外4次测试。记录并计算50%爪脱阈值(PWT),计算公式为10^[Xf+kδ]/
10 000,其中Xf表示最终丝值(对数单位),k基于最近的反应模式,δ为平均刺激差(对数单位)。
(6)热板测试:将足底热刺痛仪温度设置为55 ℃,并稳定10 min。小鼠被放置在一个有机玻璃平台上,让它们适应环境15 min。一旦小鼠静止不动,将一个辐射热源(40 W)放置在小鼠一只后爪的正下方。如果小鼠表现出后爪舔舐或退缩,则记录为阳性反应。观察并记录热刺激导致小鼠后爪退缩的光照时间。设置休息时间20 s,以防止反复刺激导致的脱敏或皮肤损伤。实验过程中,每只后爪测试3次,每次测试之间的间隔最小为10 min。
(7)甩尾测试:将鼠尾光照测痛仪进行预热,设置温度为40 W。小鼠被牢牢束缚,并将其尾巴放置在甩尾装置的指定区域。当小鼠感到疼痛时,它会立即甩尾巴,仪器会自动记录甩尾巴的时间。间隔时间设置为10 s,以避免反复刺激导致的脱敏或皮肤损伤。
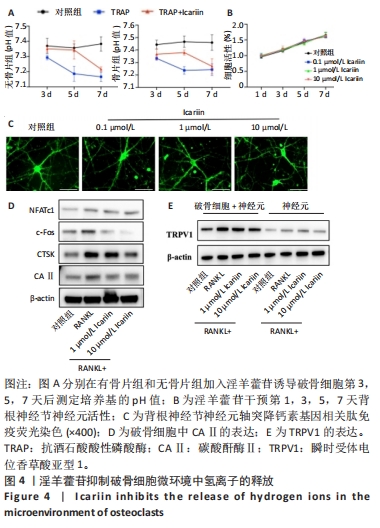
(8)小鼠股骨髓腔pH值检测:使用pH计,配备微电极pH针和参比电极(MI-407B和MI-402, Microelectrodes, USA)。小鼠被充分麻醉,放在加热的毯子上。在股骨部位做一个小切口,并用pH缓冲液校准pH计。参考电极(2 mm OD)放置在股骨附近的皮肤下。用钻头在股骨近端钻出一条隧道,将pH针电极(0.75 mm OD)插入股骨髓腔。电极保持静止,直到pH读数稳定。每次测量后重新校准电极。每个地点在2个不同的方向上进行了2次测量。
1.4.2 细胞实验
(1)小鼠骨髓巨噬细胞的提取、培养及破骨细胞诱导:从雌性C57BL/6小鼠股骨和胫骨中分离新鲜骨髓来源巨噬细胞。骨髓巨噬细胞培养在含体积分数10%胎牛血清和50 ng/mL M-CSF的完全培养基中。消化细胞,以8×107 L-1的细胞浓度接种细胞于96孔板中,每孔100 μL,用M-CSF (30 ng/mL)和RANKL (50 ng/mL)诱导细胞形成破骨细胞。诱导5 d后,破骨细胞开始分化。分化完成后,用40 g/L多聚甲醛固定破骨细胞30 min。然后加入制备好的TRAP染色液,37 ℃避光环境下孵育1 h。染色后,使用显微镜观察和拍摄照片,以便进一步分析数据。
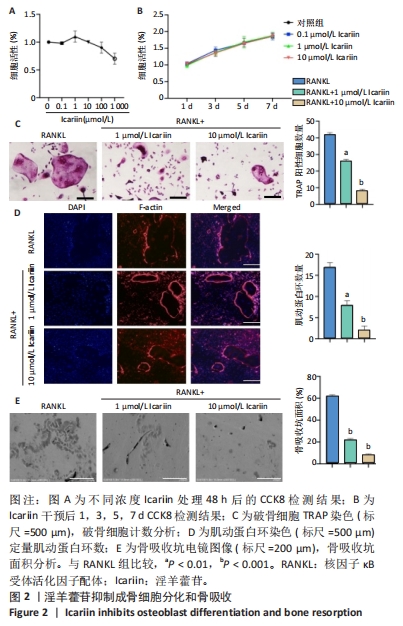
(2)体外TRAP染色:在α-MEM培养基中添加30 ng/mL M-CSF、50 ng/mL RANKL和不同浓度淫羊藿苷(1,10 μmol/L),以8×107 L-1细胞浓度将骨髓巨噬细胞接种于96孔板中,每孔100 μL。待分化完成后,去除培养基,用40 g/L多聚甲醛固定细胞,用0.1% Triton X-100通透,用TRAP溶液在37 ℃下染色一两个小时。苏木精染色细胞核。利用Image J软件对成熟破骨细胞(具有3个或更多核的TRAP阳性细胞)进行计数,并测量其吸收面积。
(3)鬼笔环肽免疫荧光染色:提取小鼠骨髓原代巨噬细胞,在细胞爬片上培养细胞,用RANKL诱导破骨细胞分化,并依据CCK8检测结果选用相对无毒性浓度的淫羊藿苷(1,10 μmol/L)处理。分化完成后,用40 g/L多聚甲醛在室温下固定20 min,用0.1% Triton X-100通透5 min,用PBS洗涤3次。用鬼笔环肽偶联异硫氰酸荧光素(FITC)染色F-actin,用4,6-二氨基-2-苯基吲哚(DAPI)染色细胞核。最后,用共聚焦显微镜采集图像,用Image J软件进行分析。
(4)骨板吸收及凹形面积测定:将骨髓巨噬细胞以4 000个/cm²的密度接种到含α-MEM完整培养基(含30 ng/mL MCSF)及骨板的24孔板上(每孔500 μL)。24 h后,换入含有30 ng/mL MCSF、50 ng/mL RANKL和不同浓度淫羊藿苷(1,10 μmol/L)的α-MEM完全培养基。细胞培养5 d,然后去除培养基并用40 g/L多聚甲醛固定。用TRAP染色或甲苯胺蓝观察破骨细胞和骨吸收窝。取骨片,用扫描电镜观察凹坑。Image J软件计算吸收坑面积百分比。
(5)体外pH值检测:提取小鼠骨髓原代巨噬细胞,培养在含体积分数10%胎牛血清和50 ng/mL M-CSF的完全培养基中。消化细胞,以4 000个/cm²的密度接种到含α-MEM完整培养基(含30 ng/mL M-CSF)及骨板(设置无骨板对照组)的24孔板上,每孔500 μL。24 h后,换入含有30 ng/mL MCSF、50 ng/mL RANKL和不同浓度淫羊藿苷(1,10 μmol/L)的α-MEM完全培养基。细胞培养5 d后,采用pH计测量细胞培养液中的pH值。
(6)小鼠背根神经节神经元的提取与培养:用阿佛丁麻醉小鼠。背部消毒,腰部下方做2 cm切口。使用骨钳暴露第4腰椎横突,仔细分离下位背根神经节神经元并置于冰培养基中。分离的背根神经节神经元用胶原酶A和TrypLE Express溶液酶解。用含胎牛血清的培养基终止后,轻轻吹打促进细胞分离。取上清,1 000 r/min离心5 min后用神经元完全培养基重悬,接种细胞于包被多聚赖氨酸的培养瓶中。
(7)CGRP免疫荧光染色:以50%密度接种神经元细胞于24孔板爬片(每孔500 μL培养基)上,并用不同浓度的淫羊藿苷(1,10 μmol/L)处理。96 h后,吸去上清,用40 g/L多聚甲醛在室温下固定20 min,用0.1% Triton X-100通透5 min,用PBS洗涤3次。用荧光标记CGRP抗体4 ℃染色过夜,用DAPI染色细胞核。最后,用共聚焦显微镜采集图像,用Image J软件进行分析。
(8)细胞CCK8检测:①收集骨髓巨噬细胞,悬浮于添加体积分数10%胎牛血清和1%青霉素/链霉素的α-MEM培养基中。以每孔1×104个细胞的密度将细胞接种于96孔板中,每孔100 μL,用30 ng/mL M-CSF培养24 h。然后,将细胞暴露于不同浓度的淫羊藿苷(0,0.1,1,10,100,1 000 μmol/L)中孵育48 h。在每孔中加入10 μL CCK8底物,37 ℃下孵育1 h。利用酶标仪在450 nm处测量每孔的吸光度值。与对照组比较,计算细胞相对活力。②收集小鼠背根神经节,将细胞暴露于不同浓度的淫羊藿苷(0.1,1,10 μmol/L)。并分别于干预第1,3,5,7 天检测2种细胞活性。
(9) Western Blot检测:破骨细胞以每孔1×105个细胞的密度培养于6孔板中,每孔2 mL。在不同浓度淫羊藿苷(1,10 μmol/L)处理的条件下,用30 ng/mL M-CSF和50 ng/mL RANKL对细胞进行诱导分化。分化完成后,用RIPA缓冲液提取总蛋白样品,用BCA蛋白测定法定量。等量的蛋白质在12% SDS-PAGE凝胶上分离2 h,然后转移到PVDF膜上。用5%脱脂牛奶在室温下封闭膜60 min。随后,将它们与稀释度为1∶1 000的NFATC1、C-fos、CathepsinK、CAⅡ、TRPV1和1∶5 000的β-actin的一抗在4 ℃下孵育过夜。在TBST中冲洗后,与相应的辣根过氧化物酶偶联二抗(1∶10 000)在室温下孵育1 h。使用Western Blot扫膜仪进行扫描拍照,使用Image J软件对图像进行捕获和定量。
1.5 主要观察指标
1.5.1 动物实验 ①小鼠疼痛行为学实验结果及疼痛的敏感性;②股骨骨量和骨微结构;③骨组织破骨细胞活性;④骨组织神经元形态及相关离子通道的表达;⑤骨髓腔pH值。
1.5.2 细胞实验 ①破骨细胞及背根神经节神经元细胞活性;②破骨细胞分化情况及肌动蛋白环结构;③破骨细胞噬骨功能;④体外培养体系pH值;⑤破骨细胞分化相关蛋白表达;⑥背根神经节神经元形态。
1.6 统计学分析 研究采用x±s表示所有实验数据。配对样本的两两比较采用配对t检验,独立样本差异采用非配对t检验。多样本均值单因素比较采用单因素方差分析(ANOVA),组间事后多组比较采用LSD检验。P < 0.05认为差异有显著性意义。定量分析采用Image J 1.8.0软件,数据可视化采用GraphPad 9.0软件。文章的统计学方法已经上海中医药大学生物统计学专家审核。