中国组织工程研究 ›› 2024, Vol. 28 ›› Issue (23): 3642-3648.doi: 10.12307/2024.414
• 口腔组织构建 oral tissue construction • 上一篇 下一篇
阿仑膦酸钠促进兔快速下颌骨牵张成骨的作用机制
叶芝魁,张志明,崔琳娜,蒋校文
- 南方医科大学口腔医学院附属郴州市第一人民医院口腔科&南华大学转化研究所,湖南省郴州市 423000
Mechanism by which alendronate promotes rapid mandibular distraction osteogenesis in rabbits
Ye Zhikui, Zhang Zhimin, Cui Linna, Jiang Xiaowen
- Department of Stomatology, the First People’s Hospital of Chenzhou City, School of Stomatology, South Medical University & Institute of Translation Medicine, University of South China, Chenzhou 423000, Hunan Province, China
摘要:
文题释义:
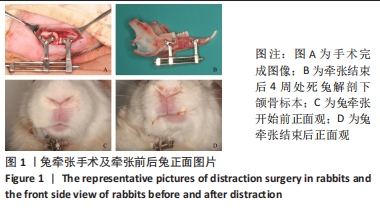
快速牵张成骨:牵张成骨是一种内源性骨组织工程,亦常被用于成骨及骨发育的研究。牵张成骨分为:①手术期:完成截骨及安放牵张器;②滞留期:使牵张间隙形成骨痂,一般为5-7 d;③牵张期:按照一定的频率和速度缓慢延长牵张间隙;④固定期:牵张结束后至拆除牵张器,目的促进牵张新生骨质矿化改建已达到足够临床强度。啮齿类动物下颌骨成骨生长较快,常利用短滞留期和快速牵张速率来建立成骨不良的牵张模型。阿仑膦酸钠:属于第3代双膦酸盐类药物,可抑制破骨、改善矿化程度、提高骨强度,预防骨质疏松,有效降低椎体、髋骨和其他部位的骨折危险,也是唯一有效降低全身各部位骨折风险的药物。
背景:有研究发现局部应用阿仑膦酸钠能够促进成骨,但少见其在牵张成骨过程中的尝试及探讨。
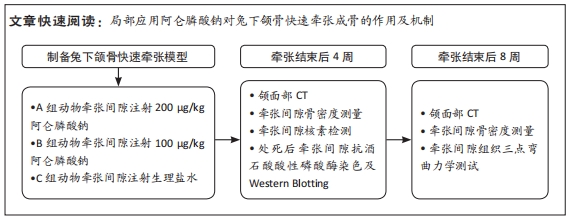
目的:观察阿仑膦酸钠对快速兔下颌骨牵张成骨的促进作用并探讨其机制。方法:36只新西兰雄性白兔在经过3 d的滞留期后以1.5 mm/12 h(3 d)的牵张速率进行快速牵张,随后实验动物被随机分为A、B和C组,每组12只。在固定期第1,3和7天,A组动物牵张间隙注射200 μg/kg阿仑膦酸钠,B组动物牵张间隙注射100 μg/kg阿仑膦酸钠,C组动物作为对照组。在固定期第4,8周,进行CT和双能量X射线骨密度测量。在第4周完成核素扫描后处死部分动物收集标本进行Western Blotting及抗酒石酸酸性磷酸酶染色;在第8周处死剩余动物后进行三点弯曲力学试验。
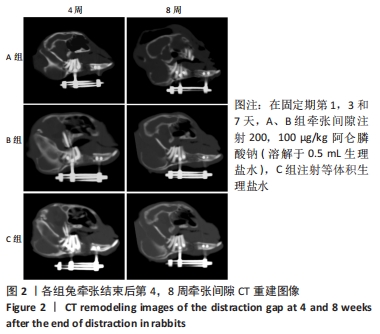
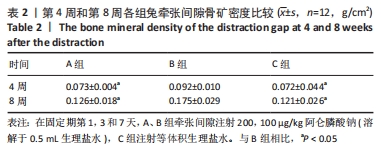
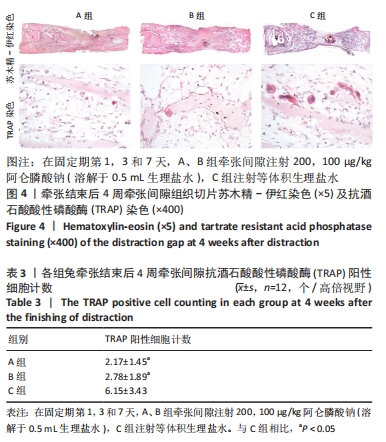
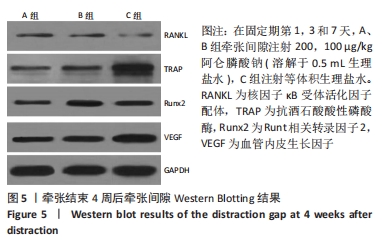
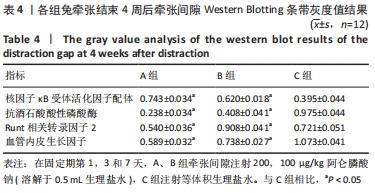
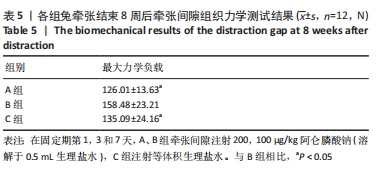
结果与结论:①CT结果发现B组兔牵张间隙新生骨质明显优于A、C组;②在第4周时B组的骨密度计数为(0.092±0.010) g/cm2,是A组的1.26倍(P < 0.001)、C组的1.28倍(P < 0.001);在第8周时B组的骨密度为(0.175±0.029) g/cm2,是A组的1.38倍(P < 0.001)、C组的1.45倍(P < 0.001);③抗酒石酸酸性磷酸酶染色发现C组切片破骨样细胞计数是A组的2.83倍(P < 0.001)、B组的2.21倍(P < 0.001);④C组牵张间隙核浓集强度高于A、B组;⑤Western Blotting结果发现B组成骨信号蛋白Runx2表达明显强于A、C组;⑥B组牵张间隙的最大力学负载(158.48±23.21) N是A组的1.26倍(P=0.007)、C组的1.31倍(P=0.003);⑦结果表明低浓度阿仑膦酸钠可能通过抑制破骨信号来促进兔下颌骨快速牵张成骨。
https://orcid.org/0009-0000-7298-8040(叶芝魁)
中国组织工程研究杂志出版内容重点:组织构建;骨细胞;软骨细胞;细胞培养;成纤维细胞;血管内皮细胞;骨质疏松;组织工程
中图分类号: