1.1 设计 细胞学体外观察实验。以多次传代导致的衰老MSCs为模型,用VEGF和bFGF对衰老细胞进行干预,通过观察细胞形态、细胞增殖、衰老标记物等探讨VEGF和bFGF是否能改善MSCs的复制性衰老。
1.2 时间及地点 实验于2021年10月至2023年4月在河南省中医院中心实验室完成。
1.3 材料
1.3.1 实验动物 2周龄SD雄性大鼠5只,体质量25-30 g,购自北京维通利华实验动物科技有限公(No.11400700270554),饲养于河南省中医院(河南中医药大学第二临床医学院)中心实验室,许可证:SYXK(豫)2021-0018,12 h光照,室温(25±2) ℃,湿度(45±10)%,自由饮食。实验方案经河南省中医院动物伦理委员会批准,批准号:PZ-HNSZYY-2020-001。
1.3.2 实验试剂 胎牛血清(Gibco,2305262RP);低糖DMEM培养基(凯基,20220623);胰蛋白酶(索莱宝,20220904);青霉素-链霉素溶液100x(Biosharp,21203590);CD90抗体(Biolegend,202526);CD44抗体(Thermo,ACVF0220061);CD31抗体(美天旎,5210706445);CD45抗体(美天旎,5210706408,PE);0.2%茜素红染色液(美伦生物,J1205A);大鼠骨髓MSCs成脂诱导分化试剂盒(OriCell,RAXMX-90031);VEGF(Peprotech,1107436 L0612);bFGF(Peprotech,0314432 C2221);CCK-8(大连美伦生物,MA0218);β-半乳糖苷酶活性染色试剂盒(北京索莱宝,20211228);鬼笔环肽(Proteintech,20010345);DAPI(中国白鲨,22104336);0.2% TritonX-100(北京索莱宝,20220621);吉姆萨染色液(Solarbio,G4640)。
1.3.3 实验仪器 CO2培养箱 (型号:3110 系列)、酶标仪(苏州赛默飞世尔仪器有限公司,FC型);流式细胞仪(美国BD公司,FACS Jazz);荧光显微镜(日本 Olympus,CKX41);超微量核酸蛋白测定仪(中国 Onedrop,OD-2000+);基因扩增仪(美国BIO-RAD,XBCX-S-25)。
1.4 实验方法
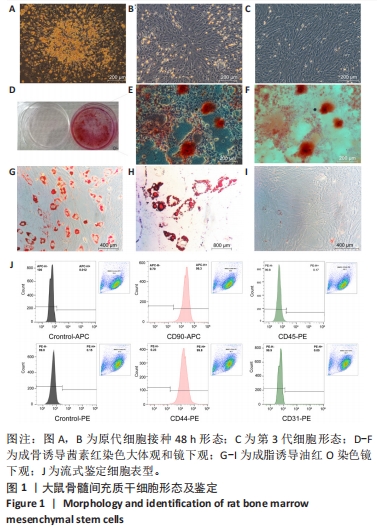
1.4.1 大鼠骨髓MSCs的提取和培养 两三周龄SPF级雄性SD大鼠5只,脱颈后乙醇浸泡5 min,分离出股骨和胫骨,彻底清除附着的肌肉和筋膜,PBS清洗3次并移入生物超净台,去除两端骨骺,用5 mL注射器吸取含体积分数10%胎牛血清的低糖DMEM培养基反复冲洗骨髓腔,将冲洗物装入培养瓶,放入培养箱,48 h后首次换液,以后每3 d换液1次,待细胞长至融合度为80%-90%时用0.25%含EDTA胰酶消化2 min,按1∶2比例传代。
1.4.2 骨髓MSCs鉴定
(1)细胞表面标志物鉴定:将第2代细胞按5×107 L-1的细胞浓度接种于6孔板(每孔2 mL),待细胞长至融合度为90%时进行流式鉴定:细胞消化后加入PBS,1 500 r/min离心5 min,清洗2次,分别加入CD90抗体5 μL、CD44抗体10 μL、CD31抗体2.5 μL、CD45抗体5 μL,室温避光孵育30 min,离心后弃上清,PBS清洗2次,再次加入1 mL PBS,流式细胞仪上机检测。
(2)成骨诱导分化:用含体积分数10%胎牛血清的低糖DMEM培养基配置含10 mmol/L β-甘油磷酸钠、50 μmol/L维生素C和100 nmol/L地塞米松的成骨诱导培养液。第2代细胞按5×107 L-1的细胞浓度接种于12孔板中(每孔1 mL),待细胞长至融合度为60%时更换为成骨诱导培养液,干预21 d后用0.2%茜素红染色,染色方法:PBS清洗2次后用40 g/L多聚甲醛固定30 min,清洗后每孔加入500 μL染色液,室温孵育5 min,PBS清洗2次,镜下观察。
(3)成脂诱导分化:用大鼠骨髓MSCs成脂诱导分化试剂盒进行诱导。具体如下:6孔板每孔加0.1%明胶,放入CO2培养箱1 h,吸去明胶晾干,将第2代细胞按5×107 L-1的细胞浓度接种于6孔板中(每孔2 mL),待细胞长至融合度为100%时,吸去培养基并加入2 mL成脂诱导分化培养基A液,诱导3 d,吸去A液并加入2 mL成脂诱导分化培养基B液,维持1 d,吸去B液,换回A液,如此A液和B液交替诱导,直至出现脂滴即可染色。染色方法:PBS清洗后用40 g/L多聚甲醛固定30 min,吸去固定液加入油红O工作液2 mL,孵育30 min,PBS清洗3次,镜下观察。
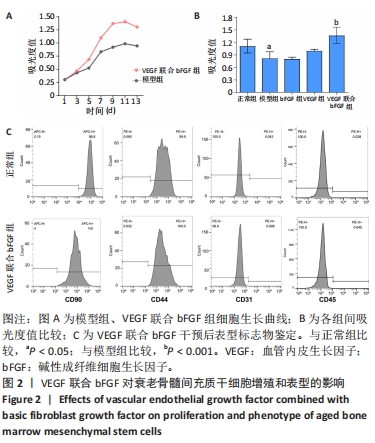
1.4.3 VEGF联合bFGF对衰老骨髓MSCs增殖的影响 细胞分组:正常组(第2代细胞)、模型组(第7代及以后代数细胞)、VEGF组、bFGF组、VEGF联合bFGF组。96孔板中每孔加入100 μL细胞悬液(5 000个细胞),置于培养箱中培养,24 h后正常组、模型组更换为低糖DMEM培养基,干预组更换为含50 μg/L VEGF和10 μg/L bFGF的低糖DMEM培养基,每3 d换1次液,分别在第1,3,5,7,9天用CCK-8法在酶标仪450 nm波长处检测每孔的吸光度值。
1.4.4 VEGF联合bFGF对衰老骨髓MSCs表型的影响 细胞分组:正常组(第2代细胞)、模型组(第7代及以后代数细胞)、VEGF联合bFGF组。将细胞按5×107 L-1的细胞浓度接种到6孔板(每孔2 mL),24 h后正常组、模型组更换为低糖DMEM培养基,干预组更换为含50 μg/L VEGF和10 μg/L bFGF的低糖DMEM培养基,每3 d换1次液,干预14 d,流式检测细胞表型CD90、CD44、CD31、CD45(流式检测方法同1.4.2)。
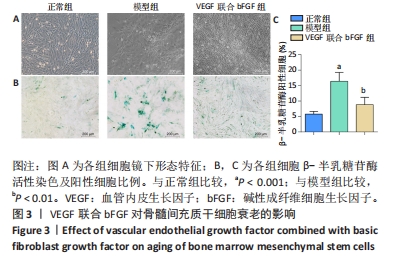
1.4.5 β-半乳糖苷酶活性染色 细胞分组:正常组(第2代细胞)、模型组(第7代及以后代数细胞)、VEGF联合bFGF组。将细胞按5×107 L-1的细胞浓度接种到6孔板(每孔2 mL),24 h后正常组、模型组更换为低糖DMEM培养基,干预组更换为含50 μg/L VEGF和10 μg/L bFGF的低糖DMEM培养基,每3 d换1次液,干预14 d 进行β-半乳糖苷酶活性染色:PBS清洗后加入1 mL β-半乳糖苷酶活性固定液,室温15 min,PBS清洗3次,每孔加入1 mL工作液,保鲜膜封闭6孔板后37 ℃孵育过夜,镜下观察并用Image J分析绿染面积。
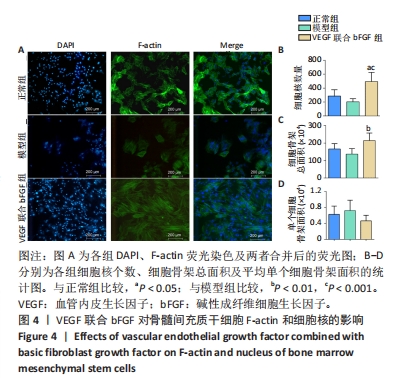
1.4.6 鬼笔环肽染色 细胞分组:正常组(第2代细胞)、模型组(第7代及以后代数细胞)、VEGF联合bFGF组。将细胞按5×107 L-1的细胞浓度接种到6孔板(每孔2 mL),24 h后正常组、模型组更换为低糖DMEM培养基,干预组更换为含50 μg/L VEGF和10 μg/L bFGF的低糖DMEM培养基,每3 d换1次液,干预14 d 进行鬼笔环肽染色:PBS清洗3次后用40 g/L多聚甲醛固定15 min;清洗后用含0.2% TritonX-100 室温透化5 min;PBS清洗3次后加入鬼笔环肽溶液(PBS∶鬼笔环肽母液=40∶1),室温孵育20 min;PBS清洗2次后每孔加入0.5 mL DAPI染色液,室温孵育5 min;PBS清洗2次,荧光显微镜下观察并用Image J分析F-actin荧光面积和细胞核个数。
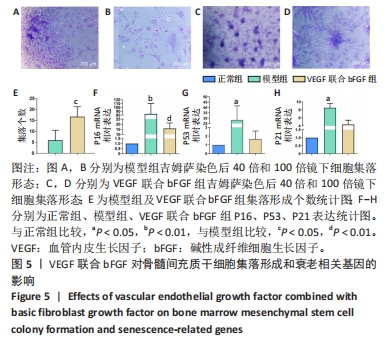
1.4.7 快速吉姆萨染色 细胞分组:正常组(第2代细胞)、模型组(第7代及以后代数细胞)、VEGF联合bFGF组。将细胞按5×107 L-1的细胞浓度接种到6孔板(每孔2 mL),24 h后正常组、模型组更换为低糖DMEM培养基,干预组更换为含50 μg/L VEGF和10 μg/L bFGF的低糖DMEM培养基,每3 d换1次液,干预第9天用吉姆萨染色液染色观察集落形成情况:用PBS洗2次,每孔加入0.5 mL染色液,室温放置2 min;直接滴加1 mL的缓冲液,轻摇6孔板后室温放置6 min;PBS洗2次后镜下观察并统计集落个数。
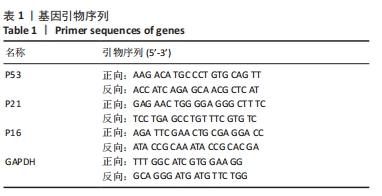
1.4.8 qRT-PCR 细胞分组:正常组(第2代细胞)、模型组(第7代及以后代数细胞)、VEGF联合bFGF组。将细胞按5×107 L-1的细胞浓度接种到6孔板(每孔2 mL),24 h后正常组、模型组更换为低糖DMEM培养基,干预组更换为含50 μg/L VEGF和10 μg/L bFGF的低糖DMEM培养基,每3 d换1次液,干预14 d后,采用Trizol法提取总RNA,然后进行RNA反转录:①去基因组DNA反应:去基因组DNA反应体系(模板RNA:总RNA 1 μg,gDNA Purge 1 μL,RNase Free Water至10 μL)轻轻混匀,离心;50 ℃孵育15 min,75 ℃孵育5 min,终止反应。②mRNA荧光定量:反应体系包括2×NovoStart® SYBR High-Sensitivy qPCR SuperMix 10 μL,上游引物终浓度0.5 μmol/L,下游引物终浓度0.5 μmol/L,模板1 μL,RNase Free Water加至总体系为20 μL;程序:预变性95 ℃,5 min;扩增(40 cycles)95 ℃,10 s;60 ℃,10 s;72 ℃,10 s。上机,根据2-ΔΔct计算结果并进行分析。基因引物序列见表1。
1.5 主要观察指标 ①CCK-8法观察细胞增殖情况;②β-半乳糖苷酶活性染色观察细胞衰老情况;③鬼笔环肽染色和吉姆萨染色观察细胞骨架大小及集落形成能力;④qRT-PCR检测衰老相关基因P16、P21和P53表达水平。
1.6 统计学分析 采用SPSS 20.0对数据进行分析,所有数据以x±s表示,方差齐时组间比较采用单因素方差分析,方差不齐时用秩和检验,P < 0.05为差异有显著性意义。文章统计学方法已通过河南中医药大学统计学专家审核。