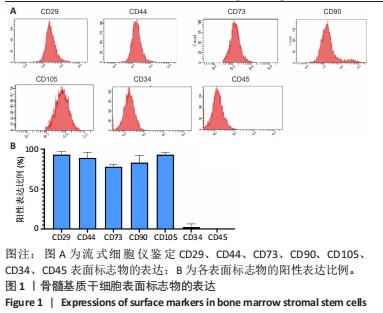
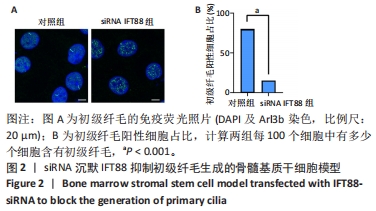
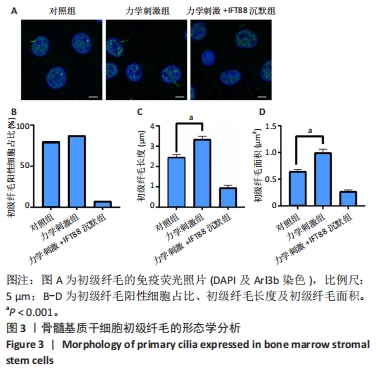
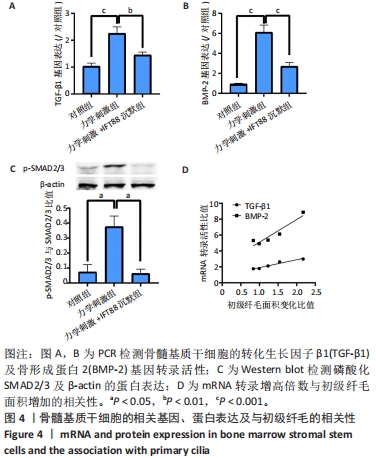
中国组织工程研究 ›› 2024, Vol. 28 ›› Issue (25): 3937-3941.doi: 10.12307/2024.192
• 骨髓干细胞 bone marrow stem cells • 下一篇
初级纤毛/鞭毛转运系统介导力学反应性信号通路促骨髓基质干细胞成骨分化
马占华,严 旭,姜 岩,曹争明,王永魁,李东哲,杨腾越,靳宜楷,付 苏,张春霖
- 郑州大学第一附属医院骨科,河南省郑州市 450000
Primary cilia/intraflagellar transport mediates mechanics-responsive signaling pathway and promotes osteogenic differentiation of bone marrow stromal stem cells
Ma Zhanhua, Yan Xu, Jiang Yan, Cao Zhengming, Wang Yongkui, Li Dongzhe, Yang Tengyue, Jin Yikai, Fu Su, Zhang Chunlin
- Department of Orthopedics, First Affiliated Hospital of Zhengzhou University, Zhengzhou 450000, Henan Province, China
摘要:

文题释义:
初级纤毛:真核细胞的长形力学感受性细胞器,介导力学信号转导及多种信号通路。鞭毛转运系统:初级纤毛的核心轴丝动力系统,维持初级纤毛长度的动态平衡。
转化生长因子β/SMAD信号通路:转化生长因子β激活信号通路,广泛参与细胞分化、凋亡等功能调控。转化生长因子β与受体相结合后,发生初级纤毛内聚集,激活SMAD等因子转移入细胞核,激活骨形成蛋白2等基因转录。
骨形成蛋白2:属于转化生长因子β超家族成员,是促进成骨分化的重要蛋白。
背景:目前已证实力学刺激可以促进骨髓基质干细胞成骨分化,但其机制未完全明了。初级纤毛是重要的力学感受器并调控TGF-β1/BMP-2/SMAD等多种信号通路,很可能是骨髓基质干细胞力学调控的重要靶点。
目的:探讨流体剪切力对骨髓基质干细胞成骨分化的影响及机制。方法:将大鼠骨髓基质干细胞分为对照组、力学刺激组(通过摇床施加流体剪切力学干预)、力学刺激+IFT88沉默组(力学刺激+使用siRNA沉默IFT88表达),干预24 h后,采用qRT-PCR检测转化生长因子β1、骨形成蛋白2的表达、Western blot检测磷酸化SMAD2/3蛋白的表达,初级纤毛免疫荧光染色及形态学分析。
结果与结论:剪切力刺激可促进骨髓基质干细胞的初级纤毛表达,转化生长因子β1及骨形成蛋白2基因转录激活,提高磷酸化SMAD2/3蛋白表达。siRNA干扰初级纤毛生成后,这一力学反应效应明显减低。骨髓基质干细胞的初级纤毛面积改变比值与转化生长因子β1及骨形成蛋白2基因转录增高比例具有Spearman相关性。结果表明:初级纤毛/鞭毛转运系统介导了流体剪切力反应性的TGF-β1/BMP-2/SMAD信号通路激活,促进骨髓基质干细胞成骨分化。
https://orcid.org/0000-0001-9565-4485 (张春霖)
中国组织工程研究杂志出版内容重点:干细胞;骨髓干细胞;造血干细胞;脂肪干细胞;肿瘤干细胞;胚胎干细胞;脐带脐血干细胞;干细胞诱导;干细胞分化;组织工程
中图分类号: