中国组织工程研究 ›› 2024, Vol. 28 ›› Issue (25): 3960-3966.doi: 10.12307/2024.189
• 骨髓干细胞 bone marrow stem cells • 上一篇 下一篇
白细胞介素4调控巨噬细胞极化及骨髓间充质干细胞的成骨分化
张 洁1,2,肖天骄2,李 丽2,康佳兵2,湛济帆2,韦 艳2,田 艾2,3
- 1贵州中医药大学第一附属医院,贵州省贵阳市 550001;2贵州医科大学口腔医学院,贵州省贵阳市 550001;3贵州医科大学附属口腔医院修复种植科,贵州省贵阳市 550001
Interleukin-4 regulates macrophage polarization and osteogenic differentiation of bone marrow mesenchymal stem cells
Zhang Jie1, 2, Xiao Tianjiao2, Li Li2, Kang Jiabing2, Zhan Jifan2, Wei Yan2, Tian Ai2, 3
- 1First Affiliated Hospital of Guizhou University of Traditional Chinese Medicine, Guiyang 550001, Guizhou Province, China; 2School of Stomatology, Guizhou Medical University, Guiyang 550001, Guizhou Province, China; 3Department of Restoration and Implant, Affiliated Stomatological Hospital of Guizhou Medical University, Guiyang 550001, Guizhou Province, China
摘要:
文题释义:
巨噬细胞极化:巨噬细胞会受到微环境中多种因子的调节与诱导,从而可以产生不同的功能状态。这种功能可塑性称为巨噬细胞极化,炎性巨噬细胞被称为经典激活的或M1巨噬细胞,而活跃于组织再生的巨噬细胞为交替激活的或M2巨噬细胞。JAK1/STAT6信号通路:此信号通路的信号传递包括JAK和STATs的磷酸化、STAT蛋白二聚化移位到细胞核。在炎症相关疾病中,以JAK/STAT6依赖的方式发挥抗炎、抗凋亡和神经保护作用,同时是骨髓间充质干细胞生理活动的决定性调节因素,在成骨代谢活动中发挥着重要作用。
NLRP3炎症小体:是由NOD样受体、凋亡相关斑点样蛋白和Caspase-1组成的多蛋白复合体,控制着Caspase-1的活性和天然免疫系统中炎症细胞因子白细胞介素1β、白细胞介素18的成熟和分泌,介导炎症,并诱导细胞焦亡。
背景:白细胞介素4可以提高骨替代材料的成骨效应,但其分子机制尚未明确,进一步阐明白细胞介素4提高成骨效应的作用机制,有助于为牙槽骨缺损患者的再生治疗找到安全、经济和有效的方法。
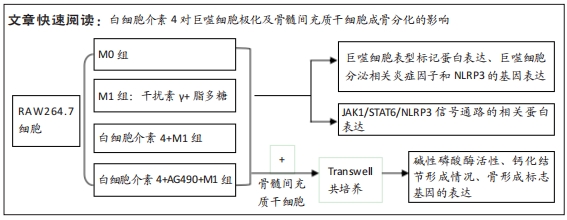
目的:探讨白细胞介素4对巨噬细胞极化转化和骨髓间充质干细胞成骨分化的影响及其可能的作用机制。方法:M1组RAW264.7细胞用干扰素γ+脂多糖诱导24 h,白细胞介素4+M1组RAW264.7细胞用干扰素γ+脂多糖诱导24 h后加入白细胞介素4诱导24 h,白细胞介素4+AG+M1组RAW264.7细胞用干扰素γ+脂多糖诱导细胞24 h后加入白细胞介素4和JAK/STAT通路抑制剂AG-490诱导24 h。干预结束后,采用免疫荧光染色分析巨噬细胞表型标记蛋白诱导型一氧化氮合酶、CD206的表达;采用ELISA试剂盒检测细胞培养上清液中白细胞介素10、肿瘤坏死因子α水平;采用RT-qPCR检测NLRP3、白细胞介素1β、caspase-1的 mRNA表达;采用 Western blot检测JAK1/p-JAK1、STAT6/p-STAT6、NLRP3、pro-IL-1β和pro-caspase-1通路蛋白的表达水平。随后将以上4组RAW264.7细胞与骨髓间充质干细胞transwell间接共培养24 h,然后进行碱性磷酸酶染色、茜素红染色,采用RT-qPCR检测碱性磷酸酶、Ⅰ型胶原和骨钙素的mRNA表达。
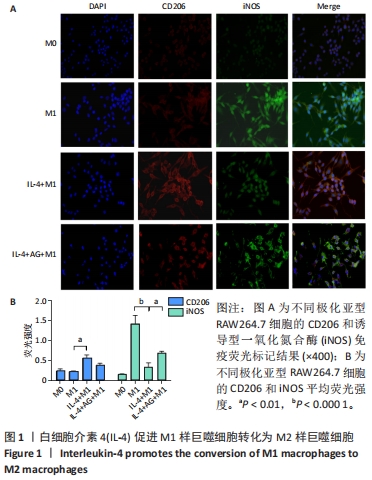
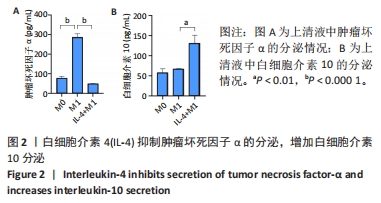
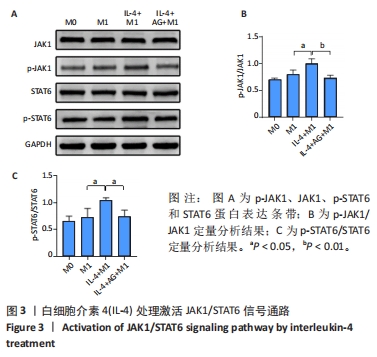
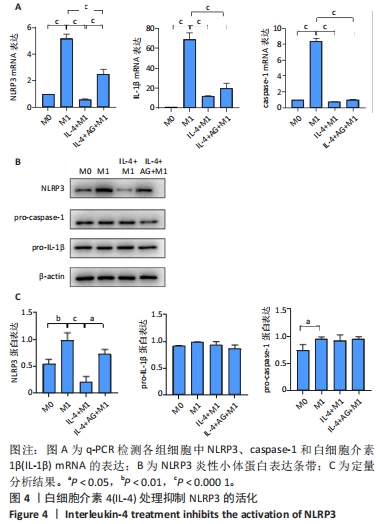
结果与结论:①免疫荧光、ELISA检测结果显示白细胞介素4可促进M2样巨噬细胞CD206和白细胞介素10的表达,抑制诱导型一氧化氮合酶和肿瘤坏死因子α的表达;②RT-qPCR结果显示白细胞介素4可抑制NLRP3、白细胞介素1β、caspase-1 mRNA表达;③Western blot结果显示白细胞介素4可促进JAK1/p-JAK1、STAT6/p-STAT6和NLRP3蛋白表达明显增加;④与白细胞介素4+M1组RAW264.7细胞共培养的骨髓间充质干细胞的碱性磷酸酶染色、茜素红染色明显增强,碱性磷酸酶、Ⅰ型胶原和骨钙素的mRNA表达明显升高。结果表明,白细胞介素4可能通过上调JAK1/STAT6通路,抑制NLRP3活化,从而促进巨噬细胞从M1向M2样极化转换,最终增强骨髓间充质干细胞的成骨分化能力。
https://orcid.org/0000-0003-4456-1144 (张洁)
中国组织工程研究杂志出版内容重点:干细胞;骨髓干细胞;造血干细胞;脂肪干细胞;肿瘤干细胞;胚胎干细胞;脐带脐血干细胞;干细胞诱导;干细胞分化;组织工程
中图分类号: