1.1 设计 体外细胞实验。组间差异采用单因素方差分析。
1.2 时间及地点 实验于2021年10至2022年11月在西南医科大学口腔颌面修复重建和再生实验室完成。
1.3 材料
1.3.1 实验动物 SPF级SD大鼠20只,2周龄,体质量80-100 g,购买于成都达硕实验动物有限公司,许可证号:SCXK(川)2020-030,实验单位使用许可证号:SYXK(川) 2018-065,西南医科大学实验动物福利伦理审查表编号:NO: 20211118-032、NO: 20211015-006。实验过程最大限度减少动物痛苦。
1.3.2 主要试剂 青霉素-链霉素溶液、BCA蛋白浓度测定试剂盒(中国,碧云天生物技术有限公司);胎牛血清(德国,PAN公司);胰蛋白酶消化液(美国,Gibco公司);α-MEM基础培养液(美国,Hyclone公司);黄连素、地塞米松、β-甘油磷酸钠、胰岛素、抗坏血酸、吲哚美辛、IBMX、1%茜素红染色液、油红O染色液(中国,Solarbio科技有限公司);碱性磷酸酶测定试剂盒(中国,南京建成生物研究工程所)。快速RNA提取试剂盒(中国,艾科瑞生物科技有限公司);PCR引物(中国,武汉天一华煜基因科技有限公司);PrimeScript™ II 1st Strand cDNA Synthesis Kit(日本,Takara公司);RIPA(强)组织细胞快速裂解液(中国,Solarbio科技有限公司);β-catenin抗体、AMPK抗体、Phospho-AMPKα抗体(英国,Abcam公司)。Dorsomorphin(Compound C,CC)(美国,MCE公司);N-乙酰半胱氨酸(N-acetyl-L-cysteine,NAC)(中国,索莱宝科技有限公司)。
1.4 实验方法
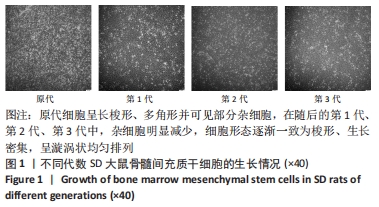
1.4.1 大鼠BMSCs的分离培养 大鼠吸入式麻醉后脱颈处死,分离股骨与胫骨,双抗+PBS清洗后剪断骨头两端的骨骺,α-MEM培养液冲洗骨髓腔并收集冲洗液,1 000 r/min离心5 min,弃上清,加入α-MEM完全培养液重悬,将细胞悬液接种于培养瓶中,放置于37 ℃、体积分数为5% CO2恒温孵育箱内培养,显微镜下观察细胞生长情况,2 d后进行半量换液,此后每2 d全量换液1次,待细胞汇合度达90%时,按1∶2传代。第3代细胞用于后续所有实验。
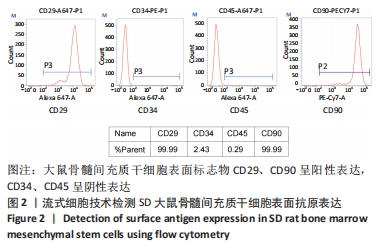
1.4.2 流式细胞术鉴定BMSCs 取第3代BMSCs,弃培养基后PBS清洗,胰酶消化,收集细胞悬液并计数,将细胞浓度调整为1×108 L-1,分别加入CD29、CD34、CD45、CD90抗体各100 μL,空白对照组不加入抗体,室温避光孵育30 min,上流式细胞仪进行检测,并用FCS Express软件进行结果分析。
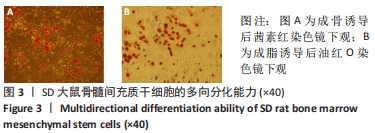
1.4.3 BMSCs成骨分化检测 取第3代处于生长对数期的BMSCs,胰蛋白酶消化收集细胞后,以2×104/cm2密度接种于6孔板中,待细胞汇合度达80%时,弃去原有培养液,加入2 mL成骨诱导液(含10-7 mol/L地塞米松、10-2 mol/L β-甘油磷酸钠、50 mg/L维生素C、体积分数10%胎牛血清的α-MEM基础培养基),每3 d更换1次成骨诱导液。诱导21 d后,弃去培养液,PBS轻柔清洗3次,每次5 min,每孔加入1 mL 40 g/L多聚甲醛溶液固定30 min,双蒸水清洗3次,每次5 min,加入茜素红染料(pH=4.2),室温下避光染色30 min,双蒸水清洗去除多余染料直到双蒸水中无色素,显微镜下观察拍照。
1.4.4 BMSCs成脂分化检测 取第3代处于生长对数期的BMSCs,胰蛋白酶消化收集细胞后,以2×104/cm2密度接种于6孔板中,待细胞汇合度达100%时,弃去原有培养液,加入2 mL成脂诱导液A液,3 d后更换为2 mL成脂诱导液B液,按上述方法不断循环连续培养21 d后,弃去培养液,PBS轻柔清洗3次,每次5 min,每孔加入1 mL 40 g/L多聚甲醛溶液固定30 min,PBS清洗3次,每次5 min,加入1 mL红油O染料,室温下避光染色30 min,PBS清洗去除多余染料直到PBS中无色素,显微镜下观察拍照。
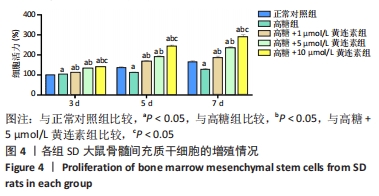
1.4.5 CCK-8法检测BMSCs增殖活力 取第3代处于生长对数期的BMSCs,胰蛋白酶消化收集细胞后,以3×103/孔密度接种于96孔板,分为5组,每组3个副孔,分别为正常对照组(培养基葡萄糖浓度为5.5 mmol/L),高糖组(培养基葡萄糖浓度为35 mmol/L),高糖+1 µmol/L黄连素组,高糖+5 µmol/L黄连素组,高糖+10 µmol/L黄连素组。第2天弃去原有培养液,按上述分组加入不同的完全培养基,培养第3,5,7天加入CCK-8工作液,避光孵育2 h,使用酶标仪在波长450 nm处检测吸光度值。
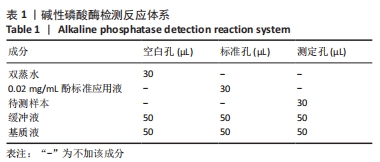
1.4.6 BMSCs的碱性磷酸酶活力检测 取第3代处于对数生长期的BMSCs,胰蛋白酶消化收集细胞后,以2×104/cm2密度接种于12孔板,分为4组,每组3个副孔,分别为正常对照组、高糖组、高糖+黄连素组(黄连素浓度为10 µmol/L)、高糖+黄连素+AMPK抑制剂组(黄连素浓度为10 µmol/L,AMPK抑制剂Dorsomorphin浓度为5 µmol/L)。待汇合度达80%时,弃去原有培养基,按上述分组加入成骨分化诱导液,避光培养,每3 d更换1次成骨诱导培养液。待培养7 d后,弃去孔内培养基,每孔加入500 µL细胞裂解液,室温下静置1 h,将孔内的裂解液转入标记好的无菌EP管中。按试剂盒步骤检测细胞内碱性磷酸酶活力,反应体系见表1。
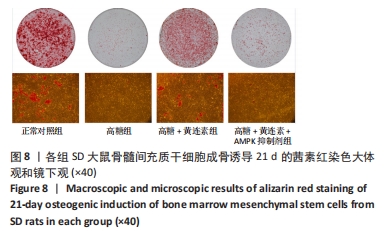
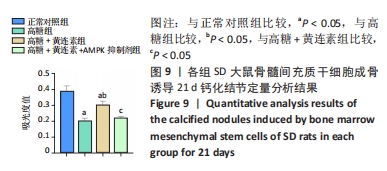
1.4.7 BMSCs茜素红染色 取第3代处于对数生长期的BMSCs,胰蛋白酶消化收集细胞后,以2×104/cm2密度接种于6孔板,分组同1.4.6,待细胞汇合度达80%时,弃去原有培养基,按上述分组加入成骨分化诱导液,避光培养,每3 d更换1次成骨诱导培养液。连续诱导21 d后,弃去培养基,PBS轻柔清洗3次,每次5 min,每孔加入1 mL 40 g/L多聚甲醛溶液固定30 min,双蒸水清洗3次,每次5 min,加入茜素红染料(pH=4.2),室温下避光染色30 min,双蒸水清洗去除多余染料直到双蒸水中无色素,显微镜下观察拍照。
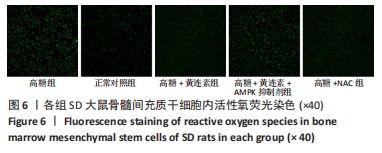
1.4.8 活性氧荧光探针检测BMSCs内活性氧水平 取第3代处于生长对数期的BMSCs,胰蛋白酶消化收集细胞后,以2×104/cm2密度接种于6孔板,分为5组,每组设置3个副孔,分别为正常对照组、高糖组、高糖+NAC组(特异性抗氧化剂NAC浓度为500 µmol/L)、高糖+黄连素组(黄连素浓度为10 µmol/L)、高糖+黄连素+AMPK抑制剂组(黄连素浓度为10 µmol/L,Dorsomorphin浓度为5 µmol/L),于恒温孵育箱内培养。第2天吸净原有培养基,按上述分组加入含不同药物的完全培养基培养48 h。按1∶1 000的比例将活性氧荧光探针溶液加入基础培养基中,配置成终浓度为10 µmol/L的活性氧荧光探针溶液。取出6孔板,每孔加入1 mL活性氧荧光探针溶液,放入孵育箱避光孵育30 min,孵育结束后,弃去活性氧荧光探针溶液,使用α-MEM清洗细胞3遍,于荧光显微镜下观察拍照。Image J软件对荧光图片进行半定量分析。
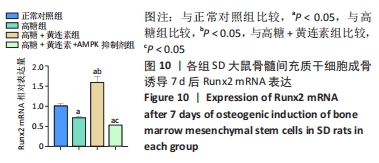
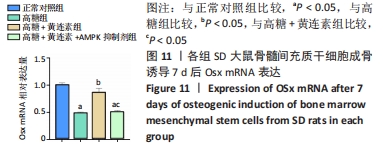
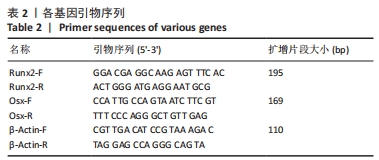
1.4.9 PCR检测成骨相关基因水平 取第3代处于对数生长期的BMSCs,胰蛋白酶消化收集细胞后,以2×104/cm2密度接种于6孔板,分组同1.4.6。待细胞汇合度达80%时,弃去原有培养基,按上述分组加入成骨分化诱导液,避光培养,每3 d更换1次成骨诱导培养液。待培养7 d后提取细胞总RNA。使用总RNA样本进行反转录和定量检测。q-PCR部分使用到的引物均参照GenBank上的引物序列,由武汉天一华煜基因科技有限公司合成。以β-actin为内参,各基因引物序列如表2所示。
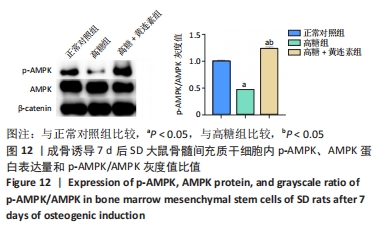
1.4.10 Western blot检测p-AMPK和AMPK的表达 根据1.4.6中分组进行成骨诱导7 d后,使用细胞裂解液提取细胞内总蛋白,BCA法测定蛋白浓度。使用上样缓冲液稀释样本并煮沸10 min。SDS-PAGE电泳分离样品,湿转法将蛋白从凝胶转至PVDF膜,室温下奶粉慢速摇床封闭1 h,将膜与一抗(anti-p-AMPK、anti-AMPK、anti-β-actin,1∶1 000)4 ℃孵育过夜,次日TBST漂洗后,室温下加入对应二抗慢速摇床孵育1 h,TBST洗去多余抗体后加入发光液,凝胶成像系统中曝光蛋白条带,使用Image J软件分析目的蛋白条带的灰度值。
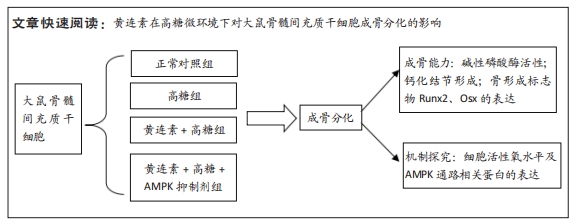
1.5 主要观察指标 ①大鼠BMSCs的形态及其成骨、成脂诱导分化潜能;②黄连素在正常/高糖微环境下对BMSCs增殖的影响;③黄连素在正常/高糖微环境下对BMSCs内碱性磷酸酶活性和钙化结节的影响;④黄连素在正常/高糖微环境下对BMSCs内活性氧水平的影响;⑤黄连素在正常/高糖微环境下对BMSCs成骨标志基因mRNA表达的影响;⑥黄连素在正常/高糖微环境下对AMPK信号通路相关蛋白表达的影响。
1.6 统计学分析 采用SPSS 26.0中的单因素方差分析方法(One-Way ANONA)进行相关数据处理,结果用x±s表示,P < 0.05为差异有显著性意义。每项实验重复3次。该文统计学方法已经西南医科大学生物统计学专家审核。