2.1 LncRNA对间充质干细胞增殖和凋亡的影响 间充质干细胞相关临床试验显示出有限的疗效,这与细胞移植后间充质干细胞的低存活率有重要关系,移植后的间充质干细胞必须面对一系列恶劣的微环境,这极大地降低了它们的存活率,从而降低了它们对靶组织的修复能力[7,27]。增强间充质干细胞的增殖能力或抑制其凋亡可加强其对组织修复的疗效,LncRNA在其中展现了不可忽视的作用[28]。

2.1.1 LncRNA促进间充质干细胞增殖和抑制凋亡 LINC01535最早被证实促进宫颈癌的进展[29],ZHAO等[30]发现LINC01535
可以促进人骨髓间充质干细胞的增殖和分化,抑制细胞凋亡。LINC01535可能是通过竞争性抑制miR-3619-5p,上调骨形态发生蛋白2的表达水平,进而促进人骨髓间充质干细胞成骨分化和细胞增殖,并抑制细胞凋亡。LncRNA H19是胎儿发育过程中的印记母性基因,已有证据表明LncRNA H19可以维持骨髓间充质干细胞的多倍体状态,并促进其增殖,此外,还有研究证实LncRNA H19在缺氧条件下可通过调节血管内皮生长因子来增强血管生成[31-32]。HOU等[33-34]研究证实LncRNA H19和血管内皮生长因子A的过表达可以促进骨髓间充质干细胞增殖和抑制凋亡,同时还能提高骨髓间充质干细胞的血管生成能力;已有的研究结果证实miR-199a-5p可以靶向抑制血管内皮生长因子A的表达[35],生物信息学预测结合功能实验和双荧光素酶报告表明LncRNA H19可以作为竞争性内源性RNA靶向结合miR-199a-5p,使得血管内皮生长因子A的表达上调。这些研究结果说明LncRNA H19/miR-199a-5p/血管内皮生长因子A是骨髓间充质干细胞增殖、凋亡和血管生成的重要调节通路,这可能为骨髓间充质干细胞用于治疗股骨头坏死、心血管疾病等提供重要的实验基础。LI等[36]发现先兆子痫患者和健康供者来源间充质干细胞相比,来源于先兆子痫患者的间充质干细胞中LncRNA MALAT1明显下调,随后的研究发现LncRNA MALAT1可以通过直接影响血管内皮生长因子启动子和解除miRNAs与血管内皮生长因子的3’ 非翻译区(3’ UTR)结合,促进了血管内皮生长因子的表达,进而促进骨髓间充质干细胞增殖、迁移、侵袭、血管生成,抑制细胞凋亡,参与调节的具体miRNA还需要进一步的实验进行验证。LncRNA HULC是最早发现的肿瘤相关LncRNA之一,有研究证实LncRNA HULC能够促进癌细胞的生长、凋亡、侵袭和血管生成[37],LI等[38]研究发现LncRNA HULC可以促使细胞周期进入S期和G2/M期,缩短G1期,从而促进细胞分裂,增加骨髓间充质干细胞的增殖能力和抑制细胞凋亡,还可以通过上调神经钙黏蛋白(N-cadherin)、波形蛋白(Vimentin)和基质金属蛋白酶2的表达促进细胞的迁移,然而其机制尚未完全证实。有趣的是,肿瘤坏死因子α、转化生长因子β1和R848等炎性因子刺激都会使间充质干细胞过表达LncRNA HULC,适当的炎症刺激可能会提高间充质干细胞的治疗效果。
XU等[39]最初对激素性股骨头坏死患者和正常人的骨髓间充质干细胞进行微阵列分析,发现LINC00473出现差异表达,明显下调。人骨髓间充质干细胞中的LINC00473在10-6mol/L 地塞米松诱导下呈时间依赖性下降,并且人骨髓间充质干细胞出现显著的细胞凋亡和增殖抑制,进一步的实验证实LINC00473可以减少地塞米松所致人骨髓间充质干细胞的凋亡,提高人骨髓间充质干细胞在地塞米松条件下的增殖能力,还增加细胞迁移能力。尽管这一作用机制尚未明确,但该研究为干预和治疗早期激素性股骨头坏死提供了一个新思路。
2.1.2 LncRNA抑制间充质干细胞增殖和诱导凋亡 LI等[40]证实了LNC000052可以抑制骨髓间充质干细胞增殖并促进凋亡,首先,他们确认了骨质疏松大鼠的骨髓间充质干细胞与正常的骨髓间充质干细胞相比,细胞活力及分化特性都显著降低,高通量测序结果显示骨质疏松模型组骨髓间充质干细胞中LNC000052显著升高,并找到了与LNC000052共表达的磷酸肌醇3激酶调节亚单位1(phosphoinositide-3-kinase regulatory subunit 1,PIK3R1),最后,该团队又利运用生物信息学网站发现miR-96-5p与LNC000052、PIK3R1都有共同结合位点,进一步实验显示下调miR-96-5p可使PIK3R1相对表达量增加,并且逆转了LNC000052对骨髓间充质干细胞的增殖抑制和凋亡促进作用。PI3K-Akt通常被认为是一种成骨途径,PIK3R1可以对下游的p-Akt/Akt进行负调节[41-42]。WU等[43]运用慢病毒转染技术使大鼠骨髓间充质干细胞低表达PIK3R1,然后检测PIK3R1功能,结果发现PIK3R1的缺失促进了骨髓间充质干细胞增殖,促进了G1-G2/S期的转变,并抑制了骨髓间充质干细胞的凋亡。上述这些研究结果最终证实LNC000052与miR-96-5p结合,解除miR-96-5p对PIK3R1的抑制作用,形成LNC000052/miR-96-5p/PIK3R1轴调节骨髓间充质干细胞的凋亡与增殖。
XIAO等[44]发现,与正常软骨相比,骨关节炎软骨中LncRNA HOTAIRM1-1表达减少和miR-125表达上升,进一步研究发现LncRNA HOTAIRM1-1与miR-125结合后,可抑制miR-125与骨形态发生蛋白2受体3’UTR的特异性结合,而骨关节炎软骨中的LncRNA HOTAIRM1-1表达减少抑制了上述过程,这抑制了间充质干细胞存活和分化并诱导凋亡,而过表达LncRNA HOTAIRM1-1并没有展现出正向的作用。更有趣的是,过表达LncRNA HOTAIRM1-1或骨形态发生蛋白2受体会抑制JNK/MAPK/ERK通路的激活,而过表达miR-125可逆转这一情况,所以JNK/MAPK/ER可能是LncRNA HOTAIRM1-1/miR-125b/骨形态发生蛋白2受体轴调节间充质干细胞凋亡、存活和分化的下游通路,这可能为延缓骨关节炎的进展提供一个有效的干预靶点。
2.1.3 LncRNA抑制间充质干细胞增殖 LI等[45]发现上调LncRNA HCG11可以抑制人脂肪间充质干细胞的分化及增殖,进一步研究证实LncRNA HCG11可通过与miR-204-5p直接结合,竞争性抑制miR-204-5p与Sirt1的3’ UTR结合导致Sirt1过度激活,使人脂肪间充质干细胞增殖减少。过表达miR-204-5p逆转了HCG11对人脂肪间充质干细胞的影响,结果证实LncRNA HCG11/miR-204-5p/Sirt1通路可参与调控人脂肪间充质干细胞增殖。
LncRNA对间充质干细胞增殖及凋亡的作用和机制,见表1。

2.2 间充质干细胞通过LncRNA调节宿主细胞的增殖和凋亡 间充质干细胞已被证明能够保护细胞免受损伤、促进愈合及组织再生,部分归因于间充质干细胞在进入目标区域后可以与宿主细胞发生细胞融合,导致宿主细胞的细胞核发生重编程,融合细胞表达间充质干细胞特异性基因,从而避免已损伤的宿主细胞发生凋亡,间充质干细胞还可通过与宿主细胞直接或间接接触、旁分泌等方式传递介质参与宿主细胞的增殖与凋亡,LncRNA在其中发挥了重要作用[46]。

2.2.1 LncRNA促进宿主细胞增殖和抑制凋亡 间充质干细胞分泌的外泌体包含了各种LncRNA和蛋白质[47],参与细胞间的通讯和细胞信号传递,这些递质可通过影响宿主细胞的增殖与凋亡参与损伤修复过程,LncRNA在其中发挥了重要作用,这可能使LncRNA成为疾病治疗的潜在靶点。例如,LIU等[48]观察到间充质干细胞来源外泌体中富集了LncRNA KLF3-AS1,更重要的是过表达KLF3-AS1进一步增强了间充质干细胞来源外泌体改善白细胞介素1β诱导的软骨细胞损伤的作用。此外,生物信息学分析提示LncRNA KLF3-AS1含有miR-206的结合位点,并且G蛋白偶联受体激酶相互作用蛋白1(GIT1) mRNA的3?-UTR含有miR-206结合序列,进一步研究证实了移植过表达lncRNA KLF3-AS1的间充质干细胞来源外泌体后,LncRNA KLF3-AS1可通过miR-206/GIT1轴促进软骨细胞增殖和抑制细胞凋亡来促进软骨修复。有趣的是,已有研究证实miR-206过表达可显著降低Ⅱ型胶原纤维α1基因(COL2A1)和聚集蛋白聚糖(aggrecan)[49],增加Runx2和基质金属蛋白酶1,从而抑制软骨细胞增殖并诱导凋亡。DENG等[50]首先发现LINC00461在多发性骨髓瘤患者的间充质干细胞和多发性骨髓瘤细胞中呈现高表达,随后证实了间充质干细胞来源外泌体可以通过LINC00461促进多发性骨髓瘤细胞增殖。RNA结合蛋白免疫共沉淀实验证实miR-15a和miR-16可直接与LINC00461结合,并且miR-15a和miR-16的上调与BCL-2的表达呈负相关,LINC00461作为miR-15a、miR-16的ceRNA解除miR-15a、miR-16对BCL-2的抑制作用,促进多发性骨髓瘤细胞增殖并且抑制其凋亡,这为间充质干细胞用于治疗多发性骨髓瘤提供了一个新的思路。LI等[51]研究间充质干细胞用于治疗糖尿病足溃疡,发现了miR-152-3p通过调节PTEN抑制成纤维细胞的增殖和迁移并诱导其凋亡,随后利用starBase数据库寻找到和miR-152-3p之间存在靶向关系的LncRNA H19,后续实验研究证实LncRNA H19通过间充质干细胞来源外泌体传递到成纤维细胞中,并进一步验证LncRNA H19可作为ceRNA竞争性抑制miR-152-3p调节PTEN表达,从而促进成纤维细胞的增殖和迁移并抑制其凋亡。此外,PTEN是PI3K/AKT信号通路的关键抑制因子,过表达或低表达LncRNA H19后,根据成纤维细胞中p85 PI3K和AKT的表达量以及AKT磷酸化的程度,提示PI3K/AKT信号通路参与了lncRNA H19/miR-152-3p/PTEN轴调节成纤维细胞增殖、迁移和凋亡。LncRNA H19还被报道在间充质干细胞治疗急性重症胰腺炎中发挥了重要作用。
间充质干细胞能显著减少缺血再灌注诱导的脑微血管内皮细胞凋亡和自噬,LI等[52]首先发现间充质干细胞与脑微血管内皮细胞共培养降低了脑微血管内皮细胞的凋亡率,而且还降低了LncRNA SNHG12在脑微血管内皮细胞中的表达。在后续的研究中,沉默SNHG12在间充质干细胞中的表达,并将这些间充质干细胞与脑微血管内皮细胞共培养,CCK-8实验提示脑微血管内皮细胞的增殖能力得到提升,免疫荧光分析及蛋白质印迹显示LC3B、caspase 3的表达显著降低,通路分析还证实SNHG12的沉默显著增强了间充质干细胞对脑微血管内皮细胞中PI3K、AKT和mTOR磷酸化的促进作用。结合大鼠体内的研究结果表明,沉默间充质干细胞中SNHG12通过激活PI3K/AKT/mTOR信号通路显著增强了脑微血管内皮细胞增殖和减少细胞凋亡与自噬,下调间充质干细胞中SNHG12的表达可能是治疗脑缺血再灌注损伤的新方法。
2.2.2 LncRNA促进宿主细胞增殖 SONG等[53]证实了间充质干细胞中的LncRNA H19可以同时竞争性抑制miR-138-5p和miR-141-3p,增加蛋白质酪氨酸激酶2和β-连环蛋白的表达,进而显著增强FAK/PDK1/AKT/mTOR途径的信号传导和β-连环蛋白靶基因c-Myc、细胞周期蛋白D1的表达,抑制胰腺细胞自噬并促进增殖。LncRNA H19主要定位于间充质干细胞的细胞质中,这提示其可能是通过传递介质的方式参与间充质干细胞治疗急性重症胰腺炎。
2.2.3 LncRNA抑制宿主细胞凋亡 YAN等[54-55]已经证明了间充质干细胞外泌体中LncRNA H19对大鼠软骨修复起着正向调节的作用,该团队为探究LncRNA H19对软骨细胞作用的具体机制[56],通过生物信息学分析发现了LncRNA H19序列中含有一个保守的miR-29b-3p靶位点,还发现了FOXO3是miR-29b-3p的推测靶标,双荧光素酶报告基因检测验证了这些结果,进一步实验将富含LncRNA H19的间充质干细胞来源外泌体与软骨细胞共培养,结果证实LncRNA H19作为ceRNA抑制miR-29b-3p,上调软骨细胞中的FoxO3,从而促进软骨细胞迁移、基质分泌,抑制细胞凋亡和衰老。有研究报道巨噬细胞移动抑制因子(macrophage migration inhibitory factor,MIF)预处理增强了间充质干细胞的治疗潜力[57],CHEN等[58]利用MIF预处理间充质干细胞来源外泌体(MSC-ExoMIF),保护了心肌细胞免于凋亡,LncRNA NEAT1在MSC-ExoMIF中的表达显著上调,然而MSC-ExosMIF的这种保护作用被沉默LncRNA NEAT1所消除,这提示MIF预处理是通过提高间充质干细胞表达LncRNA NEAT1而起到治疗效果。微阵列分析提示,被H2O2处理后的心肌细胞表达更高水平的miR-142-3p,但经历与MSC-ExoMIF共培养后,miR-142-3p的表达显著降低。后续的实验证实LncRNA NEAT1作为miR-142-3p的ceRNA,解除了miR-142-3对FOXO1的抑制作用,进而抑制H2O2诱导的心肌细胞凋亡。
2.2.4 LncRNA抑制宿主细胞增殖和诱导凋亡 有研究报道了LncRNA PTENP1可以作为ceRNA竞争性结合miRNA,从而调节几种癌症中抑癌基因PTEN的表达[59]。HAO等[60]发现人脐血间充质干细胞中的lncRNA PTENP1可以通过间充质干细胞来源外泌体转移到胶质瘤细胞,进一步研究表明过表达LncRNA PTENP1可通过竞争性结合miR-10a-5p来上调胶质瘤中PTEN的表达,从而抑制胶质瘤细胞的增殖并促进其凋亡。
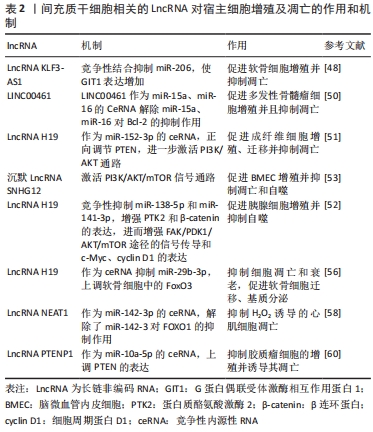
间充质干细胞相关LncRNA对宿主细胞增殖及凋亡的作用和机制,见表2。