Chinese Journal of Tissue Engineering Research ›› 2024, Vol. 28 ›› Issue (4): 615-620.doi: 10.12307/2023.962
Previous Articles Next Articles
Functions and roles of connective tissue growth factor in nervous systems
Ma Sicong1, Chen Jing2, Li Yunqing1, 2
- 1Department of Human Anatomy, School of Basic Medicine, Zunyi Medical University, Zunyi 563006, Guizhou Province, China; 2Department of Anatomy, Histology and Embryology and K.K. Leung Brain Research Centre, Air Force Medical University, Xi’an 710032, Shaanxi Province, China
-
Received:2022-12-19Accepted:2023-02-17Online:2024-02-08Published:2023-07-14 -
Contact:Li Yunqing, Professor, Doctoral supervisor, Department of Human Anatomy, School of Basic Medicine, Zunyi Medical University, Zunyi 563006, Guizhou Province, China; Department of Anatomy, Histology and Embryology and K.K. Leung Brain Research Centre, Air Force Medical University, Xi’an 710032, Shaanxi Province, China Chen Jing, Lecturer, Department of Anatomy, Histology and Embryology and K.K. Leung Brain Research Centre, Air Force Medical University, Xi’an 710032, Shaanxi Province, China -
About author:Ma Sicong, Master candidate, Department of Human Anatomy, School of Basic Medicine, Zunyi Medical University, Zunyi 563006, Guizhou Province, China -
Supported by:National Natural Science Foundation of China, No. 82130034 (to LYQ)
CLC Number:
Cite this article
Ma Sicong, Chen Jing, Li Yunqing. Functions and roles of connective tissue growth factor in nervous systems[J]. Chinese Journal of Tissue Engineering Research, 2024, 28(4): 615-620.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
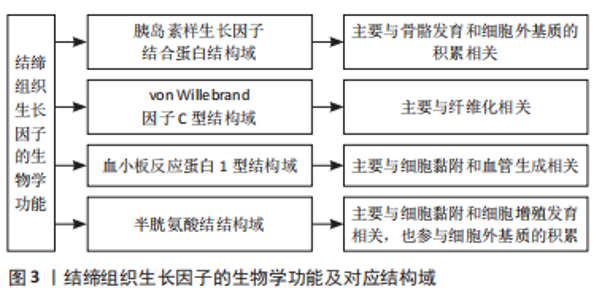
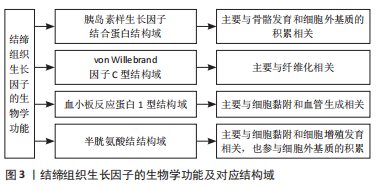
2.1 结缔组织生长因子的生物学功能 结缔组织生长因子基因由5个外显子构成,其蛋白质一级结构中含有349个氨基酸。第一个外显子编码用于分泌的信号肽,外显子2-5编码4个结构域,这些结构域与各种细胞外镶嵌蛋白中的保守区域具有同源性,包括胰岛素样生长因子结合蛋白、von Willebrand 因子C型、血小板反应蛋白1型和半胱氨酸结结构域,这些结构域既可以独立发挥相应的功能,也具有协同作用,参与更复杂的生物学活动[4]。其中von Willebrand 因子C型、血小板反应蛋白1型和C末端结构域与全长蛋白均可以激活细胞外信号调节激酶/丝裂原活化蛋白激酶,胰岛素样生长因子结合蛋白结构域可激活c-Jun氨基末端激酶途径。以上4个结构域在不同的细胞类型和特定环境下均与MAPK信号传导有关[5],作为多种信号分子和生长因子的介质,参与细胞发育、纤维化、黏附调节等多种过程[6],见图3。"

2.1.1 结缔组织生长因子与纤维化 既往研究表明,结缔组织生长因子的高表达在纤维化途径中发挥重要作用,结缔组织生长因子在皮肤修复过程中及在各种类型的纤维化疾病中发挥作用[7],且其在转化生长因子β通路中的作用较为突出[8]。VALLE-TENNEY等[9]观察到转化生长因子β1可在缺氧条件下诱导结缔组织生长因子在纤维化的骨骼肌中表达,且此诱导需要低氧诱导因子1α的参与。同年,有学者使用结缔组织生长因子的单克隆中和抗体FG-3019逆转了大鼠肌肉的纤维化[10]。结缔组织生长因子特异性地参与了组织纤维化,干预其功能可以逆转组织纤维化。FG-3019等单抗可以作为抗纤维化等拮抗结缔组织生长因子的潜在靶点,值得进一步研究。结缔组织生长因子在不同类型细胞中都能刺激细胞外基质分子的表达,有学者认为细胞外基质蛋白中的纤连蛋白是结缔组织生长因子作用的靶点[11]。此后又有学者观察到纤连蛋白是神经损伤后胶质瘢痕形成的主要组成部分[12],HERTEL等[13]借助核糖核酸酶保护实验和免疫荧光组织化学染色分析了小鼠海马CA3区单侧海人酸损伤后结缔组织生长因子和纤连蛋白的时空表达模式,观察到受损海马的神经元和胶质细胞中结缔组织生长因子mRNA和蛋白表达明显增加,纤连蛋白在海人酸损失3 d后的表达也增加,提示结缔组织生长因子在海马损伤修复中可能参与胶质瘢痕的形成。有趣的是,借助直接脑损伤或海人酸兴奋性毒性损伤模型,在损伤后以及随后的神经元死亡、胶质增生和瘢痕组织形成期间,HEUER等[14]并未观察到结缔组织生长因子mRNA表达上调,这提示需要在结缔组织生长因子敲除鼠中去进一步研究,发现结缔组织生长因子可能具有其他的潜在功能。考虑到结缔组织生长因子全敲除小鼠会由于骨骼缺陷在出生后数分钟内出现呼吸衰竭[15],存在围产期纯合致死的情况,后续的研究对象应选择条件性敲除结缔组织生长因子的转基因小鼠。 纤维化过程中影响结缔组织生长因子表达量的分子很多,例如OU等[16]在肺上皮细胞中的研究表明,转化生长因子β可激活细胞外信号调节激酶、去整合素金属蛋白酶17、CCAAT/增强子结合蛋白β和核糖体激酶1信号通路,从而诱导结缔组织生长因子的表达;转化生长因子β可增加CCAAT/增强子结合蛋白β向结缔组织生长因子启动子的募集,也增加上皮间质转化标志物——纤维连接蛋白和结缔组织生长因子的表达水平;使用siRNA或者抑制剂干扰上述相应的信号通路,均可减弱转化生长因子β诱导的结缔组织生长因子表达。亦有研究表明,结缔组织生长因子和转化生长因子β的相互作用主要通过von Willebrand 因子C型结构域来实现,结缔组织生长因子可与转化生长因子β结合并作为分子伴侣保护转化生长因子β及其受体[17]。以上研究均提供了直接证据表明转化生长因子β是结缔组织生长因子的上游分子,转化生长因子β可以通过多种信号通路促进结缔组织生长因子及其下游相关生物学功能。此外,结缔组织生长因子能增强转化生长因子β的促纤维化功能,特别是促进成纤维细胞增殖和分泌细胞外基质蛋白;增强的转化生长因子β反过来诱导结缔组织生长因子的高表达,形成正反馈效应参与纤维化过程[17-18]。LI等[19]在坐骨神经压迫损伤模型大鼠3周后观察到,与对侧相比,同侧背根神经节神经元和周围组织中转化生长因子β1/结缔组织生长因子及Ⅰ型胶原的mRNA和蛋白表达增加,周围组织中胶原纤维积聚;损伤8周后可观察到,同侧背根神经节周围组织中胶原纤维过度形成,同侧肌肉萎缩。以上为病理条件下转化生长因子β介导结缔组织生长因子参与纤维化,导致细胞外基质积累提供了证据。 2.1.2 结缔组织生长因子与细胞黏附 结缔组织生长因子可依靠半胱氨酸结构域与纤维连接蛋白作用,促进细胞的黏附和迁移[20]。结缔组织生长因子与细胞黏附介导的耐药性密切相关[21]。既往报道称,血清结缔组织生长因子水平高的肝癌患者生存率降低[22],且有学者观察到结缔组织生长因子的表达量与胶质瘤的分级和耐药有关,胶质瘤细胞在化疗药物处理后激活上游的转化生长因子β信号通路,促进结缔组织生长因子的上调[23]。前文中提到的结缔组织生长因子和转化生长因子β的相互作用可能参与增强了胶质瘤细胞之间的黏附作用,从而提升了其耐药性,干预这种相互作用能否影响细胞黏附状况亟待研究。此外,有人利用肝癌细胞球培养模型,在肝癌细胞内观察到结缔组织生长因子可调节细胞黏附介导的耐药性,且该过程不依赖转化生长因子β信号通路,而是通过诱导Ⅰ型胶原A1来实现的[24]。敲除Ⅰ型胶原A1可以减少细胞之间的黏附性,从而改善抗癌治疗的效果;使用siRNA干扰结缔组织生长因子的表达也可以降低Ⅰ型胶原A1的表达,从而降低细胞间的黏附性[25]。这两种不同的信号通路均提示结缔组织生长因子在抗癌治疗中存在不利影响,改善结缔组织生长因子相关通路的功能,可以降低细胞间的黏附作用,增强药物疗效,为患者带来更好的预后。血管紧张素Ⅱ可通过与转化生长因子β无关的Smad信号通路直接诱导结缔组织生长因子和Ⅰ型胶原A1的表达[24]。使用血管紧张素抑制剂氯沙坦可在抑制Ⅰ型胶原A1合成的同时,减弱细胞间相互作用,从而提高抗癌药物在该细胞模型的疗效[24-25]。Ⅰ型胶原A1和结缔组织生长因子/转化生长因子β之间相互作用均可以作为改善抗癌药耐药性的靶点和干预方向,进一步阐明结缔组织生长因子与细胞黏附相关的机制,分析结缔组织生长因子在不同信号通路中的作用和不同信号通路之间的相互影响,对于改善神经系统肿瘤患者的预后有推动作用。 2.1.3 结缔组织生长因子与细胞发育 结缔组织生长因子通过转化生长因子β参与细胞的发育过程。转化生长因子β是一类调节细胞生长和分化的转录因子,其不仅可以促进纤维化,还在细胞发育中发挥作用[26],其中具有转录因子功能的Smad分子尤为重要[27]。除了转化生长因子β信号通路之外,结缔组织生长因子与其他分子通路也有相互作用。骨形态发生蛋白是一类在软骨或神经发生中发挥重要作用的蛋白[28-29]。结缔组织生长因子可通过胶质源性转化生长因子促进嗅球新生神经元发生Smad依赖的凋亡[30]。MUROMACHI等[31]在牙齿中也观察到结缔组织生长因子与骨形态发生蛋白1存在相互作用,结缔组织生长因子的表达受骨形态发生蛋白1的调节,推测骨形态发生蛋白1可不依赖转化生长因子β的激活直接上调结缔组织生长因子的表达。MUNDY等[32]观察到,结缔组织生长因子在骨关节发生过程中持续过表达可导致骨形态发生蛋白2未刺激组和骨形态发生蛋白2刺激组培养物中成骨细胞成熟,还在过表达结缔组织生长因子的培养物中观察到受损成骨细胞的细胞分化伴随着Smad1/5/8磷酸化水平的降低。结缔组织生长因子对骨形态发生蛋白2诱导的信号传导和成骨细胞分化具有负调节作用,该效应与转化生长因子β信号通路对Smad蛋白的影响相反。有研究表明,结缔组织生长因子与骨形态发生蛋白的相互作用通过von Willebrand 因子C型结构域实现,其他结构域(如半胱氨酸结构域)在细胞增殖发育中也发挥作用[33]。 2.2 结缔组织生长因子在神经系统的功能及在其疾病中的作用 2.2.1 结缔组织生长因子在神经系统的分布 KONDO等[34]首次使用免疫组织化学染色观察到结缔组织生长因子蛋白阳性信号分布于神经元和星形胶质细胞。HEUER等[14]首次通过原位杂交技术观察到结缔组织生长因子mRNA强阳性信号主要分布于大脑皮质Ⅵb层(皮质下板)、内梨形背侧核(dorsal endopiriform nucleus,DEPN)以及嗅球和副嗅核的深部,在外侧嗅束核中呈中等强度,而在前脑、中脑和脑干的其他部位仅显示出极低水平的表达。SIOW等[35]在正常小鼠脑中观察到结缔组织生长因子的表达集中在嗅球、大脑皮质Ⅵb层、背侧屏状核和DEPN,但在腹侧屏状核和腹侧梨状核中未观察到结缔组织生长因子的表达。LI等[19]使用免疫荧光组织化学染色技术在大鼠L4-L6节段的背根神经节中观察到结缔组织生长因子阳性的神经元,提示结缔组织生长因子在周围神经系统和运动系统中均有分布(表1)。"


在一些经典的转基因动物疾病模型中,MANN等[36]在hAPP-J20和Tg2576两种经典阿尔茨海默症模型转基因小鼠的海马和皮质中均观察到结缔组织生长因子高度表达,与阿尔茨海默症患者脑中结缔组织生长因子表达趋势一致。GONZALEZ等[37]在经典肌萎缩侧索硬化症模型hSOD1G93A转基因小鼠中观察到结缔组织生长因子蛋白在脊髓背角和肌肉中大量分布,在脊髓前角有少量分布,结缔组织生长因子分别与神经元标志物和星形胶质细胞标志物双标。这和既往有学者观察到结缔组织生长因子在肌萎缩侧索硬化症患者去世后脊髓内的运动神经元和星形胶质细胞中上调的趋势一致[38](表1)。 2.2.2 结缔组织生长因子在神经发育中的作用 YU等[39]使用条件性缔组织生长因子敲除小鼠,特异性敲除了前脑Ⅵb层兴奋性神经元中缔组织生长因子的表达,观察到Ⅵb层内神经元的密度增高,提示缔组织生长因子在调节局部神经元密度方面具有自分泌或旁分泌功能;同正常小鼠相比,条件性敲除结缔组织生长因子可引起Ⅵb层神经元的树突分支复杂程度降低,但不影响树突生长和树突棘密度,提示结缔组织生长因子在调节树突分支中具有特殊作用。此外,YU等[39]观察到条件性敲除结缔组织生长因子可引起与Ⅵb层相邻的外囊中成熟少突胶质细胞密度增高,但不影响相隔较远的前联合中少突胶质细胞的密度,提示Ⅵb层神经元分泌的结缔组织生长因子具有抑制附近白质内少突胶质细胞成熟的旁分泌功能。这些结果与其他学者观察到的结缔组织生长因子对少突胶质细胞的成熟具有抑制作用一致[40]。 KHODOSEVICH等[30]观察到在嗅球中结缔组织生长因子阳性细胞主要为胆囊收缩素阳性的簇状神经元,在出生后早期阶段,其在僧帽细胞层的表达逐渐下降,但在小球层的表达逐渐增强并持续到成年阶段,提示结缔组织生长因子在嗅球发育中发挥作用。他们认为外界嗅觉刺激可增强结缔组织生长因子的表达,从而导致转化生长因子β2信号的活性依赖性增强,结缔组织生长因子可作为一种促凋亡因子,通过转化生长因子β2信号通路促进小球层新生的球旁中间神经元凋亡,进而影响了兴奋/抑制平衡和嗅球的功能。 OHKAWARA等[41]指出,结缔组织生长因子是脂蛋白相关受体4在神经肌肉接头中的结合伴侣,可增强突触后运动终板乙酰胆碱受体簇形成中的作用。此外,结缔组织生长因子对于突触前神经末梢突触囊泡的成熟和功能亦具有作用。在小鼠胚胎上敲除结缔组织生长因子,可影响乙酰胆碱受体簇的聚集和突触前囊泡的分布异常,进而引起突触前运动终末的活性区减少和减弱神经肌肉接头的信号传递[41]。这些结果提示,结缔组织生长因子对于神经肌肉接头的成熟至关重要。结缔组织生长因子在不同种类和不同时期的神经元中扮演着不同的角色,其作用复杂多样,阐明结缔组织生长因子在各种阶段不同种类的神经元中发挥的功能,对于进一步研究其在神经系统疾病中的作用有重要意义。 2.2.3 结缔组织生长因子在神经退行性疾病中的作用 既往研究观察到,结缔组织生长因子在肌萎缩侧索硬化症患者的脊髓和阿尔茨海默症患者与老年斑相关的神经元中表达上调[38,42]。GONZALEZ等[37]在16周龄hSOD1G93A小鼠中观察到,该转基因小鼠脊髓和肌肉中结缔组织生长因子的mRNA和蛋白水平同野生型小鼠相比均上调,运动能力降低,腹腔注射单克隆抗体FG-3019中和结缔组织生长因子后可显著改善该转基因小鼠的运动能力,提示结缔组织生长因子可能是改善肌萎缩侧索硬化症患者症状、提高生活质量的新靶点。MCCLAIN等[43]观察到结缔组织生长因子和基质金属蛋白酶3参与脂多糖模型诱导的多巴胺神经元变性,将脂多糖注入大鼠黑质诱导多巴胺能神经元变性,很好地模拟了帕金森病的发病过程;动物造模24 h后可观察到结缔组织生长因子与基质金属蛋白酶3表达显著升高,提示结缔组织生长因子可能参与了神经炎症诱导的多巴胺能神经毒性。目前认为小胶质细胞来源的炎性因子是促进多巴胺能神经元病变的维持因素[44-45],也有证据表明,结缔组织生长因子能与基质金属蛋白酶类分子结合,在阿尔茨海默症中介导淀粉样蛋白的降解,从而发挥神经保护作用[46]。基质金属蛋白酶类分子的上调和激活是神经炎症的一个重要特征,所以推测结缔组织生长因子发挥神经保护作用,降低神经炎症反应的机制之一是通过结合基质金属蛋白酶干扰基质金属蛋白酶下游分子的信号通路,从而抑制炎症因子如活性氧和肿瘤坏死因子的释放。 MANN等[36]在两种阿尔茨海默症转基因小鼠中鉴定出一种缩写为“DAG”的环肽,其完整序列为CDAGRKQKC,结缔组织生长因子是DAG肽的作用靶点,他们观察到DAG肽可以选择性识别阿尔茨海默症小鼠海马的星形胶质细胞和其他模型中神经炎症激活的星形胶质细胞,并积聚在星形胶质细胞周围,由此推测DAG肽可以作为阿尔茨海默症和其他神经系统疾病的治疗工具,如在胶质母细胞瘤、外伤性脑损伤和帕金森病的小鼠模型中,机体可以将外源性DAG肽转运到大脑,从而达到更好的治疗效果。但这种干预手段背后的分子机制尚不清楚,仍需进一步研究。 2.2.4 结缔组织生长因子在抑郁症和癫痫中的研究 在抑郁症患者去世后的脑内,TURNER等[47]观察到杏仁核中结缔组织生长因子的表达明显增高,同时在具有焦虑与抑郁样行为的大鼠中观察到齿状回结缔组织生长因子的表达也明显上调;社交挫败应激可显著增加齿状回结缔组织生长因子的表达,而借助成纤维细胞生长因子2缓解焦虑样行为可减少齿状回结缔组织生长因子的表达,从而提出结缔组织生长因子可能在海马和杏仁核中执行相似的功能,是新型的抗抑郁分子靶点。TURNER等[47]使用单克隆抗体FG-3019中和结缔组织生长因子后也观察到大鼠的抑郁行为减少,提示降低结缔组织生长因子的表达可以发挥抗焦虑和抑郁作用。PEI等[48]在抑郁症大鼠海马中观察到结缔组织生长因子高表达,升高miR-133b和抑制结缔组织生长因子的表达都可以抑制神经元凋亡、抑制炎症反应,从而对抑郁大鼠的神经损伤产生保护作用。 SIOW等[35]通过腹腔注射戊四唑的方式诱导癫痫模型,首次观察到在前脑结构中特异性敲除结缔组织生长因子对小鼠的癫痫严重程度和死亡潜伏期没有明显影响,但敲除小鼠出现癫痫发作延迟和海马的c-fos表达降低,星形胶质细胞和小胶质细胞的密度保持不变,但小胶质细胞的活性降低,从而提出抑制结缔组织生长因子功能可能在预防癫痫的发病方面具有治疗潜力。DEPN是导致癫痫的重要核团,结缔组织生长因子也在DEPN高表达[35],揭示结缔组织生长因子与DEPN内相关的神经通路有密切关系,阐明结缔组织生长因子发挥作用的神经机制可能为未来的临床试验和药物开发指明方向。抑郁症和癫痫通常能相互影响[49],抑郁症是癫痫中最常见的并发症[50]。因此,阐明结缔组织生长因子是否参与抑郁症与癫痫的相互影响,对防止癫痫进一步恶化具有重要的指导意义。 2.2.5 结缔组织生长因子在未来研究的指导思路 结缔组织生长因子和转化生长因子β的相互作用可以作为治疗纤维化的一个切入点和研究方向,是否可以利用已知针对结缔组织生长因子的单抗调控结缔组织生长因子和转化生长因子β的这种相互作用,从而改善机体的病理活动是目前亟待解决的科学问题。与此同时,转化生长因子β涉及的分子通路种类繁多,发现更多诱导结缔组织生长因子表达的分子通路也可以为逆转纤维化提供方向。对于同一个模型下蛋白和mRNA表达量不同的实验结果,结合基因敲除的实际情况,提示可以用目前常见的条件性敲除体系,如Cre-Loxp体系,结合重组腺病毒的脑立体定位注射技术和常见疾病动物模型中结缔组织生长因子的表达趋势,特异性敲除或过表达特定脑区的结缔组织生长因子,对于研究正常情况和疾病模型下结缔组织生长因子参与的分子机制具有非常重要的意义。该研究思路亦可用于研究Ⅰ型胶原A1和结缔组织生长因子/转化生长因子β之间相互作用,进一步阐明结缔组织生长因子与Ⅰ型胶原A1互作的机制,分析干预结缔组织生长因子表达之后产生的影响,可以进一步补充结缔组织生长因子参与各类生物学活动的分子机制。结合结缔组织生长因子参与的分子机制和在各类神经系统疾病中的表达变化,可以:①干预结缔组织生长因子的表达观察对各类神经细胞发育的影响,从而进一步揭示结缔组织生长因子在神经细胞生长发育中的角色,为解决神经生长发育类疾病提供思路。②结缔组织生长因子在3种经典神经退行性疾病中病变部位的表达均为上调,结缔组织生长因子是如何在神经炎症中发挥保护作用的机制目前尚不清楚,可以进一步研究。此外,病变过程中结缔组织生长因子是否参与了其他的生物学功能,从而导致了疾病的恶化也是需要解答的问题。③神经退行性疾病中结缔组织生长因子上调表现出神经保护功能,但个体抑郁和癫痫状态下,结缔组织生长因子在相关脑区如海马、DEPN中上调,后续降低其表达后焦虑抑郁症状消失。同样都是上调的表达趋势但表现出对个体不同的影响,提示结缔组织生长因子的作用多样,不能一概而论,需要更多的研究来阐明其参与的功能。④目前新型的治疗工具和诊疗手段在不断发展,如DAG肽,一方面可以根据DAG肽在结缔组织生长因子高表达脑区的附着程度诊断相关疾病,另一方面使用这种外源性多肽可以结合相关药物,将药物精准投递到结缔组织生长因子表达高的部位。未来可以增加该肽的特异性,使它能够特异性地结合脑区特定类型的神经细胞,便可从另一角度观察对结缔组织生长因子发挥功能的影响,这对于开发新型药物和诊疗手段具有前瞻性作用。"

| [1] GONZALEZ D, BRANDAN E. CTGF/CCN2 from Skeletal Muscle to Nervous System: Impact on Neurodegenerative Diseases. Mol Neurobiol. 2019; 56(8):5911-5916. [2] SUN C, ZHANG H, LIU X. Emerging role of CCN family proteins in fibrosis. J Cell Physiol. 2021;236(6):4195-4206. [3] SHEN YW, ZHOU YD, CHEN HZ, et al. Targeting CTGF in Cancer: An Emerging Therapeutic Opportunity. Trends Cancer. 2021;7(6):511-524. [4] CHEN Z, ZHANG N, CHU HY, et al. Connective Tissue Growth Factor: From Molecular Understandings to Drug Discovery. Front Cell Dev Biol. 2020;8: 593269. [5] ZAYKOV V, CHAQOUR B. The CCN2/CTGF interactome: an approach to understanding the versatility of CCN2/CTGF molecular activities. J Cell Commun Signal. 2021;15(4):567-580. [6] BARBOSA R, ACEVEDO LA, MARMORSTEIN R. The MEK/ERK Network as a Therapeutic Target in Human Cancer. Mol Cancer Res. 2021;19(3):361-374. [7] LEASK A. CCN2 in Skin Fibrosis. Methods Mol Biol. 2017;1489:417-421. [8] MOUSSAD EE, BRIGSTOCK DR. Connective tissue growth factor: what’s in a name? Mol Genet Metab. 2000;71(1-2):276-292. [9] VALLE-TENNEY R, REBOLLEDO DL, LIPSON KE, et al. Role of hypoxia in skeletal muscle fibrosis: Synergism between hypoxia and TGF-β signaling upregulates CCN2/CTGF expression specifically in muscle fibers. Matrix Biol. 2020;87:48-65. [10] BARBE MF, HILLIARD BA, AMIN M, et al. Blocking CTGF/CCN2 reverses neural fibrosis and sensorimotor declines in a rat model of overuse-induced median mononeuropathy. J Orthop Res. 2020;38(11):2396-2408. [11] FRAZIER K, WILLIAMS S, KOTHAPALLI D, et al. Stimulation of fibroblast cell growth, matrix production, and granulation tissue formation by connective tissue growth factor. J Invest Dermatol. 1996;107(3):404-411. [12] STICHEL CC, MüLLER HW. The CNS lesion scar: new vistas on an old regeneration barrier. Cell Tissue Res. 1998;294(1):1-9. [13] HERTEL M, TRETTER Y, ALZHEIMER C, et al. Connective tissue growth factor: a novel player in tissue reorganization after brain injury? Eur J Neurosci. 2000;12(1):376-380. [14] HEUER H, CHRIST S, FRIEDRICHSEN S, et al. Connective tissue growth factor: a novel marker of layer VII neurons in the rat cerebral cortex. Neuroscience. 2003;119(1):43-52. [15] IVKOVIC S, YOON BS, POPOFF SN, et al. Connective tissue growth factor coordinates chondrogenesis and angiogenesis during skeletal development. Development. 2003;130(12):2779-2791. [16] OU SC, BAI KJ, CHENG WH, et al. TGF-β Induced CTGF Expression in Human Lung Epithelial Cells through ERK, ADAM17, RSK1, and C/EBPβ Pathways. Int J Mol Sci. 2020;21(23):9084. [17] ABREU JG, KETPURA NI, REVERSADE B, et al. Connective-tissue growth factor (CTGF) modulates cell signalling by BMP and TGF-beta. Nat Cell Biol. 2002;4(8): 599-604. [18] BRIGSTOCK DR. Connective tissue growth factor (CCN2, CTGF) and organ fibrosis: lessons from transgenic animals. J Cell Commun Signal. 2010;4(1): 1-4. [19] LI Q, CHEN J, CHEN Y, et al. Chronic sciatic nerve compression induces fibrosis in dorsal root ganglia. Mol Med Rep. 2016;13(3):2393-2400. [20] PI L, DING X, JORGENSEN M, et al. Connective tissue growth factor with a novel fibronectin binding site promotes cell adhesion and migration during rat oval cell activation. Hepatology. 2008;47(3):996-1004. [21] HUANG Y, WANG Y, TANG J, et al. CAM-DR: Mechanisms, Roles and Clinical Application in Tumors. Front Cell Dev Biol. 2021;9:698047. [22] WANG GB, ZHOU XY, YUAN T, et al. Significance of serum connective tissue growth factor in patients with hepatocellular carcinoma and relationship with angiogenesis. World J Surg. 2010;34(10):2411-2417. [23] ZENG H, YANG Z, XU N, et al. Connective tissue growth factor promotes temozolomide resistance in glioblastoma through TGF-β1-dependent activation of Smad/ERK signaling. Cell Death Dis. 2017;8(6):e2885. [24] SONG Y, KIM JS, CHOI EK, et al. TGF-β-independent CTGF induction regulates cell adhesion mediated drug resistance by increasing collagen I in HCC. Oncotarget. 2017;8(13):21650-21662. [25] CHAUHAN VP, MARTIN JD, LIU H, et al. Angiotensin inhibition enhances drug delivery and potentiates chemotherapy by decompressing tumour blood vessels. Nat Commun. 2013;4:2516. [26] ROMÃO LF, MENDES FA, FEITOSA NM, et al. Connective tissue growth factor (CTGF/CCN2) is negatively regulated during neuron-glioblastoma interaction. PLoS One. 2013;8(1):e55605. [27] KINASHI H, ITO Y, SUN T, et al. Roles of the TGF-β⁻VEGF-C Pathway in Fibrosis-Related Lymphangiogenesis. Int J Mol Sci. 2018;19(9):48-65. [28] JOVANOVIC VM, SALTI A, TILLEMAN H, et al. BMP/SMAD Pathway Promotes Neurogenesis of Midbrain Dopaminergic Neurons In Vivo and in Human Induced Pluripotent and Neural Stem Cells. J Neurosci. 2018;38(7):1662-1676. [29] LOWERY JW, ROSEN V. The BMP Pathway and Its Inhibitors in the Skeleton. Physiol Rev. 2018;98(4):2431-2452. [30] KHODOSEVICH K, LAZARINI F, VON ENGELHARDT J, et al. Connective tissue growth factor regulates interneuron survival and information processing in the olfactory bulb. Neuron. 2013;79(6):1136-1151. [31] MUROMACHI K, KAMIO N, MATSUKI-FUKUSHIMA M, et al. CCN2/CTGF expression via cellular uptake of BMP-1 is associated with reparative dentinogenesis. Oral Dis. 2015;21(6):778-784. [32] MUNDY C, GANNON M, POPOFF SN. Connective tissue growth factor (CTGF/CCN2) negatively regulates BMP-2 induced osteoblast differentiation and signaling. J Cell Physiol. 2014;229(5):672-681. [33] XU R, ZHANG Z, TOFTDAL MS, et al. Synchronous delivery of hydroxyapatite and connective tissue growth factor derived osteoinductive peptide enhanced osteogenesis. J Control Release. 2019;301:129-139. [34] KONDO Y, NAKANISHI T, TAKIGAWA M, et al. Immunohistochemical localization of connective tissue growth factor in the rat central nervous system. Brain Res. 1999;834(1-2):146-151. [35] SIOW PF, TSAO CY, CHANG HC, et al. Mice Lacking Connective Tissue Growth Factor in the Forebrain Exhibit Delayed Seizure Response, Reduced C-Fos Expression and Different Microglial Phenotype Following Acute PTZ Injection. Int J Mol Sci. 2020;21(14):4921. [36] MANN AP, SCODELLER P, HUSSAIN S, et al. Identification of a peptide recognizing cerebrovascular changes in mouse models of Alzheimer’s disease. Nat Commun. 2017;8(1):1403. [37] GONZALEZ D, REBOLLEDO DL, CORREA LM, et al. The inhibition of CTGF/CCN2 activity improves muscle and locomotor function in a murine ALS model. Human Mol Genet. 2018;27(16):2913-2926. [38] SPLIET WG, ARONICA E, RAMKEMA M, et al. Increased expression of connective tissue growth factor in amyotrophic lateral sclerosis human spinal cord. Acta Neuropathol. 2003;106(5):449-457. [39] YU IS, CHANG HC, CHEN KC, et al. Genetic Elimination of Connective Tissue Growth Factor in the Forebrain Affects Subplate Neurons in the Cortex and Oligodendrocytes in the Underlying White Matter. Front Neuroanat. 2019;13:16. [40] STRITT C, STERN S, HARTING K, et al. Paracrine control of oligodendrocyte differentiation by SRF-directed neuronal gene expression. Nat Neurosci. 2009; 12(4):418-427. [41] OHKAWARA B, KOBAYAKAWA A, KANBARA S, et al. CTGF/CCN2 facilitates LRP4-mediated formation of the embryonic neuromuscular junction. EMBO Rep. 2020;21(8):e48462. [42] UEBERHAM U, UEBERHAM E, GRUSCHKA H, et al. Connective tissue growth factor in Alzheimer’s disease. Neuroscience. 2003;116(1):1-6. [43] MCCLAIN JA, PHILLIPS LL, FILLMORE HL. Increased MMP-3 and CTGF expression during lipopolysaccharide-induced dopaminergic neurodegeneration. Neurosci Lett. 2009;460(1):27-31. [44] BLOCK ML, HONG JS. Chronic microglial activation and progressive dopaminergic neurotoxicity. Biochem Soc Trans. 2007;35(Pt 5):1127-1132. [45] DUTTA G, ZHANG P, LIU B. The lipopolysaccharide Parkinson’s disease animal model: mechanistic studies and drug discovery. Fundam Clin Pharmacol. 2008; 22(5):453-464. [46] YANG CN, WU MF, LIU CC, et al. Differential protective effects of connective tissue growth factor against Aβ neurotoxicity on neurons and glia. Hum Mol Genet. 2017;26(20):3909-3921. [47] TURNER CA, SHARMA V, HAGENAUER MH, et al. Connective Tissue Growth Factor Is a Novel Prodepressant. Biol Psychiatry. 2018;84(8):555-562. [48] PEI G, XU L, HUANG W, et al. The protective role of microRNA-133b in restricting hippocampal neurons apoptosis and inflammatory injury in rats with depression by suppressing CTGF. Int Immunopharmacol. 2020; 78:106076. [49] THIJS RD, SURGES R, O’BRIEN TJ, et al. Epilepsy in adults. Lancet. 2019;393(10172):689-701. [50] GILLIAM FG, BLACK KJ, CARTER J, et al. A Trial of Sertraline or Cognitive Behavior Therapy for Depression in Epilepsy. Ann Neurol. 2019;86(4):552-560. [51] RICHELDI L, FERNáNDEZ PéREZ ER, COSTABEL U, et al. Pamrevlumab, an anti-connective tissue growth factor therapy, for idiopathic pulmonary fibrosis (PRAISE): a phase 2, randomised, double-blind, placebo-controlled trial. Lancet Respir Med. 2020;8(1):25-33. |
| [1] | Zhang Kefan, Shi Hui. Research status and application prospect of cytokine therapy for osteoarthritis [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(6): 961-967. |
| [2] | Zhang Ming, Wang Bin, Jia Fan, Chen Jie, Tang Wei. Application of brain-computer interface technology based on electroencephalogram in upper limb motor function rehabilitation of stroke patients [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(4): 581-586. |
| [3] | He Yuanjie, Chen Yuheng, Zhao Yongchao, Wang Zhenglong. Progress in epigenetic regulation of vascular smooth muscle cell remodeling in the occurrence and development of aortic aneurysms [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(4): 602-608. |
| [4] | Yan Binghan, Li Zhichao, Su Hui, Xue Haipeng, Xu Zhanwang, Tan Guoqing. Mechanisms of traditional Chinese medicine monomers in the treatment of osteoarthritis by targeting autophagy [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(4): 627-632. |
| [5] | Wang Xinyi, Xie Xianrui, Chen Yujie, Wang Xiaoyu, Xu Xiaoqing, Shen Yihong, Mo Xiumei. Electrospun nanofiber scaffolds for soft and hard tissue regeneration [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(3): 426-432. |
| [6] | Long Jundong, Shi Yehong, Wang Cheng, Chen Shijiu. Effects of different freezing techniques on the rejection of allogeneic vascular transplantation [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(3): 433-438. |
| [7] | Yang Jie, Hu Haolei, Li Shuo, Yue Wei, Xu Tao, Li Yi. Application of bio-inks for 3D printing in tissue repair and regenerative medicine [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(3): 445-451. |
| [8] | Qi Ming, Wang Lei, Zhang Zhen. CXCL5 participates in carotid plaque formation by inducing vascular calcification [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(2): 186-192. |
| [9] | Dai Xinyu, Yan Jihong, Hua Lingjun, Zheng Xiaohong. Resistance exercise improves body composition in overweight and obese people: an umbrella review [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(2): 267-271. |
| [10] | Meng Zhicheng, Qiao Weiping, Zhao Yang, Liu Hongfei, Li Kaijie, Ma Bo. Effects of immune cells and related cytokines in the pathogenesis and treatment of osteoarthritis [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(2): 280-287. |
| [11] | Long Yi, Yang Jiaming, Ye Hua, Zhong Yanbiao, Wang Maoyuan. Extracellular vesicles in sarcopenic obesity: roles and mechanisms [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(2): 315-320. |
| [12] | Chang Wanpeng, Zhang Zhongwen, Yang Yulin, Zi Yang, Yang Mengqi, Du Bingyu, Wang Nan, Yu Shaohong. Efficacy of rehabilitation exoskeleton robots on post-stroke lower limb motor dysfunction: a Meta-analysis [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(2): 321-328. |
| [13] | Long Qingxi, Zhang Pingshu, Liu Qing, Ou Ya, Zhang Lili, Yuan Xiaodong. Single-cell RNA sequencing reveals the heterogeneity of astrocytes [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(1): 139-146. |
| [14] | Nong Fuxiang, Jiang Zhixiong, Li Yinghao, Xu Wencong, Shi Zhilan, Luo Hui, Zhang Qinglang, Zhong Shuang, Tang Meiwen. Bone cement augmented proximal femoral nail antirotation for type A3.3 intertrochanteric femoral fracturalysis [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(在线): 1-10. |
| [15] | Pan Zhongjie, Qin Zhihong, Zheng Tiejun, Ding Xiaofei, Liao Shijie. Targeting of non-coding RNAs in the pathogenesis of the osteonecrosis of the femoral head [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(9): 1441-1447. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||