Chinese Journal of Tissue Engineering Research ›› 2024, Vol. 28 ›› Issue (4): 627-632.doi: 10.12307/2023.950
Previous Articles Next Articles
Mechanisms of traditional Chinese medicine monomers in the treatment of osteoarthritis by targeting autophagy
Yan Binghan1, Li Zhichao1, Su Hui1, Xue Haipeng2, Xu Zhanwang2, Tan Guoqing2
- 1Shandong University of Traditional Chinese Medicine, Jinan 250014, Shandong Province, China; 2Affiliated Hospital of Shandong University of Traditional Chinese Medicine, Jinan 250014, Shandong Province, China
-
Received:2023-01-04Accepted:2023-02-10Online:2024-02-08Published:2023-07-14 -
Contact:Tan Guoqing, MD, Associate chief physician, Affiliated Hospital of Shandong University of Traditional Chinese Medicine, Jinan 250014, Shandong Province, China -
About author:Yan Binghan, Master candidate, Shandong University of Traditional Chinese Medicine, Jinan 250014, Shandong Province, China -
Supported by:National Natural Science Foundation of China (General Program), No. 82174410 (to XZW); Natural Science Foundation of Shandong Province, No. ZR2020KH011 (to XZW); Natural Science Foundation of Shandong Province (General Program), No. ZR2020MH362 (to TGQ); National Famous Old Chinese Medicine Experts Inheritance Studio Construction Project, No. [2022]75 (to XZW)
CLC Number:
Cite this article
Yan Binghan, Li Zhichao, Su Hui, Xue Haipeng, Xu Zhanwang, Tan Guoqing. Mechanisms of traditional Chinese medicine monomers in the treatment of osteoarthritis by targeting autophagy[J]. Chinese Journal of Tissue Engineering Research, 2024, 28(4): 627-632.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
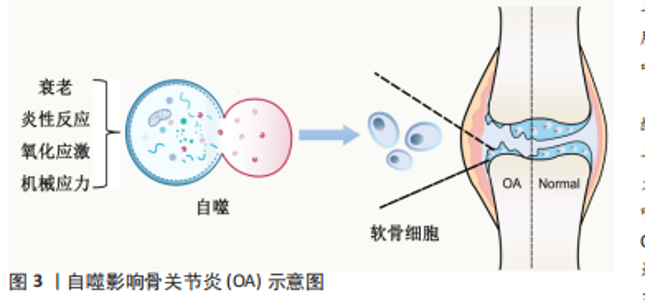
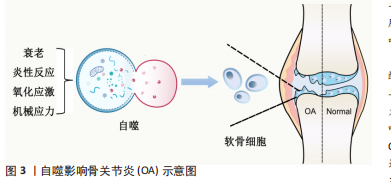
2.1 自噬与骨关节炎 自噬是一种细胞内的降解系统,通过溶酶体介导的自噬去除错误折叠的蛋白质、受损的细胞器和大分子,合成新的蛋白质,为细胞重建、再生和修复提供必要的原料,从而维持细胞的动态平衡。自噬的过程大致可以分为自噬启动、自噬小体的形成、延伸、成熟,自噬体-溶酶体的融合和降解。多种信号通路和分子参与调节自噬[10]。参与自噬的主要介质包括自噬相关蛋白(autophagy-related protein,Atg)、自噬效应蛋白(Beclin-1)、微管相关蛋白轻链3(microtubule-associated protein 1 light chain 3,LC3)。当自噬发生时,Beclin-1、LC3-Ⅱ的表达上升,自噬底物受体蛋白P62的表达下降。 自噬能够降解和清除长寿以及受损细胞器和蛋白质,随着年龄的增长自噬的水平也会随之下降,自噬与衰老性疾病密切相关。衰老已被证实与骨关节炎之间在临床和流行病学上存在一定的相关性,组织和细胞再生能力受限,炎性反应增加,氧化应激以及机械应力增加等,都能造成软骨基质和细胞的损伤,进而影响骨关节炎的发生发展[11],见图3。近年来发现骨关节炎的病理表现主要为软骨细胞的凋亡和功能障碍,软骨细胞是软骨中唯一的细胞类型,仅占软骨体积的1%,但其在维持软骨完整性方面有着不可或缺的作用[12]。最近的研究发现,自噬与细胞凋亡也密切相关,在骨关节炎早期阶段,软骨细胞中自噬水平能够保护软骨细胞,使其免于降解,而在后期阶段,自噬与凋亡一起作为软骨细胞死亡的替代途径,并能够诱导衰老的发生。这就表明,与健康人相比,骨关节炎患者的自噬水平是一种适应性的调节,适度的自噬能起到保护作用,当过度自噬时,反而能引起细胞的凋亡或衰老[13]。另一方面,自噬参与软骨的形成,自噬相关基因Atg5和Atg7的缺失会减缓软骨细胞的增殖,加剧软骨细胞的死亡[14],软骨细胞中Atg5的靶向缺失会增加活性氧的产生并促进与年龄相关的骨关节炎[15]。自噬在维持软骨的稳态方面有着不可替代的作用,自噬功能失调往往会导致骨关节炎的发生,激活自噬可以缓解骨关节炎[16]。"
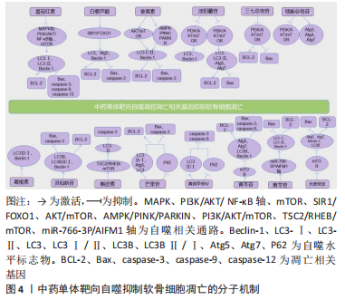
2.2 中药单体靶向自噬治疗骨关节炎 2.2.1 靶向自噬抑制软骨细胞凋亡 细胞凋亡是在发育和衰老过程中的一种程序性死亡,是一种维持组织的稳态机制,也是一种防御机制[17]。软骨细胞自噬与凋亡水平之间的平衡被认为是治疗骨关节炎的有效途径。Sirtuin 1(SirT1)是一种沉默信息调节因子,通过参与调节多种细胞通路进行抗炎、抗衰老、抗凋亡[18],SirT1的表达可能在骨关节炎的发展中对软骨起到保护作用[19],抗氧化酶上游蛋白叉头框转录因子(FOXO1)能够调节软骨细胞的发育、衰老和氧化应激。自噬和凋亡的平衡维持着软骨细胞的正常,白藜芦醇(RES)是中药单体藜芦根部提取的主要有效成分,LIANG等[20]研究发现,白藜芦醇可以通过激活SIRT1/FOXO1信号通路来调节软骨细胞自噬和凋亡的平衡,保护软骨细胞免受白细胞介素1β诱导的损伤,抑制骨关节炎软骨细胞的凋亡。灵仙新苷(C-AR)和葛根素则是可以通过激活自噬相关蛋白来有效降低细胞的死亡数和凋亡率,保护软骨细胞[21-22]。 磷脂酰肌醇3激酶(phosphatidylinositol-3-kinase,PI3K)/蛋白激酶B (protein kinase B,AKT)/哺乳动物雷帕霉素靶蛋白(mammalian target of rapamycin,mTOR)信号通路是自噬过程中的核心信号通路。姜黄素是姜黄根茎中提取的有效活性成分,ZHANG等[23]研究发现,姜黄素可以逆转在衰老过程中AKT/mTOR的激活和LC3、Beclin-1的下调,即姜黄素可以通过抑制AKT/mTOR通路增加自噬,减少软骨基质降解,最终抑制细胞的凋亡。淫羊藿苷(ICA)是从淫羊藿中提取的主要有效成分,TANG等[24]发现淫羊藿苷可以通过抑制PI3K/AKT/mTOR 信号通路激活自噬,以剂量依赖的方式降低软骨细胞的凋亡率,来减轻骨关节炎。相同的结果出现在三七总皂苷和续断总皂苷的研究中,两者均能通过抑制PI3K/AKT/mTOR 信号通路,引起自噬的增加,减少凋亡,抑制软骨细胞的衰老[25-26]。此外,商连斌等[27]还发现续断总皂苷可以上调软骨组织中的Atg3、Atg4、Atg7的表达水平,增加自噬,实现抗凋亡。mTOR通路是自噬的负调节因子,DAI等[28]通过体外和体内实验发现甘草提取物光苷草定可以抑制mTOR的表达来促进自噬,有效降低软骨细胞的凋亡率。有趣的是,王琼等[29]发现黄芩提取物黄芩苷可以通过激活mTOR通路来抑制自噬,抑制软骨细胞凋亡,进而治疗骨关节炎。虽然两项研究证实了光苷草定和黄芩苷都可以通过mTOR通路来影响自噬,但两种中药单体通过mTOR通路对自噬的调节有着截然相反的作用,选择中药单体是激活mTOR通路还是抑制mTOR通路来影响自噬,还需进一步研究。槲皮素(QUE)是金银花、桑寄生等中药中的有效活性成分,LV等[30]研究发现槲皮素可以通过TSC2-RHEB-mTOR信号通路调节骨关节炎细胞的自噬,抑制细胞凋亡。尽管自噬可以起到保护软骨细胞的作用,但相关实验研究的结果确实存在不同的中药单体通过激活或抑制mTOR通路来抑制或促进自噬,这提示不同中药可能引起不同水平的自噬,而不同水平的自噬将导致软骨细胞不同的命运。适度的自噬才能起到保护软骨细胞的作用,然而,目前的研究还未能明确如何通过mTOR信号通路去影响自噬保持在一个最佳的水平。 自噬开始于自噬体的形成,到自噬溶酶体降解和重组,并最终与溶酶体融合[31],即自噬通量。骨关节炎发病过程中,溶酶体活性降低,导致自噬体减少[32],即自噬通量减少,因此增强自噬通量可以被定义为骨关节炎的潜在治疗策略。研究发现异补骨脂和芒果苷均可以增加自噬通量来保护软骨细胞防止凋亡。异补骨脂是补骨脂中提取的成分,CHEN等[33]研究发现异补骨脂素通过降低 LC3-Ⅱ和 SQSTM1/P62的表达增加自噬通量,进一步证实异补骨脂素对白细胞介素1β诱导的细胞凋亡的保护作用(白细胞介素1β处理的软骨细胞与骨关节炎软骨细胞具有很高的相似性[34])。无独有偶,类似的研究结果也出现在了中药黄芪上,黄芪被认为可以治疗自身免疫性疾病,其有效生物成分黄芪甲苷Ⅳ(AST)也可以通过降低 SQSTM1/P62的表达以及增加LC3Ⅱ/Ⅰ表达量来激活自噬,增加软骨细胞的凋亡抵抗性[35]。芒果苷又名知母素,广泛分布于知母、龙胆、石伟等中药中[36],LI等[37]发现芒果苷可以使得LC3Ⅱ/Ⅰ和Atg5的表达增加从而增加自噬体的形成,恢复溶酶体活性,并促使自噬体与溶酶体融合,即增加自噬通量,保护软骨细胞防止凋亡。从目前的研究结果不难发现,在自噬通量方面,大多中药单体通过增加自噬通量来激活自噬进而起到保护软骨细胞、防止软骨细胞凋亡的作用。 丝裂原活化蛋白激酶(mitogen-activated protein kinase,MAPK)是一种重要的促炎症通路[38],与骨关节炎的发病机制有关,PI3K/AKT/核因子κB(Nuclear factor-κB,NF-κB)通路也是软骨细胞凋亡和炎症反应中的重要信号通路。番茄红素(LYC)是中药玫瑰花中的成分,WU等[39]发现番茄红素能够抑制MAPK磷酸化并下调软骨细胞中mTOR的表达,此外番茄红素能破坏PI3K,AKT,NF-κB和mTOR的磷酸化,激活自噬,进而影响到细胞的凋亡,为治疗骨关节炎提供新的治疗策略。腺苷酸活化蛋白激酶(AMP-activated Protein Kinase,AMPK)主要与哺乳动物的蛋白质代谢、脂质代谢、糖类代谢、自噬及线粒体稳态有关,PINK1/Parkin是激活有丝分裂的经典途径。JIN等[40]研究发现姜黄素可以通过激活AMPK/PINK1/Parkin通路激活有丝分裂,保护软骨细胞发挥抗骨关节炎作用。 间充质干细胞可以分化为许多结缔组织,是软骨修复的有力工具[41]。 来源于骨髓的间充质干细胞在治疗软骨缺损方面有较好的疗效,但高凋亡率限制了其临床上长期的疗效。LIU等[42]研究发现缺氧、血糖和血清剥夺(OGD)条件下可以促进骨髓间充质干细胞内质网的自噬,而淫羊藿苷可以通过降低Beclin-1、Atg5和LC3-Ⅱ的表达,增加LC3-Ⅰ和P62的表达来抑制自噬,内质网应激标志物(ERs)水平的降低通过限制细胞凋亡和自噬,增强了淫羊藿苷对氧糖剥夺损伤的保护作用。由此发现淫羊藿苷通过MAPK信号通路抑制内质网应激标志物介导的自噬、抑制氧糖剥夺诱导的兔骨髓间充质干细胞凋亡,为延长骨髓间充质干细胞治疗骨关节炎的疗效提供了新方法。此外,MI等[43]研究发现淫羊藿苷可以通过抑制NF-κB信号传导激活自噬并抑制凋亡。间充质干细胞是再生医学组织工程研究中的研究重点,骨髓间充质干细胞对骨关节炎的治疗作用已被证实[44],目前研究发现几种中药单体能够通过介导自噬来保护骨髓间充质干细胞,从而发挥其软骨修复的作用,为治疗骨关节炎在再生医学方面提供新思路。 miRNAs是一类小的非编码RNA,在转录后调节基因表达,关系着细胞的生长、发育、分化和凋亡[45]。表观遗传学为治疗骨关节炎提供了新视角,黄芩苷是一种主要从中药黄芩中提取的黄酮类化合物,LI等[46]通过研究首次发现黄芩苷可能通过上调 miR-766-3p 从而降低AIFM1的表达,来保护骨关节炎软骨细胞免受白细胞介素1β诱导的细胞凋亡和自噬抑制。目前治疗骨关节炎的药物只是以改善症状为主,要想从根本上解决问题,表观遗传修饰是必经之路,它将作为生物标志物以及疾病诊治的方案的一部分。上述研究已发现中药单体的有效活性成分可以在自噬以及表观遗传层面治疗骨关节炎。 中药单体靶向自噬抑制软骨细胞凋亡的具体分子机制见图4。"
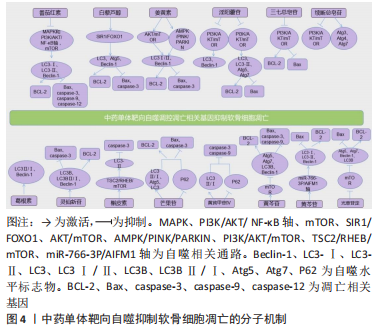
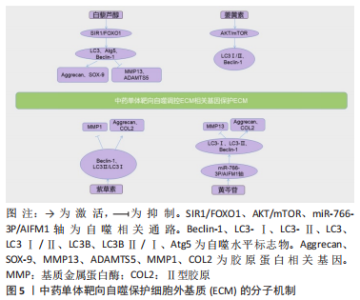
2.2.2 靶向自噬保护细胞外基质 关节软骨主要由细胞外基质和软骨细胞组成[47],细胞外基质主要分布在细胞间表面或者细胞与细胞间,维持着软骨结构的稳定,同时,细胞外基质富含多种信号通路,参与软骨细胞的增殖分化等。骨关节炎发生过程中,细胞外基质分解代谢与合成代谢的动态平衡被打破,代谢的天平倒向了分解代谢,最终导致细胞外基质的分解以及关节软骨的破坏。 LIANG等[48]发现,白藜芦醇可以通过激活SIRT1/FOXO1信号通路来激活软骨细胞自噬,减轻骨关节炎软骨细胞中细胞外基质的降解。ZHANG等[23]研究发现姜黄素能够通过激活AKT/mTOR通路来增加自噬不仅可以防止细胞凋亡,同样也能使细胞外基质降解减少。LI等[46]发现黄芩苷可以调节ACAN、COL2A以及基质金属蛋白酶13水平来保护细胞外基质免受降解。相同的结果也出现在芒果苷的研究上[37]。传统中药紫草中提取的紫草素可以改善骨关节炎细胞模型中的ADAMTS-5、基质金属蛋白酶1以及Ⅱ型胶原,研究发现这些结果的出现是紫草素通过上调自噬相关标基因Beclin-1和LC3Ⅱ/LC3Ⅰ的表达实现的,总的来说,紫草素可以激活自噬促进软骨细胞细胞外基质的合成,从而在缓解骨关节炎方面起到良好的疗效[49]。 细胞外基质的降解是发生骨关节炎的关键因素之一,因此,防止细胞外基质降解对于防止骨关节炎的发生有着至关重要的意义。中药单体通过靶向自噬或是防止细胞外基质降解,或是增加细胞外基质的合成,都能在一定程度上保护软骨细胞,防止骨关节炎的发生。 中药单体靶向自噬保护细胞外基质的具体分子机制见图5。"
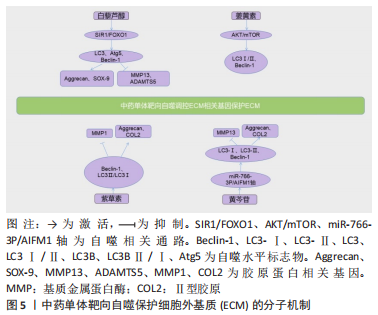
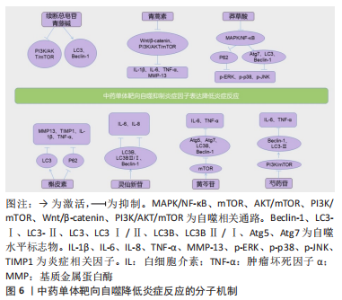
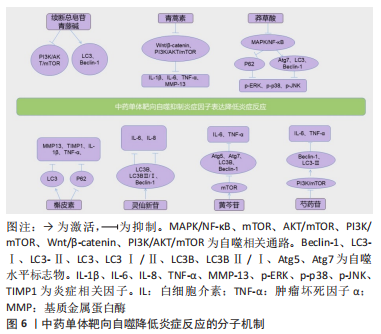
2.2.3 靶向自噬降低炎症反应 衰老的过程中,身体的炎性反应也会增加,骨关节炎的程度进而随之加重,在此过程中,骨组织的炎症途径持续激活。 抑制PI3K/AKT/mTOR信号通路,上调自噬水平,不仅仅能防止软骨细胞凋亡,同样也能够降低炎症反应,研究发现续断总皂苷可以抑制此通路来激活自噬,抗炎、抗凋亡[26]。青藤碱(SIN)是从中药单体青风藤中提取的有效活性成分,郑洁等[50]发现青藤碱可以上调Atg5、Atg12、LC3-Ⅱ和 Beclin-1的表达,抑制PI3K/AKT/mTOR信号通路,从而上调自噬水平。LI等[51]发现著名抗疟药物青蒿素(AT)也可以通过抑制软骨中的PI3K/AKT/mTOR信号传导来激活自噬,减少软骨细胞的炎症反应,从而减轻骨关节炎,与青藤碱不同的是,青蒿素是降低与PI3K/AKT/mTOR 信号通路相关性最显著的一种mRNA——TNFSF11的表达来抑PI3K/AKT/mTOR 信号通路。此外,ZHONG等[52]发现青蒿素同样也可以抑制Wnt/β-catenin信号通路,抑制细胞中促炎性趋化因子和细胞因子(白细胞介素1β,白细胞介素6,肿瘤坏死因子α和基质金属蛋白酶13)的表达发挥抗炎作用。姚旭等[53]研究发现,芍药苷抑制PI3K/AKT信号通路增加软骨细胞的自噬,从而减少炎症因子,抑制炎症反应,治疗骨关节炎。王琼等[29]发现黄芩苷可以激活mTOR通路来抑制细胞炎症反应。NF-κB在炎症反应中发挥着非常关键的作用。MAPK通路的激活有助于软骨细胞外基质中合成代谢和分解代谢失调而引起的软骨降解[54]。MAPK通路可以影响细胞凋亡的机制,而且调节炎症基因的表达[55]。YI等[56]研究发现白藜芦醇可以通过抑制 NF-κB信号通路来减弱炎性反应,但其是否影响自噬途径影响炎性反应还有待研究。莽草酸(SA)是从八角中提取的有效活性成分,YOU等[57]发现莽草酸可以通过抑制MAPK和NF-κB信号通路增加自噬通量,降低炎症反应。 中药单体除了调节与自噬相关的信号通路之外,也可以调节自噬相关蛋白的表达。徐斌等[58]发现槲皮素可以促进自噬活性标志蛋白LC3-Ⅱ的表达,同时抑制P62的过度表达,激活自噬,抑制炎症反应。李纳平等[21]发现灵仙新苷能促进Beclin-1、LC3B的表达,使LC3BⅡ/LC3BⅠ比值升高,促进自噬,抑制细胞炎症。自噬作为机体的一种保护性机制,能在炎症反应的诱导和抑制中发挥作用,不同的中药单体通过调节自噬相关信号通路以及自噬相关蛋白来影响软骨细胞的自噬,从而影响炎症因子或炎症基因的表达,为在降低炎性反应方面治疗骨关节炎提供新的参考方案。 中药单体靶向自噬降低炎症反应的具体分子机制见图6。"
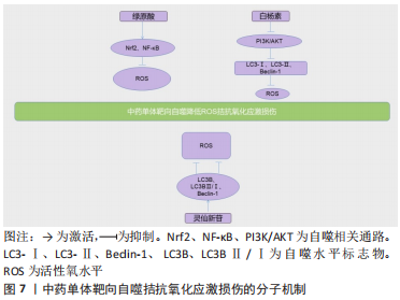
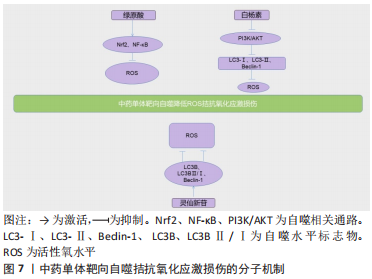
2.2.4 靶向自噬拮抗氧化应激损伤 活性氧与细胞的增殖分化等细胞活动有关,是一把双刃剑,适量的活性氧可以促进细胞的增殖,但其过量的产生会打破细胞内的氧化还原平衡,导致氧化应激[59]。氧化应激与多种骨相关疾病有关,在骨关节炎发病过程中,氧化应激可以促进软骨的退变[60]。 核因子E2相关因子2(Nuclear factor-E2 related factor 2,Nrf2)和 NF-κB信号通路能使活性氧减少,并为氧化应激下的软骨细胞提供保护。绿原酸是中药白术中提取的成分,LEE等[61]研究发现绿原酸通过激活Nrf2和 NF-κB信号通路激活自噬,保护软骨细胞免受氧化应激的损伤。白杨素存在于高良姜、黄芩等中药中,具有抗氧化、抗炎的活性,杨阳等[62]研究发现白杨素可能通过抑制PI3K/AKT信号通路,下调Beclin- 1和LC3-Ⅱ的表达抑制自噬,降低活性氧水平,减轻软骨细胞由于氧化应激的损伤。李纳平等[21]发现灵仙新苷可以明显降低细胞内氧化应激水平,减轻体外培养的膝骨关节炎软骨细胞炎症和氧化应激反应。 活性氧的过量产生和软骨细胞中的氧化应激是骨关节炎发病的主要机制之一[63],上述多种研究已经证明中药多酚能清除活性氧,激活软骨细胞的抗氧化防御系统,并通过抑制促炎症信号通路来抑制炎症,充分利用中药单体靶向自噬以及抗氧化作用,可为临床上治疗骨关节炎提供新的治疗思路。虽然目前关于中药单体靶向自噬拮抗氧化应激方面的研究较少,但值得注意的是,中药单体亦或是激活自噬,亦或是抑制自噬,其机制可能都是为了调节自噬保持在一个适度的水平,都是以降低活性氧水平、减轻软骨细胞的氧化应激损伤为目的,选择中药单体是激活还是抑制自噬来降低活性氧水平似乎是中药单体在临床使用前不可逃避的问题。 中药单体靶向自噬拮抗氧化应激损伤的具体分子机制见图7。"
| [1] MILLERAND M, BERENBAUM F, JACQUES C. Danger signals and inflammaging in osteoarthritis. Clin Exp Rheumatol. 2019;37 Suppl 120(5):48-56. [2] MANDL LA. Osteoarthritis year in review 2018: clinical. Osteoarthritis Cartilage. 2019; 27(3):359-364. [3] DUAN R, XIE H, LIU ZZ. The Role of Autophagy in Osteoarthritis. Front Cell Dev Biol. 2020;8:608388. [4] 贾笛,韦佳佳,段修权,等.基于全球视角的中国骨关节炎疾病负担分析[J].现代预防医学,2022,49(13):2312-2316. [5] 陈倩文,赵继荣,陈祁青,等.中医药靶向miRNA干预骨关节炎研究进展[J].中华中医药学刊,2023,41(5):80-85. [6] LI XZ, ZHANG SN. Recent advance in treatment of osteoarthritis by bioactive components from herbal medicine. Chin Med. 2020;15:80. [7] WANG L, ZHANG XF, ZHANG X, et al. Evaluation of the Therapeutic Effect of Traditional Chinese Medicine on Osteoarthritis: A Systematic Review and Meta-Analysis. Pain Res Manag. 2020;2020:5712187. [8] LI Z, LI D, SU H, et al. Autophagy: An important target for natural products in the treatment of bone metabolic diseases. Front Pharmacol. 2022;13:999017. [9] ARIAS C, SALAZAR LA. Autophagy and Polyphenols in Osteoarthritis: A Focus on Epigenetic Regulation. Int J Mol Sci. 2021;23(1):421. [10] KAO WC, CHEN JC, LIU PC, et al. The Role of Autophagy in Osteoarthritic Cartilage. Biomolecules. 2022;12(10):1357. [11] DUAN R, XIE H, LIU ZZ. The Role of Autophagy in Osteoarthritis. Front Cell Dev Biol. 2020;8:608388. [12] LUO P, GAO F, NIU D, et al. The Role of Autophagy in Chondrocyte Metabolism and Osteoarthritis: A Comprehensive Research Review. Biomed Res Int. 2019;2019:5171602. [13] ARIAS C, SALAZAR LA. Autophagy and Polyphenols in Osteoarthritis: A Focus on Epigenetic Regulation. Int J Mol Sci. 2021;23(1):421. [14] VUPPALAPATI KK, BOUDERLIQUE T, NEWTON PT, et al. Targeted Deletion of Autophagy Genes Atg5 or Atg7 in the Chondrocytes Promotes Caspase-Dependent Cell Death and Leads to Mild Growth Retardation. J Bone Miner Res. 2015;30(12):2249-2261. [15] LÓPEZ DE FIGUEROA P, LOTZ MK, BLANCO FJ, CARAMÉS B. Autophagy activation and protection from mitochondrial dysfunction in human chondrocytes. Arthritis Rheumatol. 2015;67(4):966-976. [16] CASTROGIOVANNI P, RAVALLI S, MUSUMECI G. Apoptosis and Autophagy in the Pathogenesis of Osteoarthritis. J Invest Surg. 2020;33(9):874-875. [17] BERTHELOOT D, LATZ E, FRANKLIN BS. Necroptosis, pyroptosis and apoptosis: an intricate game of cell death. Cell Mol Immunol. 2021;18(5):1106-1121. [18] YANG Y, LIU Y, WANG Y, et al. Regulation of SIRT1 and Its Roles in Inflammation. Front Immunol. 2022;13:831168. [19] DENG Z, LI Y, LIU H, et al. The role of sirtuin 1 and its activator, resveratrol in osteoarthritis. Biosci Rep. 2019;39(5):BSR20190189. [20] LIANG C, XING H, WANG C,et al. Resveratrol protection against IL-1β-induced chondrocyte damage via the SIRT1/FOXO1 signaling pathway. J Orthop Surg Res. 2022; 17(1):406. [21] 李纳平,涂杜鑫,邝高艳,等.灵仙新苷对膝骨关节炎软骨细胞凋亡和自噬的影响[J].中国中医药信息杂志,2023,30(3):96-101. [22] LI G, RAO H, XU W. Puerarin plays a protective role in chondrocytes by activating Beclin1-dependent autophagy.Biosci Biotechnol Biochem. 2021;85(3):621-625. [23] ZHANG G, CAO J, YANG E, et al. Curcumin improves age-related and surgically induced osteoarthritis by promoting autophagy in mice. Biosci Rep. 2018;38(4):BSR20171691. [24] TANG Y, LI Y, XIN D, et al. Icariin alleviates osteoarthritis by regulating autophagy of chondrocytes by mediating PI3K/AKT/mTOR signaling. Bioengineered. 2021;12(1): 2984-2999. [25] ZHANG Y, CAI W, HAN G, et al. Panax notoginseng saponins prevent senescence and inhibit apoptosis by regulating the PI3K AKT mTOR pathway in osteoarthritic chondrocytes. Int J Mol Med. 2020;45(4): 1225-1236. [26] 商连斌,金连峰,王哲,等.续断总皂苷对膝骨关节炎大鼠软骨组织中PI3K/AKT/mTOR信号通路影响的实验研究[J].辽宁中医杂志,2021,48(5):188-191+222. [27] 商连斌,金连峰,王伟.续断总皂苷对膝骨关节炎大鼠软骨组织中Atg3、Atg4、Atg7表达影响的实验研究[J].辽宁中医药大学学报,2021,23(6):20-23+221. [28] DAI J, ZHANG Y, CHEN D, et al. Glabridin inhibits osteoarthritis development by protecting chondrocytes against oxidative stress, apoptosis and promoting mTOR mediated autophagy. Life Sci. 2021;268:118992. [29] 王琼,曹舜,丁惠宇,等.黄芩苷改善IL-1β诱导的软骨细胞凋亡的机制分析[J].解剖学研究,2021,43(6):602-608. [30] LV S, WANG X, JIN S, et al. Quercetin mediates TSC2-RHEB-mTOR pathway to regulate chondrocytes autophagy in knee osteoarthritis. Gene. 2022;820:146209. [31] ZHAO X, SHI X, YAO Y, et al. Autophagy flux inhibition mediated by lysosomal dysfunction participates in the cadmium exposure-induced cardiotoxicity in swine. Biofactors. 2022; 48(4):946-958. [32] SABERI HOSNIJEH F, BIERMA-ZEINSTRA SM, BAY-JENSEN AC. Osteoarthritis year in review 2018: biomarkers (biochemical markers). Osteoarthritis Cartilage. 2019;27(3):412-423. [33] CHEN Z, LI C, QIAN YH, et al. Enhancement of autophagy flux by isopsoralen ameliorates interleukin-1β-stimulated apoptosis in rat chondrocytes. J Asian Nat Prod Res. 2020; 22(2):179-192. [34] RAO Z, WANG S, WANG J. Peroxiredoxin 4 inhibits IL-1β-induced chondrocyte apoptosis via PI3K/AKT signaling. Biomed Pharmacother. 2017;90:414-420. [35] LIU J, MENG Q, JING H, et al. Astragaloside IV protects against apoptosis in human degenerative chondrocytes through autophagy activation. Mol Med Rep. 2017;16(3): 3269-3275. [36] 陈宝婷,陈举亮,孙毅东,等.芒果苷在Caco-2细胞模型中转运机制的研究[J].中药新药与临床药理,2022,33(9):1248-1253. [37] LI Y, WU Y, JIANG K, et al. Mangiferin Prevents TBHP-Induced Apoptosis and ECM Degradation in Mouse Osteoarthritic Chondrocytes via Restoring Autophagy and Ameliorates Murine Osteoarthritis. Oxid Med Cell Longev. 2019;2019:8783197. [38] ASL ER, AMINI M, NAJAFI S, et al. Interplay between MAPK/ERK signaling pathway and MicroRNAs: A crucial mechanism regulating cancer cell metabolism and tumor progression. Life Sci. 2021;278:119499. [39] WU Z, ZHANG X, LI Z, et al. Activation of autophagy contributes to the protective effects of lycopene against oxidative stress-induced apoptosis in rat chondrocytes. Phytother Res. 2021;35(7):4032-4045. [40] JIN Z, CHANG B, WEI Y, et al. Curcumin exerts chondroprotective effects against osteoarthritis by promoting AMPK/PINK1/Parkin-mediated mitophagy. Biomed Pharmacother. 2022;151:113092. [41] MEHRABANI D, MOJTAHED JABERI F, ZAKERINIA M, et al. The Healing Effect of Bone Marrow-Derived Stem Cells in Knee Osteoarthritis: A Case Report. World J Plast Surg. 2016;5(2):168-174. [42] LIU D, TANG W, ZHANG H, et al. Icariin protects rabbit BMSCs against OGD-induced apoptosis by inhibiting ERs-mediated autophagy via MAPK signaling pathway. Life Sci. 2020;253:117730. [43] MI B, WANG J, LIU Y, et al. Icariin Activates Autophagy via Down-Regulation of the NF-κB Signaling-Mediated Apoptosis in Chondrocytes. Front Pharmacol. 2018;9:605. [44] MAUMUS M, PERS YM, RUIZ M, et al. Cellules souches mésenchymateuses et médecine régénératrice - Quel avenir pour l’arthrose ? Med Sci (Paris). 2018;34(12):1092-1099. [45] SALIMINEJAD K, KHORRAM KHORSHID HR, SOLEYMANI FARD S, et al. An overview of microRNAs: Biology, functions, therapeutics, and analysis methods. J Cell Physiol. 2019;234(5):5451-5465. [46] LI Z, CHENG J, LIU J. Baicalin Protects Human OA Chondrocytes Against IL-1β-Induced Apoptosis and ECM Degradation by Activating Autophagy via MiR-766-3p/AIFM1 Axis. Drug Des Devel Ther. 2020;14:2645-2655. [47] YI H, ZHANG W, CUI ZM, et al. Resveratrol alleviates the interleukin-1β-induced chondrocytes injury through the NF-κB signaling pathway. J Orthop Surg Res. 2020; 15(1):424. [48] LIANG C, XING H, WANG C, et al. Resveratrol protection against IL-1β-induced chondrocyte damage via the SIRT1/FOXO1 signaling pathway. J Orthop Surg Res. 2022; 17(1):406. [49] WANG A, FANG S, ZHONG L, et al. Shikonin, a promising therapeutic drug for osteoarthritis that acts via autophagy activation. Int Immunopharmacol. 2022;106:108563. [50] 郑洁,袁普卫,赵莉平,等.青藤碱通过PI3K/AKt-mTOR信号通路调节膝OA兔软骨自噬水平机制研究[J].辽宁中医药大学学报,2019, 21(8):30-33. [51] LI J, JIANG M, YU Z, et al. Artemisinin relieves osteoarthritis by activating mitochondrial autophagy through reducing TNFSF11 expression and inhibiting PI3K/AKT/mTOR signaling in cartilage. Cell Mol Biol Lett. 2022;27(1):62. [52] ZHONG G, LIANG R, YAO J, et al. Artemisinin Ameliorates Osteoarthritis by Inhibiting the Wnt/β-Catenin Signaling Pathway. Cell Physiol Biochem. 2018;51(6):2575-2590. [53] 姚旭,王清华,茹艺,等.芍药苷抑制PI3K/AKT信号促进细胞自噬治疗骨关节炎[J].吉林中医药,2020,40(8):1076-1079. [54] MALEMUD CJ. Negative Regulators of JAK/STAT Signaling in Rheumatoid Arthritis and Osteoarthritis. Int J Mol Sci. 2017;18(3):484. [55] MOON SM, LEE SA, HAN SH, et al. Aqueous extract of Codium fragile alleviates osteoarthritis through the MAPK/NF-κB pathways in IL-1β-induced rat primary chondrocytes and a rat osteoarthritis model. Biomed Pharmacother. 2018;97:264-270. [56] YI H, ZHANG W, CUI ZM, et al. Resveratrol alleviates the interleukin-1β-induced chondrocytes injury through the NF-κB signaling pathway. J Orthop Surg Res. 2020; 15(1):424. [57] YOU H, ZHANG R, WANG L, et al. Chondro-Protective Effects of Shikimic Acid on Osteoarthritis via Restoring Impaired Autophagy and Suppressing the MAPK/NF-κB Signaling Pathway. Front Pharmacol. 2021;12:634822. [58] 徐斌,李盛华,周明旺,等.槲皮素通过激活自噬对LPS诱导的软骨细胞基质代谢及炎症的影响[J].中国实验方剂学杂志,2022,28(14):92-98. [59] BAI Y, GONG X, DOU C, et al. Redox control of chondrocyte differentiation and chondrogenesis. Free Radic Biol Med. 2019;132:83-89. [60] ANSARI MY, KHAN NM, AHMAD I, et al. Parkin clearance of dysfunctional mitochondria regulates ROS levels and increases survival of human chondrocytes. Osteoarthritis Cartilage. 2018;26(8):1087-1097. [61] LEE DY, PARK YJ, SONG MG, et al. Cytoprotective Effects of Delphinidin for Human Chondrocytes against Oxidative Stress through Activation of Autophagy. Antioxidants (Basel). 2020;9(1):83. [62] 杨阳,何宇,史于传,等.白杨素通过PI3K/AKT信号通路抑制LPS诱导的软骨细胞自噬[J].中国药理学通报,2021,37(5):662-668. [63] ANSARI MY, AHMAD N, HAQQI TM. Oxidative stress and inflammation in osteoarthritis pathogenesis: Role of polyphenols. Biomed Pharmacother. 2020;129:110452. |
| [1] | Yang Yifeng, Huang Jian, Ye Nan, Wang Lin. Ischemia-reperfusion injury in total knee arthroplasty [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(6): 955-960. |
| [2] | Zhang Kefan, Shi Hui. Research status and application prospect of cytokine therapy for osteoarthritis [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(6): 961-967. |
| [3] | Zhang Zeyi, Yang Yimin, Li Wenyan, Zhang Meizhen. Effect of foot progression angle on lower extremity kinetics of knee osteoarthritis patients of different ages: a systematic review and meta-analysis [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(6): 968-975. |
| [4] | Shen Feiyan, Yao Jixiang, Su Shanshan, Zhao Zhongmin, Tang Weidong. Knockdown of circRNA WD repeat containing protein 1 inhibits proliferation and induces apoptosis of chondrocytes in knee osteoarthritis [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(4): 499-504. |
| [5] | Maisituremu·Heilili, Zhang Wanxia, Nijiati·Nuermuhanmode, Maimaitituxun·Tuerdi. Effect of intraarticular injection of different concentrations of ozone on condylar histology of rats with early temporomandibular joint osteoarthritis [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(4): 505-509. |
| [6] | Qiao Hujun, Wang Guoxiang. Evaluation of rat osteoarthritis chondrocyte models induced by interleukin-1beta [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(4): 516-521. |
| [7] | Liu Yuhan, Fan Yujiang, Wang Qiguang. Comparison of protocols for constructing animal models of early traumatic knee osteoarthritis [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(4): 542-549. |
| [8] | Zhang Yaru, Chen Yanjun, Zhang Xiaodong, Chen Shenghua, Huang Wenhua. Effect of ferroptosis mediated by glutathione peroxidase 4 in the occurrence and progression of synovitis in knee osteoarthritis [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(4): 550-555. |
| [9] | Xue Jingwen, Wang Fangfang, Zhang Xin, Pang Ruifeng, Wang Xiaoye, Ma Xiaoru. Effect of ganoderma spore on mitochondrial autophagy and apoptosis in testicular tissue of diabetic rats [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(4): 562-568. |
| [10] | Zhang Ming, Wang Bin, Jia Fan, Chen Jie, Tang Wei. Application of brain-computer interface technology based on electroencephalogram in upper limb motor function rehabilitation of stroke patients [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(4): 581-586. |
| [11] | He Yuanjie, Chen Yuheng, Zhao Yongchao, Wang Zhenglong. Progress in epigenetic regulation of vascular smooth muscle cell remodeling in the occurrence and development of aortic aneurysms [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(4): 602-608. |
| [12] | Liu Luxing, Di Mingyuan, Yang Qiang. Signaling pathways in the mechanism underlying active ingredients of Chinese medicine in the treatment of osteoarthritis [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(4): 609-614. |
| [13] | Ma Sicong, Chen Jing, Li Yunqing. Functions and roles of connective tissue growth factor in nervous systems [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(4): 615-620. |
| [14] | Wang Xinyi, Xie Xianrui, Chen Yujie, Wang Xiaoyu, Xu Xiaoqing, Shen Yihong, Mo Xiumei. Electrospun nanofiber scaffolds for soft and hard tissue regeneration [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(3): 426-432. |
| [15] | Long Jundong, Shi Yehong, Wang Cheng, Chen Shijiu. Effects of different freezing techniques on the rejection of allogeneic vascular transplantation [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(3): 433-438. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||