Chinese Journal of Tissue Engineering Research ›› 2024, Vol. 28 ›› Issue (6): 961-967.doi: 10.12307/2023.793
Previous Articles Next Articles
Research status and application prospect of cytokine therapy for osteoarthritis
Zhang Kefan, Shi Hui
- Binzhou Medical University Hospital, Binzhou 256600, Shandong Province, China
-
Received:2022-12-16Accepted:2023-01-31Online:2024-02-28Published:2023-07-12 -
Contact:Shi Hui, MD, Associate chief physician, Binzhou Medical University Hospital, Binzhou 256600, Shandong Province, China -
About author:Zhang Kefan, Master candidate, Binzhou Medical University Hospital, Binzhou 256600, Shandong Province, China -
Supported by:Shandong Provincial Key Clinical Specialized Discipline Construction Project, No. SLCZDZK-0302 (to SH)
CLC Number:
Cite this article
Zhang Kefan, Shi Hui. Research status and application prospect of cytokine therapy for osteoarthritis[J]. Chinese Journal of Tissue Engineering Research, 2024, 28(6): 961-967.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks

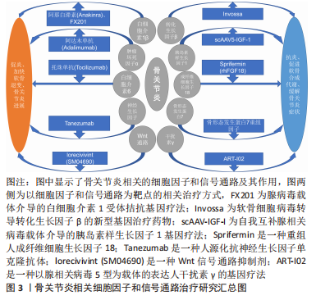
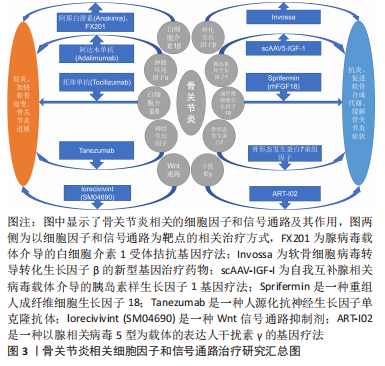
与骨关节炎相关的细胞因子主要分为促炎和分解代谢因子(白细胞介素1β,肿瘤坏死因子α,白细胞介素6,白细胞介素17和白细胞介素18等),抗炎和合成代谢因子(转化生长因子β,胰岛素样生长因子1,成纤维细胞生长因子18,骨形态发生蛋白7,干扰素γ,白细胞介素4,白细胞介素10和白细胞介素13等),以及相关的细胞信号通路[Wnt通路、丝裂原活化蛋白激酶(mitogenactivated protein kinases,MAPK)通路、核转录因子κB通路和NOTCH通路等][6]。相关的骨关节炎治疗方式包括基因治疗、间充质干细胞治疗和富血小板血浆治疗。 2.1 促炎、分解代谢因子对骨关节炎的影响 2.1.1 白细胞介素1β 是骨关节炎中主要的促炎和分解代谢细胞因子,它通过促进降解关节细胞外基质的Ⅱ型胶原、蛋白多糖和透明质酸蛋白水解酶的活性,加快骨关节炎的病变进展。白细胞介素1β的过表达可导致B细胞和T细胞活化,M1型巨噬细胞极化,破骨细胞生成以及骨关节炎滑膜细胞和脂肪细胞释放其他促炎细胞因子。白细胞介素1β还控制负责骨关节炎软骨降解的蛋白酶的生物利用度,如基质金属蛋白酶(MMPs)等[7]。 NA等[8]通过利用碘乙酸钠(MIA)注射白细胞介素1和白细胞介素17受体拮抗剂双缺陷小鼠发现,白细胞介素1受体拮抗剂缺乏不仅加速骨关节炎小鼠模型的软骨破坏,也增加了软骨炎症因子的水平;持续阻止与白细胞介素1受体的结合即使用其拮抗剂干预可以为关节炎提供持续的症状化和疾病修饰性治疗。在NIXON等[9]的一项研究中,使用一种辅助依赖腺病毒(HDAd)介导的关节内基因治疗方法,在小型和大型动物模型中实现了白细胞介素1受体拮抗剂的表达,证明了其在动物模型中的安全性和有效性。 阿那白滞素(Anakinra)是一种白细胞介素1受体拮抗剂,具有软骨保护和抗炎作用,目前广泛应用于类风湿关节炎的治疗。在以往的关节内注射阿那白滞素治疗膝骨关节炎的对照研究中,虽然阿那白滞素的耐受性良好,但是与安慰剂相比阿那白滞素对于患者症状无改善[10]。 FX201是一种新型的、关节内注射的腺病毒(HDAd)载体介导的白细胞介素1受体拮抗基因疗法,正在开发中用于治疗骨关节炎。SENTER等[11]评估了FX201的大鼠代物——辅助依赖腺病毒HDAd大鼠白细胞介素1Ra的疗效、生物分布和安全性,以及FX201在前交叉韧带横断大鼠骨关节炎模型中的生物分布。研究表明FX201和HDAd大鼠白细胞介素1Ra在注射的关节和近端组织中至少持续了92 d,很少有证据表明载体在周围扩散;最后,药物在该试验中显示出良好的安全性,没有任何局部或全身的不良反应。总之,HDAd大鼠白细胞介素1Ra具有局部治疗和疾病修饰作用,且耐受性良好,支持FX201的进一步临床开发。然而,使用白细胞介素1受体拮抗剂的治疗需要病毒载体来传递,其安全性有待评估。目前有一项Ⅰ期临床试验正在评估 FX201 在膝关节骨性关节炎患者中的安全性和耐受性[12]。 白细胞介素1受体拮抗剂在基础实验中表现良好,但是在临床试验中未展现出预期的效果。目前很多通过基因治疗的方式,改变其作用形式,具有可期待的治疗前景,其依旧是有潜力的重要治疗靶点。 2.1.2 肿瘤坏死因子α 是肿瘤坏死因子超家族的配体。它是一种多效细胞分子,在炎症、细胞凋亡和免疫系统发育中起着核心作用,其已被证明在骨关节炎中与抑制蛋白多糖、连接蛋白和Ⅱ型胶原的合成等多项病理进展相关[13]。尽管有明确的证据表明肿瘤坏死因子α在骨关节炎的病理生理学中起作用,但只有少数试验研究探讨了肿瘤坏死因子α阻断剂治疗骨关节炎的疗效。2015年一项涉及小鼠的研究表明,抑制肿瘤坏死因子α的表达有助于延缓骨关节炎的进展[14]。 阿达木单抗(Adalimumab)是第一个完全人源化抗肿瘤坏死因子α的单克隆抗体,目前广泛应用于类风湿关节炎和强直性脊柱炎的治疗。然而,在最近的使用其治疗糜烂性手骨关节炎的随机双盲安慰剂对照交叉试验中,历时12周,与安慰剂相比,阿达木单抗对伴有MRI表现有滑膜炎的糜烂性手骨关节炎患者的疼痛症状没有显示出任何有效影响。对于膝骨关节炎的疗效与安全性,目前有一项评估阿达木单抗与安慰剂相比的临床疗效和安全性的研究正在进行[15]。 肿瘤坏死因子α作为骨关节炎病理中的重要作用因子,其拮抗剂的治疗效果却并未达到预期,其中缺少基础实验探究其拮抗剂的作用机制,临床试验中也缺乏对于膝骨关节炎的疗效研究,其治疗效果和安全性需要更多的临床和基础实验证实。 2.1.3 白细胞介素6 是一种多效性炎症细胞因子,参与骨关节炎等多种疾病,它作为缺氧诱导因子2α的中介上调基质金属蛋白酶3和13的水平[16]。血清中高白细胞介素6水平是预测膝骨关节炎的独立因素,在骨关节炎患者的关节液中能够检测到高浓度的白细胞介素6[17]。研究表明,在小鼠实验模型中,对白细胞介素6进行靶向抑制可以有效延缓骨关节炎的进展[18-19]。 托珠单抗(Tocilizumab)是一种重组人源化抗人白细胞介素6受体单克隆抗体,目前主要用于类风湿疾病的治疗。虽然托珠单抗对于类风湿性关节炎患者改善病情效果尚可,但最近的一项关于探究托珠单抗在减轻手骨关节炎患者疼痛方面的研究显示,其并不比安慰剂更有效[20],故靶向抑制白细胞介素6信号可能对改善手骨关节炎症状无效。 与肿瘤坏死因子α相同的,白细胞介素6拮抗剂在手骨关节炎方面的治疗效果欠佳,考虑为骨关节炎与类风湿关节炎的病理区别,导致未能达到与后者相同的改善病情效果,该因子在将来可能会通过基因治疗方式进行骨关节炎治疗的基础和临床试验,进一步探究其作用机制和效果。 2.1.4 神经生长因子 此因子最早在神经组织中分离得到,它是调节神经生长增殖、分化、修复和存活的介质。然而,最近的研究表明,其在一些生理和病理条件下也具有诱导血管生成的潜力。正常关节软骨是无血管和神经的,但在骨关节炎患者的软骨中观察到骨软骨交界处和非钙化软骨中有血管生成,从而加快骨关节炎的发展[21]。 他尼珠单抗(Tanezumab)是一种人源化抗神经生长因子单克隆抗体,通过选择性靶向结合并抑制神经生长因子发挥作用,可以阻断该因子与其受体的相互作用,从而阻断来自传导疼痛的伤害性神经元的信号[22]。他尼珠单抗是目前研究最多的抑制神经生长因子的单克隆抗体,但由于接受他尼珠单抗治疗后,患者出现了关节损伤速度加剧和其他非靶向关节的骨关节坏死的症状[23],美国食品药品监督管理局(FDA)迅速叫停了包括他尼珠单抗在内的所有抗神经生长因子抗体临床试验。因此,神经生长因子拮抗剂产生的不良效果导致其不能成为骨关节炎治疗药物。"


2.2 抗炎及合成代谢因子对骨关节炎的影响 2.2.1 转化生长因子β 是一种抗炎和合成代谢细胞因子,控制软骨细胞的增殖和分化以及细胞外基质沉积,促进未分化间充质细胞的增殖、内皮细胞的趋化和血管生成。转化生长因子β具有刺激蛋白多糖合成和抑制肥大软骨细胞分化的能力[16],所以在维持关节软骨代谢稳态和结构完整性方面发挥着关键作用。因此其信号或成分的改变可能会影响软骨稳态,并加快骨关节炎的进程。 转化生长因子β蛋白的半衰期较短,其作用时间较短,使纯化蛋白本身成为一种虚弱而无效的工具,临床应用受到限制。因此,需要一个能够持续产生细胞因子的活细胞平台来使其表达。Invossa(TissueGene C,TG-C)是Kolon公司开发的利用基因工程软骨细胞病毒转导转化生长因子β的新型基因治疗药物。这种新的治疗方法是将软骨细胞与一种名为GP2-293的转基因细胞株混合在一起。GP2-293是一种药物工厂,能够过度生产对软骨再生和改变关节内部环境至关重要的生长因子,使用方法是将混合液注入患膝起到治疗效果。由于这些细胞的寿命很短,不能繁殖,因此在它们完成自己的工作后即会死亡,并被免疫细胞清除[24]。LEE等[25]的研究表明,该药物在骨关节炎大鼠模型中的作用显著,在56 d内可减轻骨关节炎模型的疼痛,改善软骨结构。此外,该药物引起转化生长因子β1和白细胞介素10水平升高,这些结果提示其通过诱导M2巨噬细胞主导的微环境对骨关节炎产生有益的影响。 通过转化生长因子β作用研究的基因治疗药物是最接近临床的骨关节炎基因治疗药物,因此,转化生长因子β是一个非常有潜力的细胞因子治疗靶点。但因其在骨关节炎病理中具有复杂的双重作用,缺乏和高激活状态都可能导致联合病理,使情况复杂化,仍然需要更多的有效性和安全性试验来检验。 2.2.2 胰岛素样生长因子1 是一种具有多效作用的细胞因子,它可以刺激间充质干细胞的增殖和促进其成软骨分化能力;此外,该因子还在软骨修复中发挥重要作用,可促进软骨细胞生存、增殖和软骨基质的产生。ORTVED等[26]在马动物模型中将rAAV5-胰岛素样生长因子1导入软骨细胞,观察到软骨细胞修复和Ⅱ型胶原蛋白的增加,表明了胰岛素样生长因子作为治疗靶点的可行性,同时也证明了腺相关病毒(AAV)介导的软骨细胞遗传修饰可能对临床有益。HEMPHILL等[27]利用自我互补腺相关病毒载体(scAAV)转导上述因子,并证明scAAV-胰岛素样生长因子1基因治疗载体可将胰岛素样生长因子1的产生水平提高,并通过软骨细胞的生物学反应促进软骨愈合。MAIH?FER等[28]使用重组腺相关病毒(rAAV)向量编码人类胰岛素样生长因子1 进行全层关节软骨缺损修复微创手术,术后1年与对照组相比显著改善了软骨修复参数(半定量总组织学评分、细胞浓度及基质沉积),并且未发生不良和免疫反应。该试验证明了生物材料引导的rAAV基因转移是促进软骨修复和预防骨关节炎的一种有价值的临床方法。 胰岛素样生长因子1在骨关节炎治疗中引起了研究者极大的兴趣,并显示出巨大的临床转化潜力。在多项试验中,该因子通过不同载体介导,都达到了不错的有效性和安全性。上述试验也证明了胰岛素样生长因子1作为基因治疗靶点的可行性。 2.2.3 成纤维细胞生长因子18 成纤维细胞生长因子家族是一组与核酸序列具有同源性的蛋白,在胚胎发育、细胞生长、组织修复、肿瘤生长和侵袭等病理生理过程中发挥重要作用。目前在骨关节炎领域的研究中已经报道,成纤维细胞生长因子18显著地刺激软骨细胞的增殖和细胞外基质的合成;关节内注射成纤维细胞生长因子18可减弱蛋白多糖和Ⅱ型胶原蛋白的降解,抑制金属蛋白酶13(MMP-13)的表达,减少软骨退变,最终促进退变软骨的再生和修复[29]。 Sprifermin是一种人重组成纤维细胞生长因子18(rhFGF18),用于治疗膝骨关节炎。研究显示Sprifermin能够显著促进关节软骨细胞和细胞外基质的合成[30-31],从而以剂量依赖性的方式增加软骨厚度。此外,它还能有效抑制蛋白水解酶活性(如金属蛋白酶13和血小板反应蛋白解整合素金属肽酶5),显著降低关节软骨退变[29,32]。该药物目前处于Ⅲ期临床试验阶段[33],未见局部或系统安全性问题报道,是一个值得期待的治疗靶点。 2.2.4 骨形态发生蛋白7 是转化生长因子超家族的成员之一。骨形态发生蛋白7对软骨细胞具有合成代谢和抗分解代谢作用。其能够促进软骨细胞合成软骨特异性细胞外基质蛋白,从而起到维持正常软骨稳态作用[34] 。 在HAYASHI等[35]对兔骨关节炎模型的研究中发现,每周进行关节内注射骨形态发生蛋白7可抑制现有软骨退变的进展。后来在更大的动物模型(如狗、山羊和绵羊)中进行的研究表明,骨形态发生蛋白7能够愈合骨和软骨的局灶性缺陷[34]。有学者曾在2010年进行了评估关节内骨形态发生蛋白7治疗膝骨关节炎的安全性和有效性的Ⅰ期临床试验,在接受0.1 mg和0.3 mg 剂量的参与者中,症状改善的趋势比安慰剂更大,并没有发现剂量限制性毒性[36]。CARON等[37]确定了骨形态发生蛋白7肽库中的两个区域,其中生物活性肽能够减弱骨关节炎软骨细胞表型,这些骨形态发生蛋白7衍生肽为骨关节炎提供了潜在的新的疾病治疗选择。 2.2.5 干扰素γ 是具有免疫调节功能的天然分泌蛋白家族。干扰素γ是其中的一种细胞因子,在类风湿滑膜组织中表达,具有抗炎特性,能够抑制血管生成,并在骨稳态中发挥作用。干扰素γ也调节和抑制肿瘤坏死因子α、白细胞介素1β和白细胞介素6的产生[38]。 ART-I02是一种以腺相关病毒5型(rAAV5)为载体的表达人干扰素γ的基因治疗药物。BEVAART等[39]通过对24只患有胶原诱导性关节炎的恒河猴进行了临床前研究,以评估ART-I02的生物分布、安全性和初步疗效,在注射ART-I02后未发现不良事件。ART-I02也正在进行针对骨关节炎的临床研究[40]。 文章总结了与骨关节炎相关的各细胞因子作用机制及相关治疗方式,见表1。"


2.3 相关的细胞信号通路 Wnt通路是一种高度保守和复杂的细胞信号通路,在细胞分化、发育和组织重塑中发挥重要作用。它受到多种水平的调节。在关节中,Wnt通路通过调节间充质干细胞分化为软骨细胞和成骨细胞帮助控制组织稳态。动物研究表明,它与软骨组织修复和关节再生有关。在骨关节炎中,Wnt信号的增加驱动间充质干细胞向成骨谱系转变,并刺激基质金属蛋白酶的生成,导致软骨降解。同时Wnt通路上调通过成骨细胞分化、分解代谢酶的增加和炎症参与膝骨关节炎。 lorecivivint (SM04690)是一种小分子Wnt通路抑制剂,先前在动物骨关节炎模型中证明了其通过抑制Wnt通路起到对软骨细胞的保护作用[41]。DESHMUKH等[42]研究表明在骨关节炎模型中,lorecivivint抑制炎症因子和软骨降解酶的产生,导致关节软骨增加,疼痛减轻和负重功能改善。Lorecivivint显示出改善膝骨关节炎症状的潜力。在Ⅱ期临床试验中证明了Lorecivivint对膝骨关节炎患者的治疗效果好于安慰剂[43],同时确定了未来研究的最佳剂量为0.07 mg,该药物Ⅲ期临床试验目前正在进行中[44]。这种关节内药物目前被认为是安全的,耐受性良好的,没有明显的系统性不良反应报道,但仍需大量的临床试验来证实其有效性和安全性。 MAPK、NOTCH和核转录因子κB通路已有证据表明其参与骨关节炎进程[45-47],但目前尚未出现相关靶向治疗药物研究。"


2.4 与细胞因子相关的骨关节炎治疗方式 2.4.1 基因治疗 基因治疗是一种很有前途的治疗策略,与半衰期短的重组因子的方法相比,基于基因的治疗具有药物的可控性、作用位点的特异性和长期存在等优点。使用何种载体进行转导将成为未来的研究重点。目前常用的载体包括病毒载体和非病毒载体,病毒载体中腺病毒载体、腺相关病毒载体和重组腺相关病毒载体研究较多,近期也有研究证明了其可行性[48]。但在以往的临床试验中,曾使用癌反转录病毒将注入患者关节的自体滑膜细胞进行转导,后来认识到这种载体存在致癌风险时,该方法被放弃。由于对在体内使用病毒载体的持续安全性的担忧,非病毒载体的发展正在获得更多支持,但非病毒表达载体存在转染效率低、细胞毒性大、靶向性不足等缺点。纳米技术通过靶向治疗、智能支架和新型粘胶补充剂,为改善当前骨关节炎治疗提供了一条途径。正如上所述,一些新的治疗骨关节炎技术和材料正在临床前开发中。在给药系统方面,由聚合物和脂质等组成的囊泡使疾病修饰性骨关节炎药物、核酸和生长因子的选择性、靶向给药成为可能。这些方法提供延迟、持续或触发的药物释放,增加关节内给药后药物滞留,以及减少脱靶不良反应。结合纳米设计和结构特征的支架可再现软骨,增加生物化学成分,并增强生物力学性能[49-50]。 因此,基因转移方法非常适合治疗像骨关节炎这类慢性和不可逆的疾病。基因治疗提供了局部治疗和长期效果的理想结合,因此可能是未来骨关节炎治疗管理障碍的答案。基因治疗的安全性和有效性、基因治疗药物的药代动力学和生物活性值得关注,需要大量长期的临床试验来检验。 2.4.2 间充质干细胞治疗 间充质干细胞具有自我更新和多向分化潜能,能够调节免疫、抵抗炎症、促进血管生成并促进再生[51],是极具潜力的新型治疗方式,也是细胞因子极佳的治疗载体。间充质干细胞可分为骨髓间充质干细胞、脂肪间充质干细胞及脐带间充质干细胞等,不论细胞来源如何,间充质干细胞都可以在相关细胞因子如转化生长因子 β、骨形态发生蛋白和胰岛素样生长因子刺激下发生软骨分化。在间充质干细胞培养中可以通过许多细胞外信号分子、生长因子和信号通路(如成纤维细胞再生因子、转化生长因子β、骨形态发生蛋白、MAPK通路和Notch通路)的相互作用促进细胞黏附,避免肥大性分化,诱导软骨形成[52]。WU等[53]研究使用化学合成修饰信使核糖核酸(modRNA)编码胰岛素样生长因子1的脂肪来源干细胞用来改善骨关节炎,结果表明胰岛素样生长因子1-脂肪间充质干细胞比天然脂肪来源干细胞具有更好的治疗效果,表现为组织学评分更低,软骨细胞外基质的丢失减少。表明通过某些细胞因子的修饰,能够使间充质干细胞达到更佳的治疗效果。 由于关节腔是一个相对封闭的空间,可以通过注射进行靶向治疗,与治疗需要全身注射间充质干细胞的疾病相比,注射干细胞治疗关节疾病的可行性显著。因此,选择何种的间充质干细胞进行治疗,以及使用何种细胞因子进行修饰,将是间充质干细胞研究的热点。尽管有很多研究表明了间充质干细胞的治疗效果,目前依旧需要更多的影像学和组织学数据,以及更多的患者来进行研究证明。 2.4.3 富血小板血浆治疗 富血小板血浆是通过分离自体全血制备的含有高浓度血小板的血浆,在医学的各个领域中均有广泛的应用[54]。富血小板血浆中含有多种生长因子、趋化因子和细胞因子[55]。在肌肉骨骼再生医学中,富血小板血浆是肌腱病、肌肉损伤、骨折不愈合和膝关节骨关节炎的一种有前景的治疗工具,但其作用机制目前尚无统一的结论。对于肱骨外上髁炎等肌腱病,有研究表明其治疗效果可能与自身某些基因多样性有关[56]。在骨关节炎领域中,多项研究显示关节腔内注射富血小板血浆可以提供良好的效果[57],目前在临床中作为早期骨关节炎的治疗方法越来越受到关注,并显示出优于传统治疗方法的临床效果。目前对于富血小板血浆的争议主要是精确的作用机制和标准化的制备方法仍不确定。不同的离心方式会造成富血小板血浆成分的不同,使得最终的治疗结果不能统一[58]。同样备受争议的是白细胞在富血小板血浆中的作用,有研究表明贫白细胞富血小板血浆更加适合膝骨关节炎这类无菌性炎症疾病,同时会带来更少的不良反应[59]。然而,LANA等[60]研究者反对在膝骨关节炎治疗中使用贫白细胞富血小板血浆,而推崇富白细胞富血小板血浆,他们的研究表明特定的白细胞在组织再生之前的炎症过程中起到重要作用,因为它们释放了促炎和抗炎分子;同时发现,中性粒细胞和活化血小板的组合对组织修复可能产生更积极的作用,也表明单核细胞的可塑性对于组织修复中的非炎症和修复作用很重要。而对于白细胞在富血小板血浆中的作用,目前仍然缺乏基础的实验研究来证实其作用机制,对于富血小板血浆的标准制备方式和探究其作用机制的基础实验研究无疑是将来的研究重点。"

| [1] HUNTER DJ, MARCH L, CHEW M. Osteoarthritis in 2020 and beyond: a Lancet Commission. Lancet. 2020;396(10264):1711-1712. [2] BERENBAUM F, WALLACE IJ, LIEBERMAN DE, et al. Modern-day environmental factors in the pathogenesis of osteoarthritis. Nat Rev Rheumatol. 2018;14(11):674-681. [3] LOESER RF, COLLINS JA, DIEKMAN BO. Ageing and the pathogenesis of osteoarthritis. Nat Rev Rheumatol. 2016;12(7):412-420. [4] SANCHEZ-LOPEZ E, CORAS R, TORRES A, et al. Synovial inflammation in osteoarthritis progression. Nat Rev Rheumatol. 2022;18(5):258-275. [5] KRAUS VB, BLANCO FJ, ENGLUND M, et al. Call for standardized definitions of osteoarthritis and risk stratification for clinical trials and clinical use. Osteoarthritis Cartilage. 2015;23(8):1233-1241. [6] 汪国翔,章晓云.骨关节炎病变过程中炎症细胞因子及相关信号通路的作用机制[J].中国组织工程研究,2021,25(14):2266-2273. [7] CHEVALIER X, EYMARD F, RICHETTE P. Biologic agents in osteoarthritis: hopes and disappointments. Nat Rev Rheumatol. 2013;9(7):400-410. [8] NA HS, PARK JS, CHO KH, et al. Interleukin-1-interleukin-17 signaling axis induces cartilage destruction and promotes experimental osteoarthritis. Front Immunol. 2020;11:730. [9] NIXON AJ, GROL MW, LANG H M, et al. Disease-modifying osteoarthritis treatment with interleukin-1 receptor antagonist gene therapy in small and large animal models. Arthritis Rheumatol. 2018;70(11):1757-1768. [10] MALEMUD CJ. Anticytokine therapy for osteoarthritis evidence to date. Drugs Aging. 2010;27(2):95-115. [11] SENTER R, BOYCE R, REPIC M, et al. Efficacy and safety of FX201, a novel intra-articular IL-1Ra gene therapy for osteoarthritis treatment, in a rat model. HUM GENE THER. 2022;33(9-10):541-549. [12] FLEXION THERAPEUTICS, INC. An open-label, single ascending dose study to assess the safety and tolerability of FX201 in patients with osteoarthritis of the knee: NCT04119687. clinicaltrials.gov, 2021[2022-04-14]. [13] VERBRUGGEN G, WITTOEK R, CRUYSSEN BV, et al. Tumour necrosis factor blockade for the treatment of erosive osteoarthritis of the interphalangeal finger joints: a double blind, randomised trial on structure modification. Ann Rheum Dis. 2012;71(6):891-898. [14] ZHAO YP, LIU B, TIAN QY, et al. Progranulin protects against osteoarthritis through interacting with TNF-α and β-Catenin signalling. Ann Rheum Dis. 2015;74(12):2244-2253. [15] CANADIAN RESEARCH EDUCATION IN ARTHRITIS. Osteoarthritis of the knee, inflammation, and the effect of adalimumab (OKINADA): a randomized placebo-controlled Trial: NCT02471118. clinicaltrials.gov, 2021[2022-11-30]. [16] RYU JH, YANG S, SHIN Y, et al. Interleukin-6 plays an essential role in hypoxia-inducible factor 2α-induced experimental osteoarthritic cartilage destruction in mice. Arthritis Rheum. 2011;63(9):2732-2743. [17] TSUCHIDA AI, BEEKHUIZEN M, `T HART MC, et al. Cytokine profiles in the joint depend on pathology, but are different between synovial fluid, cartilage tissue and cultured chondrocytes. Arthritis Res Ther. 2014; 16(5):441. [18] NASI S, SO A, COMBES C, et al. Interleukin-6 and chondrocyte mineralisation act in tandem to promote experimental osteoarthritis. Ann Rheum Dis. 2016;75(7):1372-1379. [19] LATOURTE A, CHERIFI C, MAILLET J, et al. Systemic inhibition of IL-6/Stat3 signalling protects against experimental osteoarthritis. Ann Rheum Dis. 2017;76(4):748-755. [20] RICHETTE P, LATOURTE A, SELLAM J, et al. Efficacy of tocilizumab in patients with hand osteoarthritis: double blind, randomised, placebo-controlled, multicentre trial. Ann Rheum Dis. 2021;80(3):349-355. [21] YU X, QI Y, ZHAO T, et al. NGF increases FGF2 expression and promotes endothelial cell migration and tube formation through PI3K/Akt and ERK/MAPK pathways in human chondrocytes. Osteoarthritis Cartilage. 2019;27(3):526-534. [22] GONDAL FR, BILAL J, KENT KWOH C. Tanezumab for the treatment of osteoarthritis pain. Drugs Today (Barc). 2022;58(4):187-200. [23] COLLISON J. Anti-NGF therapy improves osteoarthritis pain. Nat Rev Rheumatol. 2019;15(8):450. [24] MOBASHERI A, CHOI H, MARTÍN-VASALLO P. Over-production of therapeutic growth factors for articular cartilage regeneration by protein production platforms and protein packaging cell lines. Biology (Basel). 2020;9(10):330. [25] LEE H, KIM H, SEO J, et al. Tissue Gene-C promotes an anti-inflammatory micro-environment in a rat monoiodoacetate model of osteoarthritis via polarization of M2 macrophages leading to pain relief and structural improvement. Inflammopharmacology. 2020;28(5):1237-1252. [26] ORTVED KF, BEGUM L, MOHAMMED HO, et al. Implantation of rAAV5-IGF-I transduced autologous chondrocytes improves cartilage repair in full-thickness defects in the equine model. Mol Ther. 2015;23(2):363-273. [27] HEMPHILL DD, MCILWRAITH CW, SLAYDEN RA, et al. Adeno-associated virus gene therapy vector scAAVIGF-I for transduction of equine articular chondrocytes and RNA-seq analysis. Osteoarthritis Cartilage. 2016;24(5): 902-911. [28] MAIHÖFER J, MADRY H, REY‐RICO A, et al. Hydrogel‐guided, rAAV‐mediated IGF‐I overexpression enables long‐term cartilage repair and protection against perifocal osteoarthritis in a large‐animal full‐thickness chondral defect model at one year in vivo. Adv Mater. 2021;33(16):e2008451. [29] MÜLLER S, LINDEMANN S, GIGOUT A. Effects of sprifermin, IGF1, IGF2, BMP7, or CNP on bovine chondrocytes in monolayer and 3D culture. J Orthop Res. 2020;38(3):653-662. [30] ROEMER FW, KRAINES J, AYDEMIR A, et al. Evaluating the structural effects of intra-articular sprifermin on cartilage and non-cartilaginous tissue alterations, based on sqMRI assessment over 2 years. Osteoarthritis Cartilage. 2020;28(9):1229-1234. [31] EMD SERONO RESEARCH DEVELOPMENT INSTITUTE, INC. A multicenter, randomized, double-blind, placebo controlled, parallel-group trial to investigate the efficacy and safety of different intra articular (i.a.) dosages of sprifermin in subjects with primary osteoarthritis of the knee: results/NCT01919164. clinicaltrials.gov, 2020[2022-05-19]. [32] HOCHBERG MC, GUERMAZI A, GUEHRING H, et al. Effect of intra-articular sprifermin vs. placebo on femorotibial joint cartilage thickness in patients with osteoarthritis: the FORWARD randomized clinical trial. JAMA. 2019; 322(14):1360-1370. [33] ZENG N, CHEN XY, YAN ZP, et al. Efficacy and safety of sprifermin injection for knee osteoarthritis treatment: a meta-analysis. Arthritis Res Ther. 2021; 23(1):107. [34] BOON MR, VAN DER HORST G, VAN DER PLUIJM G, et al. Bone morphogenetic protein 7: a broad-spectrum growth factor with multiple target therapeutic potency. Cytokine Growth Factor Rev. 2011;22(4):221-229. [35] HAYASHI M, MUNETA T, TAKAHASHI T, et al. Intra-articular injections of bone morphogenetic protein-7 retard progression of existing cartilage degeneration: progression of existing cartilage degeneration. J Orthop Res. 2010;28(11):1502-1506. [36] HUNTER DJ, PIKE MC, JONAS BL, et al. Phase 1 safety and tolerability study of BMP-7 in symptomatic knee osteoarthritis. BMC Musculoskelet Disord. 2010;11:232. [37] CARON MMJ, RIPMEESTER EGJ, VAN DEN AKKER G, et al. Discovery of bone morphogenetic protein 7-derived peptide sequences that attenuate the human osteoarthritic chondrocyte phenotype. Mol Ther Methods Clin Dev. 2021;21:247-261. [38] ZHAO R, CHEN NN, ZHOU XW, et al. Exogenous IFN-beta regulates the RANKL-c-Fos-IFN-beta signaling pathway in the collagen antibody-induced arthritis model. J Transl Med. 2014;12:330. [39] BEVAART L, AALBERS CJ, VIERBOOM MPM, et al. Safety, Biodistribution, and efficacy of an AAV-5 vector encoding human interferon-beta (ART-I02) delivered via intra-articular injection in rhesus monkeys with collagen-induced arthritis. Hum Gene Ther Clin Dev. 2015;26(2):103-112. [40] ARTHROGEN. A single dose clinical trial to study the safety of ART-I02 in patients with arthritis: NCT02727764. clinicaltrials.gov, 2018[2022-05-01]. [41] YAZICI Y, MCALINDON TE, FLEISCHMANN R, et al. A novel Wnt pathway inhibitor, SM04690, for the treatment of moderate to severe osteoarthritis of the knee: results of a 24-week, randomized, controlled, phase 1 study. Osteoarthritis Cartilage. 2017;25(10):1598-1606. [42] DESHMUKH V, HU H, BARROGA C, et al. A small-molecule inhibitor of the Wnt pathway (SM04690) as a potential disease modifying agent for the treatment of osteoarthritis of the knee. Osteoarthritis Cartilage. 2018; 26(1):18-27. [43] YAZICI Y, MCALINDON TE, GIBOFSKY A, et al. A Phase 2b randomized trial of lorecivivint, a novel intra-articular CLK2/DYRK1A inhibitor and Wnt pathway modulator for knee osteoarthritis. Osteoarthritis Cartilage. 2021;29(5): 654-666. [44] BIOSPLICE THERAPEUTICS, INC. A phase 3, 28-week, multicenter, randomized, double-blind, placebo-controlled study to evaluate the efficacy and safety of a single injection of SM04690 injected in the target knee joint of moderately to severely symptomatic osteoarthritis subjects: NCT04385303. clinicaltrials.gov, 2022[2022-05-19]. [45] NAILWAL NP, DOSHI GM. Role of intracellular signaling pathways and their inhibitors in the treatment of inflammation. Inflammopharmacology. 2021;29(3):617-640. [46] MINGUZZI M, PANICHI V, D’ADAMO S, et al. Pleiotropic roles of NOTCH1 signaling in the loss of maturational arrest of human osteoarthritic chondrocytes. Int J Mol Sci. 2021;22(21):12012. [47] CHOI MC, JO J, PARK J, et al. NF-κB signaling pathways in osteoarthritic cartilage destruction. Cells. 2019;8(7):734. [48] ZHOU C, CUI Y, YANG Y, et al. Runx1 protects against the pathological progression of osteoarthritis. Bone Res. 2021;9(1):50. [49] LAWSON TB, MÄKELÄ JTA, KLEIN T, et al. Nanotechnology and osteoarthritis. part 1: clinical landscape and opportunities for advanced diagnostics. J Orthop Res. 2021;39(3):465-472. [50] LAWSON TB, MÄKELÄ JTA, KLEIN T, et al. Nanotechnology and Osteoarthritis. Part 2: Opportunities for advanced devices and therapeutics. J Orthop Res. 2021;39(3):473-484. [51] WEI P, BAO R. Intra-articular mesenchymal stem cell injection for knee osteoarthritis: mechanisms and clinical evidence. Int J Mol Sci. 2022; 24(1):59. [52] HUANG J, LIU Q, XIA J, et al. Modification of mesenchymal stem cells for cartilage-targeted therapy. J Transl Med. 2022;20(1):515. [53] WU H, PENG Z, XU Y, et al. Engineered adipose-derived stem cells with IGF-1-modified mRNA ameliorates osteoarthritis development. Stem Cell Res Ther. 2022;13(1):19. [54] EVERTS P, ONISHI K, JAYARAM P, et al. Platelet-rich plasma: new performance understandings and therapeutic considerations in 2020. Int J Mol Sci. 2020; 21(20):7794. [55] RIEWRUJA K, PHAKHAM S, SOMPOLPONG P, et al. Cytokine profiling and intra-articular injection of autologous platelet-rich plasma in knee osteoarthritis. Int J Mol Sci. 2022;23(2):890. [56] NIEMIEC P, SZYLUK K, BALCERZYK A, et al. Why PRP works only on certain patients with tennis elbow? Is PDGFB gene a key for PRP therapy effectiveness? A prospective cohort study. BMC Musculoskelet Disord. 2021;22(1):710. [57] NOWACZYK A, SZWEDOWSKI D, DALLO I, et al. Overview of first-line and second-line pharmacotherapies for osteoarthritis with special focus on intra-articular treatment. Int J Mol Sci. 2022;23(3):1566. [58] OUDELAAR BW, PEERBOOMS JC, HUIS IN T VELD R, et al. Concentrations of blood components in commercial platelet-rich plasma separation systems: a review of the literature. Am J Sports Med. 2019;47(2):479-487. [59] EYMARD F, ORNETTI P, MAILLET J, et al. Correction to: Intra‑articular injections of platelet‑rich plasma in symptomatic knee osteoarthritis: a consensus statement from French‑speaking experts. Knee Surg Sports Traumatol Arthrosc. 2021;29(10):3211-3212. [60] LANA JF, MACEDO A, INGRAO ILG, et al. Leukocyte-rich PRP for knee osteoarthritis: current concepts. J Clin Orthop Trauma. 2019;10(Suppl 1): S179-S182. |
| [1] | Zhang Zeyi, Yang Yimin, Li Wenyan, Zhang Meizhen. Effect of foot progression angle on lower extremity kinetics of knee osteoarthritis patients of different ages: a systematic review and meta-analysis [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(6): 968-975. |
| [2] | Lin Feng, Cheng Ling, Gao Yong, Zhou Jianye, Shang Qingqing. Hyaluronic acid hydrogel-encapsulated bone marrow mesenchymal stem cells promote cardiac function in myocardial infarction rats (III) [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(3): 355-359. |
| [3] | Xu Yinghua, Liu Jing, You Quan, Wen Zhihao, Gao Lu. Effect of neodymium-doped:yttrium aluminum perovskite laser combined with two kinds of remineralizers on remineralization of early enamel caries [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(3): 360-365. |
| [4] | Bi Yujie, Ma Dujun, Peng Liping, Zhou Ziqiong, Zhao Jing, Zhu Houjun, Zhong Qiuhui, Yang Yuxin. Strategy and significance of Chinese medicine combined with medical hydrogel for disease treatment [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(3): 419-425. |
| [5] | Wang Xinyi, Xie Xianrui, Chen Yujie, Wang Xiaoyu, Xu Xiaoqing, Shen Yihong, Mo Xiumei. Electrospun nanofiber scaffolds for soft and hard tissue regeneration [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(3): 426-432. |
| [6] | Long Jundong, Shi Yehong, Wang Cheng, Chen Shijiu. Effects of different freezing techniques on the rejection of allogeneic vascular transplantation [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(3): 433-438. |
| [7] | Yang Jie, Hu Haolei, Li Shuo, Yue Wei, Xu Tao, Li Yi. Application of bio-inks for 3D printing in tissue repair and regenerative medicine [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(3): 445-451. |
| [8] | Chen Junyan, Meng Qingqi, Li Siming. Cartilage targeting function in the drug delivery system by intra-articular injection for the treatment of osteoarthritis [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(3): 458-463. |
| [9] | Sun Yuan, Wang Qingbo, Pi Yihua, Lu Chunmin, Xu Chuanyi, Zhang Yan. Effects of early and late aerobic exercise on right heart failure induced by monocrotaline in rats with pulmonary hypertension [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(2): 177-185. |
| [10] | Liu Baofang, Xu Bin, Chen Lei. Pueraria decoction in the treatment of osteoarthritis: network pharmacology analysis and animal model validation [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(2): 193-199. |
| [11] | Dai Xinyu, Yan Jihong, Hua Lingjun, Zheng Xiaohong. Resistance exercise improves body composition in overweight and obese people: an umbrella review [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(2): 267-271. |
| [12] | Meng Zhicheng, Qiao Weiping, Zhao Yang, Liu Hongfei, Li Kaijie, Ma Bo. Effects of immune cells and related cytokines in the pathogenesis and treatment of osteoarthritis [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(2): 280-287. |
| [13] | Li Chengming, Xue Dongling, Yang Xinyu, Xiao Chi, Cui Daping. Mechanism of Chinese medicine for promoting blood circulation and removing blood stasis combined with platelet-rich plasma to improve steroid-induced necrosis of the femoral head [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(2): 288-294. |
| [14] | Long Yi, Yang Jiaming, Ye Hua, Zhong Yanbiao, Wang Maoyuan. Extracellular vesicles in sarcopenic obesity: roles and mechanisms [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(2): 315-320. |
| [15] | Chang Wanpeng, Zhang Zhongwen, Yang Yulin, Zi Yang, Yang Mengqi, Du Bingyu, Wang Nan, Yu Shaohong. Efficacy of rehabilitation exoskeleton robots on post-stroke lower limb motor dysfunction: a Meta-analysis [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(2): 321-328. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||