Chinese Journal of Tissue Engineering Research ›› 2024, Vol. 28 ›› Issue (2): 288-294.doi: 10.12307/2023.690
Previous Articles Next Articles
Mechanism of Chinese medicine for promoting blood circulation and removing blood stasis combined with platelet-rich plasma to improve steroid-induced necrosis of the femoral head
Li Chengming, Xue Dongling, Yang Xinyu, Xiao Chi, Cui Daping
- Zhongshan Hospital Affiliated to Dalian University, Dalian 116001, Liaoning Province, China
-
Received:2022-09-20Accepted:2022-10-31Online:2024-01-18Published:2023-06-30 -
Contact:Cui Daping, MD, Chief physician, Zhongshan Hospital Affiliated to Dalian University, Dalian 116001, Liaoning Province, China -
About author:Li Chengming, Master candidate, Zhongshan Hospital Affiliated to Dalian University, Dalian 116001, Liaoning Province, China -
Supported by:Bethune Public Welfare Foundation, No. X-J-2020-020 (to CDP)
CLC Number:
Cite this article
Li Chengming, Xue Dongling, Yang Xinyu, Xiao Chi, Cui Daping. Mechanism of Chinese medicine for promoting blood circulation and removing blood stasis combined with platelet-rich plasma to improve steroid-induced necrosis of the femoral head[J]. Chinese Journal of Tissue Engineering Research, 2024, 28(2): 288-294.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks

2.1 活血化瘀中药对激素性股骨头坏死的防治机制 2.1.1 改善血管内血液高凝状态 活血化瘀中药通过祛瘀、抗凝、抗血栓、降血脂等作用,明显降低血脂水平,改善血液高凝状态,疏通血管,进而抑制激素性股骨头坏死的发生、发展,有效防治激素性股骨头坏死。血液高凝状态是形成血栓的主要因素,激素药物可诱导血液黏稠度增加,造成血液高凝状态、血液瘀积、血栓形成,最终导致股骨头内微血管供血障碍,进而增加患激素性股骨头坏死的风险。HUANG等[4]通过建立大鼠气滞血瘀模型解读气血和胶囊(主要的活性成分包括当归、赤芍、红花、桃仁和延胡索)的药理活性,证明了活血化瘀药物可以改善血液流变学异常和凝血功能障碍。近年来,应用活血化瘀中药治疗激素性股骨头坏死取得了巨大进步,田伟明等[5]研究发现骨复活汤通过降低全血黏度和血浆黏度,达到防治兔激素性股骨头坏死模型的目的。段卫峰等[6]利用祛瘀法(由鹿茸、丹参、杜仲、续断、黄芪、鸡血藤、玄参、连翘等药物组成),通过干预大白兔激素性股骨头坏死模型,明显改善模型兔凝血异常状态,促进股骨头内微血管新生,加速毛细血管重塑,改善股骨头内血液供应。此外,齐振熙等[7]也发现活血化瘀中药可以降低血清胆固醇和三酰甘油水平,减轻了高脂血症程度,提高了血清中的钙磷含量,改善激素性股骨头坏死状态下的血液流变指标。活血化瘀中药及其有效果成分可明显改善血液异常(高凝)状态,从而可恢复股骨头坏死区域血供情况,达到治疗目的,见表1。"


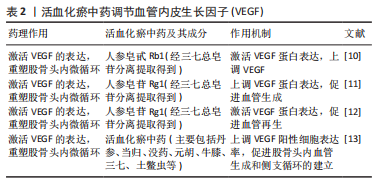
2.1.2 激活血管内皮生长因子(vascular endothelial growth factor,VEGF)的表达、重塑股骨头内微循环 VEGF是促进血管生长的重要生长因子,在目前已知的与血管新生有关的生长因子中,VEGF是最有力的血管生成因子,具有高度特异性,可修复血管、促进血管再生;而糖皮质激素可通过抑制VEGF蛋白表达来抑制正常的毛细血管生成与再生,使血管壁硬化,进而抑制成骨细胞发挥作用,最终造成骨坏死[8-9]。因此,重建血运同是活血化瘀中药治疗激素性股骨头坏死的重要方法之一。YE等[10]发现在大鼠激素性股骨头坏死模型中,人参皂甙Rb1通过激活VEGF/RUNX2/BMP-2信号通路中的VEGF表达,从而缓解激素性股骨头坏死,促进股骨头内血管重建。人参皂苷Rg1是一种从三七总皂苷分离出来的无毒皂苷,具有强大的活血化瘀、消肿定痛作用。人参皂苷Rg1能够通过上调低氧诱导因子(hypoxia inducible factor-1α,HIF-1α)及VEGF蛋白表达,促进血管生成[11]。LEUNG等[12]进一步证明人参皂苷Rg1可诱导PI3K/Akt、β-catenin水平增加,最终β-catenin进入细胞核并逐渐积累聚集,随后激活VEGF表达,促进血管再生,恢复股骨头内血运情况,进而到达治疗效果。LI等[13]在体内实验中选择使用活血化瘀中药治疗股骨头坏死大耳兔,主要包括丹参、当归、没药、元胡、牛膝、三七、土鳖虫等,同时采用免疫组化法测定股骨头坏死模型的股骨头内VEGF阳性细胞表达率,结果发现活血化瘀中药可以同时促进股骨头内血管生成和侧支循环的建立,重建股骨头内血运,达到治疗股骨头坏死效果。可见,VEGF在骨重塑和股骨头新生血管的形成过程中起到了关键作用,见表2。"
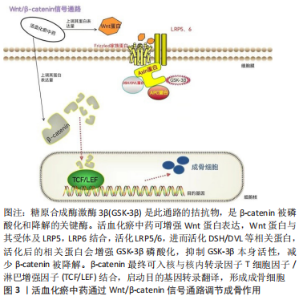
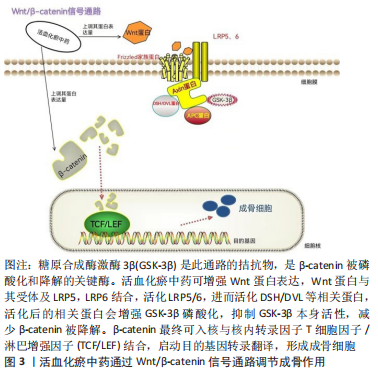
2.1.3 调控脂代谢紊乱 糖皮质激素长时间或大剂量堆积在体内,造成体内脂代谢紊乱,引发股骨头内髓腔内的脂肪细胞增多,造成股骨头内压力增高,最终形成股骨头终末动脉或小静脉脂肪栓塞,进而中断股骨头内血流,造成区域血液供应障碍,诱发激素性股骨头坏死的发生。活血化瘀中药可以纠正脂代谢异常,减少脂质在髓腔内堆积,降低骨内压,从而恢复股骨头内血运。史风雷等[14]研究发现丹参注射液对激素性股骨头坏死有较好的预防作用,其机制可能是纠正了脂代谢紊乱,从而使坏死的股骨头血供的得到恢复。此外,李峻辉等[15]发现补肾活骨方(主要成分包括骨碎补、山药、红花、淫羊藿、当归、黄芪、丹参等)可通过纠正兔激素性股骨头坏死模型脂质代谢紊乱,减少脂质在髓腔内堆积,降低股骨头内压力,改善股骨头内血液微循环。临床上也有降血脂药物治疗激素性股骨头坏死,2014年JIANG等[16]证实了激素性股骨头坏死主要是由于脂代谢紊乱,利用普伐他汀可以通过抑制过氧化物酶体增殖子活化受体γ(PPARγ)表达和激活Wnt 信号通路来预防类固醇诱导的股骨头坏死。过氧化物酶体增殖子活化受体γ是一种成脂转录因子,可促进骨髓间充质干细胞(bone marrow mesenchymal stem cells,BMSCs)成脂分化。但对于中药而言,患者更易于接受。 2.1.4 调控骨代谢过程、促进成骨作用 骨代谢主要受信号通路转导,而一些活血化瘀中药也可通过调控信号通路和激活相应蛋白表达,影响骨细胞分化增殖,维持成骨细胞与破骨细胞之间的平衡状态。骨代谢涉及基质沉积与矿化和再吸收之间的复杂平衡,现在有充分的证据表明中药可影响骨代谢过程,特别是通过抑制骨吸收进而对骨骼产生有益影响[17]。成骨细胞是形成骨骼的主要功能细胞,主要来源于骨髓基质间质干细胞,可合成骨基质,帮助骨质矿化;破骨细胞是由多个单核细胞聚集构成的多核巨细胞,其分布在骨组织表面或骨血管周围,其分泌的酶类物质可以促进骨细胞的破坏、吸收,同时将坏死或老化的骨细胞分解为成骨细胞成骨的原料,它们共同维持骨代谢平衡,缺一不可。糖皮质激素能破坏体内正常的骨代谢平衡,使成骨细胞提前凋亡,同时增加破骨细胞数量及活性[18-20],中药已被世界卫生组织作为一项有效的全球医学计划而应用[21],其中活血化瘀中药成分十分复杂,可以通过调控各种信号通路和靶点来促进骨再生,对抗激素在体内造成的不良症状。 (1)调控Wnt/β-catenin信号通路:Wnt/β-catenin信号通路可以提高成骨细胞活性、抑制成骨细胞凋亡进而增加骨密度,在骨形成过程中具有重要作用。Wnt/β-catenin信号通路主要包括Wnt蛋白、Wnt受体、β-catenin、糖原合成酶激酶3β(glycogen synthase kinase-3β,GSK-3β)、核内转录因子T细胞因子/淋巴增强因子(TCF/LEF)。Wnt蛋白作为通路的起始信号是一种分泌型糖蛋白[22],会通过旁分泌与自分泌激活相关靶基因的表达,并发挥相应的生物学效应。活血化瘀中药可上调该通路中β-catenin表达,进一步发挥其成骨作用,见图3。"
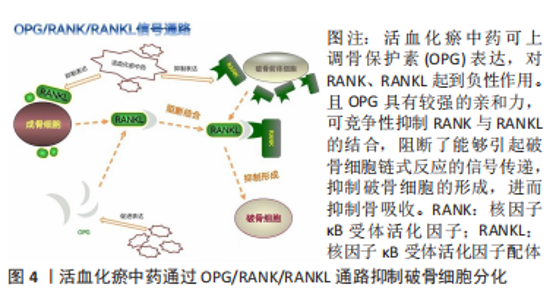
吴忠书等[23]发现活血通络胶囊(由木豆、当归、芍药、藁本、桃仁、红花、地黄7种草本植物组成,具有活血化瘀、补肾固本、通络止痛作用)能够上调β-catenin蛋白表达量,促进骨髓间充质干细胞增殖和成骨分化。陈杰等[24]通过研究发现三七总皂苷可以激活Wnt/β-catenin通路,且采用Western blot方法观察到活血化瘀中药可以上调Wnt3a、LRP5、β-catenin蛋白表达,促进成骨作用,从而缓解股骨头坏死的病情进展,达到治疗效果。此外,HUANG等[25]还从松果龙牙草中分离出来的水溶性多糖,以质量浓度为50 μg/mL进行处理,结果表明分离的多糖可以通过激活Wnt/β-Catenin信号通路、增加Wnt3及β-catenin蛋白来保护细胞免受糖皮质激素的攻击,从而预防激素性股骨头坏死。 (2)调控Hedgehog信号通路:Hedgehog信号通路主要起到调节细胞增殖和分化的作用[26],其对骨髓间充质干细胞多向分化调控具有重要作用[27-28]。骨髓间充质干细胞属于多能干细胞,可分化多种骨基质细胞,Hedgehog通路可以促进骨髓间充质干细胞向成骨细胞分化,并同时抑制向脂肪细胞方向分化[27]。Hedgehog通路主要由配体(Shh、Dhh、Ihh)、受体(SMO、Ptc)及信号分子(Gli)等组成,Hedgehog通路的活性降低及成骨-成脂分化平衡失调,是激素性股骨头坏死形成的重要原因之一。活血化瘀中药能够影响Hedgehog信号通路,从而达到减轻股骨头坏死程度。梁学振等[29]发现补肾活血胶囊能够增强Hedgehog信号通路相关因子Shh、Gli1的蛋白表达,进一步促进成骨分化。并且邓洋洋等[30]证实了Hedgehog信号通路参与骨代谢过程,同时活血化瘀中药复方(红花、桃仁、当归等)可调控细胞表面受体 Patched-1(PTCH1)和Gli3的蛋白含量,纠正骨代谢失衡。 (3)调控OPG/RANK/RANKL信号通路:OPG/RANK/RANKL信号通路在骨代谢领域调节骨重建的横轴旁分泌系统,直接影响破骨细胞分化及功能[31]。OPG/RANK/RANKL信号通路主要成分为骨保护素(OPG),又叫破骨细胞抑制因子、核因子κB受体活化因子(receptor activator of NF-κB,RANK)、核因子κB受体活化因子配体(receptor activator of NF-κB ligand,RANKL),又名破骨细胞分化因子。RANKL是决定破骨细胞分化的关键因子,RANKL和RANK相结合可激活分化成熟的破骨细胞。近年来,国内外研究表明活血化瘀中药可以激活OPG/RANK/RANKL通路,发挥其活性作用,见图4。"
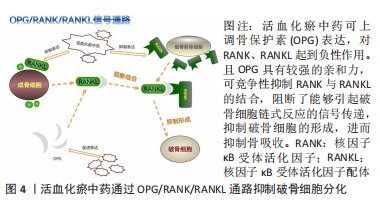

李永志等[32]报道骨复生(主要包括黄芪、丹参、三七、土元等中药组成,具有显著活血化瘀、强筋骨等作用)可以激活OPG/RANK/RANKL通路,上调骨保护素表达,阻碍破骨细胞增殖分化,从而有效干预激素性股骨头坏死。宋红梅等[33]发现温阳补肾方(淫羊藿、骨碎补、鹿角胶、丹参、郁金、三七等中药组成)具有活血化瘀、壮骨、止痛等作用,在动物实验中可以激活OPG/RANK/RANKL通路,提高激素性股骨头坏死兔股骨头组织中的骨保护素表达,进一步抑制RANK、RANKL的表达,从而抑制破骨细胞分化及功能活性,有效防治激素性股骨头坏死。SONG等[34]也证明了温阳补肾方可以上调骨保护素的表达水平,并抑制RANK和RANKL的表达水平,从而延缓激素性股骨头坏死继续向下发展。JIANG等[35]同样发现牛膝提取物可以改善激素诱导的股骨头坏死大鼠的骨小梁微结构,增加骨矿物质密度并促进血管的形成。此外还能够上调骨保护素,下调RANKL和RANK表达,以及增加血清和坏死股骨头内的骨保护素与RANKL的比率,抑制破骨细胞分化并激活骨形成标志物,从而抑制激素性股骨头坏死的发生。这表明活血化瘀中药或其有效成分均是治疗激素性股骨头坏死的一种潜在方法。 (4)调控PI3K/AKT/mTOR信号通路:PI3K/AKT/mTOR通路是一种保护性通路,包括磷脂酰肌醇3-激酶(phosphatidylinositol 3 kinase,PI3K)、蛋白激酶B (protein kinase B,AKT)、哺乳动物雷帕霉素靶蛋白(mammalian target of rapamycin,mTOR)等主要成分,不仅可以修复血管,还可调控相关骨细胞分化与凋亡,维持骨细胞代谢过程。PI3K作为该通路的起始因子,可以被多种效应因子激活,是传导细胞信号的桥梁,促使Akt活化,Akt活化后可激活下游的靶蛋白mTOR。在PI3K/AKT/mTOR通路中,mTOR的下游转录因子则包括了HIF-1α、c-Myc、FoxO等明星分子。PI3K/AKT/mTOR通路修复血管、促进血管再生的功能主要与细胞中的HIF-1α有关,当细胞处于低氧环境下,HIF-1α表达增加,同时可以刺激VEGF的转录。而HIF-1α的调节与PI3K/AKT/mTOR通路紧密相关,从而可以介导此通路,对血管产生修复及再生等作用[36]。另一方面,CAO等[37]在银杏叶中分离提取到的银杏叶提取物,具有显著活血化瘀、通络止痛、化浊降脂等作用,通过实验发现在激素性股骨头坏死小鼠模型中银杏叶提取物可激活PI3K/Akt信号通路,增加了血管内皮细胞活性,促进血管再生,并抑制甲强基的松龙诱导的细胞凋亡,有效缓解激素性股骨头坏死病情发展。在骨代谢过程中,活血化瘀中药介导PI3K/AKT通路后,可加强与Wnt/β-catenin信号通路联系,使β-catenin蛋白向细胞核内转移,与TCF/LEF结合进一步刺激成骨细胞加速分化,最终达到调控细胞的分化和代谢效果。LV等[38]从骨碎补中提取分离的骨碎补总黄酮,于大鼠激素性股骨头坏死模型中发现,骨碎补总黄酮是通过激活成骨细胞中的PI3K/AKT途径来促进增殖,保护成骨细胞免受激素损害,防治激素性股骨头坏死。显然,其他活血化瘀中药同样也可作用于PI3K/Akt信号通路中,促进成骨分化,XUE等[39]选择从红景天中分离提取单体药物红景天苷,通过激活PI3K/Akt信号通路并下调成骨细胞中caspase-3蛋白(可以诱导细胞凋亡)的表达来减轻地塞米松诱导成骨细胞的凋亡,预防激素性股骨头坏死。YANG等[40]在体内、体外研究中发现,甜菜碱能够通过雷帕霉素靶标mTOR信号级联反应,减轻股骨头坏死。mTOR是AKT的重要底物,其广泛存在于各种生物细胞中,调节细胞的生长及存活,影响激素性股骨头坏死。 (5)调控TLR4/NF-κB通路:Toll样受体 (toll-like receptors,TLRs)介导的炎症反应发挥了核心作用[41],炎症反应是造成激素性股骨头坏死形成的重要因素之一。TLR4是TLRs家族的重要成员,也是人类发现的第一个TLRs相关蛋白,其与自身免疫性疾病或炎症疾病紧密相关[42]。长时间使用糖皮质激素可导致TLR4/NF-κB信号通路异常激活,糖皮质激素可以发挥该通路的炎症作用,同时扰乱正常的生理免疫应答,诱导疾病的发生。田雷等[43]成功建立了大鼠激素性股骨头坏死动物模型,并证明激素导致TLR4信号通路过度激活而介导激素性股骨头坏死的发生。同样,TIAN等[44]采用免疫组化、实时定量PCR和Western blot检测证明皮质类固醇可通过TLR4信号通路干扰免疫反应,诱发股骨头坏死。可见,TLR4/NF-κB在股骨头坏死的发生及发展中有着重要的作用位置。因此,在TLR4/NF-κB通路中找到治疗股骨头坏死潜在的作用靶点意义重大。 TLR4/NF-κB通路在骨形成方面,众所周知,Wnt/β-catenin途径可以直接影响成骨细胞分化增殖,然而TLR4/NF-κB通路与Wnt/β-catenin途径可以相互影响、相互作用。PEI等[45]研究报道TLR4 /NF-κB的过度激活可能抑制Wnt/β-catenin通路并诱导激素性股骨头坏死发生,未来可针对TLR4/NF-κB作为激素性股骨头坏死的新型治疗策略。活血化瘀中药可抑制TLR4/NF-κB通路的相关蛋白表达,进而发挥其生物活性作用。刘金富等[46]研究发现通络生骨胶囊主要成分为木豆叶,具有显著的活血化瘀,止痛、健骨作用,研究者通过Western Blot检测TLR4蛋白表达量证明,通络生骨胶囊治疗激素性股骨头坏死的机制与抑制TLR4信号通路有关。对于血管再生,TLR4/NF-κB通路与VEGF的关系密不可分,研究表明刺激增加了NF-κB与 HIF-1α启动子的相互作用,导致启动子活性增强和HIF-1α mRNA水平增加,进而使VEGF 表达以及HIF-1活性增强,促进血管生成[47],达到治疗疾病目的。 (6)调控TGF-β/Smad信号通路:TGF-β/Smad信号通路主要参与成骨细胞分化增殖[48], 转化生长因子β(transforming growth factor-β,TGF-β)家族中包括33个成员,且均为二聚体的分泌型多肽,其中包括TGF-β1、TGF-β2、TGF-β3及骨形态蛋白(bone morphogenetic protein,BMP)及其他亚家族。其中BMP2是BMP家族中成骨诱导作用最强的一型,广泛用于骨坏死及缺损修复疾病中。此外,研究发现BMP不仅可以激活TGF-β/Smad信号通路促进骨再生,还可加强与Wnt通路之间的联系,通过积累β-catenin和下调GSK-3β来激活Wnt通路,从而促进成骨分化[49],达到防治激素性股骨头坏死目的。YANG等[50]发现将大鼠使用淫羊藿与女贞子联合治疗后,增加了TGF-β、Smad的蛋白表达量,促进骨形成,减少了骨丢失,平衡骨代谢过程,进一步说明活血化瘀中药可通过该信号通路达到治疗激素性股骨头坏死的目的。另外,CHEN等[51]选择活骨Ⅰ号(主要由党参、赤芍、桂枝、当归、川芎、熟地黄等中药组成),其活血祛瘀、通阳化气、补血化血等作用显著,可增加雌性来亨鸡激素性股骨头坏死模型中的TGF-β1、Smad4表达,进而促进坏死股骨头的修复,同时发现在实验第8周蛋白表达变化更为显著,治疗效果更明显。 (7)调控Notch信号通路:Notch信号通路主要有4种受体,分别为Notch1、Notch2、Notch3、Notch4,是一种高保守信号通路。Notch信号通路在调控成骨细胞分化及维持骨代谢过程中也发挥着重要作用,有学者从骨碎补中分离提取了活性成分柚皮苷,发现使用柚皮苷后,其成骨作用部分涉及Notch信号通路[52]。可见,活血化瘀中药激活Notch通路可促进成骨细胞分化,进一步可以预防激素性股骨头坏死,并且可能是治疗股骨头疾病的有效选择[53]。目前对Notch信号通路与成骨分化关系的研究较少,未来值得进一步深入研究其与激素性股骨头坏死的确切关系。 活血化瘀中药调控信号通路及靶点促进成骨作用的研究汇总,见表3。"


2.2 PRP技术防治激素性股骨头坏死的研究 2.2.1 PRP对激素性股骨头坏死的成骨作用 PRP最早在口腔、整形科被广泛应用,其应用在骨科中始于21世纪初[54]。在运动医学领域,局部注射PRP能够增强受损的肌腱、韧带等软组织愈合,加速受损组织的修复。对于创伤及骨关节炎疾病,PRP技术具有显著的骨、软骨再生修复及血管再生作用,加速疾病愈合。近年来,越来越多的临床证据表明,PRP 可缓解股骨头坏死患者的疼痛、延缓疾病进展,在治疗该疾病中发挥有效作用[55]。激素性股骨头坏死的病理机制主要是由于股骨头坏死区域的成骨细胞和血管缺失,PRP作为自体血小板浓缩物,其血小板中包括许多α颗粒结构,α颗粒可释放高浓度细胞生长因子,如TGF-β、血小板衍生生长因子、成纤维细胞生长因子(fibroblast growth factor,FGF)、胰岛素样生长因子(insulin-like growth factor,IGF)及VEGF等[56],这些生长因子均有助于对骨细胞及前成骨细胞的增殖起促进作用[57]。张波等[58]研究发现,PRP可提高兔血清中的VEGF含量,同时PRP使骨髓腔内骨小梁变粗、脂肪细胞减少、骨细胞增多,并通过调节BMP-2/Smads信号通路,促进股骨头成骨细胞增殖,减少骨陷窝空缺率,缓解激素性股骨头坏死发展。 2.2.2 PRP对血管再生作用 另一方面,有研究报道,α颗粒释放的VEGF是血管生成途径中的重要信号分子,局部注射PRP可以加速外科血管生成,重建血供系统[59],从而改善股骨头坏死区的血供情况,为成骨细胞的形成创造良好的条件。TONG等[60]发现PRP处理的骨坏死小鼠血清中糖皮质激素的浓度显著降低,且PRP是通过促进血管再生成对股骨头坏死的小鼠发挥有益作用。此外,其他生长因子,如血小板衍生生长因子、TGF-β也可刺激新生血管的形成[61]。值得一提的是,血管再生与新骨形成之间密不可分,血管再生是新骨形成的关键条件。另一方面,PRP技术在调节脂代谢过程及血液异常状态中也表现出一定的生物活性作用,进而可以减轻激素性股骨头坏死病情进一步发展。LIU等[62]使用PRP技术通过促进脂肪细胞中的成骨细胞分化,且在动物实验中发现PRP治疗可通过促进骨再生发挥其作用,同时还能抑制骨髓内脂肪细胞的形成。研究表明,经PRP技术治疗股骨头坏死兔模型后,可明显改善血液流变学指标,且增加了血清中VEGF含量,修复局部受损血管,促进成骨相关和血管生成相关因子的表达,以达到缓解股骨头坏死的目的[63]。同时,XU等[64]通过PRP注射治疗SD大鼠激素性股骨头坏死模型,发现PRP技术不仅可以显著提高血液流变学指标、VEGF水平及β-catenin蛋白表达,同时还降低了血液中的甘油三酸酯和总胆固醇水平,首次证明PRP通过刺激成骨形成和血管再生以及阻止脂肪生成来防治激素性股骨头坏死的发展。 2.2.3 PRP的抗炎作用 炎症作用亦是形成激素性股骨头坏死的众多因素之一,同时炎症因子也会破坏正常的血管内皮,导致血管损伤,最终形成一系列并发症,且激素药物在炎症作用中发挥其核心作用。研究表明,激素性股骨头坏死与滑膜炎有关,因坏死病灶和滑膜中都存在炎症细胞和促炎细胞因子[65]。ADAPALA等[66]发现一些促炎细胞因子,如白细胞介素1β、肿瘤坏死因子α和白细胞介素6在坏死股骨头中的表达显著增加,证明其均参与股骨头坏死的病理过程。PRP技术可以降低炎症因子的表达,进一步下调炎症反应程度,中断炎症作用延缓激素性股骨头坏死病情发展,从而起到防治作用。研究者已在动物实验中发现,经PRP技术治疗的激素性股骨头坏死模型小鼠体内的炎症因子,白细胞介素17A、白细胞介素1β、肿瘤坏死因子α、核因子κB配体受体激活因子、白细胞介素6和干扰素γ表达均下调,减轻了其炎症反应,证明PRP技术可缓解激素性股骨头坏死病情,同时与对照组相比发现,PRP干预组小鼠血清中的糖皮质激素浓度明显降低[60]。总体来说,PRP技术能够通过改善血液异常状态、促进血管再生及成骨分化增殖、调控脂代谢、缓解炎症反应等方面防治激素性股骨头坏死。 2.3 活血化瘀中药联合PRP技术的应用前景 现代研究表明,在激素性股骨头坏死的治疗过程中,恢复血供、促进血管再生是治疗关键。无论是活血化瘀中药单体,还是中药复方,基本都是通过恢复或重建股骨头内坏死区域血运、改善骨代谢,促进成骨分化,增加骨形成,有效防治激素性股骨头坏死。PRP也具有促进成骨生成及血管再生等重要功能,其也可从根本上解决股骨头坏死过程中“血运”“股骨头塌陷”两个主要问题,恢复股骨头内坏死区域的正常血运情况,提高股骨头成活率[67]。且目前用于治疗该病的主要中药包括牛膝、骨碎补、淫羊藿、红花[68]、莪术、姜黄、木鳖子、天葵子、赤芍、丹参等,其都具有活血化瘀、消肿止痛等功效。根据中医理论认为,红花作为一种活血化瘀的中药在中国和许多其他亚洲国家被广泛使用[69],其成分十分复杂,主要包括醌式查尔酮苷类、黄酮类、脂肪酸类、生物碱类、木脂素类、甾醇类、有机酸类、聚炔类、多糖类、亚精胺类等,其作用广泛,具有抗凝、抗血栓、抗炎、抗氧化性、对脑血管系统及神经系统的保护、镇痛、降血脂、降血压、抗肿瘤、抗衰老、兴奋子宫、抗菌等多方的作用,并且红花是当前是骨组织活血中应用相对较多的活性成分[70]。作者所在课题组从红花中分离提取纯化得到的红花多糖,将该多糖作用在激素性股骨头坏死细胞模型中,发现红花多糖可通过抑制caspsae-3介导的细胞凋亡来缓解地塞米松相关的骨坏死[71];在进一步的动物实验中发现,对激素性股骨头坏死小鼠模型分别胃内灌药质量浓度为25 mg/kg和100 mg/kg红花多糖,连续60 d治疗发现股骨头内细胞凋亡率明显逆转,证明活血化瘀中药治疗激素性股骨头坏死效果显著[72]。2020年,作者课题组进一步研究证明了红花多糖防治激素性股骨头坏死的疗效,分别以25,100和200 mg/kg的红花多糖连续给药60 d治疗激素性股骨头坏死兔模型,通过空骨陷窝率、平均骨髓脂肪细胞大小的下降证明了股骨头异常组织病理学改变和凋亡得到了明显恢复,同时证实红花多糖的使用显著降低了Bax和caspase-3蛋白的表达,并增加了Bcl-2的蛋白表达[73],Bax蛋白、caspase-3蛋白都可以诱导细胞凋亡,而Bcl-2蛋白是一种癌基因,具有明显的抑制细胞凋亡作用,进而达到红花多糖防治激素性股骨头坏死作用。 活血化瘀中药及PRP均具有促进坏死区域股骨血管再生、重建血供微循环的作用。PRP可以通过启动和调节增殖、分化和增加血管生成的各种细胞因子水平,另外,PRP除了自身含有丰富的高浓度细胞生长因子外,还可以上调VEGF表达。值得一提的是,虽然PRP自身含有各种高浓度的细胞生长因子,每种因子均可诱导血管修复再生及成骨作用,一旦超过规定的阈值范围则可能抑制骨形成,加速骨吸收过程。活血化瘀中药与PRP联合治疗方法在临床中较为罕见,且PRP常常应用于股骨头坏死的保髋治疗当中,如髓芯减压联合PRP保髋治疗。利用活血化瘀中药独特的药理性质与PRP生物作用,二者联合治疗在临床中应能取得更加明显的治疗效果,徐辉辉等[74]报道,桃红四物汤作为活血化瘀中药的代表,与PRP技术联合治疗可以发挥其强效的成骨及血管再生作用,治疗效果更佳显著;且通过动物实验证明PRP联合桃红四物汤可以对VEGF、β-catenin蛋白的分泌起到正向作用,从而提高新血管和新骨形成效率,改善股骨头内的血运情况,促进坏死区成骨,进而修复激素性股骨头坏死。Sun等[75]发现补肾活血法联合PRP可以降低血清中的炎症因子白细胞介素1、白细胞介素6水平,也可增加VEGF表达,从而促进血管再生,恢复股骨头内的血供,达到治疗目的。对于二者联合治疗过程,活血化瘀中药在股骨头坏死早期的恢复中效果定不如PRP明显,中医药药效需长期使用才能够完全表现出来,此时对于股骨头坏死患者早期恢复阶段而言,完全是PRP技术发挥其自身生物活性作用,二者联合治疗,可相互辅佐,发挥二者强劲的生物作用,以达到更加明显的激素性股骨头坏死治疗效果。因此,今后研究者应结合现代科研方法加强对活血化瘀中药单体成分的分离提取,中国拥有丰富的中药资源,应该充分利用,以此寻找多方位、多效应、不良反应小、成本低的中药与PRP技术联合治疗激素性股骨头坏死,发挥二者强劲的血管再生及成骨作用,进而恢复或重建股骨头内血运、促进成骨分化、改善血液异常状态,共同防治激素性股骨头坏死,延缓激素性股骨头坏死进一步发展。活血化瘀中药联合PRP技术具有作用明确、效果显著的特点,应用前景十分广阔,值得临床推广。"

| [1] 李泰贤,陈志伟,王荣田,等.基于文献计量学分析中医药治疗股骨头坏死的研究现状[J].中国中医骨伤科杂志,2017,25(4):41-46. [2] LI SM, XU H, CHEN KJ. The diagnostic criteria of blood-stasis syndrome: considerations for standardization of pattern identification. Chin J Integr Med. 2014;20(7):483-489. [3] 包杭生,李逸群,涂泽松.血液流变学在骨伤科疾病中的应用[J].中国中医骨伤科杂志,2010,18(10):67-69. [4] HUANG YX, XU DQ, YUE SJ, et al. Deciphering the Active Compounds and Mechanisms of Qixuehe Capsule on Qi Stagnation and Blood Stasis Syndrome: A Network Pharmacology Study. Evid Based Complement Alternat Med. 2020;2020:5053914. [5] 田伟明,王文智,王鑫国.骨复活汤对激素性股骨头坏死血液流变学及脂代谢的影响[J].中国中药杂志,2002,27(10):769-771. [6] 段卫峰,刘骏逸,杜志军,等.补肾祛瘀法对激素诱导股骨头坏死兔血脂及凝血指标的影响[J].西部中医药,2019,32(11):26-31. [7] 齐振熙,曹阳.活血化瘀中药防治激素性股骨头缺血性坏死的实验研究[J]中国临床康复,2001,5(24):118-119. [8] 方圣杰,章轶立,朱嘉,等.糖皮质激素抑制Leptin,VEGF蛋白表达诱导骨质疏松作用机制研究[J].中国骨质疏松杂志,2022,28(3):320-324,367. [9] SUZUKI O, BISHOP AT, SUNAGAWA T, et al. VEGF-promoted surgical angiogenesis in necrotic bone. Microsurgery. 2004;24(1):85-91. [10] YE J, WEI D, PENG L, et al. Ginsenoside Rb1 prevents steroid‑induced avascular necrosis of the femoral head through the bone morphogenetic protein‑2 and vascular endothelial growth factor pathway. Mol Med Rep. 2019;20(4):3175-3181. [11] LEUNG KW, NG HM, TANG MK, et al. Ginsenoside-Rg1 mediates a hypoxia-independent upregulation of hypoxia-inducible factor-1α to promote angiogenesis. Angiogenesis. 2011;14(4):515-522. [12] LEUNG KW, PON YL, WONG RN, et al. Ginsenoside-Rg1 induces vascular endothelial growth factor expression through the glucocorticoid receptor-related phosphatidylinositol 3-kinase/Akt and beta-catenin/T-cell factor-dependent pathway in human endothelial cells. J Biol Chem. 2006;281(47):36280-36288. [13] LI JH, WU YL, YE JH, et al. Effects of blood-activating and stasis-removing drugs combined with VEGF gene transfer on angiogenesis in ischemic necrosis of the femoral head. J Tradit Chin Med. 2009;29(3):216-219. [14] 史风雷,任丽霞,孙升云,等.复方丹参注射液预防激素性股骨头坏死的初步研究[J].中医正骨,2002,14(4):3-5. [15] 李峻辉,栾晓文,宁亚功,等. 补肾活骨方对激素性股骨头坏死模兔血液流变学及血脂影响的研究[J].中国中医基础医学杂志,2002,8(7):20-22. [16] JIANG Y, ZHANG Y, ZHANG H, et al. Pravastatin prevents steroid-induced osteonecrosis in rats by suppressing PPARγ expression and activating Wnt signaling pathway. Exp Biol Med (Maywood). 2014;239(3):347-355. [17] PUTNAM SE, SCUTT AM, BICKNELL K, et al. Natural products as alternative treatments for metabolic bone disorders and for maintenance of bone health. Phytother Res. 2007;21(2):99-112. [18] YUN SI, YOON HY, JEONG SY, et al. Glucocorticoid induces apoptosis of osteoblast cells through the activation of glycogen synthase kinase 3beta. J Bone Miner Metab. 2009;27(2):140-148. [19] 高彦淳,冯勇,张长青.激素性股骨头坏死发生机制的研究进展[J].国际骨科学杂志,2018,39(4):231-234 [20] JIA D, O’BRIEN CA, STEWART SA, et al. Glucocorticoids act directly on osteoclasts to increase their life span and reduce bone density. Endocrinology. 2006;147(12):5592-5599. [21] GAO ZR, FENG YZ, ZHAO YQ, et al. Traditional Chinese medicine promotes bone regeneration in bone tissue engineering. Chin Med. 2022;17(1):86. [22] CLEVERS H, NUSSE R. Wnt/β-catenin signaling and disease. Cell. 2012;149(6):1192-1205. [23] 吴忠书,韦雨柔,陈哓俊,等.活血通络胶囊促进骨髓间充质干细胞成骨中的ERα-Wnt/β-catenin信号通路[J].中国组织工程研究,2022,26(25):3937-3943. [24] 陈杰,张堃,孔令俊,等.三七总皂苷通过调控Wnt/β-catenin通路减轻家兔股骨头坏死[J].中药药理与临床,2019,35(4):95-99. [25] HUANG W, JIN S, YANG W, et al. Protective effect of Agrimonia pilosa polysaccharides on dexamethasone-treated MC3T3-E1 cells via Wnt/β-Catenin pathway. J Cell Mol Med. 2020;24(3):2169-2177. [26] LO WW, WUNDER JS, DICKSON BC, et al. Involvement and targeted intervention of dysregulated Hedgehog signaling in osteosarcoma. Cancer. 2014;120(4):537-547. [27] 迟博婧,刘光源,邢磊,等. Hedgehog 信号通路调控骨形成及BMSCs成骨分化的研究进展[J].中国修复重建外科杂志,2016,30(12):1545-1550. [28] 吴修团,李文良,谢柳蓉,等. Hedgehog 信号通路调节成骨细胞 RANKL表达的研究进展[J].中国组织工程研究,2017,21(8):1294-1300. [29] 梁学振,杨曦,李嘉程,等.补肾活血胶囊介导Hedgehog信号通路调控大鼠骨髓间充质干细胞成骨成脂分化 [J].中国组织工程研究,2022,26(7):1020-1026. [30] 邓洋洋,刘明欣,孙鑫,等.Hedgehog信号通路与“肾虚血瘀”骨代谢失常的实验研究[J].中国骨质疏松杂志,2021,27(8):1112-1116. [31] MA X, LIU Y, ZHANG Y, et al. Jolkinolide B inhibits RANKL induced osteoclastogenesis by suppressing the activation NF-κB and MAPK signaling pathways. Biochem Biophys Res Commun. 2014;445(2):282-288. [32] 李永志,董博,欧国峰,等.骨复生对激素性股骨头坏死大鼠骨组织中OPG及RANK表达的影响[J].中国中医骨伤科杂志,2018,26(11):1-6. [33] 宋红梅,魏迎辰,吴斌,等.温阳补肾方对兔激素性股骨头坏死组织RANKL/RANK/OPG通路的影响[J].中华中医药杂志,2016,31(1):302-305. [34] SONG HM, WEI YC, LI N, et al. Effects of Wenyangbushen formula on the expression of VEGF, OPG, RANK and RANKL in rabbits with steroid-induced femoral head avascular necrosis. Mol Med Rep. 2015;12(6):8155-8161. [35] JIANG Y, ZHANG Y, CHEN W, et al. Achyranthes bidentata extract exerts osteoprotective effects on steroid-induced osteonecrosis of the femoral head in rats by regulating RANKL/RANK/OPG signaling. J Transl Med. 2014;12:334. [36] KAR S, SAMII A, BERTALANFFY H. PTEN/PI3K/Akt/VEGF signaling and the cross talk to KRIT1, CCM2, and PDCD10 proteins in cerebral cavernous malformations. Neurosurg Rev. 2015;38(2):229-236;discussion 236-237. [37] CAO F, QIN KR, KANG K, et al. Ginkgo biloba L. extract prevents steroid-induced necrosis of the femoral head by rescuing apoptosis and dysfunction in vascular endothelial cells via the PI3K/AKT/eNOS pathway. J Ethnopharmacol. 2022;296:115476. [38] LV W, YU M, YANG Q, et al. Total flavonoids of Rhizoma drynariae ameliorate steroid‑induced avascular necrosis of the femoral head via the PI3K/AKT pathway. Mol Med Rep. 2021;23(5):345. [39] XUE XH, FENG ZH, LI ZX, et al. Salidroside inhibits steroid-induced avascular necrosis of the femoral head via the PI3K/Akt signaling pathway: In vitro and in vivo studies. Mol Med Rep. 2018;17(3):3751-3757. [40] YANG Q, YIN W, CHEN Y, et al. Betaine alleviates alcohol-induced osteonecrosis of the femoral head via mTOR signaling pathway regulation. Biomed Pharmacother. 2019;120:109486. [41] 朱道宇,杨前昊,高悠水,等.TLR4通路与激素性股骨头坏死关系的研究进展[J].中国骨与关节杂志,2019,8(1):75-79. [42] LI H, SUN B. Toll-like receptor 4 in atherosclerosis. J Cell Mol Med. 2007;11(1):88-95. [43] 田雷,周东生,孙水,等.Toll样受体4信号通路过度激活在大鼠激素性股骨头坏死中的作用[J].西安交通大学学报(医学版),2014,35(5):622-629. [44] TIAN L, WEN Q, DANG X, et al. Immune response associated with Toll-like receptor 4 signaling pathway leads to steroid-induced femoral head osteonecrosis. BMC Musculoskelet Disord. 2014;15;15:18. [45] PEI J, FAN L, NAN K, et al. Excessive Activation of TLR4/NF-κB Interactively Suppresses the Canonical Wnt/β-catenin Pathway and Induces SANFH in SD Rats. Sci Rep. 2017;7(1):11928. [46] 刘金富,曾平,农焦,等.通络生骨胶囊对激素性股骨头坏死模型大鼠Toll样受体4信号通路的影响[J].中国组织工程研究,2021,25(26):4150-4155. [47] RIDDELL JR, MAIER P, SASS SN, et al. Peroxiredoxin 1 stimulates endothelial cell expression of VEGF via TLR4 dependent activation of HIF-1α. PLoS One. 2012;7(11): e50394. [48] 王楠锴,刘浩,张天久,等.转化生长因子β信号通路相关因子在幼兔激素性股骨头坏死模型中的表达及意义[J].中华实用儿科临床杂志,2021,36(23):1811-1814. [49] QIAN C, ZHU C, YU W, et al. Bone morphogenetic protein 2 promotes osteogenesis of bone marrow stromal cells in type 2 diabetic rats via the Wnt signaling pathway. Int J Biochem Cell Biol. 2016;80:143-153. [50] YANG Y, NIAN H, TANG X, et al. Effects of the combined Herba Epimedii and Fructus Ligustri Lucidi on bone turnover and TGF-β1/Smads pathway in GIOP rats. J Ethnopharmacol. 2017;201:91-99. [51] CHEN WH, KONG XY, WAN R, et al. Effects of huogu I formula (I) on correlated factors of bone regeneration in chickens with steroid-induced necrosis of femoral head. Chin J Integr Med. 2012;18(5):378-384. [52] YU GY, ZHENG GZ, CHANG B, et al. Naringin Stimulates Osteogenic Differentiation of Rat Bone Marrow Stromal Cells via Activation of the Notch Signaling Pathway. Stem Cells Int. 2016;2016:7130653. [53] HUANG D, LI Z, CHEN B, et al. Naringin protects against steroid‑induced avascular necrosis of the femoral head through upregulation of PPARγ and activation of the Notch signaling pathway. Mol Med Rep. 2018;17(2):3328-3335. [54] 刘禄林,黄为民,刘午阳.富血小板血浆治疗早期股骨头缺血性坏死的研究进展[J]. 赣南医学院学报,2022,42(4):399-403,410. [55] HAN J, GAO F, LI Y, et al. The Use of Platelet-Rich Plasma for the Treatment of Osteonecrosis of the Femoral Head: A Systematic Review. Biomed Res Int. 2020;2020:2642439. [56] EVERTS P, ONISHI K, JAYARAM P, et al. Platelet-Rich Plasma: New Performance Understandings and Therapeutic Considerations in 2020. Int J Mol Sci. 2020;21(20):7794. [57] 吴晓斌,刘朝阳.股骨头坏死手术治疗及其自体PRP在保髋手术中的应用进展[J].中国骨科临床与基础研究杂志,2017,9(3):186-191. [58] 张波,韦冰丹,甘坤宁,等.富血小板血浆联合骨髓间充质干细胞对兔股骨头坏死BMP-2/Smads通路的影响[J].中国骨质疏松杂志,2016,22(2):131-134,227. [59] YOKOTA K, ISHIDA O, SUNAGAWA T, et al. Platelet-rich plasma accelerated surgical angio-genesis in vascular-implanted necrotic bone: an experimental study in rabbits. Acta Orthop. 2008;79(1):106-110. [60] TONG S, YIN J, LIU J. Platelet-rich plasma has beneficial effects in mice with osteonecrosis of the femoral head by promoting angiogenesis. Exp Ther Med. 2018;15(2):1781-1788. [61] WU PI, DIAZ R, BORG-STEIN J. Platelet-Rich Plasma. Phys Med Rehabil Clin N Am. 2016;27(4):825-853. [62] LIU HY, WU AT, TSAI CY, et al. The balance between adipogenesis and osteogenesis in bone regeneration by platelet-rich plasma for age-related osteoporosis. Biomaterials. 2011;3(28):6773-6780. [63] ZHANG XL, SHI KQ, JIA PT, et al. Effects of platelet-rich plasma on angiogenesis and osteogenesis-associated factors in rabbits with avascular necrosis of the femoral head. Eur Rev Med Pharmacol Sci. 2018;22(7):2143-2152. [64] XU H, LI S, FANG L, et al. Platelet- rich plasma promotes bone formation, restrains adipogenesis and accelerates vascularization to relieve steroids-induced osteonecrosis of the femoral head. Platelets (Edinburgh). 2021;32(7):950-959. [65] YAMAGUCHI R, KAMIYA N, ADAPALA NS, et al. HIF-1-Dependent IL-6 Activation in Articular Chondrocytes Initiating Synovitis in Femoral Head Ischemic J Bone Joint Surg Am. 2016;98(13):1122-1131. [66] ADAPALA NS, YAMAGUCHI R, PHIPPS M, et al. Necrotic Bone Stimulates Proinflammatory Responses in Macrophages through the Activation of Toll-Like Receptor 4. Am J Pathol. 2016;186(11):2987-2999. [67] 沈烈军,李展振.股骨头坏死的减压植骨联合唑来膦酸和富血小板血浆[J].中国矫形外科杂志,2022,30(9):785-790. [68] 洪坤豪,马振尉,刘军,等.基于数据挖掘的股骨头坏死用药规律研究 [J].世界中西医结合杂志,2015,10(8):1042-1044. [69] XIA Q, MA Z, MEI X, et al. Assay for the developmental toxicity of safflower(Carthamus tinctorius L.) to zebrafish embryos/larvae. J Traditional Chin Med Sci. 2017;4(1):71-81. [70] ZHANG LL, TIAN K, TANG ZH, et al. Phytochemistry and Pharmacology of Carthamus tinctorius L. Am J Chin Med. 2016;44(2):197-226. [71] CUI D, ZHAO D, WANG B, et al. Safflower (Carthamus tinctorius L.) polysaccharide attenuates cellular apoptosis in steroid-induced avascular necrosis of femoral head by targeting caspase-3-dependent signaling pathway. Biol Macromol. 2018;116:106-112. [72] CUI D, ZHAO D, HUANG S. Beneficial contribution of a safflower (Carthamus tinctorius L.) polysaccharide on steroid-induced avascular necrosis of the femoral head in rats. Int J Biol Macromol. 2019;123:581-586. [73] CUI D, ZHAO D, HUANG S. Structural characterization of a safflower polysaccharide and its promotion effect on steroid-induced osteonecrosis in vivo. Carbohydr Polym. 2020;233:115856. [74] 徐辉辉,李索咪,范梦强,等.富血小板血浆联合桃红四物汤对激素性股骨头坏死大鼠股骨头组织VEGF、CD31、ALP、β-catenin蛋白表达的影响[J].中华中医药杂志,2020,35(3):1501-1504. [75] SUN Z, SU W, WANG L, et al. Clinical Effect of Bushen Huoxue Method Combined with Platelet-Rich Plasma in the Treatment of Knee Osteoarthritis and Its Effect on IL-1, IL-6, VEGF, and PGE-2. J Healthc Eng. 2022;2022:9491439. |
| [1] | Lin Tianye, Wu Zhiming, Zhang Wensheng, He Xiaoming, He Mincong, Zhang Qingwen, He Wei, Wei Qiushi, Li Ziqi. Mechanism of compound Shengmai Chenggu capsule in the repair of steroid-induced osteonecrosis of the femoral head [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(2): 200-207. |
| [2] | Ma Suilu, He Zhijun, Liu Tao, Li Yan, He Yuanxu, He Bo, Wang Weiwei, Wei Xiaotao. Traditional Chinese medicine monomer in the prevention and treatment of flap necrosis by regulating “autophagy” [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(1): 153-158. |
| [3] | Sun Jing, Liao Jian, Sun Jiangling, Cheng Ping, Feng Hongchao. Recombinant human growth hormone promotes osteogenic differentiation of human dental pulp stem cells [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(1): 56-61. |
| [4] | Zheng Hongrui, Zhang Wenjie, Wang Yunhua, He Bin, Shen Yajun, Fan Lei. Femoral neck system combined with platelet-rich plasma in the treatment of femoral neck fracture [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(9): 1390-1395. |
| [5] | Tang Liang, Li Xiheng, Niu Ruijuan, Li Xinyue, Zou Xinying, Mao Tianjiao, Li Jiang. Naringin regulates the function of RAW264.7 macrophages to affect the osteogenic differentiation of MC-3T3-E1 cells [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(8): 1205-1210. |
| [6] | Lian Shilin, Zhang Yan, Jiang Qiang, Zhang Hanshuo, Li Tusheng, Ding Yu. Interventional effects of whole blood and platelet-rich plasma with different preparation methods on nucleus pulposus cells [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(8): 1199-1204. |
| [7] | Xu Xingxing, Wen Chaoju, Meng Maohua, Wang Qinying, Chen Jingqiao, Dong Qiang. Carbon nanomaterials in oral implant [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1062-1070. |
| [8] | Tang Haotian, Liao Rongdong, Tian Jing. Application and design of piezoelectric materials for bone defect repair [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1117-1125. |
| [9] | Xu Yan, Li Ping, Lai Chunhua, Zhu Peijun, Yang Shuo, Xu Shulan. Piezoelectric materials for vascularized bone regeneration [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1126-1132. |
| [10] | Song Li, Lu Mao, Tang Yi, Liu Yanlin. A systemic review of the effectiveness and safety of fractional CO2 laser combined with platelet-rich plasma in the treatment of atrophic acne scars [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(35): 5734-5740. |
| [11] | Xu Zhengyi, Wan Qianbing, Chen Junyu. Natural small molecular compounds in the treatment of bone-related diseases by regulating type H blood vessels and its application in tissue engineering [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(34): 5546-5553. |
| [12] | Zhao Mingyue, Yang Shun, Tu Xiling, Gao Li, Yang Kun, Liu Qi. Application of platelet-rich plasma combined with electrospun nanoscaffolds in bone and soft tissue [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(34): 5554-5560. |
| [13] | Ning Ziwen, Wang Xu, Shi Zhengliang, Qin Yihua, Wang Guoliang, Jia Di, Wang Yang, Li Yanlin. Meniscal injury repair methods for non-blood supply area [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(3): 420-426. |
| [14] | Zhang Lichen, Chen Liang, Gu Yong. Inorganic ion bionic periosteum regulates immune microenvironment to promote bone repair [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(3): 346-353. |
| [15] | Tian Yuyi, Liu Lihong. Osteoimmunological effects of macrophages [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(29): 4712-4722. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||