Chinese Journal of Tissue Engineering Research ›› 2024, Vol. 28 ›› Issue (2): 295-301.doi: 10.12307/2023.863
Previous Articles Next Articles
Atg-mediated autophagy, exercise and skeletal muscle aging
Wang Jingfeng, Wen Dengtai, Wang Shijie, Gao Yinghui
- College of Physical Education, Ludong University, Yantai 264025, Shandong Province, China
-
Received:2022-11-24Accepted:2023-01-04Online:2024-01-18Published:2023-06-30 -
Contact:Wen Dengtai, PhD, Associate professor, Master’s supervisor, College of Physical Education, Ludong University, Yantai 264025, Shandong Province, China -
About author:Wang Jingfeng, Master candidate, College of Physical Education, Ludong University, Yantai 264025, Shandong Province, China -
Supported by:National Natural Science Foundation of China, No. 32000832 (to WDT); Natural Science Foundation of Shandong Province, No. ZR2020QC096 (to WDT)
CLC Number:
Cite this article
Wang Jingfeng, Wen Dengtai, Wang Shijie, Gao Yinghui. Atg-mediated autophagy, exercise and skeletal muscle aging[J]. Chinese Journal of Tissue Engineering Research, 2024, 28(2): 295-301.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
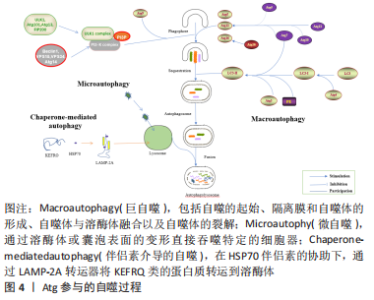
2.1 Atg基因与自噬过程 Atg基因在进化过程中是高度保守的,从酵母和果蝇到脊椎动物和人类中都可以找到参与自噬的同源基因。自噬途径由一组高度有序的连续阶段组成,负责吸引和破坏错误折叠的蛋白质,以及回收分解的废物。已经确定了3种类型的自噬:微自噬、伴侣素介导的自噬和巨自噬[1-2],一般来说,自噬是指巨自噬。Atg蛋白在自噬的连续过程中参与并相互作用(图4)。在自噬体构建之前,ULK/Atg1复合物被激活以介导自噬信号。下游Atg蛋白和上游营养或能量整合器哺乳动物雷帕霉素靶蛋白(mammalian target of rapamycin,mTOR)参与自噬体的创建,ULK/Atg1复合物作为二者之间的桥梁,可使各种下游蛋白磷酸化[1]。其中,ULK1/2是自噬信号通路中唯一具有丝氨酸/苏氨酸激酶活性的核心蛋白[3]。囊泡成核导致形成一个孤立的吞噬细胞集群[4]。在成核阶段,即ULK/Atg1复合物产生后,Ⅲ类磷脂酰肌醇激酶复合物C1(class III phosphatidylinositol kinase complex C1,PI3KC3-C1)的发展是一个关键过程[5-6]。为了将磷脂酰肌醇(phosphatidyl inositol,PI)转化为磷脂酰肌醇3磷酸 (phosphatidyl inositol 3 phosphate,PI3P),PI3KC3-C1被激活并被运送到内质网和线粒体上的吞噬核部位[7]。囊泡成核后,细胞质中的吞噬团伸长并扩大,以双膜杯状包围着其间物质[8]。"
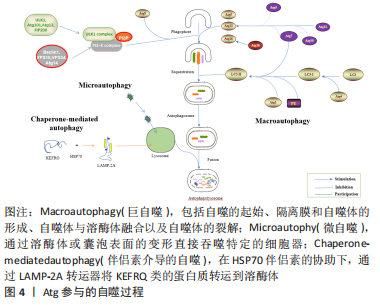
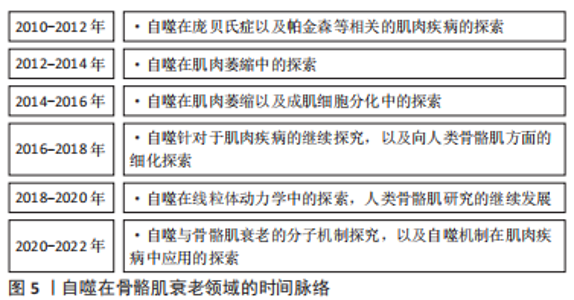
Atg12、微管相关蛋白1轻链3α/β(microtubule Associated protein 1 light chain 3 Alpha/Beta,MAP1LC3A/MAP1LC3B)和LC3是酵母Atg8的人类同源物[9-10],它在吞噬细胞膜的伸长和扩张中起着关键作用。Atg12与Atg5共轭,由Atg7和Atg10介导,然后与Atg16进行非共价作用[11-12]。Atg4的半胱氨酸肽酶在C端裂解LC3,产生LC3-Ⅰ,然后在一个类似泛素化的过程中与磷脂酰乙醇胺(phosphatidyl ethanolamine,PE)相连,期间需要Atg7和Atg3来产生LC3-Ⅱ[1,13]。吞噬细胞在成熟阶段的闭合导致了细胞质成分的分离和自噬囊泡的形成,随着成熟过程的推进,自噬囊泡与内体、囊泡(酵母和植物)或溶酶体(动物细胞)融合形成自噬泡,导致内体及其内容物的分解;随之而来的分解代谢产物,如氨基酸和脂肪酸,被送回细胞质并在细胞代谢中加以利用,提供内部能量生产的来源和分解代谢的初始成分[1,14-15]。 2.2 自噬背景下骨骼肌细胞衰老的机制 近些年来自噬在骨骼肌衰老中的作用备受人们关注(图5),了解在自噬背景下骨骼肌衰老的细胞机制对于明确自噬对于骨骼肌的调节作用尤为重要。"
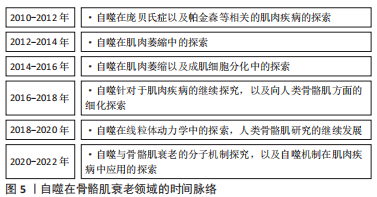

2.2.1 自噬与线粒体 线粒体功能失调被认为是导致生物衰老的主要因素之一,包括氧化能力下降和氧化损伤增加[16]。活性氧作为“氧化还原信使”,在正常生理环境下控制细胞内的信号传递,然而过多的活性氧会对细胞造成不可弥补的损害,并通过线粒体控制的内在凋亡途径导致细胞死亡。为了应对衰老过程中的氧化应激,自噬会消除受损的线粒体,并作为细胞清道夫和抗凋亡的防御措施[17]。线粒体生物生成和自噬之间存在着密切的关系。细胞的适应和抗压能力取决于这两个过程之间的平衡关系[18]。这种平衡的破坏可能是有害的,并导致线粒体损伤的积累,这可能加速人们增龄性的细胞凋亡[19]。线粒体功能障碍对骨骼肌衰老有着显著的影响[20]。最近的研究表明,由于线粒体自噬功能下降,衰老的骨骼肌会出现线粒体功能障碍的堆积[21-22]。保持适当的线粒体功能需要通过线粒体自噬来控制,此过程与通过线粒体融合以及裂解进行的形态调节同时发生[23]。裂解可能阻止健康细胞中线粒体的持续伸长,这可能会导致细胞衰老。自噬清除已受损的细胞器有助于延缓细胞衰老。在线粒体DNA异常患者的成肌纤维细胞中发现了对受损线粒体的选择性破坏(也被称为线粒体吞噬),并且在这些患者的细胞中,已经观察到了高于平均水平的自噬反应,这一点也证明了自噬在延缓骨骼肌衰老中的作用[24]。由上述结果不难看出,自噬与骨骼肌线粒体的功能结构有关,并随时影响骨骼肌衰老的走向。 2.2.2 自噬与卫星细胞 骨骼肌的再生依赖于卫星细胞(肌肉干细胞),尽管它们通常处于休眠状态[25]。随着年龄的增长,肌肉细胞的再生能力下降,卫星细胞停止休眠[26]。长时间的静止状态可以通过自噬来维持,并且干细胞需要自噬来消除静止阶段产生的细胞废物[27]。蛋白质和细胞器的周转是由基础自噬进行的,在静止的卫星细胞中是活跃的[26]。肌肉干细胞的再生速度随着人们的年龄增长而减慢[28],从正常静止状态转变为不可逆的衰老状态,这种减少随着年龄的增长体现的最为明显。生理衰老中卫星细胞自噬的异常或者年轻细胞自噬基因的损伤导致卫星细胞功能和数量的下降,通过蛋白质平衡的丧失、线粒体功能障碍和氧化压力的增加,最终导致衰老[29]。在针对于老年小鼠的研究中发现,基础自噬通量受损导致了受损蛋白质和亚细胞器(包括线粒体)的堆积[26],这些有害废物在卫星细胞中的堆积损害了它们的健康,使它们无法进入真正的静止状态。重组自噬功能可逆转衰老,并恢复老年卫星细胞的再生功能[29]。因此,自噬与肌肉再生有关,是决定肌肉干细胞的静止和衰老命运转变的关键因素之一[3]。 2.3 Atg基因介导的自噬与骨骼肌衰老 在进化保守的Atg基因的参与下,自噬是一个关键的分解代谢过程,影响骨骼肌的物质周转以及能量的产生和消耗。来自转基因动物模型的数据表明,运动产生的自噬对身体锻炼的适应是必要的[30]。由此,研究Atg基因如何在运动中影响骨骼肌意义深远。在此依据Atg基因(表1)的细胞成分将Atg基因分为4类阐述其介导的自噬在骨骼肌中的作用:Atg1/ULK1复合体、Atg5-12-16复合体、吞噬体组装位点、其他细胞成分。"


2.3.1 运动介导的Atg基因对骨骼肌衰老的影响 (1)Atg1/ULK1复合物(ULK1):有研究结果表明,短期有氧运动通过人类骨骼肌ULK1刺激自噬信号,这表明自噬的开始是人类对运动的一个重要生理反应。运动是一种常见的AMP依赖的蛋白激酶(adenosine 5‘-monophosphate (AMP)-activated protein kinase,AMPK)激活剂[31-32],在已有的研究中已经证实了这一点。在生物体内进行的研究显示,在耐力运动后,肌肉自噬增加,而来自培养细胞的研究结果表明,AMPK有能力使ULK1 Ser555位点磷酸化[33]。AMPK-Thr172是人类骨骼肌中ULK1 Ser555位点的上游激酶,并且AMPK-Thr172的增加与ULK1 Ser555的磷酸化程度之间存在正相关关系,这进一步证明了运动诱导的人体骨骼肌自噬是由AMPK-ULK1信号通路介导的[34]。在对小鼠肌肉的研究中表明,胰岛素刺激和急性运动会减少肌肉自噬体的数量,而运动训练可能会增加自噬体的合成能力。此外,运动时激活AMPK似乎不足以控制肌肉中自噬体的数量,而胰岛素限制自噬的能力可能是通过哺乳动物中雷帕霉素靶蛋白C1(mammalian target of rapamycin C1, mTORC1)的靶点ULK1介导的[35-36]。此外,ULK1与骨骼肌如何适应运动训练的代谢有关。在比较ULK1和ULK2在运动训练后对于骨骼肌胰岛素的改善作用的实验中发现Ulk1是必要的,而不是ULK2 [37],这进一步证实ULK1在运动时骨骼肌中的调节作用。 (2)Atg5-12-16复合物(Atg5/12/16):传统自噬的关键过程包括LC3的脂化和ATG12-ATG5/ATG16L1复合物的形成。LC3脂化所必需的E3类连接酶活动不能由ATG12-ATG5/ATG16L1复合物的单个成分完成[38]。这种联合作用的模式在体育训练中得到了深刻的体现。例如,在为期8周的阻力训练后,蛋白Atg5、Atg12和Atg16表达的上升[39]。另一方面,Atg12和Atg16似乎受到低级炎症的影响。最近的研究发现,各种分解代谢条件下的肌肉萎缩与促炎症细胞因子及其受体Fn14有关。Fn14敲除小鼠与野生型小鼠相比,泛素化蛋白水平和Atg12的表达急剧减少[40]。在评估高强度训练对与炎症和自噬相关的特定基因表达变化的影响的研究中,同样发现了ATG12、ATG16L1表达的变化(增加)[41]。 尽管一些研究涉及到ATG12-ATG5 /ATG16L1在骨骼肌中的一些变化,但直接涉及ATG12-ATG5 /ATG16L1在骨骼肌中作用机制的研究很少,需要进一步的实验探究。 (3)吞噬体组装位点(Beclin-1、Atg7/9/18):一些研究结果表明,在从事长期有氧运动和阻力运动时,衰老的骨骼肌会表达更多的自噬相关蛋白。与自噬有关的蛋白质的表达因运动的种类和程度不同而有明显的差异[42]。在训练后,老龄小鼠的Beclin-1表达量提高,腓肠肌质量与体质量的比例明显增加(长期的) [43]。这些数据表明,自噬调节能力在老年骨骼肌中减弱。而且当动物接受运动训练时,这种效应被上调。此外,和肌纤维类型转换之间似乎有关联。来自营养匮乏的自噬因子1(nutrient-depleted autophagy factor-1,Naff-1)敲除小鼠的骨骼肌显示出向慢肌纤维(Ⅰ型)的明显转变以及对肌肉疲劳的更大抵抗,Naff-1基因敲除小鼠的肌肉发力能力明显降低[44],这一发现不仅证明了自噬调节因子Naff-1在维持骨骼肌平衡中的作用,而且为研究病态肌纤维的转化提供了新的研究视角。自噬的丧失可促进细胞核的迁移和聚集,抑制Atg9可抑制形态异常的肌纤维萎缩,同样沉默Atg9、Atg5和Atg18可促进肌纤维纵向的减少,也证明了这一点[45]。由于敲除Atg9和Atg18增加了肌纤维的纵向直径,由此更宽的肌肉纤维可能有助于在极性迁移过程中细胞核从内轴横向位移[45-46],这为自噬基因如何控制肌肉纤维的形状变化提供了一个新的视角。Atg7基因敲除小鼠表现出自噬异常,导致了小鼠氧化应激、线粒体功能失调以及细胞器和蛋白质的堆积[47-49],加速了小鼠的衰老。此外,在肌肉特异性Atg7基因敲除小鼠中观察到了异常的线粒体、混乱的肌浆、网状扩张以及不典型的同心膜结构。这些数据表明Atg7基因在维持肌肉质量和肌肉纤维完整性方面的作用。另外,LC3-Ⅱ、p62(自噬受体,也称为SQSTM1蛋白)、Atg5、Atg7和Beclin-1被证明在Rpt3(蛋白酶)缺陷小鼠的自噬途径中蛋白表达升高,这种上调可能是由于补偿性的蛋白质水解激活造成的[50]。 (4)其他细胞成分(Atg14):Atg14,又被称为Atg14L或Barkor(Beclin-1的一个重要调节器),参与了许多生物过程,包括发育、免疫、肿瘤抑制以及对一些心脏和神经系统疾病的防御[13,51]。由于Atg14 Ser29和ULK1磷酸化之间的正相关关系,ULK1 Ser555激活位点的磷酸化似乎代表了ULK1的激酶活性[52]。有研究表明,在合成代谢和分解代谢情况下,急性运动通过ULK1促进人体骨骼肌的自噬信号。从上述数据可以反映出骨骼肌中自噬信号的增加与Atg14的参与密不可分。缺少ULK1-ULK2、Atg14或Rb1cc1时,骨骼肌中的空泡会堆积[9]。研究人员发现,Atg14敲除小鼠和RB1的诱导卷曲蛋白RB1CC1抗体(rabbit Anti-RB1CC1/FIP200 antibody,Rb1cc1)敲除小鼠的骨骼肌都显示出泛素+SQSTM1+沉积的自噬空泡性肌病(autophagic vacuolar myopathy,AVM)特征,而且Rb1cc1敲除小鼠的骨骼肌还显示出TARDBP/TDP-43+(神经退行性疾病致病基因)病理和其他类似于ULK1/ULK2敲除小鼠描述的肌病的症状[7,53]。大多数糖酵解型的Ⅱ型肌纤维受到衰老(肌肉疏松症)、不运动和长期禁食条件(饥饿)带来的骨骼肌萎缩的影响,但氧化型的Ⅰ型肌纤维却能正常保存下来[54],这是由Ⅲ类磷脂酰肌醇激酶(vacuolar protein sorting 34,Vps34)蛋白水平的下降带来的,该蛋白不依赖于mTORC1,但依赖于STAT3(转录激活蛋白,STAT蛋白质家族成员),以及Vps34/p150/Beclin1/Atg14复合物1 [55],提示自噬基因Beclin1/Atg14在维持氧化型肌纤维中的重要意义[56]。 2.3.2 其他Atg基因介导的自噬与骨骼肌衰老 (1)Atg1/ULK1复合物(Atg1、Atg13):在关键组织中,Atg1的局部激活可以以非细胞自主的方式延缓衰老。Atg1的神经元上调对于诱导衰老过程中的组织间效应和延长寿命是必要的[57]。有研究表明甘氨酸-酪氨酸-苯丙氨酸 (Glycine-Tyrosine-Phenylalanine,Gyf)介导的自噬调节对于维持神经肌肉内稳态和预防组织退行性病变非常重要[58]。据报道,GIGYF2位点的人类突变与帕金森病相关,而Gyf又是GIGYF1(Grb10相互作用的Gyf蛋白1)和GIGYF2的同源基因。Gyf的沉默可以完全抑制Atg1-Atg13激活在刺激自噬通量中的作用,影响泛素化蛋白聚集物的清除。由此可以推测在帕金森病的形成过程中Atg1-Atg13复合物可能会出现缺陷。此外,有结果表明Pink1/Parkin促进衰老肌肉线粒体泛素化的自噬,并以Atg1依赖的方式延长寿命[59]。在间接飞行肌,线粒体泛素化以年龄依赖的方式增加,在间接飞行肌中过表达Pink1或Parkin可以消除线粒体泛素化(PINK1/Parkin介导的线粒体自噬在运动性骨骼肌损伤中的作用),恢复ATP水平和延长寿命,而通过Atg1敲除阻断自噬可以抑制衰老间接飞行肌中的这些作用[60]。令人惊讶的是Pink1和Parkin同样是两个与帕金森病相关的家族基因,这佐证了针对于Atg1缺陷时可能伴随着帕金森疾病产生的推测,为探索帕金森疾病的提供了一个新的研究方向。 ULK1复合体由ULK1(或ULK2)、FIP200、Atg13和Atg101组成,在自噬的初始阶段起作用。先前的研究表明ULK1和FIP200可以在自噬以外的通路中发挥作用[61]。然而,Atg13和Atg101的作用是否与ULK1和FIP200相似仍是未知的。有研究生成了Atg13敲除小鼠。结果发现Atg13缺陷小鼠在子宫内死亡,这与大多数其他类型的Atg缺陷小鼠不同,缺乏Atg13的胚胎表现为生长迟缓和心肌生长缺陷。在培养的成纤维细胞中,缺乏Atg13会阻碍自噬体在上游的形成。此外,Atg13缺失增强了对肿瘤坏死因子α诱导的细胞凋亡的敏感性,而其他Atg蛋白以及ULK1和ULK2的同时缺失则不起作用[61]。这些结果表明Atg13具有自噬和非自噬功能,后者对心脏发育至关重要,可能与FIP200共享,但与ULK1/2不相同。另外,有研究发现了在肌少症发生之前,线粒体质量控制和自噬通量的早期改变会使肌肉微环境恶化。而Atg13和LC3-Ⅱ升高以及P62和溶酶体相关膜蛋白1(lysosome-associated membrane protein 1,LAMP1,又称为CD107a)积累可能是造成自噬通量受损的直接原因[62]。还有就是Atg13在肌痛性脑脊髓炎患者中的表现,研究发现Atg13释放到血清后自噬受损可能是肌痛性脑脊髓炎的病理信号;Atg13在肌痛性脑脊髓炎患者的血清中被强烈上调,表明自噬代谢事件受损[63]。这些研究结果均可以反映出Atg13在自噬以及非自噬调节过程中的特异性,相信对其做进一步的研究将会是有趣的。 (2)其他细胞成分(Atg4、Atg8/LC3、Atg3):Atg4是一种高度特异性的蛋白酶,对自噬起着至关重要的作用[64]。在Atg4b-/-小鼠(自噬缺陷)模型中,首次描述了系统性自噬下降的代谢足迹。不同组织的代谢组中自噬缺乏的影响是高度依赖于组织的,在骨骼肌中比在心脏中更严重,而在肝组织中不明显,在这方面可以认为Atg4B缺乏可能以组织依赖的方式影响自噬[65]。 在酵母中,自噬启动、物质识别、废物吞噬以及囊泡闭合均依赖于Atg8。在高等真核生物中,Atg8已经进化为LC3/GABARAP蛋白家族(LC3A、LC3B、LC3C、GABARAP、GABARAPL1和GABARAPL2)[66]。 在诱导自噬体降解过程中,LC3-Ⅰ被脂化为LC3-Ⅱ,并与物质隔离膜结合,允许自噬体形成。LC3的脂化导致LC3-Ⅱ/LC3-Ⅰ比值增加,该比值是多种组织自噬的常用标记物,包括骨骼肌[67]。MAP1LC3是哺乳动物Atg8同源物之一,同样通过哺乳动物Atg7和Atg3催化的泛素样偶联以及涉及哺乳动物Atg4的脱溶反应进行调控。因此,脂质偶联的MAP1LC3 (MAP1LC3- Ⅱ)也通常被用作自噬结构的标记物[68]。 LC3B是研究最多的家族蛋白,与自噬体的发育和成熟有关,并被用于监测自噬活性[69]。在骨骼肌中,ULK1-ULK2、Atg14或Rb1cc1的缺失会导致囊泡的积累[70-71]。研究发现ULK1-ULK2、Atg14或Rb1cc1的缺失损害了自噬通量,但并不能完全消除Atg8家族成员的脂化以及LC3B+自噬体的生成(Atg5或Atg7的缺失也是如此),这表明LC3B+自噬体的存在(尽管水平降低)对肌肉空泡病理的发生是必需的[72]。当Atg3和Atg7处于非活性状态时,由于与其底物LC3的稳定共价作用而免受氧化侵蚀。当Atg3和Atg7被激活时,由于LC3转移到磷脂酰乙醇胺(脂化),这种相互作用变得短暂,而这一过程对功能性自噬至关重要[73]。在老年小鼠的骨骼肌中,LC3B-Ⅰ与磷脂酰乙醇胺的结合也下降,可能是由于Atg3和Atg12-Atg5蛋白水平下降所导致。在衰老过程中,巨噬细胞也有类似的下降,但对伴侣介导的自噬(chaperone-mediated autophagy,CMA)、线粒体周转以及肌肉与心脏的代谢功能失调有着不同的影响[74]。 很明显,Atg家族介导的自噬在骨骼肌衰老的过程中所扮演的角色不可或缺。并且有许多证据可以证明Atg家族基因的作用具有一定的联合性,大都不是一个Atg基因介导自噬过程,而是相互协调配合。在不同形式的运动干预下,Atg家族基因有着相应的表达,参与调节自噬过程的各个方面。 2.4 运动介导的自噬与骨骼肌衰老 虽然不同的运动模式,如开始运动的年龄、运动时间和运动强度,可能对自噬相关蛋白的表达有异质性的影响,但长期的有氧运动可以调节自噬相关蛋白,诱导骨骼肌自噬,并延缓肌肉质量的损失。虽然短期的低强度运动(干预期小于12周,频率小于每周3次)可能不会超过运动诱导自噬的阈值,但高强度运动有可能引起过度自噬[75-77]。人们发现,急性阻力运动可以激活Vps34,而自噬与运动后的蛋白质分解代谢有关[78-79]。然而在针对于人类的一项研究中发现,急性阻力运动减少了LC3的脂化(LC3-Ⅰ到LC3-Ⅱ的转化和骨骼肌中p62水平的降低),表明自噬可能在肌肉中被下调[80]。此类发现在骨骼肌的线粒体中也有体现,其中BNIP3(Bcl-2/E1B-19 kDa, Bcl-2蛋白家族,线粒体促凋亡蛋白)表达增加,为自噬清除线粒体堆积废物提供了额外的证据[81-82]。此外,在中等强度耐力运动后的大鼠中发现了较高的Atg7、Beclin1和LC3蛋白水平,表明了适度的有氧运动增加了老年小鼠的自噬水平(Atg7和Beclin1)[83]。并且,有研究表明,9周的阻力运动训练促进了自噬,减少了老年大鼠骨骼肌的凋亡,避免了肌肉质量和力量的损失[84]。 体育锻炼可能会损害细胞结构,需要自噬机制的作用来清除和修复受损的细胞成分。有研究提取了股外侧肌肉(200 km跑)样本,发现了自噬蛋白Atg4、LC3和Atg12表达[85]。此外,还发现自噬蛋白的水平在进行超级马拉松之后表达更高[86]。虽然体育运动有益于身体健康,但高强度的运动,如超耐力运动,可能会使机体承受代谢压力进而损害线粒体的功能[6]。在这种情况下,自噬被激活,以消除受损的蛋白质和细胞器,并在能量不足时提供氨基酸[87-88]。从长远来看,精确控制运动量对于最大限度地发挥运动的益处至关重要。"

| [1] SHIRAKABE A, IKEDA Y, SCIARRETTA S, et al. Aging and Autophagy in the Heart. Circ Res. 2016;118(10):1563-1576. [2] RUBINSZTEIN DC, MARINO G, KROEMER G. Autophagy and Aging. Cell. 2011;146:682-695. [3] XIA Q, HUANG X, HUANG J, et al. The Role of Autophagy in Skeletal Muscle Diseases. Front Physiol. 2021;12:638983. [4] RYTER SW, CHOI AM. Autophagy in lung disease pathogenesis and therapeutics. Redox Biol. 2015;4:215-225. [5] STJEPANOVIC G, BASKARAN S, LIN MG, et al. Vps34 Kinase Domain Dynamics Regulate the Autophagic PI 3-Kinase Complex. Mol Cell. 2017;67(3):528-534.e3. [6] DIKIC I, ELAZAR Z. Mechanism and medical implications of mammalian autophagy. Nat Rev Mol Cell Biol. 2018;19(6):349-364. [7] GALLUZZI L, BAEHRECKE EH, BALLABIO A, et al. Molecular definitions of autophagy and related processes. EMBO J. 2017;36(13):1811-1836. [8] LAMB CA, YOSHIMORI T, TOOZE SA. The autophagosome: origins unknown, biogenesis complex. Nat Rev Mol Cell Biol. 2013;14(12):759-774. [9] NAKATOGAWA H. Two ubiquitin-like conjugation systems that mediate membrane formation during autophagy. Essays Biochem. 2013;55:39-50. [10] ZHANG S, YAZAKI E, SAKAMOTO H, et al. Evolutionary diversification of the autophagy-related ubiquitin-like conjugation systems. Autophagy. 2022;18(12):2969-2984. [11] ROMANOV J, WALCZAK M, IBIRICU I, et al. Mechanism and functions of membrane binding by the Atg5-Atg12/Atg16 complex during autophagosome formation. EMBO J. 2012;31(22):4304-4317. [12] WALCZAK M, MARTENS S. Dissecting the role of the Atg12-Atg5-Atg16 complex during autophagosome formation. Autophagy. 2013;9(3):424-425. [13] ZHU M, ZHAN M, XI CJ, et al. Molecular characterization and expression of the autophagy-related gene Atg14 in WSSV-infected Procambarus clarkii. Fish Shellfish Immunol. 2022;125:200-211. [14] OHSUMI Y. Historical landmarks of autophagy research. Cell Res. 2014;24:9-23. [15] SAKAKIBARA K, EIYAMA A, SUZUKI SW, et al. Phospholipid methylation controls Atg32-mediated mitophagy and Atg8 recycling. EMBO J. 2015;34(21):2703-2719. [16] SON JM, LEE C. Mitochondria: multifaceted regulators of aging. BMB Rep. 2019;52(1): 13-23. [17] LYAMZAEV KG, TOKARCHUK AV, PANTELEEVA AA, et al. Induction of autophagy by depolarization of mitochondria. Autophagy. 2018;14(5):921-924. [18] PALIKARAS K, TAVERNARAKIS N. Mitochondrial homeostasis: the interplay between mitophagy and mitochondrial biogenesis. Exp Gerontol. 2014;56:182-188. [19] GONZALEZ-FREIRE M, DE CABO R, BERNIER M, et al. Reconsidering the Role of Mitochondria in Aging. J Gerontol A Biol Sci Med Sci. 2015;70(11):1334-1342. [20] 张雪,漆正堂,丁树哲.线粒体介导骨骼肌重塑在运动抵御癌症恶病质中的作用研究进展[J].上海体育学院学报,2021,45(1):78-85. [21] GOUSPILLOU G, SGARIOTO N, KAPCHINSKY S, et al. Increased sensitivity to mitochondrial permeability transition and myonuclear translocation of endonuclease G in atrophied muscle of physically active older humans. FASEB J. 2014;28(4):1621-1633. [22] O’LEARY MF, VAINSHTEIN A, IQBAL S, et al. Adaptive plasticity of autophagic proteins to denervation in aging skeletal muscle. Am J Physiol Cell Physiol. 2013;304(5):C422-430. [23] VAKIFAHMETOGLU-NORBERG H, OUCHIDA AT, NORBERG E. The role of mitochondria in metabolism and cell death. Biochem Biophys Res Commun. 2017;482(3):426-431. [24] LI P, MA Y, YU C, et al. Autophagy and Aging: Roles in Skeletal Muscle, Eye, Brain and Hepatic Tissue. Front Cell Dev Biol. 2021;9:752962. [25] 金晶,冯祎中,黄伟,等.运动通过激活卫星细胞功能延缓和改善骨骼肌衰减症的研究进展[J].体育科学,2019,39(8):73-80. [26] GARCIA-PRAT L, MUNOZ-CANOVES P, MARTINEZ-VICENTE M. Dysfunctional autophagy is a driver of muscle stem cell functional decline with aging. Autophagy. 2016;12:612-613. [27] Revuelta M, Matheu A. Autophagy in stem cell aging. Aging Cell. 2017;16:912-915. [28] 王震,蔺海旗,何霏,等.运动激活骨骼肌卫星细胞:增龄性肌衰减症及肌肉损伤修复的运动预防和治疗[J].中国组织工程研究,2021,25(23):3752-3759. [29] GARCÍA-PRAT L, MARTÍNEZ-VICENTE M, PERDIGUERO E, et al. Autophagy maintains stemness by preventing senescence. Nature. 2016;529(7584):37-42. [30] 钱帅伟,丁树哲.运动性细胞自噬是调节骨骼肌代谢稳态的内置机制[J].体育科学, 2015,35(10):55-65. [31] KJØBSTED R, MUNK-HANSEN N, BIRK JB, et al. Enhanced Muscle Insulin Sensitivity After Contraction/Exercise Is Mediated by AMPK. Diabetes. 2017;66(3):598-612. [32] 张坦,孙易,丁树哲.运动介导AMPK调控线粒体质量控制的机制研究进展[J].中国体育科技,2018,54(6):97-102 [33] KIM J, KUNDU M, VIOLLET B, et al. AMPK and mTOR regulate autophagy through direct phosphorylation of Ulk1. Nat Cell Biol. 2011;13(2):132-141. [34] MøLLER AB, VENDELBO MH, CHRISTENSEN B, et al. Physical exercise increases autophagic signaling through ULK1 in human skeletal muscle. J Appl Physiol (1985). 2015;118(8):971-979. [35] FRITZEN AM, MADSEN AB, KLEINERT M, et al. Regulation of autophagy in human skeletal muscle: effects of exercise, exercise training and insulin stimulation. J Physiol. 2016;594(3):745-761. [36] 张鑫愉,周晓勐,牛燕媚,等.mTOR复合物在有氧运动改善小鼠骨骼肌糖代谢过程中的作用[J].中国运动医学杂志,2018,37(12):1017-1023. [37] DRAKE JC, WILSON RJ, CUI D, et al. Ulk1, Not Ulk2, Is Required for Exercise Training-Induced Improvement of Insulin Response in Skeletal Muscle. Front Physiol. 2021;12: 732308. [38] CHANGOTRA H, KAUR S, YADAV SS, et al. ATG5: A central autophagy regulator implicated in various human diseases. Cell Biochem Funct. 2022; 40(7):650-667. [39] MEJÍAS-PEÑA Y, ESTÉBANEZ B, RODRIGUEZ-MIGUELEZ P, et al. Impact of resistance training on the autophagy-inflammation-apoptosis crosstalk in elderly subjects. Aging (Albany NY). 2017;9(2):408-418. [40] TAJRISHI MM, SATO S, SHIN J, et al. The TWEAK-Fn14 dyad is involved in age-associated pathological changes in skeletal muscle. Biochem Biophys Res Commun. 2014;446(4):1219-1224. [41] KOSTRZEWA-NOWAK D, TRZECIAK-RYCZEK A, WITYK P, et al. Post-Effort Changes in Autophagy- and Inflammation-Related Gene Expression in White Blood Cells of Healthy Young Men. Cells. 2021;10(6):1406. [42] WANG C, LIANG J, REN Y, et al. A Preclinical Systematic Review of the Effects of Chronic Exercise on Autophagy-Related Proteins in Aging Skeletal Muscle. Front Physiol. 20224;13:930185. [43] KIM YA, KIM YS, OH SL, et al. Autophagic response to exercise training in skeletal muscle with age. J Physiol Biochem. 2013;69(4):697-705. [44] CHANG NC, NGUYEN M, BOURDON J, et al. Bcl-2-associated autophagy regulator Naf-1 required for maintenance of skeletal muscle. Hum Mol Genet. 2012;21(10):2277-2287. [45] ZHUANG X, CHUNG KP, CUI Y, et al. ATG9 regulates autophagosome progression from the endoplasmic reticulum in Arabidopsis. Proc Natl Acad Sci U S A. 2017;114(3):E426-E435. [46] KULEESHA, FENG L, WASSER M. Spatial pattern analysis of nuclear migration in remodelled muscles during Drosophila metamorphosis. BMC Bioinformatics. 2017; 18(1):329. [47] COSGROVE BD, GILBERT PM, PORPIGLIA E, et al. Rejuvenation of the muscle stem cell population restores strength to injured aged muscles. Nat Med. 2014;20(3):255-264. [48] CHAKKALAKAL JV. JONES KM, BASSON MA, et al. The aged niche disrupts muscle stem cell quiescence. Nature. 2012;490(7420):355-360. [49] SOUSA-VICTOR P, GUTARRA S, GARCÍA-PRAT L, et al. Geriatric muscle stem cells switch reversible quiescence into senescence. Nature. 2014;506(7488):316-321. [50] KITAJIMA Y, SUZUKI N, YOSHIOKA K, et al. Inducible Rpt3, a Proteasome Component, Knockout in Adult Skeletal Muscle Results in Muscle Atrophy. Front Cell Dev Biol. 2020;8:859. [51] ZHANG H, GE S, NI B, et al. Augmenting ATG14 alleviates atherosclerosis and inhibits inflammation via promotion of autophagosome-lysosome fusion in macrophages. Autophagy. 2021;17(12):4218-4230. [52] PARK JM, SEO M, JUNG CH, et al. ULK1 phosphorylates Ser30 of BECN1 in association with ATG14 to stimulate autophagy induction. Autophagy. 2018;14(4):584-597. [53] LI D, VOGEL P, LI-HARMS X, et al. ATG14 and RB1CC1 play essential roles in maintaining muscle homeostasis. Autophagy. 2021;17(9):2576-2585. [54] NICHENKO AS, SORENSEN JR, SOUTHERN WM, et al. Lifelong Ulk1-Mediated Autophagy Deficiency in Muscle Induces Mitochondrial Dysfunction and Contractile Weakness. Int J Mol Sci. 2021;22(4):1937. [55] SANTOS-ARAUJO S, BOMFIM L, ARARIPE LO, et al. Silencing of ATG6 and ATG8 promotes increased levels of triacylglycerol (TAG) in the fat body during prolonged starvation periods in the Chagas disease vector Rhodnius prolixus. Insect Biochem Mol Biol. 2020; 127:103484. [56] YAMADA E, BASTIE CC, KOGA H, et al. Mouse skeletal muscle fiber-type-specific macroautophagy and muscle wasting are regulated by a Fyn/STAT3/Vps34 signaling pathway. Cell Rep. 2012;1(5):557-569. [57] ULGHERAIT M, RANA A, RERA M, et al. AMPK modulates tissue and organismal aging in a non-cell-autonomous manner. Cell Rep. 2014;8(6):1767-1780. [58] KIM M, SEMPLE I, KIM B, et al. Drosophila Gyf/GRB10 interacting GYF protein is an autophagy regulator that controls neuron and muscle homeostasis. Autophagy. 2015; 11(8):1358-1372. [59] SI H, MA P, LIANG Q, et al. Overexpression of pink1 or parkin in indirect flight muscles promotes mitochondrial proteostasis and extends lifespan in Drosophila melanogaster. Plos One. 2019;14(11):e0225214. [60] IMAI Y. PINK1-Parkin signaling in Parkinson’s disease: Lessons from Drosophila. Neurosci Res. 2020;159:40-46. [61] KAIZUKA T, MIZUSHIMA N. Atg13 Is Essential for Autophagy and Cardiac Development in Mice. Mol Cell Biol. 2015;36(4):585-595. [62] LIU HW, CHANG YC, CHAN YC, et al. Dysregulations of mitochondrial quality control and autophagic flux at an early age lead to progression of sarcopenia in SAMP8 mice. Biogerontology. 2020;21(3):367-380. [63] GOTTSCHALK G, PETERSON D, KNOX K, et al. Elevated ATG13 in serum of patients with ME/CFS stimulates oxidative stress response in microglial cells via activation of receptor for advanced glycation end products (RAGE). Mol Cell Neurosci. 2022;120:103731. [64] YANG M, CHANG Z, JI H. Characterization and expression analysis of ATG4 paralogs in response to the palmitic acid induced-ER stress in Ctenopharyngodon idellus kidney cells. Comp Biochem Physiol B Biochem Mol Biol. 2021;252:110525. [65] MARTINEZ-GARCIA GG, PEREZ RF, FERNANDEZ AF, et al. Autophagy Deficiency by Atg4B Loss Leads to Metabolomic Alterations in Mice. Metabolites. 2021;11(8):481. [66] SCHAAF MB, KEULERS TG, VOOIJS MA, et al. LC3/GABARAP family proteins: autophagy-(un)related functions. FASEB J. 2016;30(12):3961-3978. [67] FRITZEN AM, FRØSIG C, JEPPESEN J, et al.Role of AMPK in regulation of LC3 lipidation as a marker of autophagy in skeletal muscle. Cell Signal. 2016;28(6):663-674. [68] ZHU J, WANG KZ, CHU CT. After the banquet: mitochondrial biogenesis, mitophagy, and cell survival. Autophagy. 2013;9(11):1663-1676. [69] CERULLI RA, SHEHAJ L, BROWN H, et al. Stapled Peptide Inhibitors of Autophagy Adapter LC3B. Chembiochem. 2020;21(19):2777-2785. [70] NEMAZANYY I, BLAAUW B, PAOLINI C, et al. Defects of Vps15 in skeletal muscles lead to autophagic vacuolar myopathy and lysosomal disease. EMBO Mol Med. 2013;5(6):870-890. [71] WANG B, MAXWELL BA, JOO JH, et al.ULK1 and ULK2 Regulate Stress Granule Disassembly Through Phosphorylation and Activation of VCP/p97. Mol Cell. 2019;74(4):742-757.e8. [72] LI D, VOGEL P, LI-HARMS X, et al. ATG14 and RB1CC1 play essential roles in maintaining muscle homeostasis. Autophagy. 2021;17(9):2576-2585. [73] FRUDD K, BURGOYNE T, BURGOYNE JR. Oxidation of Atg3 and Atg7 mediates inhibition of autophagy. Nat Commun. 2018;9(1):95. [74] ZHOU J, CHONG SY, LIM A, et al. Changes in macroautophagy, chaperone-mediated autophagy, and mitochondrial metabolism in murine skeletal and cardiac muscle during aging. Aging-Us. 2017;9(2):583-599. [75] WANG C, LIANG J, REN Y, et al. A Preclinical Systematic Review of the Effects of Chronic Exercise on Autophagy-Related Proteins in Aging Skeletal Muscle. Front Physiol. 2022; 13:930185. [76] 崔新雯,张一民,汪赞,等.长期高强度间歇训练对中年大鼠骨骼肌蛋白合成和降解的影响[J].中国体育科技,2021,57(2):12-19. [77] 李方晖,艾竞一,李涛,等.高强度间歇训练对大鼠骨骼肌细胞自噬的影响及其调节机制[J].体育科学,2019,39(2):29-38. [78] GLYNN EL, FRY CS, DRUMMOND MJ, et al. Muscle protein breakdown has a minor role in the protein anabolic response to essential amino acid and carbohydrate intake following resistance exercise. Am J Physiol Regul Integr Comp Physiol. 2010;299(2):R533-540. [79] MACKENZIE MG, HAMILTON DL, MURRAY JT, et al. mVps34 is activated by an acute bout of resistance exercise. Biochem Soc Trans. 2007;35(Pt 5):1314-1316. [80] FRY CS, DRUMMOND MJ, GLYNN EL, et al. Skeletal muscle autophagy and protein breakdown following resistance exercise are similar in younger and older adults. J Gerontol A Biol Sci Med Sci. 2013;68(5):599-607. [81] LO VERSO F, CARNIO S, VAINSHTEIN A, et a. Autophagy is not required to sustain exercise and PRKAA1/AMPK activity but is important to prevent mitochondrial damage during physical activity. Autophagy. 2014;10(11): 1883-1894. [82] VAINSHTEIN A, TRYON LD, PAULY M, et al. Role of PGC-1α during acute exercise-induced autophagy and mitophagy in skeletal muscle. Am J Physiol Cell Physiol. 2015;308: C710-C719. [83] ROCCHI A, HE C. Activating Autophagy by Aerobic Exercise in Mice. J Vis Exp. 2017;(120):55099. [84] LUO L, LU AM, WANG Y, et al. Chronic resistance training activates autophagy and reduces apoptosis of muscle cells by modulating IGF-1 and its receptors, Akt/mTOR and Akt/FOXO3a signaling in aged rats. Exp Gerontol. 2013;48(4):427-436. [85] JAMART C, BENOIT N, RAYMACKERS JM, et al. Autophagy-related and autophagy-regulatory genes are induced in human muscle after ultraendurance exercise. Eur J Appl Physiol. 2012;112(8):3173-3177. [86] JAMART C, FRANCAUX M, MILLET GY, et al. Modulation of autophagy and ubiquitin-proteasome pathways during ultra-endurance running. J Appl Physiol (1985). 2012; 112(9):1529-1537. [87] SANDRI M. Protein breakdown in muscle wasting: role of autophagy-lysosome and ubiquitin-proteasome. Int J Biochem Cell Biol. 2013;45(10):2121-2129. [88] FERRARO E, GIAMMARIOLI AM, CHIANDOTTO S, et al. Exercise-induced skeletal muscle remodeling and metabolic adaptation: redox signaling and role of autophagy. Antioxid Redox Signal. 2014;21(1):154-176. |
| [1] | Xie Peng, Zhang Jiang, Deng Xiaolei, Wei Bo, Hou Decai. A systematic review of mouse model construction for sarcopenia [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(2): 263-266. |
| [2] | Guo Xiangying, Peng Zifu, He Yimin, Fang Hongbo, Jiang Ning. MiRNA-122 contributes to the effect of exercise on non-alcoholic fatty liver [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(2): 272-279. |
| [3] | Sun Yuan, Wang Qingbo, Pi Yihua, Lu Chunmin, Xu Chuanyi, Zhang Yan. Effects of early and late aerobic exercise on right heart failure induced by monocrotaline in rats with pulmonary hypertension [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(2): 177-185. |
| [4] | Yin Linwei, Huang Xiarong, Qu Mengjian, Yang Lu, Wang Jinling, Jia Feiyang, Liao Yang, Zhou Jun. Effects of treadmill exercise on osteoporosis and wnt/beta-catenin signal pathway in aged rats [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(2): 231-236. |
| [5] | Ma Suilu, He Zhijun, Liu Tao, Li Yan, He Yuanxu, He Bo, Wang Weiwei, Wei Xiaotao. Traditional Chinese medicine monomer in the prevention and treatment of flap necrosis by regulating “autophagy” [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(1): 153-158. |
| [6] | Deng Rui, Huang Keming, Luo Jian, Chen Gong, Feng Jian, Huang Weiyi, Wei Gang. Effect of heme oxygenase-1-mediated atorvastatin on macrophage polarization and cholesterol accumulation [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(1): 62-67. |
| [7] | Wang Ji, Zhang Min, Yang Zhongya, Zhang Long. A review of physical activity intervention in type 2 diabetes mellitus with sarcopenia [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(8): 1272-1277. |
| [8] | Nie Chenchen, Su Kaiqi, Gao Jing, Fan Yongfu, Ruan Xiaodi, Yuan Jie, Duan Zhaoyuan, Feng Xiaodong. The regulatory role of circular RNAs in cerebral ischemia-reperfusion injury [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(8): 1286-1291. |
| [9] | Liang Jiaqi, Liu Hengxu, Yang Jinxin, Yang Yi, Deng Xuhui, Tan Mingjian, Luo Jiong. Health benefit relationship between exercise and intestinal bacteria [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(8): 1292-1299. |
| [10] | Huang Linke, Wei Linhua, Jiang Jie, Liu Qian, Chen Weiwei. Effects of estrogen combined with treadmill exercise on bone mass and articular cartilage in ovariectomized mice [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(8): 1166-1171. |
| [11] | Ruan Ling, Wang Guanghua, Wu Rongping, Jin Zhan, Lyu Zhenqing, Zhang Nan, Li Shoubang. Correlation between exercise intensity and lipid metabolism disorder and oxidative stress in a high-diet rat model [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(8): 1149-1155. |
| [12] | Zhang Yan, He Ruibo, Wang Qingbo, Pi Yihua, Lu Chunmin, Xu Chuanyi, Ma Gang, Peng Peng. Effects of aerobic exercises with different load volumes on inflammatory response and insulin signaling pathway of skeletal muscle in obese rats [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(8): 1237-1244. |
| [13] | Wu Dongzhe, Gao Xiaolin, Li Chuangtao, Wang Hao. Constructing the prediction model of maximal oxygen uptake by back-propagation neural network based on the cardiorespiratory optimal point [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(8): 1224-1231. |
| [14] | Li Long, Li Guangdi, Shi Hao, Deng Keqi. Circular RNA as a competing endogenous RNA is involved in the regulation of osteoarthritis [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(5): 751-757. |
| [15] | Li Zhichao, Tan Guoqing, Su Hui, Xu Zhanwang, Xue Haipeng. Regulatory role of non-coding RNAs as potential therapeutic targets in spinal cord injury [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(5): 758-764. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||