中国组织工程研究 ›› 2014, Vol. 18 ›› Issue (32): 5209-5213.doi: 10.3969/j.issn.2095-4344.2014.32.021
• 干细胞基础实验 basic experiments of stem cells • 上一篇 下一篇
NDRG2基因反转录病毒载体的构建及表达
欧剑锋1,任 晖2,王存邦1,白 海1
- 解放军兰州军区兰州总医院,1血液病科,2乳腺科,甘肃省兰州市 730050
Construction and expression of NDRG2 retroviral vector
Ou Jian-feng1, Ren Hui2, Wang Cun-bang1, Bai Hai1
- 1Department of Hematology, Lanzhou General Hospital of PLA, Lanzhou 730050, Gansu Province, China; 2Department of Breast Surgery, Lanzhou General Hospital of PLA, Lanzhou 730050, Gansu Province, China
摘要:
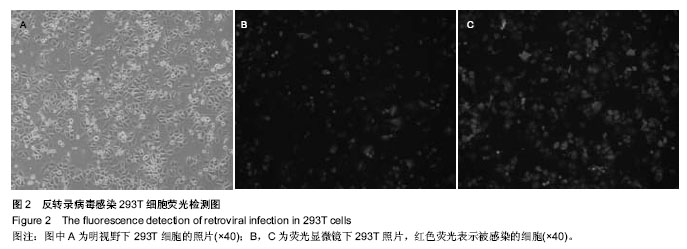
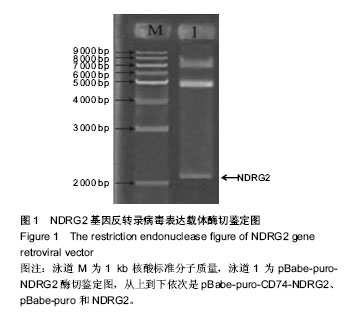
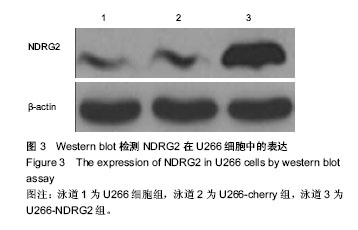
背景:NDRG2(N-Myc Downstream Regulated Gene 2)是一个新的抑癌基因,既可以增强经典抑癌通路的抗肿瘤效应,又可以对正常细胞的癌变起到监控。有关NDRG2在骨髓瘤发生中的功能和作用至今还未见报道。 目的:构建NDRG2基因反转录病毒表达载体,利用包装的病毒感染人骨髓瘤细胞系U266,检测NDRG2的表达情况。 方法:设计与合成引物,提取U266细胞的RNA,反转录和PCR扩增,经BamHⅠ和TaqⅠ双酶切,琼脂糖凝胶电泳,切胶回收进行连接转化,并再次酶切鉴定;并将构建的载体包装为反转录病毒,感染U266细胞,筛选出稳定表达NDRG2的U266细胞(U266-NDRG2)克隆扩大培养,利用Western blot实验检测筛选到的U266细胞中NDRG2的表达。 结果与结论:成功构建了携带NDRG2基因表达的重组载体pBaba-puro-NDRG2,并包装为反转录病毒,筛选到的U266细胞(U266-NDRG2)中NDRG2蛋白表达明显高于U266-cherry细胞和U266细胞。结果可见利用反转录病毒载体基因重组技术成功构建出携带相应基因的反转录病毒,为研究NDRG2在人骨髓瘤中的作用奠定了实验基础。
中图分类号: