中国组织工程研究 ›› 2021, Vol. 25 ›› Issue (11): 1658-1663.doi: 10.3969/j.issn.2095-4344.3085
• 皮肤粘膜组织构建 skin and mucosal tissue construction • 上一篇 下一篇
高压氧能减轻大鼠延迟皮瓣基底部瘢痕粘连和缩短延迟皮瓣血运重建时间
胡益高,李高峰
- 湖南师范大学附属第一医院湖南省人民医院整形激光美容外科,湖南省长沙市 410000
Hyperbaric oxygen alleviates scar adhesion at the base and shortens the time of revascularization of delayed skin flap in rats
Hu Yigao, Li Gaofeng
- Department of Laser and Aesthetic Surgery, Hunan Provincial People’s Hospital, First Affiliated Hospital of Hunan Normal University, Changsha 410000, Hunan Province, China
摘要:
文题释义:
高压氧:是一种成熟的临床治疗方法,在整形外科领域高压氧被用于皮片移植、皮瓣移植术后及慢性创面的治疗。
延迟皮瓣法耳再造术:利用耳后延迟皮瓣覆盖自体肋软骨支架行外耳再造,手术分2至3期进行。一期手术为耳后皮瓣延迟术,二期即自体肋软骨支架再造、延迟皮瓣覆盖及自体中厚皮片移植外耳再造术。术后耳郭的立体形态结构完全具备,再造耳外形良好。二期手术后半年视情况决定是否进行三期手术,三期手术包括耳屏再造、耳甲腔成形和再造耳局部修整。
背景:高压氧能提高皮瓣的存活率,但是关于高压氧治疗能否减少延迟皮瓣与基底的瘢痕粘连,以及是否能够缩短延迟皮瓣血运重建时间尚未有文献报道。
目的:观察高压氧治疗后大鼠背部延迟皮瓣与基底部瘢痕组织的变化,寻求一种更安全且需时更短的延迟皮瓣形成方法。
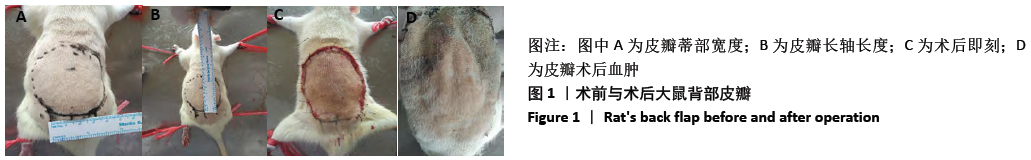
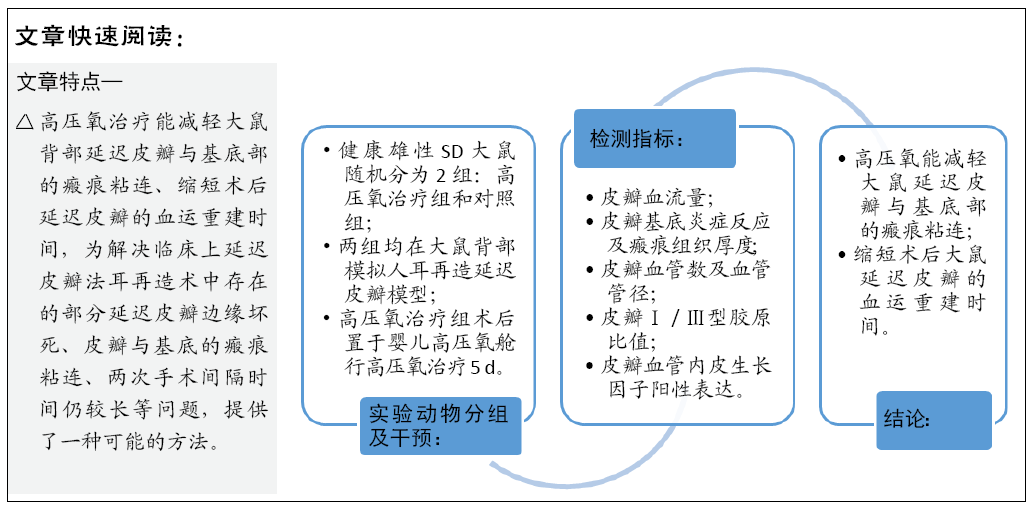
方法:健康雄性SD大鼠随机分为2组:高压氧治疗组和对照组,均在SD大鼠背部模拟人耳再造的延迟皮瓣模型,高压氧治疗组在术后置于婴儿高压氧舱行高压氧治疗5 d,记录术前及术后每日皮瓣血流量,术前、术后第1,7,14,21天皮瓣瘢痕组织厚度、Ⅰ /Ⅲ型胶原比值、皮瓣血管数、血管管径、皮瓣血管内皮生长因子表达阳性细胞数。
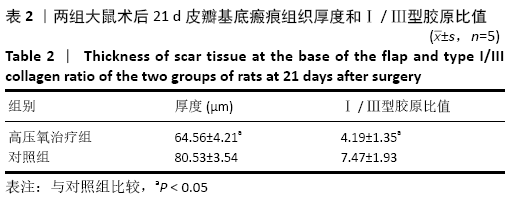
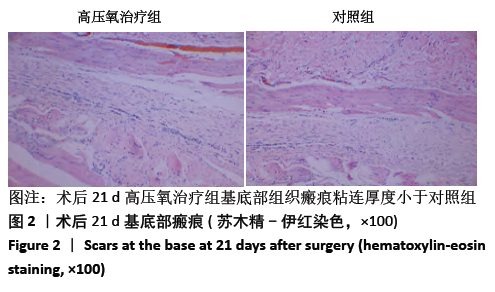
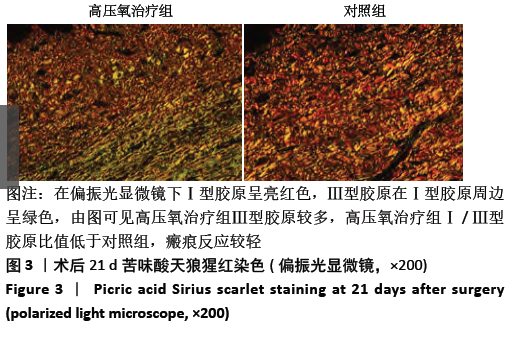
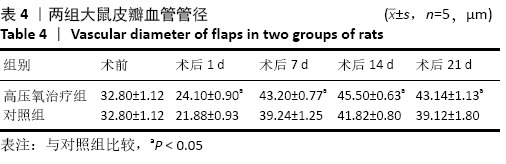
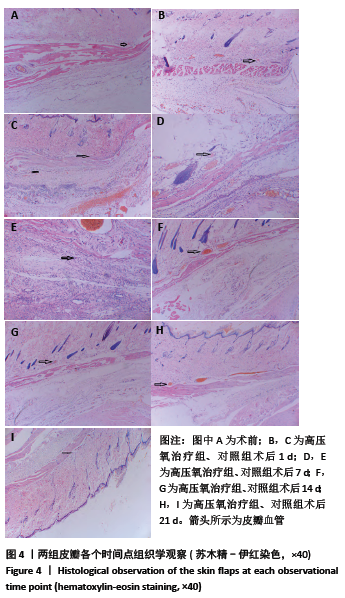
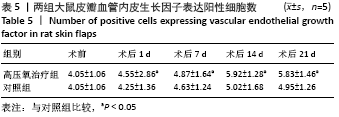
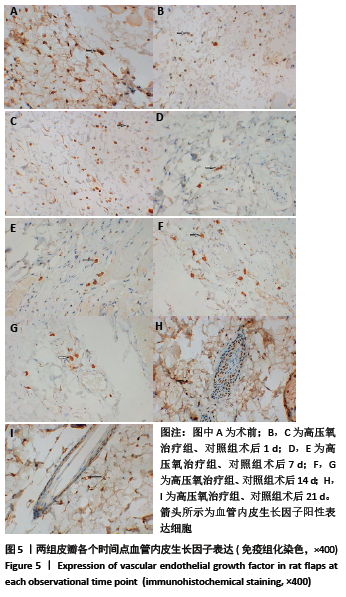
结果与结论:①两组皮瓣血流量均在术后1 d明显降低,之后血流量开始上升。高压氧治疗组术后1,7,14,21 d皮瓣血流量均高于对照组 (P < 0.05);②高压氧治疗组术后皮下组织水肿较对照组轻,组织炎性细胞浸润较少;③术后21 d高压氧治疗组基底部组织瘢痕粘连厚度小于对照组(P < 0.05),Ⅰ /Ⅲ型胶原比值低于对照组(P < 0.05);④术后第7,14,21天,高压氧治疗组血管数高于对照组(P < 0.05)。两组皮瓣血管管径均在术后1 d最小,术后14 d时最大。高压氧治疗组从术后1 d开始血管管径大于对照组(P < 0.05);⑤两组皮瓣血管内皮生长因子阳性细胞数均在术后1 d即开始升高,在术后14 d时到达最大值;高压氧治疗组术后各个时间点血管内皮生长因子阳性细胞数均高于对照组(P < 0.05);⑥结果表明,高压氧能减轻大鼠延迟皮瓣与基底部的瘢痕粘连,提高大鼠延迟皮瓣的血流量,其机制可能与促进血管生成有关。
https://orcid.org/0000-0002-4996-7488 (胡益高)
中国组织工程研究杂志出版内容重点:组织构建;骨细胞;软骨细胞;细胞培养;成纤维细胞;血管内皮细胞;骨质疏松;组织工程
中图分类号: