早在20世纪初期欧洲的,Lexer
[9-10]和Drachter
[11]就开展了对唇腭裂患者牙槽突裂的植骨修复。20世纪50至60年代,国外已有应用自体肋骨、胫骨进行修复的临床报道。20世纪70年代,Boyne等
[1]在关闭口鼻瘘时,于骨裂隙中植入少量的自体髂骨松质骨,通过骨细胞的成活与诱导来促进修复位点的骨生长。至今,这种方法仍在临床中广泛应用,并被认为是牙槽裂修复的金标 准
[12]。虽然自体骨移植有种种优点
[12-13],但毕竟以牺牲健康组织为代价,且会在供骨区造成继发损伤及并发症,同时,自体骨移植后常伴受骨区移植骨的吸收、恢复骨量不足,导致术后效果不佳
[14-15]。因此研究具有优良生物学性能和适宜力学性能的人工骨替代材料,仍是牙槽突裂修复重建领域的发展方向。
犬类具有双牙列,牙周和颅面结构及骨愈合机制类似于人类
[16-17],因此实验选择比格犬的外科手术诱导犬牙槽突裂模型。该动物模型最早由Hossain
[18]创造,并被证明在实验期间骨缺损无法自行愈合,为一种临界性骨缺损
[8]。犬类8周龄后乳牙出齐,8月龄恒牙换齐,其中6月龄相当于人类9-11岁,处于替牙颌期,符合现实临床手术时机
[1]。此前多数实验均采用成年犬恒牙列形成缺损后即刻移植修复
[8],这样虽然节约了研究时间和经费,但实际上却没有真正做到模拟现实临床软硬组织的实际情况。目前国内较为公认的牙槽突裂植骨年龄为9-11岁,此时尖牙牙根半萌出,牙冠覆盖有骨质,植骨有利于恢复牙弓完整性,矫正鼻基底凹陷,植骨成活后裂隙两侧的尖牙或侧切牙萌出,带来的咬合活动能提供机械力传导至植骨区,减少移植骨的吸收。另外此时期手术也不会影响上颌骨的发育
[1, 19]。因此实验选择幼龄犬乳牙列(3月龄)应用外科手术建立牙槽突裂模型,待到6月龄替牙颌时二次手术行移植修复。
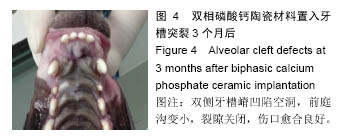
研究组前期实验已制备出异位成骨佳的骨诱导性磷酸钙陶瓷。但由于牙槽突不同于其他长骨承重部位,具有其特殊的生物学特性:它允许牙胚及牙在其中正常发育并移动萌出,并且在整个生命活动过程中,牙槽突均保持活跃的改建能力。而牙槽突裂手术治疗的目的主要是通过植骨使牙槽突恢复骨的连续性和关闭软组织间隙,从而达到:①为邻近裂隙和未萌出的牙提供骨性支持;②封闭口鼻瘘和前腭裂;③提供稳固的上颌牙弓,防止裂隙侧骨段的塌陷;④为唇和鼻底提供一个稳固的支撑支架,提高和支撑鼻翼基底,使面貌可得到满意的改善
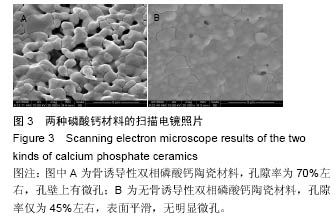
[20]。这就意味着置入材料需要与牙槽骨类似,使植骨区的牙槽间隔完全形成并维持应有的高度,并且牙齿可在植骨区萌出。因此实验中通过改善工艺适当增大β-磷酸三钙的含量及孔隙率,适当降低力学性能,制备出了更适用于修复牙槽突裂的骨诱导性磷酸钙陶瓷材料。该材料具疏松多孔的特点,强度较弱,便于术中塑形和填埋,不会对恒压萌出造成太大的阻力,非常适合修复牙槽突裂缺损。同时作者制备出化学成分一致,大孔结构相似,但微结构不同的无骨诱导性磷酸钙材料作为对照。并同期在犬大腿肌肉内进行埋植,检测两种材料在肌肉组织中异位成骨的表现。
四环素和二甲粉橙为无毒、非放射性的活性荧光染料。钙黄绿素呈黄色,有绿色荧光,是络合滴定法测钙用的金属指示剂。利用以上3种荧光指示剂通过血流与新生骨中的钙离子螯合而可沉积在骨矿化前沿,在不脱钙切片上通过荧光显微镜可观察到骨小梁表面出现明显的荧光标线,以此来了解新骨生成的情况。多年的研究已使四环素等活性染料成为标记骨形成的成熟方法,已被广泛应用于骨生长代谢、新骨形成定位及速率测定研究中
[21-24]。现已有学者利用荧光染料成功示踪骨诱导性磷酸钙陶瓷中新骨的形成情况,证实用荧光染料技术评价磷酸钙陶瓷骨诱导性是切实可行的
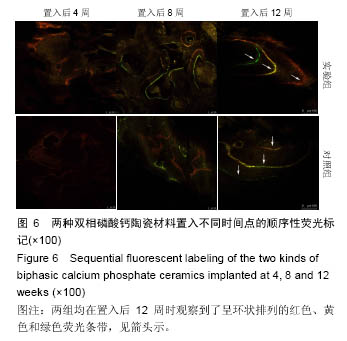
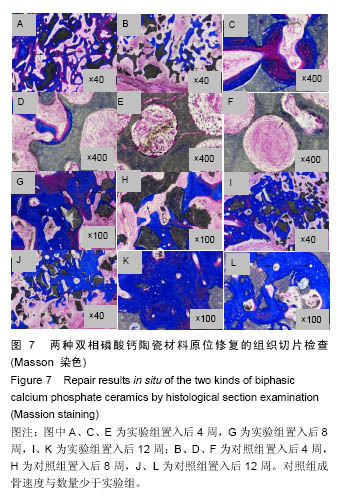
[8, 25-26]。在实验中,4周时注射的二甲粉橙荧光为红色,8周时注射的四环素的荧光为黄色,12周时注射的钙黄绿素荧光为绿色。在两组材料中,3种荧光均可看到,说明在材料原位修复的第4周就有新骨形成并矿化。在以往的异位骨诱导实验中,对照组在材料置入4周内并没有观察到荧光,说明在原位骨缺损的修复中,由于周围自体骨的存在,提高了材料成骨速度,新骨生成明显快于异位诱导骨生成。
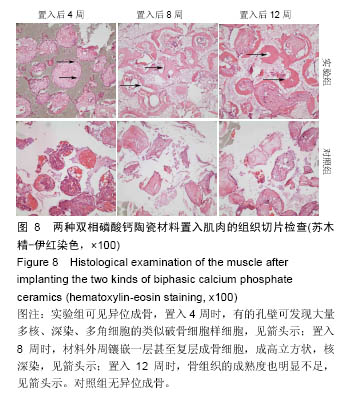
在肌肉组织中,实验组材料在第4周就发现了异位骨形成,并在材料孔隙边缘观察到大量破骨细胞样细胞,证明了此材料的优良的固有骨诱导性,早期就可诱导骨生成。值得注意的是在其诱导新骨生成过程,与原位成骨非常类似,说明了此种材料的异位成骨并非是病理性钙化,而是通过材料的特殊表面诱导细胞分化成骨形成的,是典型的骨膜成骨方式。对照组材料在直到12周内都未发现明显新骨形成,仅发现少量钙化沉积和多核巨细胞,说明该材料在异位无法诱导新骨成骨。两种材料化学成分相同,物理结构微观形态不同,就产生了巨大的骨诱导差异。
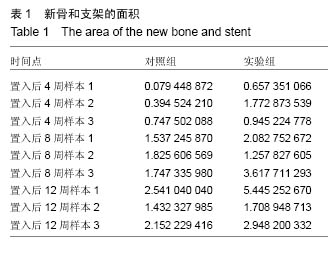
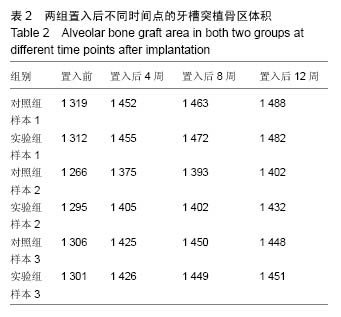
在原位成骨初期,实验组材料远离自体骨的部位,有大量类破骨细胞样的细胞和核深染的成骨细胞附着,并可见少量钙盐沉积和新骨形成。相对的在对照组材料中却只见到少量异物巨细胞,未观察到成骨现象。材料的以上表现非常类似于在异位肌肉材料中的早期成骨表现,说明在原位,实验组材料的固有骨诱导性使之启动新骨形成要早于无骨诱导性的对照组材料。因此实验组材料相对于对照组材料原位置入早期具有成骨方面的优势。这对早期启动骨缺损修复无疑是个福音。材料置入8,12周后,实验组材料与对照组材料的成骨差异相对减小。两者都可在镜下观察到大量新骨与血管从材料的孔隙隙中形成。在材料置入12周后,实验组骨小梁明显增粗并可见大量哈弗氏管结构,说明此时形成的新骨已较为成熟。而对照组新生的骨小梁则较细,哈弗氏管的数量也比实验组低。除了新骨成熟度不同外,两组材料在修复原位骨缺损的后期并没有其他细胞形态学上的差异。将两组材料成骨体积比进行统计学分析,显示在置入材料后第4周,实验组成骨体积比显著高于于对照组,而在第8,12周两者成骨体积比无统计学差异,这证明了实验组材料的特殊表面结构,在原位骨缺损的早期修复中起到明显促进作用。分析原因可能是由于实验组材料的特殊表面改变了局部微环境,远离自体骨部分通过诱导自体间充质干细胞更快地黏附和分化,更早启动骨生成。而对照组虽然没有骨诱导性,导致新骨形成较慢,但还是具有传统磷酸钙陶瓷良好的骨传导性和生物相容性,在后期成骨也获得了较满意的修复效果。综上所述,新型固有骨诱导性磷酸钙陶瓷材料在修复牙槽突裂缺损中较传统磷酸钙陶瓷材料成骨启动更早,成骨速度更快,成骨量更多。
比较实验组材料在肌肉(异位)和牙槽突(原位)内的成骨表现,在牙槽突内形成的新骨厚度明显较厚,骨小梁较粗,骨组织成熟度也较高。因此材料在原位所表现的成骨能力远高于在异位。原因可能是在原位缺损中周围组织含有大量细胞因子和成骨干细胞,具备良好的成骨环境,而在肌肉中则缺乏这些成骨条件,因而产生较大的成骨差异。
临床上成功的植骨可使单尖牙从植骨区正常萌出,可拥有完整的牙列。据国内外报道,有80%-96%的患者尖牙萌出后尚需经正畸矫正至正常位
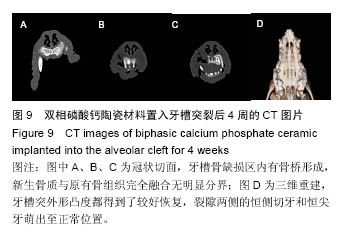
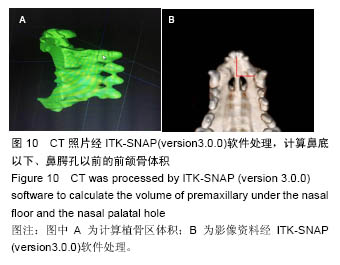
[27-29]。对难以萌出或缺失的牙齿,则需义齿修复或种植体修复。因此,牙齿能否在植骨区内移动和萌出时评判该材料是否可以应用于修复牙槽突裂缺损的重要指标。通过材料置入后的CT检查,可看到裂隙两侧的恒侧切牙和恒尖牙萌出至正常位置,证明该材料并不影响牙齿在其中的移动。
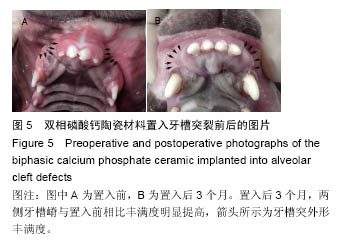
临床上使用自体骨修复牙槽突裂最常见的并发症就是植入骨的吸收,导致术后牙槽突外形恢复不佳
[14-15]。根据材料置入后所拍摄的CT图像及后期的统计学分析证明,置入的材料很好恢复了两侧牙槽突的外形,在材料置入后的4,8,12周都未发生植骨区吸收和塌陷。因此此次实验使用的新型磷酸钙材料能在新骨完全形成前保持支架外形,避免了术后牙槽突外形塌陷的不良后果。
然而由于所使用的为普通螺旋CT,精度有限,无法通过其灰阶来区分材料和骨,因而无法进一步分析其三维数据和成骨量。锥束CT相较传统CT检查计量低、空间分辨率高、扫描快,对于三维分辨能力有显著优势,特别适用于成像范围较小的口腔领域
[30]。未来有望通过锥束CT更深一步取得材料的三维实验数据。此次实验显示,具备固有骨诱导性、高孔隙率和低力学性能的双向磷酸钙陶瓷在修复牙槽突裂原位缺损中较传统磷酸钙陶瓷材料更具有优势。
.jpg)
.jpg)
.jpg)
.jpg)