中国组织工程研究 ›› 2017, Vol. 21 ›› Issue (6): 928-933.doi: 10.3969/j.issn.2095-4344.2017.06.019
• 药物控释材料 drug delivery materials • 上一篇 下一篇
四川省医疗器械生产企业无菌和植入性医疗器械生产现况:31家企业调查分析
周 晶1,2,叶 祥3,蒋学华1
- 1四川大学华西药学院,四川省成都市 610041;2四川省食品药品审查评价及安全监测中心,四川省成都市 610017;3四川省药械集中采购服务中心,四川省成都市 610041
Current situations of sterile and implantable medical device manufacturing in Sichuan Province: an investigation in 31 production enterprises
Zhou Jing1, 2, Ye Xiang3, Jiang Xue-hua1
- 1West China School of Pharmacy, Sichuan University, Chengdu 610041, Sichuan Province, China; 2Center for Food and Drug Evaluation, Inspection & Monitoring, Sichuan Drug and Food Administration, Chengdu 610017, Sichuan Province, China; 3Purchasing Service Center for Drug and Facilities of Sichuan Province, Chengdu 610041, Sichuan Province, China
摘要:
文章快速阅读:
.jpg)
文题释义:
医疗器械及产品:医疗器械,是指直接或者间接用于人体的仪器、设备、器具、体外诊断试剂及校准物、材料以及其他类似或者相关的物品,包括所需要的计算机软件;其效用主要通过物理等方式获得,不是通过药理学、免疫学或者代谢的方式获得,或者虽然有这些方式参与但是只起辅助作用的产品。国家对医疗器械产品按照风险程度高低实行分类管理,分为第一类、第二类、第三类医疗器械。
医疗器械生产质量管理规范:为加强医疗器械生产监督管理,规范医疗器械生产质量管理,国家食品药品监督管理总局组织修订了《医疗器械生产质量管理规范》,要求:医疗器械生产企业在医疗器械设计开发、生产、销售和售后服务等过程中应当遵守本规范的要求;应当按照本规范的要求,结合产品特点,建立健全与所生产医疗器械相适应的质量管理体系,并保证其有效运行;应当将风险管理贯穿于设计开发、生产、销售和售后服务等全过程,所采取的措施应当与产品存在的风险相适应。
背景:国家食品药品监督管理局(以下简称国家总局)于2009年12月16日发布《关于印发医疗器械生产质量管理规范(试行)的通知》,要求于2011年1月1日首先在风险较高的无菌和植入性医疗器械生产企业实施。修订后的《规范》于2014年12月29日公告发布,并于2015年3月1日起施行。
目的:分析四川省31家无菌和植入性医疗器械生产企业的现状以及实施《规范(试行)》的情况,并提出针对性建议。
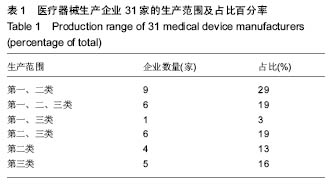
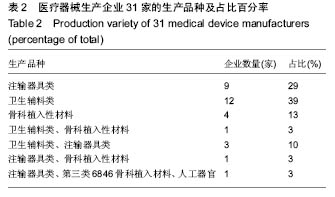
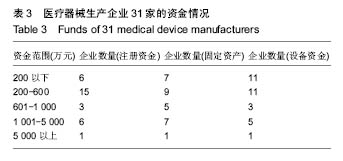
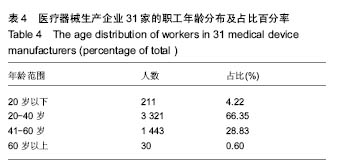
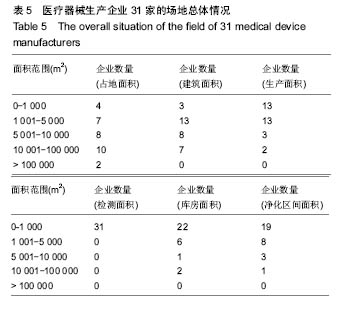
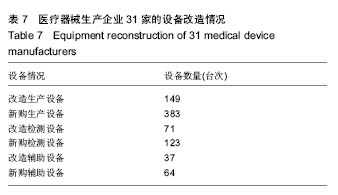
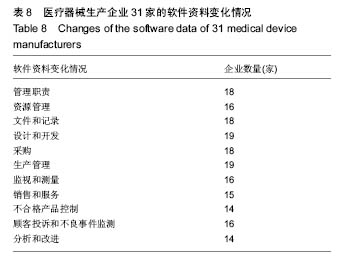
方法:通过质量管理体系考核、监督检查、飞行检查、问卷调查等形式收集了四川省31家无菌和植入性医疗器械生产企业的相关数据资料,并对数据进行了统计分析。
结果与结论:四川省医疗器械生产企业整体规模偏小,设备不够先进,从业人员素质偏低,资金不足,管理不到位。在此基础上,作者从生产和监管2个方面出发,为《规范》有效实施提出了指导性建议。
中图分类号:

.jpg)