中国组织工程研究 ›› 2020, Vol. 24 ›› Issue (23): 3636-3642.doi: 10.3969/j.issn.2095-4344.2645
• 骨组织构建 bone tissue construction • 上一篇 下一篇
牛膝甾酮干预SD乳鼠成骨细胞的增殖与分化
姜 涛1,2,3,邵 敏3,陈庆真1,3,凌翠敏4,申 震1,2,王 刚1,2,霍少川5,林燕平1,2,3,刘海全3,汪钦生3,曾振明3
- 1广州中医药大学,广东省广州市 510405;2广州中医药大学岭南医学研究中心骨伤科实验室,广东省广州市 510405;3广州中医药大学第三附属医院,广东省广州市 510240;4广东省第二中医院,广东省广州市 510095;5南方医科大学,广东省广州市 510515
Inokosterone effects on proliferation and differentiation of osteoblasts from neonatal Sprague-Dawley rats
Jiang Tao1, 2, 3,
Shao Min3, Chen Qingzhen1, 3, Ling Cuimin4,
Shen Zhen1, 2, Wang Gang1, 2, Huo Shaochuan5, Lin Yanping1, 2, 3, Liu Haiquan3, Wang Qinsheng3,
Zeng Zhenming3
- 1Guangzhou University of Chinese Medicine; 2Laboratory of Orthopedics and Traumatology of Lingnan Medical Research Center, Guangzhou University of Chinese Medicine; 3The Third Affiliated Hospital of Guangzhou University of Chinese Medicine; 4Guangdong Second Traditional Chinese Medicine Hospital; 5Southern Medical University
摘要:

文题释义:
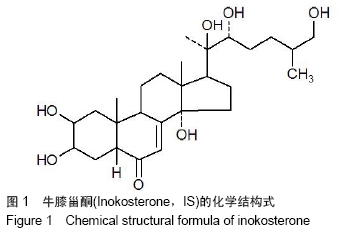
牛膝甾酮:牛膝为苋科植物牛膝的干燥根,主要含有甾酮类、皂苷类及多糖类成分,具有调节糖代谢、抗炎、镇痛、降血糖、免疫调节等作用,牛膝甾酮是其活性成分之一,目前尚无文献报道其对成骨细胞的生物学效应。
成骨细胞:由间充质干细胞分化而来,直接参与骨形成,其增殖、分化缺陷是骨质疏松症发病的重要原因,研究表明改善成骨细胞功能可有效治疗骨质疏松症。
背景:促进成骨细胞的增殖以及分化是治疗骨质疏松症的有效手段之一,但关于牛膝甾酮对成骨细胞增殖、分化的影响却没有报道。
目的:研究牛膝甾酮对SD乳鼠成骨细胞增殖、分化的影响及其潜在的分子机制。
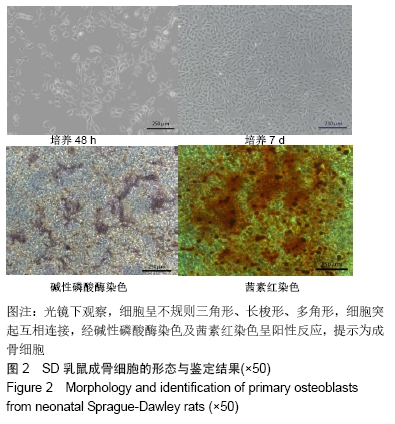
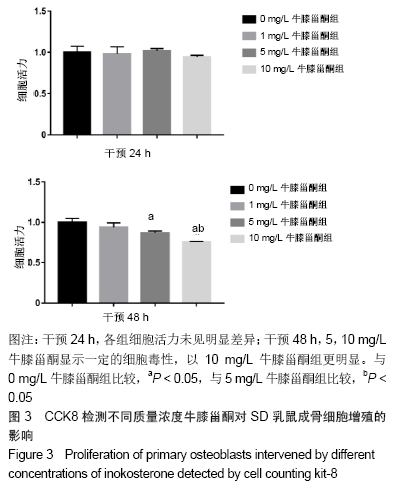
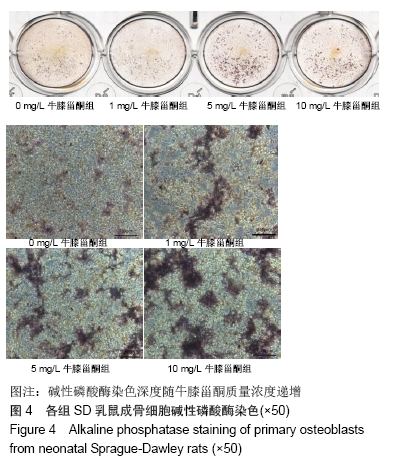
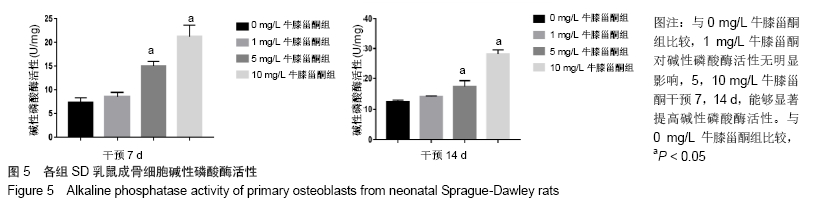
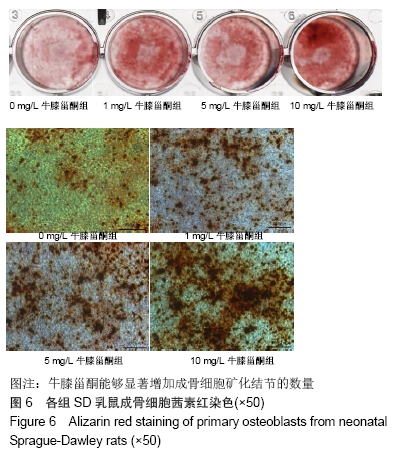
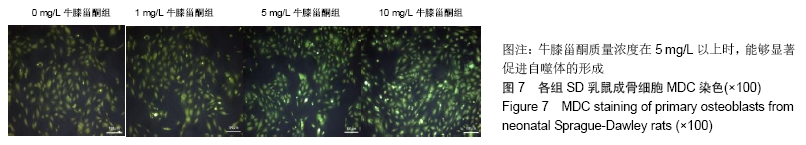
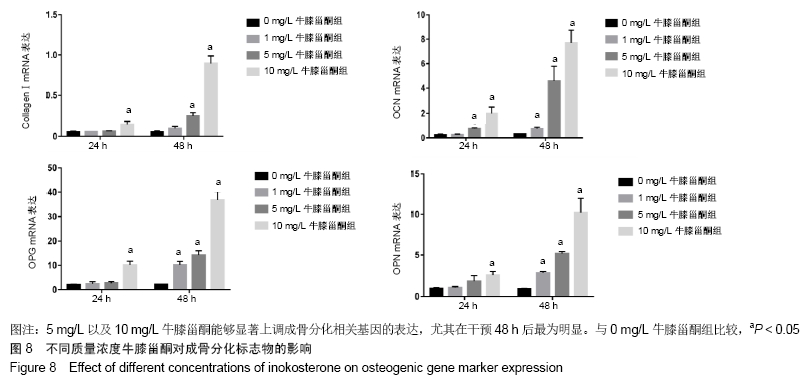
方法:通过酶消化法获得SD乳鼠成骨细胞,体外诱导培养并鉴定;采用CCK8法检测不同质量浓度牛膝甾酮(1,5,10 mg/L)对成骨细胞活力的影响;采用碱性磷酸酶染色及碱性磷酸酶活性试剂盒评价成骨细胞的早期分化能力;采用茜素红染色观察钙结节的形成数量,评估成骨细胞的矿化能力;采用实时荧光定量PCR法检测成骨分化标志物的表达水平;采用MDC染色检测自噬小体数量。
结果与结论:①相对于不加药对照组,牛膝甾酮在一定程度上抑制成骨细胞的增殖(P < 0.05),但却能够显著促进碱性磷酸酶活性及矿化结节的形成(P < 0.05),同时上调成骨分化标志物CollagenⅠ、OPG、OPN、OCN的表达水平,此外牛膝甾酮还能够促进自噬小体的形成;②结果提示,牛膝甾酮能够通过上调成骨分化相关基因及刺激自噬体的形成而促进成骨细胞的分化。
ORCID: 0000-0002-2837-6347(姜涛)
中国组织工程研究杂志出版内容重点:组织构建;骨细胞;软骨细胞;细胞培养;成纤维细胞;血管内皮细胞;骨质疏松;组织工程
中图分类号: