中国组织工程研究 ›› 2020, Vol. 24 ›› Issue (17): 2759-2769.doi: 10.3969/j.issn.2095-4344.2537
• 组织构建综述 tissue construction review • 上一篇 下一篇
血管内皮生长因子有望成为加速骨折愈合的全新治疗手段
钱洲曜,王勇平
- 兰州大学第一医院骨科,甘肃省兰州市 730000
-
收稿日期:2019-07-30修回日期:2019-08-02接受日期:2019-09-21出版日期:2020-06-18发布日期:2020-03-30 -
通讯作者:王勇平,博士,博士后,硕士生导师,兰州大学第一医院骨科,甘肃省兰州市 730000 -
作者简介:钱洲曜,男,1997年生,江苏省无锡市人,汉族,兰州大学在读本科生。 -
基金资助:国家自然科学基金项目(81960398);甘肃省高等学校科研项目(2018B-013);兰州市科技计划项目(2017-4-58);兰州市城关区科技计划项目(2018-1-2);兰州大学第一医院科研项目(ldyyyn2017-21,ldyyyn2018-47)
Vascular endothelial growth factor intervention: a new approach for accelerating fracture healing
Qian Zhouyao, Wang Yongping
- Department of Orthopedics, First Hospital of Lanzhou University, Lanzhou 730000, Gansu Province, China
-
Received:2019-07-30Revised:2019-08-02Accepted:2019-09-21Online:2020-06-18Published:2020-03-30 -
Contact:Wang Yongping, MD, Master’s supervisor, Department of Orthopedics, First Hospital of Lanzhou University, Lanzhou 730000, Gansu Province, China -
About author:Qian Zhouyao, Department of Orthopedics, First Hospital of Lanzhou University, Lanzhou 730000, Gansu Province, China -
Supported by:the National Natural Science Foundation of China, No. 81960398; Gansu Provincial Higher Education Research Project, No. 2018B-013; Lanzhou Science and Technology Plan Project, No. 2017-4-58; Lanzhou Chengguan District Science and Technology Plan Project, No. 2018-1-2; Lanzhou University First Hospital Research Project, No. ldyyyn2017-21 and ldyyyn2018-47
摘要:
文题释义:
血管内皮生长因子:一种高度保守的同源二聚体糖蛋白,广泛分布于人和动物的器官与组织中,如:肺、肾、脾、成骨细胞、软骨细胞、肥大细胞中,主要作用为促进内皮细胞增生、提高内皮细胞通透性、维持血管稳定性,是调节细胞生长,促进细胞分裂、迁移及增殖的重要因素。
骨折愈合:骨折愈合的标准有局部无压痛,无纵向叩击痛;局部无异常活动;X射线照片显示骨折线模糊,有连续性骨痂通过骨折线等。根据组织学及细胞学的变化,将骨折愈合分为3期,即:血肿炎症机化期、原始骨痂形成期和骨板形成塑形期。
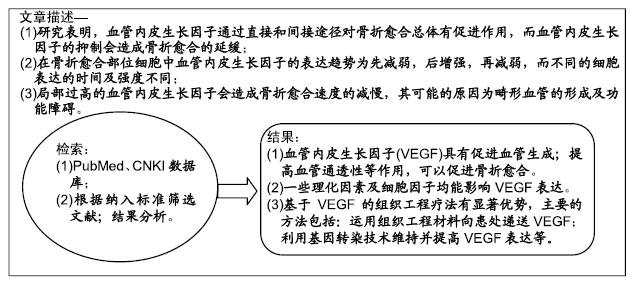
背景:血管内皮生长因子是一种多功能的细胞因子,具有促进血管生成、提高血管通透性、维持血管稳定性等功能,对骨折愈合及骨再生过程有积极意义,基于血管内皮生长因子的治疗方法有望成为加速骨折愈合的全新治疗手段。
目的:探讨血管内皮生长因子对骨折愈合的影响,并对其影响因素及临床应用进行综述。
方法:检索 CNKI,PubMed 数据库2014年1月至2019年3月文献,以“血管内皮生长因子,骨折愈合”为中文检索词,“vascular endothelial growth factor,fracture healing”为英文检索词,检索有关血管内皮生长因子对骨折愈合影响作用的文章。共检索到 167篇文献,通过阅读文题、摘要进行初筛,排除无关的或内容重复的文献,最后纳入符合标准的85篇文献作进一步分析。
结果与结论:①血管内皮生长因子存在于骨折断端不同细胞内,且不同细胞内表达具有显著的周期性;②血管内皮生长因子具有促进血管生成、提高血管通透性、维持血管正常形态及完整性的作用,并由此促进骨折愈合及骨再生过程;③一些理化因素及细胞因子均能影响血管内皮生长因子表达,从而影响骨折愈合过程;④基于血管内皮生长因子的组织工程疗法有显著优势,主要的方法包括:运用组织工程材料向患处递送血管内皮生长因子;利用基因转染技术维持并提高血管内皮生长因子表达;将血管内皮生长因子与其他细胞因子及外源性干细胞联合应用;基于提高血管内皮生长因子的生物涂层应用;⑤随着医学研究的重点向“交叉学科”发展,相信未来基于血管内皮生长因子的组织工程学治疗会是医学研究的热点。
ORCID:0000-0001-8045-9767(钱洲曜)
中国组织工程研究杂志出版内容重点:组织构建;骨细胞;软骨细胞;细胞培养;成纤维细胞;血管内皮细胞;骨质疏松;组织工程
中图分类号:
引用本文
钱洲曜, 王勇平. 血管内皮生长因子有望成为加速骨折愈合的全新治疗手段[J]. 中国组织工程研究, 2020, 24(17): 2759-2769.
Qian Zhouyao, Wang Yongping. Vascular endothelial growth factor intervention: a new approach for accelerating fracture healing[J]. Chinese Journal of Tissue Engineering Research, 2020, 24(17): 2759-2769.
2.1 VEGF及其受体的结构特点及生物学作用 VEGF是相对分子质量为34 000-45 000的二聚体糖蛋白,其由2个相同的相对分子质量23 000的亚基经二硫键连接而成。人的VEGF基因位于染色体的6p21,3上,全长28 kb。编码VEGF的基因长约14 kb,由7个内含子和8个外显子交替构成。VEGF蛋白由一系列多肽同种型组成,通过初级转录物的可变剪接从单拷贝基因产生。目前发现有6种单体,根据氨基酸的长短依次命名为VEGF206(包含所有外显子及部分第7内含子)、VEGF189(包含8个外显子)、VEGF183、VEGF165(缺少外显子6)、VEGF145(缺少外显子7)、VEGF121(缺少外显子6和7)。各单体本身无活性,但除同型二聚体VEGF121外,其余VEGF亚型的同二聚体生物活性基本相同,均可在体外结合肝素并在体内结合细胞外基质的乙酰肝素衍生物。此外,VEGF还存在 5 种同源性蛋白,分别是胎盘生长因子(placental growth factor,PGF)、VEGF B、VEGF C、VEGF D 和口疮病毒(orfvirus VEGF,VEGF E),这些同源性蛋白均能不同程度地促进血管生成[7]。VEGF 通过旁分泌和自分泌形式产生后,其必须与相应的受体结合才能产生促进血管生成的效应。
现在公认的VEGF的经典受体有2种: VEGFR-1(Flt-1)和VEGFR- 2( KDR/Flk-1),它们均属于Ⅲ酪氨酸激酶受体,主要位于血管内皮细胞。此外还存在的受体有VEGFR-3(Flt-4)与neuropilin(NRP)[2]。与大多数肽生长因子相似,VEGF与其受体在靶标的细胞表面上结合(见图2)。
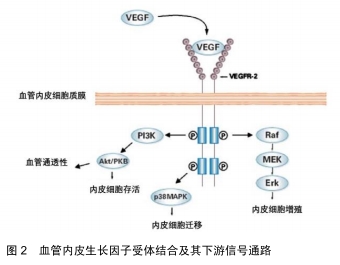
VEGF mRNA在多种正常成人组织中、胚胎发育过程中和许多肿瘤中表达。在SHIFREN等[2]的研究中,所有胎儿组织中均检测到编码VEGF的mRNA,其中人胎肺、肾和脾表达最多;心脏、肾上腺、胰腺、肠、肝、睾丸、皮肤、肌肉和大脑表达次之;胸腺和胎盘表达最少。在VEGF过表达的位点,Flt-1和Flk-1在相邻的微血管内皮细胞中通常也存在过表达。VEGF一级蛋白质序列与胎盘生长因子具有同源性,VEGF和胎盘生长因子都含有八-半胱氨酸残基序列特征,因此同型二聚体PGF/PGF和VEGF/VEGF和异二聚体PGF/VEGF均具有活性。VEGF同源二聚体与Flt-1和 Flk-1受体结合;胎盘生长因子同型二聚体仅与Flt-1受体结合。而NPR主要位于细胞内,NPR可通过提高Flk-1的活性,促进与VEGF的结合;同时,NPR是VEGF特异性的受体亚型,可增加有丝分裂原和 VEGF165 的趋化活性,但NPR对 VEGF121作用不明显。DVORAK等[3]在研究中指出由于VEGF121及VEGF165对细胞表面蛋白聚糖具有更大的亲和力,所以它们多以可溶形式分泌。另外,虽然VEGF最初是基于与肝素的亲和力而纯化的,但VEGF165对肝素的亲和力却显著低于其他典型的肝素结合生长因子如碱性成纤维细胞生长因子,而较小的VEGF121同种型则不与肝素结合。VEGF通过与不同的内皮细胞受体结合起作用,该作用效果类似于内皮细胞与其激动剂如凝血酶和组胺结合,但该过程中VEGF不受凝血酶和组胺抑制剂的影响。当VEGF与内皮细胞受体结合时,内皮细胞内钙离子浓度升高,同时伴有von Willebrand因子释放增加。VEGF刺激IP3,使其积累并通过磷酸肌醇特异性磷脂酶C起作用,从而促进内皮细胞的分裂、迁移和增殖[3]。此外,VEGF通过旁分泌机制,刺激体内新血管的生成,增加血管通透性,对维持血管的正常状态和完整性具有重要意义[1-2,8]。
VEGF是已知的最有效的血管透化剂之一, 它被用于提高许多部位血管床的通透性,包括皮肤、腹膜壁、肠系膜和膈肌等。VEGF的血管透化作用发生迅速,在VEGF注射的几分钟内就明显出现。但是单次注射VEGF所引起的血管通透性提高是暂时且可逆的,若持续时间<30 min,则与内皮细胞或其他微血管成分的可检测损伤无关。VEGF的血管透化作用不被抗组胺药或包括抑制血小板活化因子在内的各种炎症抑制剂阻断。细胞器-囊泡-液泡细胞器(VVO)为血浆和血浆蛋白提供了离开循环并进入组织的途径,VEGF通过VVO的功能活性,显著增加了微血管的通透性。除肿瘤细胞的细胞质中,强免疫组织化学染色显示VEGF也持续存在于邻近的高渗透性和复制性微血管中。超微结构免疫细胞化学将肿瘤微血管结合的VEGF更精确地定位于内皮细胞质膜的近腔表面和VVO。研究者还发现VEGF可以起到打开“窗孔”的作用,从而促进血浆蛋白等的外渗。VEGF还刺激小鼠单核细胞和胎牛成骨细胞的迁移,这是VEGF对血管内皮细胞以外的细胞发挥的直接生物学作用。另外,VEGF改变内皮细胞基因活化的模式,上调纤溶酶原激活物(PA)、尿激酶纤溶酶原激活剂(uPA)、组织型纤溶酶原激活剂(tPA)以及纤溶酶原激活物抑制剂PAI-1的表达。此外,VEGF还诱导间质胶原酶和组织因子的表达。VEGF的组成型过表达与表型转化和生长在体内的血管化、原发性、可移植的肿瘤有关。这种VEGF沉积模式可以反映与特定VEGF受体的结合。VEGF与内皮细胞的结合除具有细胞信号传导的功能外,还具有许多其他功能,例如,它可以用于保持VEGF定位,有效防止VEGF的大面积传播并阻止其潜在的生物活性危害。此外,在没有肿瘤细胞的情况下,向豚鼠中植入交联的纤维蛋白能诱导新血管和成纤维细胞进行性地向内生长,这些血管和成纤维细胞一起产生许多肿瘤中发现的血管化基质。纤维蛋白可能是通过其arg-gly-asp(RGD)序列提供的细胞黏附和迁移功能,从而发挥其促血管生成作用。这些发现表明在成体组织中,为响应不同的刺激,血管的生成均是由VEGF过表达和血管通透性增加所引发[1-2,8]。
2.2 VEGF在骨折愈合的表达及作用 骨折过程中,在细胞因子、生长因子和转录因子的控制下,骨折后的骨折愈合是极其漫长且复杂的修复过程[9]。骨折后受伤部位周围会立即形成血肿,而后受伤部位会有免疫细胞渗入;此后,纤维组织在受伤部位生长,并进一步发展成为含有新生软骨的软骨痂;软骨周围毗邻的血管会沿软骨向内生长,使其生长为硬骨痂,并对骨折愈合具有支持作用;最后由皮质骨和髓质骨对其进行替代[10]。根据以上特点将骨折愈合分为3个期:血肿机化期、骨痂形成期和骨痂改造塑形期。
曾中华等[11]通过Wistar大鼠的股骨骨折愈合模型,采用免疫组织化学、苏木精-伊红染色等方法,发现VEGF在骨折后1 d即呈现阳性表达,骨折后7-28 d为VEGF的表达高峰期,骨折晚期VEGF仅在破骨细胞呈阳性表达。贾勇等[12]在研究中利用Western blot技术对骨折端VEGF的表达检测发现,骨折后8 h VEGF表达出现明显增高,在24 h有所降低,之后又迅速回升,并在骨折后72 h-3周维持在较高的状态,5-8周表达出现连续的降低。施红光等[13]在研究中运用RT-PCR方法检测大鼠骨折不同阶段骨痂组织中VEGF基因的动态表达及变化,发现骨折后3-6 d VEGF表达量较弱,大约在骨折后3周VEGF mRNA表达量达到高峰,为初期的8.0-9.0倍。武永刚等[14]在研究中利用RT-PCR技术分析骨痂组织中VEGF165 mRNA含量,发现在骨折初期VEGF的表达呈现平稳的由弱增强再减弱的趋势,当2周时达到最强,约为初期的2.4倍。刘志奎等[15]构建了大鼠股骨骨折模型,通过免疫组织化学和原位杂交方法检测可见术后1-4周的骨折部位,不同时间有多种组织细胞参与VEGF及VEGF mRNA的表达。由骨痂中VEGF及VEGF mRNA平均阳性细胞百分率得出其表达趋势也是相似的,即创伤后7 d骨折位点均表达增强,14,21 d仍保持高水平表达,28 d骨折位点表达降低。阳春华[16]采用光镜观察(苏木精-伊红染色)和免疫组织化学(SP-9000法)对行关节置换手术治疗的股骨颈骨折患者的股骨头标本进行组织学观察及VEGF检测后,发现股骨颈骨折患者(骨折后1个月内)股骨头中VEGF的表达随着受伤后时间的延长呈增高趋势。
由于骨折后7-28 d为VEGF的表达高峰期,同时为血管生成的高峰期,所以曾中华等[11]认为VEGF与骨折端血管重建相关。同时,由于骨折后期仅破骨细胞内表达VEGF,他们推测VEGF参与骨折端的塑性过程,施红光等[13]的研究也得出了相似的观点。刘磊[17]通过X射线摄片,苏木精-伊红染色细胞组织学评价,统计学分析骨折断端软骨细胞骨化率,对使用VEGF的小鼠胫骨骨折模型的研究中得出VEGF能通过增加骨折端血流量、促进骨折端及周围软组织血管的生成,从而使内皮细胞增殖、调节破骨细胞活性。同时,VEGF还参与软骨的成熟和吸收,促进软骨内成骨与成骨细胞相互作用,诱导骨形成,最终促进骨愈合。已有的研究证实骨折愈合过程中浸润的骨祖细胞保留了软骨形成和/或成骨分化的能力[18],而VEGF对骨祖细胞在向骨组织的转化至关重要。HAUSMAN等[19]发现在大鼠骨折模型中进行抗血管生成治疗后,骨折愈合反应严重受损,缺乏软骨分化,均表明VEGF的抑制会造成骨折愈合的抑制或延迟。同时,在生长板的骨修复过程中,VEGF也起到了相似的作用[20]。VEGF(特别是VEGFA同种型)的表达分为2个阶段,首先使软骨膜血管化,然后使肥大软骨细胞区血管化[21]。另外,VEGF在骨生长和骨折修复期间通过肥大软骨细胞分泌到软骨基质中,后者可以局部重现软骨内骨化的过程。VEGF与基质中的硫酸乙酰肝素结合,并通过骨/软骨细胞衍生的乙酰肝素酶的作用释放[22]。YUASA等[23]通过结合骨血管造影和可重复的小鼠股骨骨折模型的新技术,克服了经典的移位骨折血运重建模型的局限性,首次证明了移位/稳定性骨折血运重建的完整时空模式。移位骨折愈合过程中新骨的形成是通过膜内和软骨内骨化来实现。在膜内骨化期间,内皮细胞和成骨细胞通过VEGF受体(包括VEGFR1)对VEGF-A的趋化和增殖反应调节新骨形成。YUASA等[23]通过免疫荧光观察,发现膜内骨化的初始部位为骨膜区域,其中表达最强的是VEGF-A。在同一位置,存在许多在形态上与成骨细胞和内皮细胞一致的VEGFR1和VEGFR2阳性细胞。由此,他们认为一方面膜内骨化和血运重建的初始部位发生在骨折部位的近端和远端部位,其中骨膜插入相邻的未受累的皮质骨,其原因为该处是髓内血流分流到骨膜的部位;另一方面,尽管VEGF释放的起始信号尚不清楚,但该位点骨膜中VEGF-A的免疫定位可能有助于VEGFR1和VEGFR2-阳性间充质细胞,内皮细胞和成骨细胞的募集和/或活化,从而在骨膜下间隙支持膜内血管生成和骨形成。另外,他们通过对软骨内骨化的观察情况认为一方面VEGF-A/VEGFR系统是从软组织愈伤组织向硬组织愈伤组织转变的必要组分,并由此导致血管形成和骨愈合;另一方面,软骨细胞肥大和VEGF-A的释放导致极化,通过在愈伤组织周围募集脉管系统和间充质骨祖细胞来形成骨。但是局部的VEGF浓度过高也会导致畸形血管的形成及功能障碍[24],不利于骨折愈合。
2.3 物理因素对VEGF的影响
2.3.1 X射线 宋祥胜[25]在右侧股骨中段闭合骨折模型中,对大鼠进行总量为1 Gy的低剂量全身照射。MicroCT断层扫描提示术后2周实验组血管体积总量及血管体积分数明显高于对照组(P < 0.05)。使用ELISA法发现在术后第2和3周,实验组血清VEGF含量明显高于对照组(P < 0.05)。RT-PCR和Western-blot法显示骨痂中两组VEGF mRNA及VEGF蛋白在骨折愈合期也都有表达,并分别在术后第2和3周达到高峰,且此时实验组也显著强于对照组(P < 0.05)。免疫组织化学染色表明在术后第2和3周,实验组骨痂处的CD31、CD34、VEGF和VEGFR2表达强于对照组(P < 0.05)。因此,研究者认为低剂量的X射线照射能上调VEGF的表达,从而能促进血管新生,而这两者也是促进骨痂矿化的原因,并且术后第2和3周可能是关键的作用时间点。
2.3.2 固定方式 骨折修复包括纤维骨痂、软骨骨痂和成熟的骨性骨痂,而骨折的固定方式可使骨痂中不同组织成分的比例发生改变。内固定多以膜内成骨方式在骨皮质间形成直接骨愈合,其原因为骨折断端周围的骨痂产生很少, 骨折间的活动减少;而在闭合性骨折外固定中, 骨折周围可产生大量的纤维骨痂及软骨骨痂。武永刚等[26]在研究中指出在骨折修复过程中的早、中期外固定组骨痂中的VEGF表达明显高于内固定组, 外固定组的骨痂形成速度及数量上高于内固定组,血管形成的量及时间也早于内固定组。但随着内固定材料的飞速发展,骨折切开内固定的手术指征也逐渐增宽。
2.3.3 磁场 沈建国[27]研究发现恒磁场促进深创面愈合的机制可能和在创面愈合早、中期增强VEGF的表达有关;同时,应用0.32 T恒磁片较0.16 T恒磁片能使SD大鼠深创面在愈合过程早、中期VEGF表达增高。研究者推测磁场强度越高,促进成纤维细胞和血管内皮细胞产生定向移动的速度越快有关,越有益于创面愈合。
2.3.4 海水浸泡 林建宁等[28]对骨折部位采取海水浸泡的方式,通过对VEGF的表达情况测定发现,采用海水浸泡法的VEGF表达与一般的开放骨折愈合过程的VEGF表达无显著差异(P > 0.05)。所以,他们认为虽然海水浸泡使骨折骨痂形成不良率增高,骨折愈合过程有延迟倾向,但其与VEGF无显著关联。
2.3.5 手术时机 董黎强等[29]在大鼠股骨骨折模型造模后的不同时间分别行切开复位内固定手术,通过免疫组织化学染色观察骨折端VEGF表达情况。他们发现第7,11天手术组能较好地促进骨折端VEGF表达,且持续时间长,第14天手术组次之。其余各组VEGF表达情况均不理想。所以,他们认为手术时机影响骨折端VEGF的表达,从而影响骨折愈合情况。最佳手术时机应在第1,2周时段,骨折后几天内即进行手术操作可能不利于骨折的愈合,而且可能加速二次损伤。
2.3.6 微动 乔林[30]研究发现微动促进骨折端的局部血流量,通过微动组的骨痂弯曲刚度、扭转刚度、扭转强度显著高于固定组及微动组骨折端转化生长因子β、碱性成纤维细胞生长因子、VEGF蛋白及mRNA表达显著增高,他们认为微动可促进骨折愈合。
2.3.7 超声 VAVVA等[31]在研究中发现超声可以改变VEGF传递情况,增强成骨细胞中VEGF含量,并由此加快新生血管的形成,从而改善骨折愈合的情况。
2.3.8 高压氧 CHEN等[32]使用高压氧治疗短暂海水浸泡后兔胫骨开放性骨折,他们发现VEGF主要在成骨细胞、软骨细胞和骨细胞的细胞质中表达,并在不同时间点表现出显著变化;同时,高压氧治疗组骨折区骨性骨痂和成熟骨细胞未见炎性细胞浸润;第4周时,高压氧治疗组丙二醛含量较低,超氧化物歧化酶活性较高,而在第8,12周,两组间无显著差异。因此,研究者认为高压氧治疗可减轻炎症反应和再灌注损伤,有利于骨细胞增殖和骨折愈合。
2.3.9 骨折稳定性 HISTING等[33]将21只CD-1小鼠在股骨中段骨折后用髓内螺钉稳定,允许微动和软骨内愈合;在另外22只小鼠中,对股骨骨折未使用稳定操作。研究者通过生物力学分析发现,未稳定骨折的生物力学刚度较低;通过放射学及组织形态学分析,发现在骨折愈合的早期阶段,非稳定性骨折显示出较低量的骨组织和较高量的软骨组织,在骨折愈合的晚期阶段非稳定性骨折仍显示大量骨痂组织和大量编织骨,但稳定性骨折中,整个板层骨几乎被完全重塑。有趣的是,骨痂组织的蛋白质印迹分析表明,在非稳定性骨折中,VEGF的表达显著降低,骨形态发生蛋白2和胶原蛋白10的表达略微降低。所以,研究者认为与稳定性骨折相比,小鼠未稳定的股骨骨折显示骨愈合明显延迟。
2.3.10 远程缺血后处理(RIPC) ZHOU等[34]应用远程缺血后处理技术研究大鼠胫骨骨折模型,通过微计算机断层扫描及生物力学测试,发现远程缺血后处理可显著促进骨折愈合,增高其机械强度。而由反转录定量聚合酶链反应、蛋白质印迹分析和免疫组织化学得出VEGF的表达在mRNA和蛋白水平显著增加。所以他们认为远程缺血后处理可上调VEGF表达,进而促进骨折愈合。
2.3.11 其他物理因素 此外,ROSSO等[35]还发现脉冲电磁场(PEMF)和体外冲击波治疗(ESWT)也可上调VEGF表达,有益于骨折愈合。
2.4 VEGF与骨形态发生蛋白的关系 骨形态发生蛋白属于转化生长因子β超家族,是唯一具有异位成骨能力的细胞因子,可促进诱导性骨源性前体细胞向确定性骨源性前体细胞分化[36-37]。同时,它与VEGF的表达及分泌密切相关,当骨形态发生蛋白与VEGF联合应用时似乎对骨折愈合极为有效[38]。已有的研究表明当VEGF与骨形态发生蛋白4协同作用于间充质细胞时,可以通过促进间充质细胞增殖来加强软骨内骨化早期阶段的软骨生成[39],同时,加快软骨吸收,使骨再生能力加强。还有研究发现骨形态发生蛋白可以通过p70S6激酶来干预成骨细胞中VEGF的合成[40],并具有剂量依赖性。DECKERS等[41]对前成骨样细胞(KS483)系进行体外培养,分别用骨形态发生蛋白2、骨形态发生蛋白4和骨形态发生蛋白6来加强骨结节形成、骨钙素表达;他们发现整个过程都伴有剂量依赖性VEGF蛋白水平表达的增强。若给予了VEGF抗体,无论是否由骨形态发生蛋白调控的血管生成都会受到抑制。因此,他们认为骨形态发生蛋白可对VEGF的表达起到正向调控作用,同时VEGF直接参与骨形态发生蛋白诱导的骨形成过程,并促进骨形成部位的血管形成。而TSIRIDIS等[42]的研究表明该过程似乎受转录因子Cbfa1/Runx2.7的表达调节。曾中华等[11]的实验中VEGF在骨折后1 d后即表达而骨形态发生蛋白2在骨折后3 d才表达,所以他们认为VEGF在一定程度上可能启动或促进了骨形态发生蛋白2的表达,从而促进了骨折愈合。
同时,在体外培养的成骨细胞、骨髓细胞、间充质干细胞等细胞中,骨形态发生蛋白和VEGF可以相互促进表达[43- 44]。DECKERS等[41]在体外培养鼠成骨细胞发现骨形态发生蛋白可诱导成骨细胞表达VEGF-A。BOULETREAU等[44]的实验表明骨折愈合过程中,低氧环境或运用外源性的VEGF 24-48 h后可促进骨形态发生蛋白2 mRNA及其蛋白的表达。同时,他们的实验提示血管内皮细胞除经典的新血管形成作用外,骨折端 骨形态发生蛋白2的表达加强时,亦具有成骨作用。最近,ARYAL等[45]回顾了骨形态发生蛋白2和VEGF在骨折中对于骨组织再生的作用,虽然单独使用骨形态发生蛋白2已经取得了不错的效果,但由于缺乏新生血管来加速血液供应,因此单独使用骨形态发生蛋白2存在缺陷。当应用骨形态发生蛋白拮抗剂评估体内间充质干细胞分化时,成骨细胞VEGF产生显著降低;与此同时,VEGF抗体表现出一种对骨形态发生蛋白介导的血管生成的阻断效果,所以VEGF与骨形态发生蛋白之间的作用是同时相互影响的[46]。KUMAR等[47]将VEGF和骨形态发生蛋白2联合运用于间充质干细胞,发现双重治疗组形成的新骨显示胫骨骨折后峰值负荷,韧性和僵硬度显著增加,也证明了这种骨修复的协同效应。
但是,有研究发现在皮质缺损愈合期间由骨形态发生蛋白2诱导的过量VEGF会抑制缺损中的骨形成,并可能抑制骨折愈合[48]。此外,研究者还发现成骨细胞中的VEGFR2可以抑制成骨细胞矿化和成熟。因此,研究者提出由重组骨形态发生蛋白2诱导的细胞外VEGF水平的增加可抑制间充质祖细胞的分化并抑制其进一步的成骨成熟[49]。有研究指出VEGF与骨形态发生蛋白2联合应用时的比例似乎影响骨形态发生蛋白2在骨修复中的作用。低VEGF/骨形态发生蛋白2比(1∶5)比高比例(5∶1)对骨再生有更好的诱导作用[50],表明高剂量rVEGF降低重组骨形态发生蛋白2的再生潜力。HU等[49]通过推注PBS或可溶性VEGFR1(sVEGFR1)(VEGF的诱饵受体)处理小鼠胫骨近端皮质骨缺损(直径为1 mm的钻孔),研究VEGF对骨形态发生蛋白2诱导皮质骨缺损的修复作用。他们发现骨形态发生蛋白2和sVEGFR1的共同递送逆转了骨形态发生蛋白2对膜内骨形成的抑制。此外,通过共同递送骨形态发生蛋白2和sVEGFR1,也可以防止骨形态发生蛋白2治疗组中缺失的胶原蛋白累积并且防止骨基质蛋白的产生。他们的数据表明,引入VEGF结合蛋白,如sVEGFR1,以降低细胞外VEGF水平,可能会增强骨形态发生蛋白2对膜内骨形成的影响。
2.5 其他细胞因子及激素对VEGF的影响 其他细胞因子及激素也对VEGF的表达有调节作用,它们对VEGF具体调节情况的研究见表1。
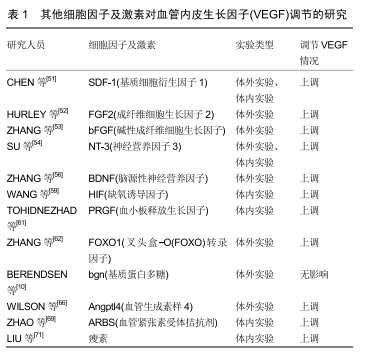
2.5.1 基质细胞衍生因子1 CHEN等[51]在体内与体外实验中均发现基质细胞衍生因子1可以提高VEGF的表达,并推测基质细胞衍生因子1与VEGF的信号通路之间存在关联,增多的VEGF可能导致骨髓间充质干细胞的血管化。
2.5.2 成纤维细胞生长因子 HURLEY等[52]在研究中指出成纤维细胞生长因子2可以促进成骨细胞释放VEGF,同时,血小板衍生生长因子为该作用的正调节因子。ZHANG等[53]在研究中发现碱性成纤维细胞生长因子与VEGF和血小板衍生生长因子存在协同效应,能增加新生血管形成,有益于骨折愈合。
2.5.3 神经营养因子 神经营养因子超家族包含神经营养因子3、脑源性神经营养因子等。SU等[54]在研究中发现神经营养因子3在受损生长板、矿化培养的大鼠骨髓间充质干细胞和内皮细胞中诱导VEGF表达。同时,他们的体外实验表明重组人神经营养因子3增强大鼠骨髓间充质干细胞成骨培养物中的VEGF表达,诱发血管形成。另外,在人骨髓基质细胞培养物中加入脑源性神经营养因子或神经营养因子3也能使VEGF蛋白分泌增加[55]。因此,他们认为神经营养因子3可通过VEGF的介导而增强生长板处血管生成及骨形成的能力,从而有益于骨折愈合。而ZHANG等[56]在研究中通过脑源性神经营养因子以剂量和时间依赖性方式刺激从SD大鼠分离的成骨细胞,发现在骨折愈合期间,脑源性神经营养因子可能通过TrkB /ERK1/2信号传导途径刺激成骨细胞中VEGF的表达和分泌,从而促进骨折愈合。
2.5.4 缺氧诱导因子 VEGFA是缺氧诱导因子的靶基因,有研究表明,上调缺氧诱导因子反应基因的脯氨酰羟化酶抑制剂可增加小鼠的愈伤组织大小和血管分 布[57-58]。WANG等[59]构建的转基因小鼠的股骨骨折模型中,成骨细胞中过度表达缺氧诱导因子α,由microCT显示骨量及血管分布均增加,并且通过股骨纵向切片的原位杂交显示股骨小梁骨中VEGFA的表达增加。WAN等[60]的研究表明,在成骨细胞中过表达缺氧诱导因子1α的转基因小鼠在牵张成骨反应中产生更多的骨,并且增加其血管分布。
2.5.5 血小板释放生长因子 TOHIDNEZHAD等[61]在实验中通过ELISA表明,用血小板释放生长因子诱导处理后VEGF的蛋白质水平增高。实时RT-PCR数据显示血小板释放生长因子处理后VEGF的基因表达上调。在血小板释放生长因子存在下,通过双荧光素酶报告分析系统发现ARE的活性增加了50%。蛋白质印迹表明Nrf2的核积累增强,同时发现Nrf2下游靶标的蛋白质表达的增加。因此,研究者认为血小板释放生长因子不仅可以增加内源性VEGF,还可以通过Nrf2-ARE信号通路参与预防氧化损伤,从而改善骨折愈合。
2.5.6 FOXO1 FOXO1是一种叉头盒-O(FOXO)转录因子,在软骨细胞中表达,已被证明可调节软骨细胞及软骨细胞的下游基因靶点活性。ZHANG等[62]在研究中发现软骨细胞中的FOXO1缺失显著降低了这些细胞中的VEGFA表达并且减少了与软骨相邻的过渡区中的血管形成。在体外实验中还发现软骨细胞以FOXO1依赖性方式表达VEGFA。另外,通过ChIP测定得到了FOXO1与VEGFA启动子结合,通过共转染实验表明FOXO1调节VEGFA转录活性。与此同时,通过荧光素酶和qPCR等实验证实了FOXO1的转录活性随着乙酰化水平的增高而降低。所以,他们认为FOXO1通过VEGF,对骨折愈合起重要作用。
2.5.7 其他细胞因子 血小板衍生生长因子、肝细胞诱导因子、富含血小板血浆、Nrf2(核因子红细胞2相关因子2)、PTX(己酮可可碱)均能诱导VEGF表达,由此促进新生血管形成[63-65]。
2.5.8 Bgn(基质蛋白多糖) BERENDSEN等[10]通过测量His标记的重组Bgn及固相结合测定人核心Bgn(缺乏附着的GAG链),均发现Bgn与VEGF存在剂量依赖性。另外,他们通过检查Bgn对体外人脐静脉内皮细胞中VEGF诱导的信号传导,发现 Bgn核心蛋白和Bgn的蛋白多糖形式均未增强VEGF诱导的VEGFR2磷酸化或ERK1/2磷酸化。因此,他们认为虽然Bgn可以与VEGF结合,但其在调节下游信号传导中的功能似乎是间接的,并且可能与VEGF储存或稳定性有关。
2.5.9 Angptl4(血管生成素样4) 在WILSON等[66]的研究中,血管生成素样4和VEGFA mRNA的时间表达相互平行,并推测血管生成素样4可能通过VEGF的调节实现血管化。WANG等[67]还显示血管生成素样4和VEGFA mRNA在人脂肪细胞中在1%氧气和缺氧模拟物CoCl2下的平行时间表达。重组血管生成素样4增加VEGFA在分化成骨细胞中的表达,表明血管生成素样4可以调节VEGFA表达。但将中国仓鼠卵巢细胞分泌的血管生成素样4移植到绒毛尿囊膜上,结果为不依赖于VEGF信号传导而诱导新生血管形成。另外,血管生成素样4基因敲除小鼠视网膜发育过程中血管分支形成、血管成熟情况发生了改变,提示VEGF或VEGFR2 mRNA水平的变化[68]。鉴于血管生成素样4在骨折愈伤组织中的表达,其由缺氧诱导因子a激活及对VEGFA表达的影响,研究者认为其可能在骨再生中起重要作用。
2.5.10 血管紧张素受体拮抗剂 研究者通过免疫组织化学分析,认为血管紧张素受体拮抗剂替米沙坦在骨折后2周的骨折修复中具有积极作用[69],这可能是由于肥大软骨细胞中VEGF表达的抑制。另一方面,增加的VEGF表达量也可能是细胞增殖和分化改变的结果,如通过替米沙坦处理的动物骨痂组织中增殖细胞核抗原含量的增加而表明。
2.5.11 甲状旁腺激素 据报道间歇性低剂量注射甲状旁腺激素可发挥骨合成代谢作用并促进骨折愈合[70]。研究者利用PTH敲除(PTHKO)小鼠骨折模型,发现缺乏内源性PTH可通过下调PKA/pAKT/缺氧诱导因子1α/ VEGF途径的活性来降低骨髓间充质干细胞来源的成骨细胞中的VEGF表达,从而通过血管生成和骨生成的减少影响软骨内骨形成,最终导致骨折愈合延迟。
2.5.12 瘦素 LIU等[71]的实验中,由放射学显示瘦素联合CoCl2组大鼠骨折愈合进展从第2周开始优于对照组;且其生物力学性能在第4周明显高于对照组。同时,瘦素与CoCl2结合可显著提高HIF1A,VEGFA,Runx2,骨形态发生蛋白2,Bglap和Alpl的mRNA表达水平。因此,研究者认为瘦素联合CoCl2通过激活HIF1A通路对大鼠股骨骨折愈合有积极作用。
2.6 VEGF的研究进展
2.6.1 VEGF直接作用 余旭辉等[72]直接对新西兰兔骨折部位注射VEGF,通过对骨折端骨形态发生蛋白、碱性成纤维细胞生长因子1的Western免疫印迹及Western blot分析,同时进行骨化程度的评价,得出VEGF显著促进了碱性成纤维生长因子1的表达及骨蛋白的形成,由此促进了骨折愈合过程。虽然采用直接注射的方式操作简单,但由于VEGF的半衰期短,故需持续注射以维持VEGF浓度。同时,直接注射的方式无法使VEGF定向释放。为解决这些问题,CHEN等[73]通过在微球中包封生长因子实现其持续和延迟释放。ZHANG等[74]采用了改良空心螺钉结合VEGF/聚乳酸乙醇酸/纤维蛋白胶对犬股骨颈骨折进行治疗。他们选用聚乳酸乙醇酸作为以持续,受控方式递送VEGF的有效载体,同时,将常用作粘合剂的纤维蛋白胶作为生长因子给药的载体基质以减少生长因子的丢失。另外,改良的空心螺钉不仅为骨折愈合提供了足够的稳定性,而且还通过螺钉侧壁的侧孔实现了VEGF的定向释放。通过X射线检查及放射性核素骨扫描等观察发现实验组骨折部位血运重建情况明显改善,且骨折愈合的质量及速度均有提高。同样地,LI等[75]构建了一种载有VEGF的纳米石墨烯涂层螺钉,能将VEGF安全地引入骨折部位,可有效治疗股骨颈骨折和预防股骨头缺血性坏死。而LI等[76]将VEGF加入纳米银中,并利用离子液体1-十二烷基-3-甲基咪唑氯化物,采用微波辅助法有效合成了球形Ag纳米粒子。生物学分析表明含有VEGF分子的Ag纳米颗粒促进了人间充质干细胞的细胞黏附和增殖。适当浓度的Ag NP具有良好的生物相容性,以促进细胞增殖、细胞因子释放和趋化性等细胞活化特性。同时,使用离子液体改善合成Ag NPs的表面形态已显示出有利于细胞活性,并且还改善了用于股骨骨折再生的VEGF的材料性能。
2.6.2 利用VEGF的基因转染 使用VEGF-质粒转染的成纤维细胞的方法显示兔的节段性骨缺损的血管化和桥接得到改善,而未修饰的成纤维细胞不支持骨再生[77]。LIN等[78]在研究中发现由杂交杆状病毒(BV)转导的脂肪来源干细胞的移植可以使骨形态发生蛋白2/VEGF持续表达,并使骨缺损恢复。同时,他们利用X射线、正电子发射断层扫描/计算机断层扫描和组织病理学检测未发现异位骨形成和肿瘤形成。由此,他们认为基因工程脂肪来源干细胞和延长的骨形态发生蛋白2/VEGF表达不仅可以治愈和重塑节段性骨缺损,且可以改善其结构及生物力学性质,而没有明显的不良反应。值得注意的是,该杂合载体依赖于细胞内的FLP表达和基因重组。脂肪来源干细胞中过多的FLP表达可能损害细胞活力。因此,应仔细确定最佳载体剂量和转导时间。
2.6.3 VEGF与其他物质联合治疗 将VEGF与其他生长因子或外源性干细胞结合,对骨折愈合似乎有着更好的疗效,例如,VEGF已经与骨形态发生蛋白2组合应用。大多数研究表明骨形态发生蛋白2具有强烈的骨诱导作用,然而进一步添加VEGF虽然增加血管密度,但骨形成没有明显增强[79]。KEMPEN提出了一种传递系统,可以顺序释放这两种生长因子,他将骨形态发生蛋白2包封在聚乳酸乙醇酸微球中,其在由载有VEGF的明胶水凝胶包围的聚(丙烯)支架中递送[80]。GAO等[81]研究了将间充质干细胞加入到推注有VEGF的胶原支架中,并对小鼠股骨干骨中产生的骨缺损进行了测试。装载间充质干细胞的支架快速整合并矿化到宿主骨中,这在空支架中未见,并且在无VEGF存在的间充质干细胞支架中较少见。RUIZ-IBAN等[82]的研究也得出了相似的结论,然而,这项研究是为了评估关于骨折以外的缺陷的应用,例如由感染或肿瘤引起的缺陷[83]。
2.6.4 基于提高VEGF表达的治疗 在植入物上涂上生物可吸收的磷酸钙层,可为成骨细胞创造了有利的介质并确保了生物活性离子的持续增殖;而KALINICHENKO等[84]认为VEGF和转化生长因子β2是介导生物活性涂层表面成骨活化的因子,所以开发具有生物吸附涂层的金属植入物有益于靶向组织再生。成骨细胞外基质片是一种片状材料,其骨诱导和骨传导能力良好,具有成为新兴无支架材料运用于骨折愈合的潜力。ONISHI等[85]研究中发现成骨细胞外基质片与使用高浓度SDS(十二烷基苯磺酸钠)的化学处理相比,在液氮中冻融循环后,仍能保持其片状结构并保留较多的骨诱导生长因子,包括骨形态发生蛋白2,VEGF-A,碱性成纤维细胞生长因子和转化生长因子β1。但其仍存在包括成骨细胞外基质片中包含的死细胞可能会影响巨噬细胞的活化,并在骨再生过程中加剧局部炎症等问题。

| [1] VINCENTI V, CASSANO C, ROCCHI M, et al.Assignment of the vascular endothelial growth factor gene to human chromosome 6p21.3. Circulation.1996;93(8):1493-1495. [2] SHIFREN JL, DOLDI N, FERRARA N, et al. In the human fetus, vascular endothelial growth factor is expressed in epithelial cells and myocytes, but not vascular endothelium: implications for mode of action.J Clin Endocrinol Metab.1994;79(1): 316-22. [3] DVORAK HF, NAGY JA, FENG D, et al.Vascular permeability factor/vascular endothelial growth factor and the significance of microvascular hyperpermeability in angiogenesis.Curr Top Microbiol Immunol.1999;237:97-132. [4] KASPAR D, NEIDLINGER WC, HOLBEIN O, et al.Mitogens are increased in the systemic circulation during bone callus healing.J Orthop Res.2003;21(2):320-325. [5] SPECTOR JA, MEHRARA BJ, GREENWALD JA, et al. Osteoblast expression of vascular endothelial growth factor is modulated by the extracellular microenvironment.Am J Physiol Cell Physiol.2001;280(1):C72-80. [6] MELDER RJ, KOENIG GC, WIRWER BP, et al. During angiogenesis, vascular endothelial growth factor and basic fibroblast growth factor regulate natural killer cell adhesion to tumor endothelium. Nat Med.1996;2(9):992-997. [7] SOKER S.Neuropilin in the midst of cell migration and retraction. Int J Biochem Cell Biol.2001;33(4):433-437. [8] LEI J, JIANG A, PEI D. Identification and characterization of a new splicing variant of vascular endothelial growth factor: VEGF183. Biochim Biophys Acta.1998;1443(3):400-406. [9] MANIGRASSO MB, O'CONNOR JP.Characterization of a closed femur fracture model in mice. J Orthop Trauma.2004; 18(10):687-695. [10] BERENDSEN AD, PINNOW EL, MAEDA A, et al. Biglycan modulates angiogenesis and bone formation during fracture healing.Matrix Biol.2014;35: 223-231. [11] 曾中华,余黎,龚玲玲,等.骨折愈合过程中BMP-2和VEGF的表达[J].武汉大学学报(医学版),2005,26(4):467-469+552. [12] 贾勇,关玉成.骨折后骨痂中VEGF的表达[J].新疆中医药,2005, 23(5):10-12. [13] 施红光,吴信华,赵剑,等.骨折愈合修复过程中血管内皮生长因子的表达及其动态改变[J].中国临床康复,2005,9(10): 92-93+278. [14] 武永刚,陈君长,王坤正.血管内皮细胞生长因子在骨折愈合过程中的表达[J].西安医科大学学报,2001,22(1):51-53+61. [15] 刘志奎,张柳,穆树林.大鼠骨折骨痂中血管内皮生长因子的表达[J].实用预防医学,2008,15(6):1749-1751. [16] 阳春华. 股骨颈骨折后1个月内不同时期VEGF在股骨头中的表达及意义[D].长沙:中南大学,2010. [17] 刘磊. 血管内皮生长因子促进骨折愈合的实验研究[D].济南:山东大学, 2007. [18] AUBIN JE. Osteoprogenitor cell frequency in rat bone marrow stromal populations: role for heterotypic cell-cell interactions in osteoblast differentiation. J Cell Biochem.1999; 72(3): 396-410. [19] HAUSMAN MR, SCHAFFLER MB, MAJESKA RJ.Prevention of fracture healing in rats by an inhibitor of angiogenesis. Bone.2001;29(6):560-564. [20] CHUNG R, FOSTER BK, XIAN CJ.The potential role of VEGF-induced vascularisation in the bony repair of injured growth plate cartilage.J Endocrinol.2014;221(1):63-75. [21] ZELZER E, MCLEAN W, NG YS, et al.Skeletal defects in VEGF(120/120) mice reveal multiple roles for VEGF in skeletogenesis. Development.2002;129(8):1893-1904. [22] SAIJO M, KITAZAWA R, NAKAJIMA M, et al. Heparanase mRNA expression during fracture repair in mice. Histochem Cell Biol, 2003;120(6):493-503. [23] YUASA M, MIGNEMI NA, BARNETT JV, et al.The temporal and spatial development of vascularity in a healing displaced fracture.Bone.2014;67: 208-221. [24] OZAWA CR, BANFI A, GLAZER NL, et al. Microenvironmental VEGF concentration,not total dose,determines a threshold between normal and aberrant angiogenesis.J Clin Invest. 2004;113(4): 516-527. [25] 宋祥胜.低剂量X线照射通过上调血管内皮生长因子的表达促进骨痂微血管新生而加速骨痂矿化[D].苏州:苏州大学,2011. [26] 武永刚,陈君长,王坤正,等.不同固定方式对骨痂中血管内皮细胞生长因子表达的影响[J].中国矫形外科杂志,2001,8(6): 63-65. [27] 沈建国.恒磁场对SD大鼠深创面愈合的影响[D].杭州:浙江大学, 2007. [28] 林建宁,阮狄克.海水浸泡开放性骨折伤愈合过程中组织病理学和血管内皮细胞生长因子(VEGF)表达[J].中华创伤骨科杂志, 2004,6(8):50-53. [29] 董黎强,尹航,王维佳,等.不同手术时间对骨折愈合过程中VEGF表达的影响[J].浙江医学,2013,35(10):889-891+894. [30] 乔林.微动对骨愈合的影响及作用机理[D].北京:中国人民解放军军医进修学院,2004. [31] VAVVA MG, GRIVAS KN, CARLIER A, et al.Effect of ultrasound on bone fracture healing: A computational bioregulatory model.Comput Biol Med.2018;100:74-85. [32] CHEN X, CHENG X, MA W, et al.Effects of hyperbaric oxygen therapy on open tibial fractures in rabbits after transient seawater immersion. Undersea Hyperb Med.2017; 44(3):235-242. [33] HISTING T, HEERSCHOP K, KLEIN M, et al. Characterization of the healing process in non-stabilized and stabilized femur fractures in mice.Arch Orthop Trauma Surg.2016;136(2): 203-211. [34] ZHOU M, LU S, LU G, et al.Effects of remote ischemic postconditioning on fracture healing in rats. Mol Med Rep. 2017;15(5):3186-3192. [35] ROSSO F, BONASIA DE, MARMOTTI A, et al.Mechanical Stimulation (Pulsed Electromagnetic Fields "PEMF" and Extracorporeal Shock Wave Therapy "ESWT") and Tendon Regeneration: A Possible Alternative.Front Aging Neurosci. 2015;7: 211. [36] MIDY V, PLOUËT J.Vasculotropin/vascular endothelial growth factor induces differentiation in cultured osteoblasts. Biochem Biophys Res Commun.1994;199(1): 380-386. [37] SCHLAEPPI JM, GUTZWILLER S ,FINKENZELLER G, et al.1,25-Dihydroxyvitamin D3 induces the expression of vascular endothelial growth factor in osteoblastic cells. Endocr Res.1997;23(3):213-229. [38] GRIFFIN SK, KORBIN B, DAVIS M, et al.Evolution of Bone Grafting: Bone Grafts and Tissue Engineering Strategies for Vascularized Bone Regeneration.2015;13:232-244. [39] KOZAWA O, MATSUNO H, UEMATSU T.Involvement of p70 S6 kinase in bone morphogenetic protein signaling: vascular endothelial growth factor synthesis by bone morphogenetic protein-4 in osteoblasts.J Cell Biochem. 2001; 81(3):430-436. [40] MAYR WU, WALTENBERGER J, HAUSSER H, et al.Vascular endothelial growth factor stimulates chemotactic migration of primary human osteoblasts.Bone.2002;30(3):472-477. [41] DECKERS MM, BEZOOJIEN RL, HORST G, et al.Bone morphogenetic proteins stimulate angiogenesis through osteoblast-derived vascular endothelial growth factor A. Endocrinology.2002;143(4):1545-1553. [42] TSIRIDIS E, GIANNOUDIS PV. Transcriptomics and proteomics: advancing the understanding of genetic basis of fracture healing. Injury.2006;37 Suppl 1: S13-19. [43] MUSGRAVE DS, PRUCHNIC R, BOSCH P, et al.Human skeletal muscle cells in ex vivo gene therapy to deliver bone morphogenetic protein-2.J Bone Joint Surg Br.2002;84(1):120-7. [44] BOULETREAU PJ, WARREN SM, SPECTOR JA, et al. Hypoxia and VEGF up-regulate BMP-2 mRNA and protein expression in microvascular endothelial cells: implications for fracture healing.Plast Reconstr Surg.2002;109(7): 2384-2397. [45] ARYAL R, CHEN XP, FANG C, et al.Bone morphogenetic protein-2 and vascular endothelial growth factor in bone tissue regeneration: new insight and perspectives. Orthop Surg.2014;6(3):171-178. [46] BEAMER B, HETTRICH C, LANE J.Vascular endothelial growth factor: an essential component of angiogenesis and fracture healing.Hss J.2010;6(1):85-94. [47] KUMAR S, WAN C, RAMASWAMY G, et al.Mesenchymal stem cells expressing osteogenic and angiogenic factors synergistically enhance bone formation in a mouse model of segmental bone defect.Mol Ther.2010;18(5):1026-1034. [48] HU K, OLSEN BR. Osteoblast-derived VEGF regulates osteoblast differentiation and bone formation during bone repair.J Clin Invest.2016;126(2):509-526. [49] HU K, BESSCHETNOVA TY, OLSEN BR. Soluble VEGFR1 reverses BMP2 inhibition of intramembranous ossification during healing of cortical bone defects.J Orthop Res.2017; 35(7): 1461-1469. [50] PENG H, USAS A, OLSHANSKI A, et al.VEGF improves, whereas sFlt1 inhibits, BMP2-induced bone formation and bone healing through modulation of angiogenesis.J Bone Miner Res.2005;20(11):2017-2027. [51] CHEN G, FANG T, QI Y, et al.Combined Use of Mesenchymal Stromal Cell Sheet Transplantation and Local Injection of SDF-1 for Bone Repair in a Rat Nonunion Model.Cell Transplant.2016;25(10):1801-1817. [52] HURLEY MM, ADAMS DJ, WANG L, et al. Accelerated fracture healing in transgenic mice overexpressing an anabolic isoform of fibroblast growth factor 2.J Cell Biochem. 2016;117(3):599-611. [53] ZHANG H, KOT A, LAY YE, et al. Acceleration of Fracture Healing by Overexpression of Basic Fibroblast Growth Factor in the Mesenchymal Stromal Cells. Stem Cells Transl Med. 2017;6(10):1880-1893. [54] SU YW, CHUNG R, RUAN CS, et al. Neurotrophin-3 Induces BMP-2 and VEGF Activities and Promotes the Bony Repair of Injured Growth Plate Cartilage and Bone in Rats. J Bone Miner Res.2016;31(6): 1258-74. [55] SHEN L, ZENG W, WU YX, et al.Neurotrophin-3 accelerates wound healing in diabetic mice by promoting a paracrine response in mesenchymal stem cells. Cell Transplant.2013; 22(6):1011-1021. [56] ZHANG Z, ZHANG Y, ZHOU Z, et al.BDNF regulates the expression and secretion of VEGF from osteoblasts via the TrkB/ERK1/2 signaling pathway during fracture healing.Mol Med Rep. 2017;15(3):1362-1367. [57] SCHIPANI E, RYAN HE, DIDRICKSON S, et al.Hypoxia in cartilage: HIF-1alpha is essential for chondrocyte growth arrest and survival. Genes Dev.2001;15(21): 2865-2876. [58] SHEN X, WAN C, RAMASWAMY G, et al.Prolyl hydroxylase inhibitors increase neoangiogenesis and callus formation following femur fracture in mice.J Orthop Res.2009;27(10): 1298-1305. [59] WANG Y, WANG C, DENG L, et al.The hypoxia-inducible factor alpha pathway couples angiogenesis to osteogenesis during skeletal development. J Clin Invest.2007;117(6): 1616-1626. [60] WAN C, GILBERT SR, WANG Y, et al.Activation of the hypoxia-inducible factor-1alpha pathway accelerates bone regeneration. Proc Natl Acad Sci U S A.2008;105(2):686-691. [61] TOHIDNEZHAD M, WRUCK CJ, SLOWIK A, et al.Role of platelet-released growth factors in detoxification of reactive oxygen species in osteoblasts.Bone.2014;65:9-17. [62] ZHANG C, FEINBERG D, ALHARBI M, et al. Chondrocytes Promote Vascularization in Fracture Healing Through a FOXO1-Dependent Mechanism.J Bone Miner Res.2019; 34(3):547-556. [63] BISSELL L, TIBREWAL S, SAHNI V, et al.Growth factors and platelet rich plasma in anterior cruciate ligament reconstruction. Curr Stem Cell Res Ther.2015;10(1):19-25. [64] LIPPROSS S, BECKMANN R, STREUBESAND N, et al. Nrf2 deficiency impairs fracture healing in mice. Calcif Tissue Int. 2014; 95(4): 349-361. [65] CAKMAK G, SAHIN MS, OZDEMIR BH, et al.Effect of pentoxifylline on healing of segmental bone defects and angiogenesis. Acta Orthop Traumatol Turc.2015;49(6): 676-682. [66] WILSON SS, WONG A, TOUPADAKIS CA, et al. Expression of angiopoietin-like protein 4 at the fracture site: Regulation by hypoxia and osteoblastic differentiation. J Orthop Res.2015; 33(9):1364-1373. [67] WANG B, WOOD IS, TRAYHURN P. Dysregulation of the expression and secretion of inflammation-related adipokines by hypoxia in human adipocytes.Pflugers Arch.2007;455(3): 479-492. [68] PERDIGUERO EG, GALAUP A, DURAND M, et al.Alteration of developmental and pathological retinal angiogenesis in angptl4-deficient mice.J Biol Chem.2011;286(42): 36841-36851. [69] ZHAO X, WANG JX, FENG YF, et al.Systemic treatment with telmisartan improves femur fracture healing in mice.PLoS One. 2014;9(3):e92085. [70] DING Q, SUN P, ZHOU H, et al.Lack of endogenous parathyroid hormone delays fracture healing by inhibiting vascular endothelial growth factormediated angiogenesis.Int J Mol Med.2018;42(1):171-181. [71] LIU P, LIU J, XIA K, et al.Effect of leptin combined with CoCl2 on healing in Sprague Dawley Rat fracture model.Sci Rep. 2016;6:30754. [72] 余旭辉,张雪珍,余辉映.血管内皮生长因子对骨折愈合的影响分析[J].医学综述,2014,20(18):3390-3391+3457. [73] CHEN FM, ZHANG M, WU ZF.Toward delivery of multiple growth factors in tissue engineering. Biomaterials.2010; 31(24):6279-6308. [74] ZHANG L, ZHANG L, LAN X, et al.Improvement in angiogenesis and osteogenesis with modified cannulated screws combined with VEGF/PLGA/fibrin glue in femoral neck fractures.J Mater Sci Mater Med.2014;25(4):1165-1172. [75] LI S, YUAN H, PAN J, et al. The treatment of femoral neck fracture using VEGF-loaded nanographene coated internal fixation screws.PLoS One.2017;12(11):e0187447. [76] LI X, LIU M, CHENG H, et al. Development of ionic liquid assisted-synthesized nanosilver combined with vascular endothelial growth factor as wound healing in the care of femoral fracture in the children after surgery.J Photochem Photobiol B.2018;183:385-390. [77] LI R, STEWART DJ, SCHROEDER HP, et al. Effect of cell-based VEGF gene therapy on healing of a segmental bone defect.J Orthop Res.2009;27(1):8-14. [78] LIN CY, CHANG YH, SUNG LY,et al.Long-term tracking of segmental bone healing mediated by genetically engineered adipose-derived stem cells: focuses on bone remodeling and potential side effects.Tissue Eng Part A.2014;20(9-10): 1392-1402. [79] CAI WX, ZHENG LW, LI CL, et al.Effect of different rhBMP-2 and TG-VEGF ratios on the formation of heterotopic bone and neovessels. Biomed Res Int.2014;2014:571510. [80] KEMPEN DH, LU L, HEIJINK A, et al. Effect of local sequential VEGF and BMP-2 delivery on ectopic and orthotopic bone regeneration. Biomaterials.2009;30(14): 2816-2825. [81] GAO C, HARVEY EJ, CHUA M, et al. MSC-seeded dense collagen scaffolds with a bolus dose of VEGF promote healing of large bone defects.Eur Cell Mater.2013;26: 195-207; discussion 207. [82] RUIZ-IBAN MA, GONZALEZ LF,DIZA HJ,et al.Effect of VEGF-A165 addition on the integration of a cortical allograft in a tibial segmental defect in rabbits. Knee Surg Sports Traumatol Arthrosc. 2015;23(5):1393-1400. [83] SINCLAIR KL, MAFI P, MAFI R, et al.The Use of Growth Factors and Mesenchymal Stem Cells in Orthopaedics: In particular, their use in Fractures and Non-Unions: A Systematic Review.Curr Stem Cell Res Ther.2017;12(4): 312-325. [84] KALINICHENKO SG, MATVEEVA NY, KOSTIV RE, et al. Role of Vascular Endothelial Growth Factor and Transforming Growth Factor-beta2 in Rat Bone Tissue after Bone Fracture and Placement of Titanium Implants with Bioactive Bioresorbable Coatings.Bull Exp Biol Med.2017;162(5): 671-675. [85] ONISHI T, SHIMIZU T, AKAHANE M, et al. Osteogenic extracellular matrix sheet for bone tissue regeneration. Eur Cell Mater.2018;36:68-80. |
| [1] | 侯婧瑛, 于萌蕾, 郭天柱, 龙会宝, 吴 浩. 缺氧预处理激活HIF-1α/MALAT1/VEGFA通路促进骨髓间充质干细胞生存和血管再生[J]. 中国组织工程研究, 2021, 25(7): 985-990. |
| [2] | 樊全宝, 罗惠娜, 王丙云, 陈胜锋, 崔连旭, 江文康, 赵明明, 王静静, 罗冬章, 陈志胜, 白银山, 刘璨颖, 张 晖. 低氧培养犬脂肪间充质干细胞的生物学特性[J]. 中国组织工程研究, 2021, 25(7): 1002-1007. |
| [3] | 杨卫强, 丁 童, 杨卫可, 蒋振刚. 组合式可变应力接骨板内固定干预山羊股骨骨折断端的骨组织细胞功能及骨密度变化[J]. 中国组织工程研究, 2021, 25(6): 890-894. |
| [4] | 张 咪, 吴赛璇, 董 明, 陆 颖, 牛卫东. 根尖周炎模型小鼠白细胞介素24的表达[J]. 中国组织工程研究, 2021, 25(5): 679-684. |
| [5] | 杨 洋, 姚 羽, 沈孝天, 刘佳佳, 薛建华. 退变腰椎间盘中白细胞介素21的表达及意义[J]. 中国组织工程研究, 2021, 25(5): 690-694. |
| [6] | 邓桢翰, 黄 勇, 肖璐璐, 陈昱霖, 朱伟民, 陆 伟, 王大平. 骨形态发生蛋白在关节软骨再生过程中的作用与应用[J]. 中国组织工程研究, 2021, 25(5): 798-806. |
| [7] | 成世高, 王万春, 蒋 栋, 李腾飞, 李 洵, 任 炼. 标准柄与加长柄骨水泥型假体置换治疗高龄转子间骨折的比较[J]. 中国组织工程研究, 2021, 25(3): 362-367. |
| [8] | 谢程欣, 王 维, 王成龙, 李清龙, 尹 东. 骨形态发生蛋白治疗急性胫骨骨折的系统评价及Meta分析[J]. 中国组织工程研究, 2021, 25(3): 486-492. |
| [9] | 李 上, 黄 骧, 陈 铭, 雷明星, 程 实, 张里程, 尹鹏滨, 唐佩福. 信号蛋白3A有望成为骨骼肌损伤修复的新靶点[J]. 中国组织工程研究, 2021, 25(20): 3232-3238. |
| [10] | 李祥泽, 卜宪敏, 李冬梅, 池玉磊, 苏 强, 靳欣桐, 赵 键, 张高天, 吴 彬, 孟纯阳. 创伤性脑外伤促进骨折愈合中的干细胞、细胞因子、激素、神经肽及基因[J]. 中国组织工程研究, 2021, 25(19): 3057-3063. |
| [11] | 汪 鎏, 宋东哲, 黄定明. 骨形态发生蛋白9调控干细胞分化与骨再生[J]. 中国组织工程研究, 2021, 25(19): 3064-3070. |
| [12] | 毛国庶, 周 敏, 李晓明, 周子红, 殷渠东. 第三骨块对股骨干骨折髓内钉固定后骨愈合效果的影响[J]. 中国组织工程研究, 2021, 25(15): 2405-2409. |
| [13] | 刘治军, 刘少津, 魏合伟, 万 雷, 黄宏兴, 乔荣勤. 补肾健脾活血方干预去势大鼠肌肉骨骼转化生长因子β/骨形态发生蛋白2信号通路的变化[J]. 中国组织工程研究, 2021, 25(14): 2219-2223. |
| [14] | 吴钰坤, 韩 杰, 温帅波. 骨折愈合过程中Runx2基因的作用机制[J]. 中国组织工程研究, 2021, 25(14): 2274-2279. |
| [15] | 吴胜祥, 刘 园, 陆 帅. 迷你锁定钛板系统内固定治疗腕舟骨骨折[J]. 中国组织工程研究, 2021, 25(12): 1874-1878. |
血管内皮生长因子(vascular endothelial growth factor,VEGF),也称血管通透因子或血管促进素,是一种高度保守的同源二聚体糖蛋白[1]。1989年FERRARA 等人首次从牛脑垂体黏液滤泡-星状细胞条件培养基中分离得到了一种蛋白质,它能特异地作用于靶细胞,尤其是血管内皮细胞,该蛋白质具有促进血管内皮细胞的生长活性作用,遂将其命名为VEGF[2]。1999年DVORAK等[3]发现VEGF作为一种肿瘤分泌蛋白,还可以显著提高血液循环中大分子的渗透性,自此VEGF因其高度诱导新血管形成和大幅提高血管通透性的能力而受到广泛关注。
VEGF具有极高的亲和力,可直接或间接促进血管生成[3]。此外,通过旁分泌机制,VEGF的表达产物还可促进新血管形成、增加血管通透性及维持血管正常状态和完整性[4]。SPECTOR等[5]研究发现,对成骨细胞进行体外培养,VEGF对成骨细胞增殖不起作用,但VEGF可使成骨细胞发生迁移及分化,并且极少量的VEGF(浓度约为骨形态发生蛋白1%时)即有此作用。如今,VEGF在医学领域作为一种重要的生长因子而广泛使用。在骨科,VEGF因其能促进血管生成、提高血管通透性而在骨缺损的恢复、骨折愈合、异体骨移植等方面得到广泛应用。
骨折是骨科常见疾病,骨折后骨再生是由细胞因子、生长因子和转录因子参与的连续且复杂漫长的组织修复过程。在生物力学状况适宜、生物学反应良好的情况下,多种控制骨细胞系活性的因子上调,使骨痂形成,激活骨髓间充质干细胞及前成骨细胞,最终促进骨折修复形成正常骨结构。近年来,围绕生长因子促进骨再生的实验研究报道增多,主要参与因子有VEGF、成纤维细胞生长因子、转化生长因子α、β、血小板生长因子、前列腺素E及肿瘤坏死因子等,其中VEGF至关重要,在血管生成过程中不可或缺[6]。为了探究血管内皮生长因子及其受体的结构特点、生物学作用、VEGF对骨折愈合的影响,为真正的临床应用提供理论依据,作者进行了数据库检索,并做简要综述。
1.1 资料来源 第一作者使用计算机检索 CNKI 、PubMed 数据库,检索数据时限为2014年1月至2019年3月,以“血管内皮生长因子,骨折愈合”为中文检索词、“vascular endothelial growth factor,fracture healing”为英文检索词,检索有关血管内皮生长因子对骨折愈合影响的文献。
1.2 入选标准
纳入标准:①与血管内皮生长因子调控成骨相关基础研究的文献;②涉及血管内皮生长因子骨再生修复应用研究方面相关文献;③近期发表于相关医学领域权威杂志的论点清晰、论据可靠的有关文献。
排除标准:①与入选标准无关、重复报道或发表年限过于陈旧的文献;②无法进行详细资料和数据提取的文献;③内容为中文或英文以外的文献。
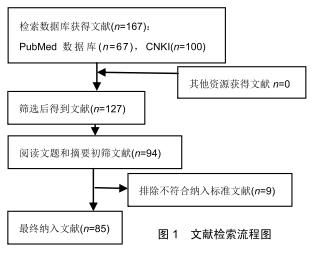
1.3 数据提取 共检索到167篇文献,通过阅读文题、摘要进行初筛,排除内容无关的或内容重复的文献,最后纳入符合标准的85篇文献作进一步分析。文献检索流程见图1。
VEGF从发现至今已有40年历史,因其强大的血管新生及提高通透性而为人熟知。近十几年来,对VEGF的研究已从一种普通的生长因子转向基于VEGF的组织工程研究。如今,对VEGF及其受体的基本结构特点及其生物学作用、基本的信号通路有了大致清晰的认识,对骨折愈合的影响也有了更深入的研究。已有的研究表明VEGF通过直接和间接途径对骨折愈合总体有促进作用,而VEGF的抑制会造成骨折愈合的延缓。在骨折愈合部位细胞中VEGF的表达趋势为先减弱,后增强,再减弱,而不同的细胞表达的时间及强度不同。但局部过高的VEGF会造成骨折愈合速度的减慢,其可能的原因为畸形血管的形成及功能障碍。同时,随着对各种物理化学因素对VEGF影响的了解,可以结合具体情况将各因素作为利用VEGF进行临床治疗的辅助方法。VEGF与骨形态发生蛋白的关系极为密切,未来对VEGF的基础研究主要向VEGF与骨形态发生蛋白联合研究的方向发展。由于VEGF存在半衰期短、需持续释放的问题,促使人们研发更多的新兴生物材料以使其稳定持续释放;同时,也极大地提高了基因转染技术的发展,将基于VEGF的基因转染技术应用于临床治疗需注意最佳的载体剂量与转导时间。另外,VEGF最初的发现为一种肿瘤分泌蛋白,具有诱发肿瘤生长的可能,也使人们将VEGF应用于临床治疗时更为谨慎。同时,基于提高VEGF表达以促进骨折愈合的治疗方式中,其不良反应也日益明显,未来的治疗方式应以克服不良反应为研究的突破点。现在医学研究的重点向“学科交叉”的方式集中,对VEGF的进一步研究将向着多学科、多领域的方向发展,相信VEGF是未来医学研究的热点。

文题释义:
血管内皮生长因子:一种高度保守的同源二聚体糖蛋白,广泛分布于人和动物的器官与组织中,如:肺、肾、脾、成骨细胞、软骨细胞、肥大细胞中,主要作用为促进内皮细胞增生、提高内皮细胞通透性、维持血管稳定性,是调节细胞生长,促进细胞分裂、迁移及增殖的重要因素。
骨折愈合:骨折愈合的标准有局部无压痛,无纵向叩击痛;局部无异常活动;X射线照片显示骨折线模糊,有连续性骨痂通过骨折线等。根据组织学及细胞学的变化,将骨折愈合分为3期,即:血肿炎症机化期、原始骨痂形成期和骨板形成塑形期。
骨折过程中,在细胞因子、生长因子和转录因子的控制下,骨折后的骨折愈合是极其漫长且复杂的修复过程。骨折后受伤部位周围会立即形成血肿,而后受伤部位会有免疫细胞渗入。此后,纤维组织在受伤部位生长,并进一步发展成为含有新生软骨的软骨痂。软骨周围毗邻的血管会沿软骨向内生长,使其生长为硬骨痂,并对骨折愈合具有支持作用。最后由皮质骨和髓质骨对其进行替代。
| 阅读次数 | ||||||
|
全文 |
|
|||||
|
摘要 |
|
|||||