1.1 设计 随机对照动物实验。
1.2 时间及地点 实验于2019年1至12月在南京中医药大学动物实验中心及南京中医药大学附属医院中心实验室完成。
1.3 材料
1.3.1 实验动物 SPF级雄性自发高血压(spontaneous hypertension,SHR)大鼠40只,体质量200-250 g,6周龄,购自上海西普尔-必凯实验动物中心(动物合格证号:SCXK沪-2018-0006),饲养于南京中医药大学动物实验中心。该研究经过南京中医药大学附属医院动物伦理委员会批准。
1.3.2 药品及试剂 右归饮药物组成:熟地黄30 g、山药
6 g、山茱萸3 g、枸杞子6 g、炙甘草6 g、姜杜仲6 g、肉桂6 g、制附子3 g,中药饮片由江苏省中医院中药房提供。肠杆菌内毒素(Biosharp公司);地塞米松磷酸钠注射液 (1 mL,
5 mg,湖北药业有限公司);青霉素G(8×105 U,利康药业);庆大霉素(8×104 U,利康药业);泮托拉唑(40 mg,奥德赛制药);胎牛血清(500 mL,Hyclone公司);L-DMEM培养基(Cyagen公司);苏木精、伊红(四季青公司);SD大鼠骨髓间充质干细胞成骨、成脂诱导培养基(Cyagen公司);茜素红、油红O染液、噻唑蓝、二甲基亚砜、Percoll、B-ALP试剂盒(国药集团化学试剂有限公司);P53、Beclin-1、LC3Ⅱ抗体(Cyagen公司);辣根过氧化物酶(Cyagen公司);一抗及二抗稀释液由江苏省中医院病理科提供。
1.3.3 实验仪器 3.0T核磁共振(Siemens公司);倒置相差显微镜(上海光学仪器厂);石蜡包埋及脱水机(武汉俊杰电子公司,JB-P5);石蜡超薄切片机(武汉俊杰电子公司,RM2016);Image-pro plus 6.0(IPP);恒温恒湿孵育箱(Heraeus公司);蛋白交互仪(Beckman公司);凝胶电泳仪(BIO-RAD公司);转膜及成像系统(Beckman公司);激光共聚焦显微镜(ZEISS公司)。
1.4 实验方法
1.4.1 造模 所有40只SHR大鼠入组前均于SPF动物房饲养2周排除隐匿性疾病,单笼饲料饲养。随机选出8只大鼠不进行任何造模或干预,作为空白对照组。另外32只大鼠采用高剂量马血清静脉注射联合地塞米松肌注的方法诱导股骨头坏死模型,具体步骤:20 μg/kg肠杆菌内毒素经尾静脉缓慢推注,隔日1次,5次后予10 mg/kg地塞米松臀部肌肉注射,隔日1次,共10次;空白对照组均予等体积生理盐水作为安慰剂同步注射。全部造模过程结束后对各组大鼠进行
3.0T MRI检查,并进行尾骨骨髓穿刺苏木精-伊红染色,以MRI显示股骨头内广泛水肿且骨髓苏木精-伊红染色较空白对照组存在骨髓纤维组织广泛增生、细胞减少、骨小梁稀疏为造模成功标志。
1.4.2 分组与干预 将造模完成的32只大鼠分为4组,分别为模型组、低剂量右归饮干预组、中剂量右归饮干预组、高剂量右归饮干预组,加上未进行造模的8只作为空白对照组。右归饮的制备方法如下:各药饮片水煎至200 mL,调整基础倍率生药质量浓度为0.5 g/mL。药物干预的剂量换算比例按照前期研究的方法进行:低、中、高剂量组倍增系数分别为 1,2,3,每日灌胃剂量公式为:200(mL)÷人类平均体质量(kg)×大鼠实际体质量(kg)×倍增系数,按照人类平均体质量50 kg计算,则低、中、高剂量组分别每日灌胃4,8,12 mL/kg。空白对照组及模型组给予每日8 mL/kg生理盐水灌胃。以上干预过程共进行6周。
1.5 主要观察指标
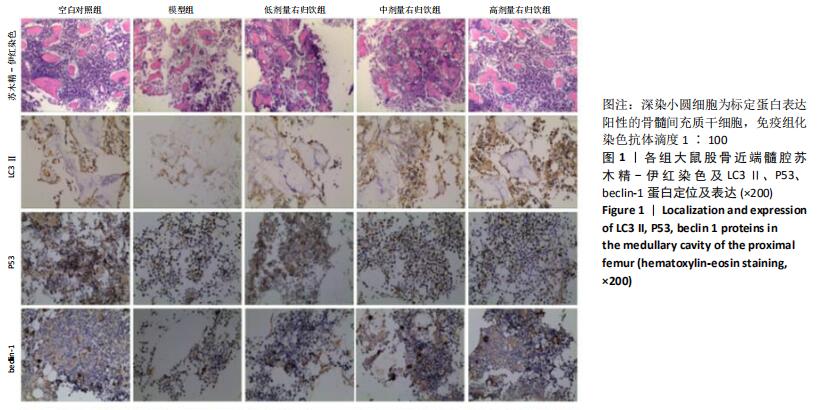
1.5.1 股骨近端髓腔组织苏木精-伊红染色及LC3Ⅱ、P53、beclin-1免疫组化染色 手术完整取出各组大鼠右侧股骨,放进20 mL离心管内,加入40 g/L多聚甲醛,在离心管管壁上标注分组及编号、取材时间。将股骨头沿冠状面剖开,10%EDTA脱钙后冠状面切取2 mm厚组织做石蜡切片,脱水、石蜡包埋后切成厚3.0-4.0 μm的切片并脱蜡进行苏木精-伊红染色。脱钙完成后同时进行免疫组化:将脱钙后的近端髓腔内组织小刮匙均匀刮取3份,标记编号,固定于PBS溶解的40 g/L多聚甲醛中,梯度乙醇和二甲苯脱水,石蜡包埋,切片预先用多聚赖氨酸处理,层厚4.0-5.0 μm进行切片,
60 ℃恒温箱内温养3 h,37 ℃过夜,二甲苯脱蜡2次,然后用梯度乙醇脱苯,冲洗,体积分数为3%H2O2室温孵育
10 min以消除内源性过氧化物酶的活性,微波热修复抗原后室温冷却,PBS清洗,加入山羊血清封闭20 min,去血清,加入兔抗大鼠多克隆抗体LC3Ⅱ、P53及beclin-1,加入山羊抗兔IgG孵育20 min,加入辣根过氧化物酶,37 ℃孵育
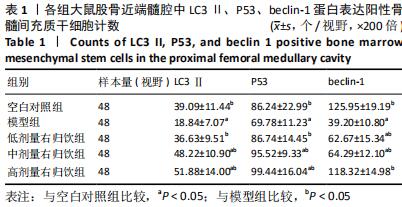
20 min,显色后苏木精轻度复染,梯度乙醇脱水,二甲苯透明,中性树胶封固。200倍镜下随机选取6个视野,计数髓腔有效区域的深染阳性细胞数。
1.5.2 骨髓间充质干细胞的提取和培养 将各组大鼠左侧股骨近端髓腔直接在无菌条件下放于L-DMEM培养基中,冲洗,冲出的骨髓细胞悬液1 000 r/min离心10 min,弃上清、脂肪及杂质,加入少量DMEM培养基重悬,沿离心管壁缓慢滴入含等量体积的Percoll(密度为1.073 g/mL)分离液中,
3 000 r/min离心10 min,取中间云雾状细胞层置于另一离心管中,PBS冲洗2次,把得到的有核细胞用L-DMEM培养基培养,每48 h换液1次,换液3次后骨髓间充质干细胞得以纯化。将纯化的骨髓间充质干细胞以1×104/cm2的浓度接种于L-DMEM培养基中,置于37 ℃、体积分数为5%CO2、饱和湿度的培养箱中培养,每3 d换液1 次,细胞达90%融合后以0.25%胰蛋白酶消化,各组传代前冻存部分原代细胞备用。
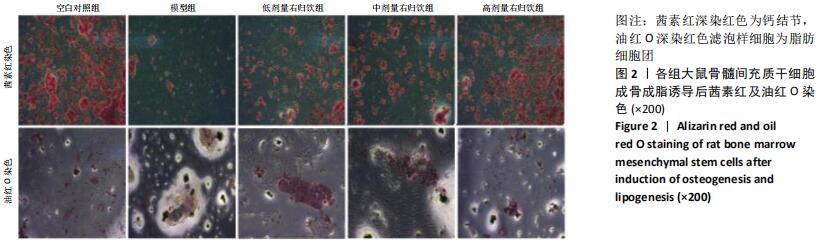
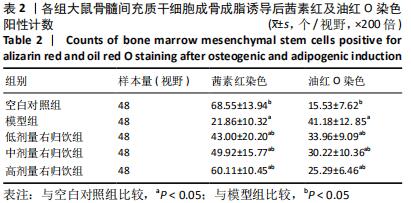
1.5.3 茜素红染色 使用成骨诱导培养基对各组传代1次的骨髓间充质干细胞进行成骨诱导培养21 d,以Tris-HCl配制茜素红溶液至pH值4.2左右,染色30 min,200倍镜下随机选取6个视野,对红染钙矿化结节进行计数并进行组间对比。
1.5.4 油红O染色 使用成脂诱导培养基对各组传代1次的骨髓间充质干细胞进行成脂诱导培养12 d,油红O染液浸染30 min,苏木精染液浸染1 min,200倍镜下随机选取6个视野,对红染脂肪细胞进行计数并进行组间对比。
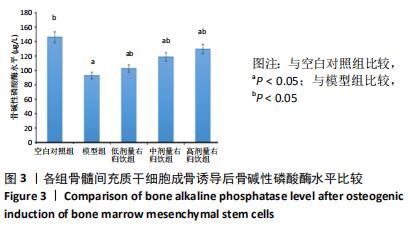
1.5.5 骨碱性磷酸酶定量 各组骨髓间充质干细胞按1×104/孔接种在36孔板上,每组6孔,成骨诱导培养基培养2周,使用骨碱性磷酸酶ELASA试剂盒进行检测,将各组上清吸取约50 μL,加入样本孔,而后加入辣根过氧化物酶100 μL,37 ℃孵育60 min,弃去液体,拍干,洗涤液洗涤,反复5次,每孔加入底物50 μL,37 ℃避光孵育15 min,每孔加入终止液KOH 50 μL,酶联免疫监测仪检测各孔 450 nm波长的吸光度值,根据标准品计量。
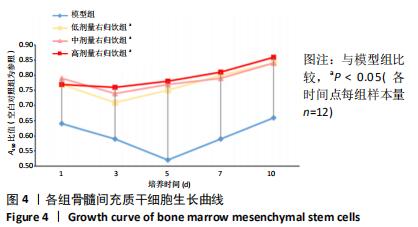
1.5.6 MTT检测细胞增殖情况 取各组骨髓间充质干细胞,加入0.25%胰蛋白酶消化,以5×103/孔接种于96孔板,每组12孔,放入37 ℃、体积分数为5%CO2、饱和湿度标准培养箱中连续培养10 d,分别于第 1,3,5,7,10天每孔加入MTT(5 g/L)20 µL,4 h后每孔加入150 µL二甲亚砜,振荡
10 min,使结晶物充分溶解,于酶标仪450 nm波长测定各孔吸光度值。以时间为横坐标,吸光度值为纵坐标绘制细胞生长曲线。
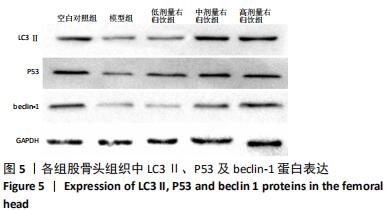
1.5.7 Western blot检测自噬蛋白LC3Ⅱ、P53及beclin-1表达 将股骨头放入液氮中10 min,取出剪碎,边加液氮边研磨至粉末颗粒,加入溶解液,14 000 r/min离心15 min,取上清液,BAC法测定蛋白质的浓度,在恒压下进行电泳后将PVDF膜转膜,然后加入5%的脱脂奶粉室温封闭1 h,加入P53、Beclin-1、LC3Ⅱ抗体,4 ℃孵育过夜,次日PBS冲洗3次,加入兔抗鼠二抗(HRP)IgG抗体(稀释,1∶2 000)室温孵育1 h,最后加入显影液进行曝光,使用ECL试剂盒进行可视化,对显影带进行灰度扫描分析。以β肌动蛋白作为内部对照,使用Image J软件对印迹定量分析。
1.6 统计学分析 实验数据均使用SPSS 19.0软件进行统计处理,计量资料以x±s表示,采用重复测量数据的方差分析,LSD法进行两两比较,P < 0.05为差异有显著性意义。