中国组织工程研究 ›› 2015, Vol. 19 ›› Issue (30): 4800-4804.doi: 10.3969/j.issn.2095-4344.2015.30.009
• 组织工程口腔材料 tissue-engineered oral materials • 上一篇 下一篇
60Co放射及微量元素锌对钛种植体骨融合的影响
陈海军1,张安生2,朱孝春3,钱奇春1,于淑湘1,杨博程1,张静波1,南福清1,林均舟1
- 1解放军第九十七医院口腔科,江苏省徐州市 221004; 2解放军73087部队医院,江苏省徐州市 221011; 3解放军73068部队卫生队,江苏省徐州市 221000
Effect of 60Co irradiation and trace element zinc on implant-bone fusion
Chen Hai-jun1, Zhang An-sheng2, Zhu Xiao-chun3, Qian Qi-chun1, Yu Shu-xiang1, Yang Bo-cheng1, Zhang Jing-bo1, Nan Fu-qing1, Lin Jun-zhou1
- 1Department of Stomatology, the 97th Hospital of Chinese PLA, Xuzhou 221004, Jiangsu Province, China; 2Hospital of the 73087 Troop of Chinese PLA, Xuzhou 221011, Jiangsu Province, China; 3Health Team of the 73068 Troop of Chinese PLA, Xuzhou 221000, Jiangsu Province, China
摘要:
背景:前期实验证实补锌可以加速种植体的骨融合。
目的:观察60Co放射及微量元素锌对种植体骨融合的影响。
方法:取成年雄性家兔36只,双侧胫骨近心端各植入1枚钛种植体,建立钛种植体动物模型,随机均分为4组,补锌组种植后24 h肌注10 g/L硫酸锌4 mg/kg,1次/d;对照组种植后24 h肌注9 g/L生理盐水4 mg/kg,1次/d;放射组于种植后第2,4,6天给予双侧胫骨近心段60Co照射,15 Gy/d,同时种植后24 h肌注9 g/L生理盐水4 mg/kg,1次/d;放射补锌组于种植后第2,4,6天给予双侧胫骨近心段60Co照射,15 Gy/d,同时种植后24 h肌注10 g/L硫酸锌4 mg/kg,1次/d。种植后1,4,12周利用显微镜观察种植体骨界面组织形态。
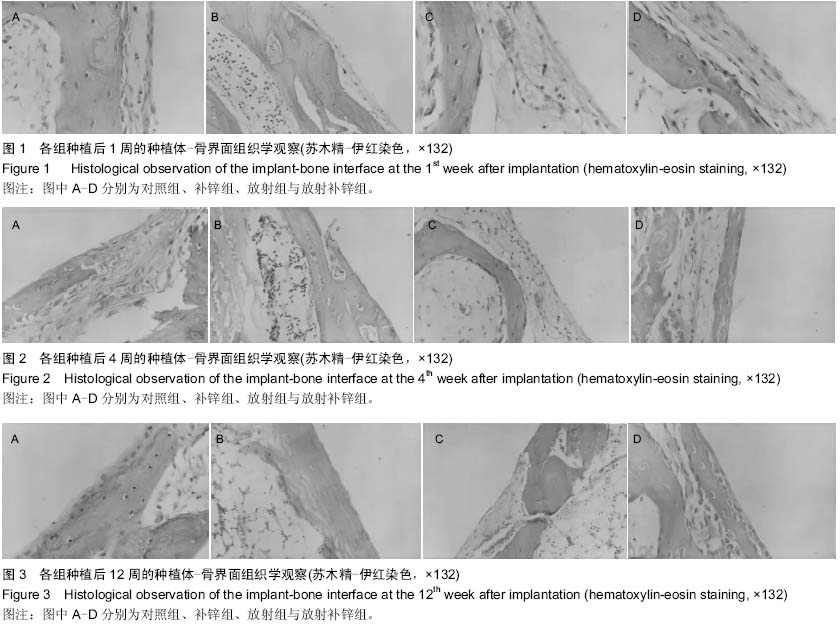
结果与结论:在相同时间段内,与其他各组相比,放射组种植体周围成纤维细胞数量较多,纤维性结合较多,而骨性组织特别是成熟骨组织形成较少。在相同时间段内,与其他各组相比,补锌组种植体表面成骨细胞数量更多,骨性结合更多,在第4周时即可见成熟骨组织出现,说明补锌能在种植后早期(1-4周)即形成骨性愈合。放射补锌组在第4,12周时也较放射组产生更多骨性结合,说明即使在60Co照射后,微量元素锌的补充仍可以促进种植体-骨融合。提示60Co照射会延缓种植体骨愈合,放射治疗后适量补锌能够减轻其对种植体骨融合的不利影响。
中国组织工程研究杂志出版内容重点:生物材料;骨生物材料; 口腔生物材料; 纳米材料; 缓释材料; 材料相容性;组织工程
中图分类号: