2.1 OPG-RANKL-RANK信号系统的概述
2.1.1 骨保护素 骨保护素是1997年Simonet等
[4]在测序胎鼠小肠cDNA文库时发现的段序列,它所表达的蛋白能明显抑制破骨细胞的形成,并引起骨密度的升高。骨保护素属于肿瘤坏死因子受体超家族成员,是一种分泌型糖蛋白,在体内多种组织细胞分泌。如骨保护素mRNA在骨髓基质细胞、成骨细胞、成纤维细胞、主动脉平滑肌细胞、成骨肉瘤细胞、乳腺癌细胞及单核细胞、树突状细胞。B淋巴细胞中均有表达
[5]。在破骨细胞的分化微环境中,骨保护素由成骨细胞、基质细胞分泌,与成骨细胞和基质细胞表面有高度的亲和力。骨保护素的蛋白有7个结构域,形成3个功能区:①肿瘤坏死因子受体包括1-4结构域,是骨保护素的主要结构域,执行抑制破骨细胞的功能。②同源区5-6属于死亡域,与Fas蛋白跨膜区形成融合蛋白具有很强的细胞毒性,可以引起细胞的凋亡。③肝素结合属于第7结构域,其作用尚不清楚
[6]。
2.1.2 RANKL 于1998年Lacey等用骨保护素做探针,发现了成骨细胞或基质细胞表面表达骨保护素配体蛋白,称之为OPGL和ODF,与此前发现的TNF配体家族的两个成员TRANCE和RANKL是同一物质。属于Ⅱ型跨膜蛋白。人RANKL基因位于染色体13q14,其分子由317个氨基酸组成,有3种亚型,跨膜蛋白RANKL1、RANKL2和分泌型RANKL3。以RANKL1存在最为广泛。研究发现RANKLmRNA在骨髓和骨中表达最高,在淋巴组织也高表达,在单核/巨噬细胞,成骨细胞,骨髓干细胞及T、B淋巴细胞中均有表达
[7]。RANKL可促进破骨细胞的分化,增强成熟破骨细胞的活力,阻止破骨细胞凋亡,是破骨细胞分化成熟和维持功能所需的重要因子。
2.1.3 RANK RANK于1997年Anderson等在分析树突状细胞的cDNA序列时,发现了RANK(receptor activator of NF-kB)
[8],证明了破骨细胞的发育与成骨细胞关系密切。研究发现,RANK在骨骼肌、小梁骨、肝脏、小肠以及肾上腺均有表达,主要分布于单核巨噬细胞系,破骨细胞的前体,T、B淋巴细胞。树突状细胞以及成纤维细胞表面。由616个氨基酸组成,可与TRAF1,2,3,5,6结合,激活转录因子NF-kB和JNK
[9],从而促进破骨细胞的增殖、分化、成熟以及增强骨吸收活性。
2.1.4 OPG-RANKL-RANK信号系统之间的作用机制RNAKL除了与RANK的配体结合外,还与骨保护素结合。RANK被激活后,产生一系列的信号转导通路,使分化中的破骨细胞达特异性的基因,使成熟的破骨细胞执行骨吸收功能并维持破骨细胞的存活。RANKL的信号经RANK传递给TRAF,在经过TRAF激活下游多种信号分子,引起一系列的信号转导反应和细胞生物学效应
[2]。
OPG-RANKL-RANK信号系统的作用机制为:①RANKL与RANK的结合激活相关的信号通路6条,即NF-кB通路、JNK/AP-1通路、CN/NFATc1通路、ERK通路、P38MAPK通路、PI3K/Akt通路。RANK信号转导途径激活,将刺激信号传递给NF-Kb, NF-Kb活化并转运到细胞核内,增加c-Fos的表达,c-Fos进一步与活化的T细胞核因子结合并相互作用,启动破骨细胞细胞生成基因的转录,最终诱导成熟的破骨细胞形成
[10]。②蛋白激酶C的活化剂可以激活骨保护素的分泌,蛋白激酶C的拮抗剂可以拮抗蛋白激酶C的活化剂诱导的骨保护素表达增加。因此蛋白激酶C途径在骨保护素的表达中具有重要的作用
[11]。③RANKL可以提高NF-кB和c-Jun氨基末端蛋白激酶(JNK)的活性
[12]。因此NF-кB、蛋白激酶C途径、JNK与OPG-RANKL-RANK信号系统的激活有关。OPG-RANKL-RANK信号系统激活产生一系列的信号级联反应,启动和调控基因的转录来调节破骨细胞的分化、功能和凋亡。
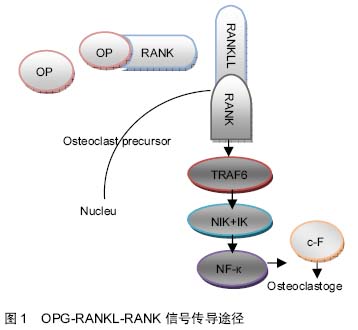
2.2 OPG-RANKL-RANK信号系统与破骨细胞的关系RANKL与RANK的结合驱动破骨细胞从造血前体细胞的发育并活化为成熟的破骨细胞提供了关键的信号。骨保护素可以阻断RANKL与RANK的结合,因此起着负调控作用,并因此抑制由破骨细胞介导的骨转换。见
图1。
RNAKL信号与破骨细胞前体细胞膜上的RANK结合,将信号传递与TRAF6,通过NIK和IKK活化NF-кB,活化NF-кB迅速与IKK分离进入细胞核,使c-Fos的高表达,c-Fos进一步与活化的T细胞核因子结合并相互作用,启动相应的靶基因的表达和转录,最终诱导成熟破骨细胞的形成
[13]。骨保护素与RANK竞争性的结合RANKL,从而阻断RANKL与前体细胞膜上的RANK的结合,延缓前体破骨细胞的分化,降低骨吸收。骨保护素对RANKL的竞争结合能力优于RANK,因而阻断使前体破骨细胞的分化为成熟破骨细胞的信号传递,RANKL和骨保护素比率的动态平衡在骨吸收中起重要的控制作用
[14]。在骨组织中,骨保护素作为一个与RANK竞争抑制的受体,从而封闭RANKL与破骨细胞表面的RANK结合,抑制破骨细胞的分化成熟。
成骨细胞和基质细胞均表达RANKL和骨保护素,都能与破骨细胞表面的RANK结合,RANKL与破骨细胞细胞膜上的RANK结合,促使破骨细胞的分化以及成熟,并且抑制破骨细胞的凋亡;而骨保护素与破骨细胞细胞膜上的RANK结合,将阻断RANKL与RANK的结合,因而抑制破骨细胞的形成与成熟过程。因此,骨保护素、RANKL、RANK之间的比例关系将对破骨细胞的形成起着重要的调控作用。骨髓基质干细胞向成骨细胞分化的过程中,骨保护素与RANKL的比值处于动态变化之中,随着成骨细胞与基质细胞的分化成熟,RANKL/OPG的比值缩小,最后将失去对破骨细胞的分化及成熟过程的调控,从而使骨形成与骨吸收达到动态平衡
[15]。因此,OPG-RANKL-RANK信号系统组成了破骨细胞形成、分化、成熟的三角调控关系,并最终影响骨的密度和骨的强度。
OPG-RANKL-RANK信号系统在调节成功细胞和破骨细胞的动态平衡,在预防骨量减少保证正常的骨更新中扮演着重要的角色。骨吸收的刺激因子并不能直接刺激破骨细胞,而是成功细胞接受骨吸收的刺激因子后分泌RANKL,RANKL与M-CSF结合到破骨细胞的前体细胞表面受体RANK和M-CSFR上,RANK胞内区的特异性位点与破骨细胞内的肿瘤坏死因子受体相关蛋白(TRAFs)结合,即TRAF6结合,引起破骨细胞下游信号的的链式反应
[16]。骨保护素的结合能力强于RANK,有效的竞争性的抑制RANKL与RANK的结合,阻断信号成功细胞向破骨细胞的传递,从而抑制破骨细胞的分化和成熟,并且加快破骨细胞的凋亡
[17]。总之,骨保护素和RANKL的动态平衡,将影响正常骨的重建和骨量的稳定性。
2.3 OPG-RANKL-RANK信号系统与骨质疏松的关系
2.3.1 原发性骨质疏松症 雌激素是维持体内骨吸收与骨形成动态平衡的重要激素,促进降钙素的分泌,抑制破骨细胞的活性,促进成功细胞的作用。绝经后雌激素分泌减少,导致破骨细胞增殖分化,骨吸收能力增强,骨形成降低,骨吸收大于骨形成,从而抑制骨胶原的成熟和钙化,继发性钙盐减少及骨组织微结构的改变,导致骨代谢的负平衡,造成高转换型骨质疏松症。
绝经后妇女性腺功能衰退,雌激素分泌减少,骨量丢失加速,是导致骨形成和骨吸收亢进的高转换型骨质疏松的主要原因之一。雌激素同时抑制骨形成和骨吸收之间的代谢转换,维持骨密度
[18]。雌激素受体(ER)位于胞质和细胞核内,分为雌激素受体和雌激素受体β两种亚型,具有转录因子的作用。成功细胞和破骨细胞均存在雌激素受体。雌激素与雌激素受体结合可抑制骨吸收,抑制蛋白水解酶的产生,研究表明雌激素直接刺激成功细胞,抑制破骨细胞的作用,即雌激素分泌减少则骨吸收亢进,骨形成抑制
[19]。雌激素直接与雌激素受体和雌激素受体β结合,通过细胞膜上的雌激素受体进行信号转导,激活靶基因的转录与表达
[20]。雌激素与成骨细胞雌激素受体结合,促进分泌胶原酶,释放细胞因子,发挥骨形成作用,并与生长骨板中软骨细胞雌激素受体结合,影响骨的生长和生长骨板闭合。雌激素通过雌激素受体途径直接作用于破骨细胞前体或成熟的破骨细胞,抑制破骨细胞分化、成熟及活性,促使破骨细胞凋亡,从而减少破骨细胞数量,减弱骨吸收效应
[21]。另外雌激素雌激素还可以负调控炎症因子(如白细胞介素1、肿瘤坏死因子а)的产生,以及上调转化生长因子β的表达促进破骨细胞的凋亡。
骨骼系统在多种细胞因子及其受体的调控下处于动态平衡之中。绝经后雌激素分泌量减少,则M-CSF、RANKL的表达增加,破骨细胞的分化成熟增多,衰退期延缓,骨吸收能力增强,骨吸收与骨形成偶联失衡,导致骨量减少,骨小梁变细、间隙增大。在实验中发现去势大鼠RANKL的mRNA在第4周达到高峰,其蛋白在第6周达到高峰,此后并且维持在较高水平;其骨保护素的mRNA在第4周达到高峰,其蛋白水平第2周达到高峰,此后逐渐降低
[22]。在去势大鼠的骨质疏松中,骨髓细胞主要是RANKL得表达增强,使OPG/RANKL的比率下降,导致造血干细胞向破骨细胞的转化增加,破骨细胞的活性增强,破骨功能亢进,骨吸收增强
[23]。
老年性骨质疏松症属于低转换型,随老龄化的漫进,体内干细胞向脂肪细胞的转化,趋于成骨细胞的分化减少,功能下降,而破骨细胞在多种细胞因子的调控下分化增加,骨代谢处于负平衡。肿瘤坏死因子а在骨代谢中扮演着重要角色,能够促进骨吸收及骨基质胶原的合成,减弱成功细胞对维生素D的转录反应;抑制细胞外基质的沉积并刺激基质金属蛋白酶的合成,从而降解有机物;并且可以促进M-CSF和RANKL的表达
[24]。肿瘤坏死因子а通过增加c-fms在骨髓前体细胞表面的表达来调节骨髓中破骨前体细胞的充裕量,c-fms的表达产物是M-CSF的受体;并且肿瘤坏死因子а可损伤肾血管-基底膜屏障,导致血管通透性增高,影响钙磷的平衡。IFN-γ是破骨细胞的分化的启动因子,它可以促进组织相容性复合体Ⅱ类抗原(MHC-Ⅱ)的表达,进而促进T细胞的增殖与活化,导致RANKL、肿瘤坏死因子а的高表达,致使破骨细胞的分化,诱发骨质疏松症
[25]。
2.3.2 继发性骨质疏松症 长期大量使用某些药物如激素等可引起骨质疏松,糖皮质激素促进成骨细胞RANKL的表达;活化RANKL可以增加骨基质的通透性,引起成功细胞和骨细胞的凋亡,并且促进破骨细胞的分化和成熟。研究表明肌肉注射糖皮质激素后,大鼠骨组织中的骨保护素mRNA表达水平明显下降,而RANKLmRNA的表达水平明显升高
[26]。糖皮质激素能促进成功细胞中RANKL的表达,其可以促进破骨细胞的分化与成熟,并且活化的RANKL可以增加骨基质的通透性,引起成功细胞与骨细胞的凋亡,减少骨量
[27]。实验证实糖皮质激素会使RANKL与骨保护素的比率产生变化,促进骨吸收,是激素介导骨质疏松症发生的重要机制。
长期卧床、牵引制动导致骨的质量及强度下降,骨的微细结构变化,制脆性增加,属于继发性骨质疏松症的一种特殊类型。骨承受力及骨小梁的方向与外力的强度相一致。制动可以增加骨吸收。Bateman等
[28]通过实验证明,骨保护素可抑制与制动相关的骨流失。Sanchez等
[29]运用加压方式研究高强度对破骨细胞的影响,发现破骨细胞受到应力刺激后,骨保护素mRNA的表达下降,RANKLmRNA的表达没有明显变化。根据Wolf定律,骨小梁微细结构的排列方向随外界应力的变化而变化。长期制动使骨小梁的微细结构缺少机械外力的刺激,致使骨小梁的微细结构紊乱,RANKL的表达减少,骨丢失增加。
2.3.3 OPG-RANKL-RANK信号系统的靶向治疗 OPG-RANKL-RANK信号系统是调节骨形成和骨吸收的关键信号通路,其相关信号分子也成为备受关注的治疗靶点。并且从基因及分子水平进行了深入的探索。通过基因转染技术治疗肿瘤和骨吸收等代谢性骨病中骨改建速率有一定的进展,证实骨保护素与RANKL基因转染技术的应用,能够显著增强成骨及骨改建的速率
[30]。直接抑制RANKL主要基于RANKL的中和抗体或天然抑制物骨保护素。RANKL-Fc作为decoy受体用于抑制RANKL。RANKL全人源单抗denosumab已进入临床阶段,用于低骨量骨质疏松女性,提高骨密度
[31]。重组的骨保护素与抗体Fc段融合的镶嵌抗体OPG-Fc,具有抗骨吸收的作用,对破骨细胞的发育、分化和存活具有多重效应
[32]。OPG-RANKL-RANK信号系统不仅激活破骨细胞发育所需的许多下游信号通路,并且与其他信号通路相互作用,相互协同,实现骨的稳态。因此,OPG-RANKL-RANK信号系统的特异性靶向治疗,将会为骨质疏松症的治疗带来福音。
