中国组织工程研究 ›› 2015, Vol. 19 ›› Issue (18): 2911-2916.doi: 10.3969/j.issn.2095-4344.2015.18.022
• 器官移植动物模型 organ transplantation and animal model • 上一篇 下一篇
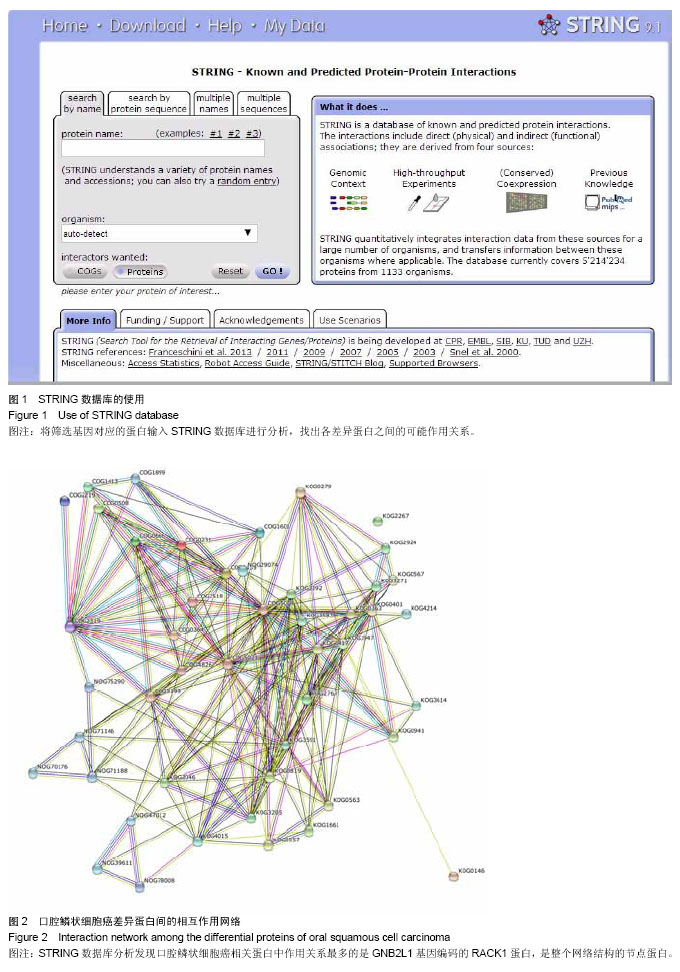
构建以RACK1为核心口腔鳞状细胞癌差异基因间相互作用的关系网路
郑建伟1,2,利小平2,董俊英2,曾宪丽2,梁友龙2,韩帮峰2,杨德群2,罗 刚1
- 1南方医科大学附属广东省口腔医院,广东省广州市 510280;2广东省深圳牙科医疗中心,广东省深圳市 518001
Constructing an interaction network of differential genes of oral squamous cell carcinoma with RACK1 as a core
Zheng Jian-wei1, 2, Li Xiao-ping2, Dong Jun-ying2, Zeng Xian-li2, Liang You-long2, Han Bang-feng2, Yang De-qun2, Luo Gang1
- 1Guangdong Provincial Stomatological Hospital, Southern Medical University, Guangzhou 510280, Guangdong Province, China; 2Shenzhen Dental Medical Center in Guangdong Province, Shenzhen 518001, Guangdong Province, China
摘要:
背景:RACK1与口腔鳞状细胞癌的发生发展密切相关,但肿瘤的发生发展不是一个基因或蛋白决定的,是多基因、多分子呈网络结构,多步骤、多阶段共同作用的长期复杂过程,各肿瘤基因之间相互协同作用促使肿瘤细胞形成和发展。因此要揭示口腔鳞状细胞癌的作用机制将不能局限于单个蛋白或基因,而要着眼于与口腔鳞状细胞癌差异蛋白或基因相关的信号网络通路,研究整个信号通路中相关蛋白或基因的表达变化,进而分析研究这些分子之间的相互作用机制。 目的:筛选出的口腔鳞状细胞癌相关差异基因,使用STRING数据库通过生物信息学的方法构建它们之间的相互作用关系网络,为后续实验提供线索。 方法:根据作者所在课题组前期口腔鳞状细胞癌的经典蛋白组学实验结果和基因表达谱芯片实验的数据结果,选择表达一致且差异相对较大的基因作为实验的差异基因。将筛选的差异基因输入STRING数据库进行分析,找出差异基因对应蛋白之间的可能作用关系,构建相互作用网络结构图。 结果与结论:口腔鳞状细胞癌的19个差异基因对应蛋白相互间构成一个复杂的作用网络,各差异蛋白间通过多条相互作用通路进行调节,RACK1蛋白是整个网络的节点蛋白。GNB2L1的编码蛋白RACK1蛋白通过WD40重复蛋白亚基(编号COG2319)和β-G蛋白亚基(编号KOG0279)与其他差异蛋白的亚基间相互作用。其中WD40重复蛋白(编号COG2319)与其中5个差异蛋白直接作用并构建了10条相互作用通路,β亚基G蛋白(编号KOG0279)与其中8个差异蛋白直接作用并构建了11条相互作用通路。说明通过STRING数据库分析构建了这19个差异基因相互作用的结构网络图发现RACK1蛋白的2个亚基共与8个相关差异蛋白直接作用,产生18条相互作用通路。在这个网络结构中RACK1蛋白是中心,提示其是口腔鳞状细胞癌的一个关键节点蛋白。
中图分类号: