2.1 中国临床试验注册中心关于干细胞治疗脑梗死的项目 中国临床试验注册中心是2007年6月由卫生部正式确认的,是代表中国的世界卫生组织临床试验注册机构,也是全球第4个成立的世界卫生组织国际临床
试验注册平台的一级注册机构。中国临床试验注册中心的成立大力推广临床试验报告规范,从临床试验的入口和出口把关临床试验质量,为医生提供临床科研方法学指导和培训,指导完善临床试验的设计,提供中央随机和隐蔽分组服务,指导试验报告和论文写作[21]。中国临床试验注册中心关于干细胞治疗脑梗死的相关信息有2条。
2011年,武警总医院干细胞移植中心研究脐带间充质干细胞移植治疗脑干疾病的疗效获得注册。
研究类型:干预性研究。
研究阶段:Ⅱ期临床试验。
研究设计:无对照研究。
纳入标准: ①脑干疾病慢性期:包括脑干出血、脑干梗死以及脑干损伤等病因导致的脑干软化灶形成。②头部CT或MRI明确显示脑干病灶。
排除标准: ①脑血管疾病急性期。②严重心血管疾病。③免疫力低下或正在使用免疫抑制剂。
实施时间:2011-09-01/2012-12-31。
样本量:20例。
测量指标:电生理FIM评分。
年龄范围:5-80岁。
性别:男女均可。
随机方法:方便选择。
研究情况:结束。
2012年,解放军第105医院神经内科研究脐带间充质干细胞移植治疗脑梗死的疗效和安全性获得注册。
研究类型:观察性研究。
研究阶段: Ⅱ期临床试验。
研究设计:非随机对照试验。
纳入标准: ①年龄18-80岁。②CT或MRI证实脑梗死后14 d以上。③TCD检测脑梗死病灶区的血管恢复再通。④美国国立卫生研究所脑卒中评分为4-17。
排除标准: ①脑梗死同侧颈内动脉硬化斑块阻塞>50%。②脑梗死继发脑水肿或脑出血后美国国立卫生研究所脑卒中评分>4。③血液高凝状态或原发性血液系统疾病。④mRS评分>2。⑤神经系统变性疾病。⑥自身免疫性疾病。⑦心肌梗死病史。⑧败血症。⑨恶性肿瘤。⑩肾功能不全等。
实施时间:2009-09-27/2014-12-01。
样本量:干细胞治疗组75例,对照组50例。
测量指标:美国国立卫生研究院卒中量表。
年龄范围:18-80岁。
性别:男女均可。
随机方法:非随机试验,根据患者的入组的先后次序生成。
研究情况:正在进行。
2.2 细胞因子对脑梗死后神经干细胞增殖、迁移的影响 神经干细胞移植在修复神经功能损伤时,一方面通过移植的细胞替代受损细胞发挥作用,另一方面细胞自身分泌和促进宿主分泌细胞因子来修复损伤,如神经生长因子、碱性成纤维细胞生长因子、脑源性神经营养因子等[12]。
2.2.1 表皮生长因子 成年动物脑梗死后脑室管膜下区的神经干细胞有增殖的反应,并可以向梗死灶区域迁移,但迁移距离较短。余剑等[13]研究发现表皮生长因子可以对大鼠脑梗死后室管膜下区神经干细胞有调节作用。采用肾血管性高血压大鼠复制成一侧大脑中动脉皮层支闭塞模型。大脑中动脉皮层支闭塞术后24 h,64只表皮生长因子组大鼠在立体定位仪下,用微量注射器在侧脑室注入10 μL表皮生长因子(0.1 g/L),连续2 d,共注入2 μg(20 μL);64只vehicle组大鼠只注入不含表皮生长因子的等量溶液。研究发现表皮生长因子组大鼠梗死灶同侧脑管膜下区内巢蛋白染色更强,从脑管膜下区沿胼胝体向梗死灶迁移的巢蛋白阳性细胞带;Western blotting显示表皮生长因子促使脑梗死灶同侧巢蛋白、神经细胞粘附分子和瑞林蛋白更早期和更高的表达。可见表皮生长因子可能通过促使卒中后巢蛋白、神经细胞粘附分子和瑞林蛋白等神经可塑性物质的早期高峰表达而调节脑管膜下区内神经干细胞增殖和向梗死灶迁移。
2.2.2 脑源性神经生长因子 臧大维等[14]研究脑源性神经生长因子对脑梗死后神经干细胞的影响,将24只大鼠分为盐水对照组和实验组,实验组于梗死后 24 h给予脑起源神经营养因子,采用ALZET锇药物泵缓慢释放,28 d内持续缓慢释放药物。运动功能测试脑起源神经营养因子治疗组小鼠在Rotarod上的停留时间延长,运动功能的恢复明显优于盐水对照组,差异有显著性意义(P < 0.01)。实验组小鼠脑内出现免疫荧光阳性表达的内源性神经干细胞,表达数量明显高于盐水对照组。实验组分化为神经元的比例明显高于盐水对照组(36%,15%),分化为星形胶质细胞的比例低于盐水对照组(54%,77%),分化为少突胶质细胞的比例二者基本相似(10%,8%)。
2.2.3 胰岛素样生长因子1 叶飞等[15]观察胰岛素样生长因子1在脑梗死大鼠神经干细胞增殖、迁移和分化中的作用,将80只SD大鼠随机分为对照组和实验组,每组40只。造模后实验组大鼠通过尾静脉注射胰岛素样生长因子1,按100 μg/kg计算,连续注射 6 d;对照组给予等剂量的生理盐水。分别于干预后7,14,21,28 d断头去脑,各组分别在处死前1 d腹腔注射5-溴脱氧尿嘧啶。5-溴脱氧尿嘧啶阳性细胞、PSA-NCAM阳性细胞数均在缺血后7 d最多;BrdU+PSA-NCAM双标阳性细胞在缺血后双侧室管膜下区和海马齿状回区均可以检测到,于7 d计数最多,之后逐渐减少;BrdU+MAP2双阳性细胞却从14 d开始逐渐增多,随BrdU+PSA-NCAM双阳性表达的逐渐降低,BrdU+MAP2双阳性表达逐渐增高,呈现此消彼涨的变化。提示静脉给予胰岛素样生长因子1能诱导大鼠缺血性脑损伤后神经干细胞的增殖、分化和迁移。
2.3 针灸及中医药与脑梗死后神经干细胞移植的影响
2.3.1 电针 唐强等[16]观察头穴丛刺法对室管膜下区神经干细胞增殖、迁移、分化的调控作用,为促进成年神经再生、修复和重建神经网络提供理论依据。实验大鼠注射荧光染料Dil以预标记室管膜下区细胞;栓线法制备大鼠局灶性脑缺血模型。将造模成功的Wistar大鼠随机分成模型组12只,头针组12只,头针丛刺法组12只,假手术组4只。采用脉冲式的5-溴脱氧尿嘧啶标记方法标记新生细胞;采用激光共聚焦显微镜检测预标记原始SVZNSC后。再检测双蕈免疫荧光染色所确定的分化的细胞。模型组、头针组、头穴丛刺法组均可见Dil标记的室管膜下区细胞迁移至梗死周边的纹状体和皮质,并且分化成神经元或胶质细胞。两种方法标记后不同时间细胞计数,见表1。
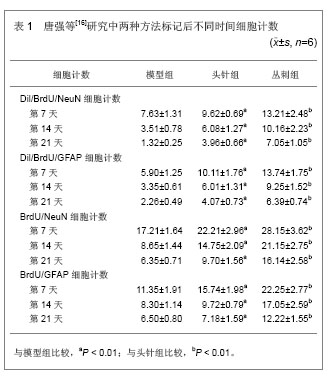
头穴丛刺法组Dil/BrdU/NeuN或Dil/BrdU/GFAP标记的细胞明显增多,与其他两组比较差异有显著性
(P < 0.01);头穴丛刺法组BrdU/NeuN及BrdU,GFAP阳性细胞表达均多于其他两组,组间比较差异有显著性意义(
P < 0.01)。头穴丛刺法能促进脑缺血后SVZ区神经干细胞增殖,并且随时间递增减少其增殖衰减;可以促进Dil标记的室管膜下区细胞均迁移至梗死周边的纹状体和皮质。并且分化成神经元或胶质细胞;还能促进局灶性脑缺血后室管膜下区神经干细胞的迁移和分化。
2.3.2 中医药 冯云等[17]研究夏天无对脑梗死大鼠神经干细胞及突触素影响,采用栓线法制作大鼠永久性大脑中动脉闭塞模型。通过常规苏木精-伊红染色观察大鼠海马及皮质的形态学改变,免疫组化荧光法测突触素及5-溴脱氧尿嘧啶标记的神经干细胞表达情况,见表2。
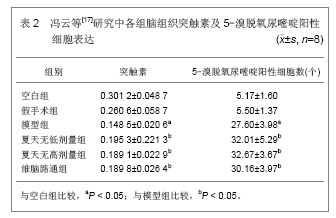
模型组大鼠神经细胞破坏明显,空白组和假手术组大鼠5-溴脱氧尿嘧啶阳性细胞及突触素表达差异无显著性意义;模型组5-溴脱氧尿嘧啶阳性细胞及突触素表达较其它组差异有显著性意义;夏天无低剂量组和维脑路通组及夏天无低、高剂量组之间比较均差异无显著性意义。可见,夏天无可以促进大鼠脑梗死模型脑组织神经干细胞增殖和突触素的表达,增强脑梗死大鼠大脑可塑性。
2.4 基因调控与脑梗死后神经干细胞的移植
2.4.1 低氧诱导因子1α基因 脑梗死后神经干细胞的增殖和分化与脑内微环境密切相关,梗死区域有大量的神经细胞丢失,低氧诱导因子1是低氧应答过程中起重要作用的转录因子,对缺血缺氧神经元具有保护作用[18]。低氧诱导因子1主要以异二聚体形式存在,由低氧诱导因子1α和低氧诱导因子1β亚基组成,生物学功能主要取决于低氧诱导因子1α亚基的蛋白质水平和活性。低氧诱导因子1α通过诱导糖酵解基因、血管内皮生长因子、一氧化氮合酶、红细胞生成素的表达,从而使缺氧的组织细胞保持氧稳定及耐受低氧状态。吴万福[19]对低氧诱导因子1α基因在大鼠局灶性脑缺血后内源性神经干细胞的增殖、分化以及血管新生方面进行研究,并分析低氧诱导因子1α对内源性神经干细胞增殖、分化及血管新生的作用机制。首先建立大鼠大脑中动脉缺血再灌注模型,1 d后将神经缺失功能评分在7-12分的大鼠随机分为生理盐水组、单纯腺病毒组和低氧诱导因子1α组,并分别注射生理盐水、单纯腺病毒和低氧诱导因子1α到模型大鼠缺血侧侧脑室,5-溴脱氧尿嘧啶标记内源性神经干细胞的增殖与分化。移植后各时间点大鼠神经功能缺失评分和脑室管膜下区阳性细胞数比较,见表3。
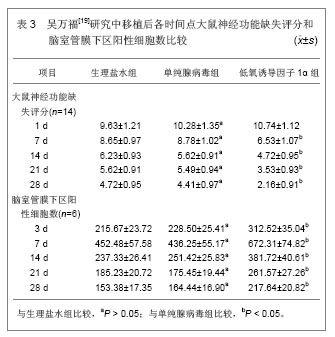
研究发现低氧诱导因子1α组在第7,14,21,28天神经缺失功能评分优于生理盐水组和单纯腺病毒组(
P < 0.05)。低氧诱导因子1α组各时间点低氧诱导因子1α、血管内皮细胞生长因子以及红细胞生长素的表达有所增强,5-溴脱氧尿嘧啶标记细胞数明显增加;新生细胞分化结果显示28 d时,低氧诱导因子1α组5-溴脱氧尿嘧啶/NF200(47.74±13.52) %、5-溴脱氧尿嘧啶/GFAP(67.83±20.75)%,与其它组相比差异均有显著性意义(
P < 0.05)。低氧诱导因子1α组Ⅷ因子阳性细胞数与生理盐水组和单纯腺病毒组比较差异有显著性意义(
P < 0.01)。
可见,低氧诱导因子1α基因可以促进大鼠局灶性脑缺血后内源性神经干细胞的增殖与分化以及新生血管的形成,从而促进神经功能的恢复。同时,研究还发现携带低氧诱导因子1α基因的腺病毒在体外可以感染神经干细胞,得到低氧诱导因子1α的表达,增强神经干细胞增殖能力和分化的神经元样细胞钠电流及对缺氧的耐受能力;低氧诱导因子1α基因还可以促进神经干细胞的存活、迁移以及新生血管的形成,对脑缺血大鼠有治疗作用。
2.4.2 Brca-1基因 方力群等
[20]通过雌激素上调Brca-1基因表达,促进成体神经干细胞增殖,然后移植用于治疗脑梗死。线栓法建立大鼠急性脑梗死模型,立体定位的方法向大鼠脑室内注射PBS溶液、常规培养的神经干细胞、10
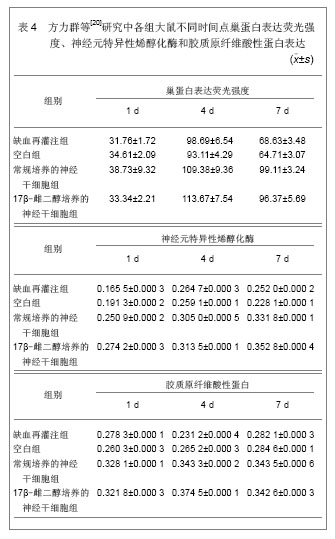
-5 mol/L 17β-雌二醇培养的神经干细胞。发现常规培养的神经干细胞组和17β-雌二醇培养的神经干细胞组大鼠神经功能恢复较其余两组要好,各组大鼠不同时间点巢蛋白表达荧光强度、神经元特异性烯醇化酶、胶质原纤维酸性蛋白表达,见表4。
由表4可见,激光共聚焦显微镜显示脑缺血再灌注组和空白组在4 d时荧光强度最强,在7 d时荧光表达减弱,17β-雌二醇培养的神经干细胞组在4 d时荧光强度也最强,而且在7 d时荧光表达仍然很强。17β-雌二醇培养的神经干细胞组神经元特异性烯醇化酶和胶质原纤维酸性蛋白表达阳性结果高于常规培养的神经干细胞组。用雌激素上调Brca-1基因表达的神经干细胞移植后治疗脑缺血再灌注的效果优于常规培养的神经干细胞。