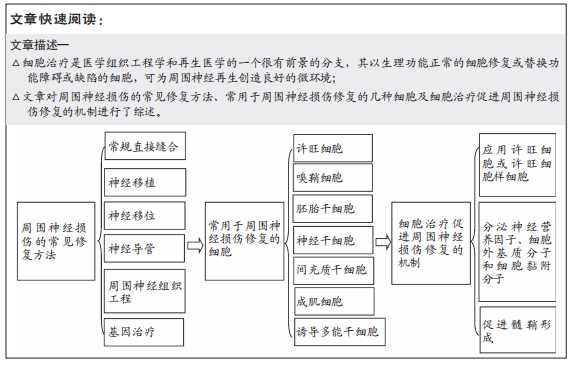
2.1 周围神经损伤的常见修复方法

众所周知,周围神经损伤后其轴突具有一定的再生能 力[8],提供适当的方法可使损伤神经与远端相应靶组织重新建立突触联系,并且加速轴突再生的任何方法都可以促进周围神经损伤发生后的功能恢 复[1,9]。周围神经损伤的修复方法多种多样,主要包括常规直接缝合、神经移植、神经移位、神经导管、周围神经组织工程、细胞治疗和基因治疗等,这些治疗方法均各有利弊,具体治疗策略取决于周围神经损伤的类型和程度[6-7]。
2.1.1 常规直接缝合 对于损伤区近侧残端神经可用、具有良好的血供和软组织覆盖[6],且间隙< 5 mm的周围神经[1],临床上通常直接采用显微外科手术进行常规一期端端缝合修复;当损伤神经的近侧残端不可用或无法到达,或为撕脱伤时,可考虑采用端侧缝合或神经移位修复[6],但在直接缝合修复后,可能存在间隙较大、缝合线张力过大等缺陷,并可能会引起神经损害和炎症反应等,然而,由于缺乏针对其他周围神经损伤修复方法的良好对照人体试验,因此常规直接缝合修复周围神经损伤仍未受到质疑[1]。
2.1.2 神经移植 对于缺损间隙>3 cm或不能进行无张力缝合的周围神经损伤,自体神经移植多年来一直被视为“金标准”,其可提供对轴突再生必不可少的神经营养因子和存活的许旺细胞[6,10],并且在张力状态下的神经再生效果最好[11],但因供体来源有限、供体部位发病率、组织结构和大小存在差异等缺陷而限制了其临床应用[6,10-11]。
同种异体神经移植是自体神经移植的一种替代方法,其相对更容易获得,且不存在供体部位发病率,但需要接受全身免疫抑制治疗,这可能会导致机会性感染甚至肿瘤形成[12]。然而,研究发现,使用的某些免疫抑制剂如他克莫司可进一步增强周围神经再生[6-7]。通过化学清洗剂、酶降解和照射等特定的处理,可将同种异体移植物制备成脱细胞异体神经移植物,以避免免疫抑制,其神经内部结构包括神经内膜管、基底膜和层粘连蛋白等仍然保留,为轴突再生提供了理想的结构环境[6-7,12]。但脱细胞神经移植物对长段周围神经损伤的再生效果有限,因此,需要联合神经营养因子或种子细胞等来增强它们的神经再生作用[10]。
2.1.3 神经移位 神经移位是一种将健康的次要功能神经束与远端更为重要的神经段连接的周围神经损伤修复方法,其将近端损伤转化为远端损伤[13-15],适应证包括臂丛神经损伤,特别是近侧神经残端无法使用的损伤、距离目标运动终板较远的撕脱伤以及神经功能节段性丧失的损伤等,其中最常见的应用为肘关节屈曲、肘关节伸展、肩外展等[13-14]。相对于神经移植,神经移位具有在大多数情况下仅有一个神经吻合部位、可使神经再生距离最小化等优势[13,16],目的是通过快速再支配失神经运动目标,从而最大程度地实现功能恢复[13]。但供体神经部位也可能丧失功能,并且供体部位肌肉可能不再是肌肉移位的理想供体[6]。诸多学者在临床前和临床研究中取得了令人鼓舞的结果,证实了神经移位的有效性[13-14,16]。
2.1.4 神经导管 研究表明,神经可通过各种导管(如静脉、生物可吸收管等)在短神经间隙中再生,因此对于缺损间隙< 3 cm的小直径神经或< 0.5 cm的大直径神经,可考虑采用神经导管进行修复重建[13],其中经体积分数为70%乙醇脱细胞处理后的合适大小的静脉被认为是最好的选择[17],某些生物可降解导管如聚乙醇导管应用于周围神经损伤的临床恢复效果与自体神经移植相当,因此神经导管是一种可行的自体神经移植替代方案[13],
其可作为轴突延伸的导管,保护神经不受周围组织和瘢痕形成的影响,并调节神经损伤的微环境,以及引导再生轴突进入远侧神经残端与相应的靶神经元重新连接[6],但是导管本身并不对神经修复的结果产生影响。神经导管可消除如宿主-供体神经存在的直径差异、神经束数量和形态、以及横截面形状和面积不匹配等问题[18],已成功应用于临床。但各种导管也有其各自的局限性[13],如生物导管对长段周围神经损伤的神经再生效率较低,不可降解合成导管可促使瘢痕组织的形成,缺乏弹性和稳定性,并且可能引起慢性异物反应和炎症等[11],因此关于神经导管材料的研究仍需继续深入。
2.1.5 周围神经组织工程 为了增强神经导管的再生效果并延长神经再生的距离,大量学者对周围神经组织工程进行了深入研究,将支架材料、种子细胞和神经营养因子作为添加剂加入到导管腔内对周围神经损伤进行修复是研究最为广泛的方法。研究表明,这3种基本元素的结合可产生协同效应,并且在修复周围神经损伤时发挥物理和营养支持作用,从而增强周围神经损伤的修复与再生效果[19],另外,无需二次手术[13],因此可以替代神经移植。
基于种子细胞的治疗,即细胞治疗,是组织工程和再生医学的一个很有前景的分支,因其具有可利用细胞自身的生物学特性,以生理功能正常的细胞修复或替换功能障碍或缺陷的细胞,可作为一种促生长因子传递系统和移植物替代物,较小分子化学药、大分子蛋白药等更容易治愈疾病、不良反应更小等优势[20],近些年来已成为周围神经损伤修复的重要前沿探索领域,并已取得了诸多进展。与此同时,各种相关辅助技术也得到了发展,如脉冲电磁场和电刺激已被证明可有效提高神经轴突再生的速度和准确性,神经超声可检测外伤性神经损伤进展情况[13,19],自主运动可促进人骨骼肌干细胞移植导管桥接后长段神经缺损的修复等[21]。然而,周围神经组织工程也存在一些问题,如神经营养因子的选择、固定操作和缓释技术、释放动力学及其与再生的关系等都需要进一步研究[19]。
2.1.6 基因治疗 基因治疗是自体神经移植的另一种替代方案,亦可增强周围神经损伤的修复与再生[14],其主要优点是经病毒转染的细胞可在较长时间内稳定表达某一特定基因,从而产生更多的神经营养因子、细胞外基质分子和转录因子等[6,11,14],并且基因治疗具有选择性、区域性和特异性,已被成功应用于啮齿动物模型中。但也存在很多因素阻碍其向临床转化,包括选择正确的神经营养因子和靶细胞、插入的神经营养因子半衰期较短、关于载体的生物安全性以及存在包括诱变在内的长期风险等。随着基因技术的不断发展,基因治疗终将成为临床工作中必不可少的治疗措施[14]。
2.2 细胞治疗促进周围神经损伤修复 尽管已经开发了多种策略来促进周围神经损伤发生后的修复与再生,但是在细胞大量丢失的情况下,如在严重损伤后很可能需要完全替换细胞[13]。在进行细胞治疗时,植入的细胞可产生神经营养因子、结构性和黏附性细胞外基质分子等[14,19],为周围神经轴突再生和功能回路重建创造了良好的微环境,从而刺激和支持近端残端的轴突再生,是修复长段周围神经损伤的一种有前景的治疗策略[22]。用于周围神经损伤修复的细胞类型主要包括成熟体细胞如许旺细胞、嗅鞘细胞,干细胞如胚胎干细胞、神经干细胞、间充质干细胞、成肌细胞和诱导多能干细胞等。
2.2.1 成熟体细胞
(1)许旺细胞:众所周知,许旺细胞是周围神经的主要结构和功能细胞,在华勒变性过程中许旺细胞募集巨噬细胞,与巨噬细胞一起清除退化的轴突和髓鞘碎片[5,23-24];在再生阶段,许旺细胞形成Büngner带,为轴突生长提供再生通道,并增加表面细胞黏附分子和细胞外基质分子的合成,以物理方式将轴突引导至远端神经支配目标[5,22,25]。许旺细胞可分泌多种神经营养因子,如神经生长因子、脑源性神经营养因子和睫状神经营养因子等,有助于创造良好的微环境,以促进神经元存活及轴突和髓鞘再生等[5,22,25],因此是周围神经损伤修复过程中最重要、也是首选的种子细胞。然而,因自体许旺细胞的获取需牺牲健康神经、短期内需进行二次手术以及扩增所需时间较长等不足而限制了其临床应用[5,24,26-27]。
(2)嗅鞘细胞:研究表明,嗅鞘细胞与许旺细胞和星形胶质细胞具有相同的特征[24,28],能够清除退化的轴突和髓鞘碎片,创造引导新轴突再生的通道[9,24];可产生多种神经营养因子和细胞外基质分子,为受伤神经元的存活和轴突的再生提供了直接营养支持作用和微环境[9,11,24,28];具有髓鞘形成能力,可使脱髓鞘的轴突重新髓鞘化,实现快速脉冲传导[9,11,28]。此外,嗅鞘细胞与许旺细胞均不会积累导致生长锥体塌陷的蛋白聚糖[9],并且较许旺细胞具有更大的迁移潜力和更早的营养支持作用,可促使再生轴突在瘢痕组织形成之前穿过损伤部位[9,28]。因此,嗅鞘细胞较许旺细胞可能更适合作为周围神经修复的候选细胞。但嗅鞘细胞的来源有限,并且修复周围神经损伤的研究较少(只集中在啮齿动物),因此,还需要更多的临床前和临床试验[11,28]。
2.2.2 干细胞
(1)胚胎干细胞:胚胎干细胞是一类源于胚泡内细胞群(早期胚胎)的全能干细胞,理论上可分化发育为机体所有组织和器官中的细胞类型,如分化为具有许旺细胞形态和分子特征的细胞[19,29-30]。胚胎干细胞可表达神经生长因子和血管内皮生长因子等多种神经营养因子[31],并可与轴突发生物理相互作用,从而促进轴突再生、髓鞘形成和血管生成等[29,31],是周围神经损伤修复的一种潜在的种子细胞。但其存在来源受限、伦理学争议等缺陷,并且可能具有免疫原性和致瘤性[29-34],所以需要寻找其他的良好替代品。
(2)神经干细胞:神经干细胞是一群存在于神经系统中的成体干细胞,可分化为神经元和胶质细胞(如许旺细胞和星形胶质细胞等)[26,29,31],它的成功发现打破了神经细胞不能再生的传统观念[26]。研究表明,神经干细胞具有激活固有许旺细胞与分泌多种重要神经营养因子和细胞外基质分子的能力,可促进轴突再生和再髓鞘化[26,29,31],同时可延缓失神经肌肉萎缩[26,29]。另外,神经干细胞还具有迁移能力强、免疫原性低等特性[19,26],因此是用于周围神经损伤修复的一种合适的供体细胞。但其取材来源的限制、神经母细胞瘤高发生率以及神经细胞系定向分化困难等问题而限制了其在周围神经损伤修复中的广泛应用[29,31]。
(3)间充质干细胞:间充质干细胞是一群源于中胚层的成体干细胞,可从骨髓、脂肪、胎盘等组织获取。间充质干细胞可分化为多种组织细胞,具有旁分泌效应和免疫调节特性[30-31,35],是一种理想的种子细胞。研究表明,间充质干细胞的自身形态(未分化)或许旺细胞形态(转分化),均可通过调节固有许旺细胞的行为、表达神经营养因子和细胞外基质分子,引导轴突生长、增加髓鞘形成、抑制炎症反应和减少肌肉萎缩,显著促进了神经再生和功能恢复[30-31,35-36]。间充质干细胞促进神经再生的另一种方式是通过直接分化为血管内皮细胞和间接的旁分泌效应促进血管生成[3-4,29]。但间充质干细胞也存在一些缺陷,如骨髓间充质干细胞的获取具有侵袭性[3-4,29-30]、脂肪间充质干细胞和骨髓间充质干细胞的生物学特性均受采集部位和供者年龄的影响等[3-4,29],因此仍需继续进行深入研究。
(4)成肌细胞:成肌细胞是一群位于骨骼肌肌纤维基底膜与肌膜之间的多能干细胞,因其来源丰富、获取容易以及在氧化和缺氧条件下仍具有出色的生存能力等特性而备受研究者的青睐。成肌细胞可分化为神经、血管再生所需的细胞和分泌多种二者再生所需的神经营养因子[33,37-38],同时还可通过募集其他辅助细胞如巨噬细胞,调节免疫反应、旁分泌和内分泌因子发出信号来协调机体做出反应[32],减轻甚至逆转失神经肌肉萎缩[32,37],并且因血管化的增强和纤维化的减少,成肌细胞可有效防止周围神经损伤部位神经瘤的形成。但成肌细胞也存在目前尚未建立标准化的分离纯化方法、特异性标志物仍未完全阐明等缺陷[32]。
(5)诱导多能干细胞:诱导多能干细胞是一类通过基因重编程,使人或动物体细胞具有胚胎干细胞功能的多能干细胞[10,31,39-40]。但诱导多能干细胞克服了胚胎干细胞的局限性,并可通过非侵入性方法获取[10,31]。与其他干细胞一样,诱导多能干细胞用于周围神经损伤修复依赖于细胞与神经营养因子和细胞外基质分子的双重作用,显著改善了周围神经损伤功能的恢复[10,31,39],并且其沿神经系分化的方法已经建立[4],但诱导多能干细胞表现出的免疫原性以及表观遗传记忆和染色质畸变可能导致的高致瘤率等,引起了人们对其安全性的担忧[10,40],尽管如此,诱导多能干细胞领域的惊人成就和快速发展为其未来的研究创造了乐观的前景[40]。
2.3 细胞治疗促进周围神经损伤修复的机制

众所周知,细胞、细胞因子和细胞外基质均是神经修复与再生过程中的重要因素,并且神经修复与再生依赖于三者之间复杂的相互作用[22]。因此,在近几十年中,细胞治疗和组织工程受到了极大的关注,并且被广泛用于各个领域。迄今为止,细胞治疗促进周围神经损伤修复的机制尚未完全阐述清楚,仍需继续深入研究,但从目前的研究来看,主要表现在应用许旺细胞或许旺细胞样细胞,分泌神经营养因子、细胞外基质分子和细胞黏附分子,促进髓鞘形成3个方面,见图1[3-5,29-30]。
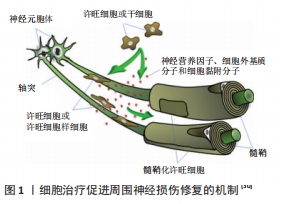
2.3.1 应用许旺细胞或许旺细胞样细胞 许旺细胞是周围神经损伤修复与再生过程中最重要的细胞,参与华勒变性、轴突再生以及髓鞘形成等过程,其与周围微环境的相互作用可促进轴突以1-4 mm/d的速度萌发[2],但因其存在诸多缺陷[26-27],因此细胞治疗周围神经损伤的研究主要集中在具有许旺细胞特性的其他细胞上[1],并且许旺细胞样细胞已成为周围神经损伤修复中细胞来源的主要选择。研究发现,干细胞植入受损神经组织后可继续增殖,并在适当的微环境刺激下可进一步分化为必要的支持细胞类型,如许旺细胞样细胞等[4];并且,干细胞在体外适当的微环境下亦可分化成许旺细胞样细胞和其他神经表型,体外常用的诱导方案主要包括神经营养因子(如神经生长因子、脑源性神经营养因子和睫状神经营养因子等)、小分子化合物(即化学诱导剂,如视黄酸、β-巯基乙醇和二甲基亚砜等)、基因转染、与神经细胞共培养以及神经营养因子联合化学诱导剂等[4-5,30]。MATHOT等[36]指出,神经营养因子联合化学诱导剂诱导间充质干细胞神经分化是目前获得许旺细胞样细胞最成熟的方法,经典诱导方案是依次暴露或转染化学诱导剂和生长因子,包括β-巯基乙醇(24 h)和视黄酸(72 h)、毛喉素、碱性成纤维细胞生长因子、血小板源性生长因子和神经调节蛋白家族成员(神经调节蛋白1 β1)、胶质生长因子2或Hereglin β1,其中β-巯基乙醇和视黄酸触发间充质干细胞向神经胶质细胞系的转分化,毛喉素、碱性成纤维细胞生长因子、血小板源性生长因子和神经调节蛋白家族成员进行诱导[4,30,36]。骨髓间充质干细胞可以通过转染notch的跨膜区和胞内区表达神经干细胞标记,或通过转染Noggin分化为神经球细胞[4]。细胞直接移植或经体外转分化后移植至周围神经损伤部位,通过调节固有细胞的行为以及表达神经营养因子、细胞外基质分子和细胞黏附分子等,从而加速轴突再生,实现更好的再髓鞘化和功能恢复[5,30-32]。
2.3.2 分泌神经营养因子、细胞外基质分子和细胞黏附分子 移植的许旺细胞或许旺细胞样细胞在周围神经损伤部位可合成和分泌多种神经营养因子(如神经生长因子、脑源性神经营养因子、神经营养因子3、血管内皮生长因子等)、细胞外基质分子(如纤维粘连蛋白、层粘连蛋白)和细胞黏附分子(如整合素、钙黏蛋白)等,这些分子为神经细胞存活和神经突生成提供了良好的微环境[4-5,26-27,30],并可作用于局部或更远的胶质细胞,刺激或支持固有许旺细胞的增殖、成熟和分化等[5,27,30]。
神经营养因子合成后逆行转运至神经体细胞中[5],传递近端和远端神经的信息或旁分泌信号,通过与其特异性受体结合(如神经生长因子与TrkA、脑源性神经营养因子与TrkB、神经营养因子3/4/5与TrkC等)激活或抑制某些信号通路(如PI3K/Akt信号通路、Ras-ERK信号通路、cAMP/PKA信号通路以及PLC-γ依赖性信号通路等),从而促进神经元存活、加速轴突和血管生长、刺激神经纤维再生、防止细胞凋亡、诱导许旺细胞迁移增殖、髓鞘形成以及减缓肌肉萎缩等,逆转周围神经损伤的负面影响(如阻止轴突损伤导致的细胞死亡)[4-5,41-42]。例如,脂肪间充质干细胞可上调脑源性神经营养因子、神经调节蛋白1、血管内皮生长因子、肝细胞生长因子和胰岛素样生长因子的蛋白表达,并可通过神经营养因子依赖性的方式抑制caspase-3活性来减轻背根神经节的丢失[4]。移植的许旺细胞或许旺细胞样细胞在周围神经损伤部位除了具有直接旁分泌作用外,还能诱导固有许旺细胞产生神经营养递质。在大鼠许旺细胞和间充质干细胞共培养研究中,许旺细胞的存活率和增殖率均有所提高,神经生长因子、脑源性神经营养因子和Trk/p75NTR受体的mRNA和蛋白水平均高表达,同时还发现间充质干细胞促进了大鼠外周神经修复模型中许旺细胞的生成,并促进了许旺细胞介导的神经营养功能[5]。此外,干细胞(如肌源性干细胞)可以通过分泌生长因子(如血管内皮生长因子)和分化为血管内皮细胞刺激体内新血管的生长[38],间接提高损伤部位神经营养素的产生。血管细胞产生脑源性神经营养因子和青蒿素(胶质细胞源性神经营养因子家族的一种神经营养物质),吸引不断生长的交感神经纤维,同时促进沿血管走行的神经纤维形成[30]。
细胞外基质分子、细胞黏附分子对神经再生和功能恢复同样重要。细胞外基质分子(如层粘连蛋白和Ⅳ型胶原蛋白等)可通过形成非神经元细胞迁移的底物和作为许旺细胞分泌神经营养因子的储存库等参与神经再生过程[43],例如层粘连蛋白可能与神经调节蛋白1协同作用,促进轴突的发芽和生长、负责许旺细胞在神经再生过程中的增殖和迁移以及Büngner带的形成。一些免疫球蛋白样细胞黏附分子对轴突引导也很重要,如整合素、神经细胞黏附分子和钙黏蛋白(如N-钙黏蛋白),其中神经细胞黏附分子可能优先促进感觉轴突的生长[33]。
2.3.3 促进髓鞘形成 髓鞘形成是周围神经损伤再生的另一个重要过程,其决定了神经再生的质量和功能的恢复[4-5,30]。
一般来说,通过促进内源性修复机制或提供髓鞘细胞的外源性来源,可以实现髓鞘再生和随后神经功能的恢复[30]。研究发现,许旺细胞和多种类型的成体干细胞(以许旺细胞样细胞的形式)均具有髓鞘化神经元细胞和再生神经的能力。在周围神经损伤发生后的再生过程中,当许旺细胞或许旺细胞样细胞进一步分化为髓鞘形成细胞时,细胞内cAMP水平升高,髓鞘蛋白如髓鞘碱性蛋白、髓鞘蛋白P0、外周髓鞘蛋白22以及其他在髓鞘结构和功能中发挥关键作用的含量较低的蛋白等大量合成并分泌,从而促进再生期间和再生后轴突的再髓鞘化[4,30]。如许旺细胞样分化的骨髓间充质干细胞可通过增强髓鞘因子mRNA的表达,显著增加髓鞘化轴突的数量,从而促进面神经功能的恢复[44]。牙龈间充质干细胞和诱导神经前体细胞可能通过调节拮抗性髓鞘调节因子c-Jun和Krox-20/EGR2介导许旺细胞的再髓鞘化,促进周围神经修复与再生[45]。另外,许旺细胞或许旺细胞样细胞分泌的某些神经营养因子对髓鞘形成也具有促进作用,例如周围神经损伤发生后,胰岛素样生长因子1、神经调节蛋白1Ⅰ型和Ⅲ型等表达增加,轴突排列以及髓鞘化基因的表达都得到增强,从而增加了髓鞘厚度和节间长度[5,33]。通过透射电子显微镜和免疫荧光染色发现,移植的肌源性干细胞可以分化为支持性细胞系(如许旺细胞)、释放神经营养因子并促进新生轴突成熟等方式参与再生神经中髓鞘的重建[38]。