Chinese Journal of Tissue Engineering Research ›› 2024, Vol. 28 ›› Issue (14): 2267-2273.doi: 10.12307/2024.325
Previous Articles Next Articles
Long non-coding RNA and periodontitis
Tong Tong1, Liu Chunyan2, Liu Bing3, Zhao Fei3
- 1School/Hospital of Stomatology, Hebei Medical University, Hebei Province Key Laboratory of Stomatology, Hebei Province Clinical Medical Research Center of Oral Diseases, Shijiazhuang 050017, Hebei Province, China; 2Department of Orthodontics, 3Department of Periodontics I, School of Stomatology, Hebei Medical University, Shijiazhuang 050017, Hebei Province, China
-
Received:2023-04-11Accepted:2023-05-22Online:2024-05-18Published:2023-07-28 -
Contact:Liu Bing, Master, Chief physician, Associate professor, Department of Periodontics I, School of Stomatology, Hebei Medical University, Shijiazhuang 050017, Hebei Province, China -
About author:Tong Tong, Master candidate, School/Hospital of Stomatology, Hebei Medical University, Hebei Province Key Laboratory of Stomatology, Hebei Province Clinical Medical Research Center of Oral Diseases, Shijiazhuang 050017, Hebei Province, China -
Supported by:2021 Government-funded Provincial Medical Excellent Talents Project, No. 361029 (to LCY); 2022 Hebei Provincial Medical Scientific Research Project, No. 20221454 (to ZF); 2019 Hebei Provincial Government-funded Clinical Medical Excellent Talents Training and Basic Topics Research Project, No. [361029(MXZB00271)] (to LB)
CLC Number:
Cite this article
Tong Tong, Liu Chunyan, Liu Bing, Zhao Fei. Long non-coding RNA and periodontitis[J]. Chinese Journal of Tissue Engineering Research, 2024, 28(14): 2267-2273.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks

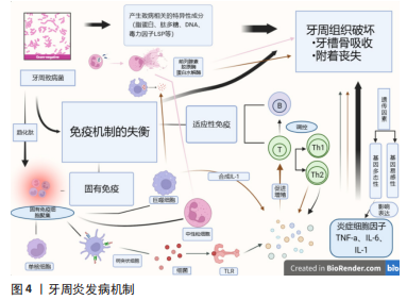
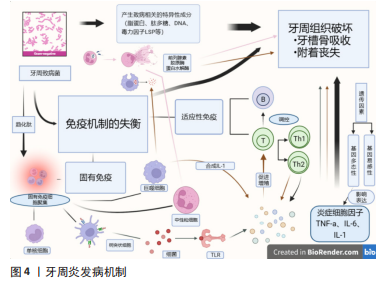
2.1 lncRNA与牙周炎 lncRNA最初被发现与牙周炎相关是通过发现侵袭性牙周炎与冠心病在遗传学及流行病学上存在着相关性,两者间有潜在的共同遗传学基础。后深入研究发现,在人9 p21.3中,与冠心病有关的2 个相邻连锁不平衡区域与侵袭性牙周炎也呈较高的关联度,并分别与lncRNA ANRIL的基因表达水平相一致[7]。自此lncRNA与牙周炎相关研究进一步发展,人们又通过探究侵袭性牙周炎与冠心病共同致病菌牙龈卟啉单胞菌后发现,lncRNA ANRIL可能参与牙周炎的发病机制[8]。在牙周炎炎症反应中脂肪酸与糖代谢相关基因脂连蛋白受体、小泡相关膜蛋白、跨膜蛋白258与lncRNA ANRIL的表达存在时间依赖性[9]。因多项研究显示lncRNA在牙周炎的基因表达和疾病发病机制中可能起关键作用,ZOU等[10]对牙周炎及正常组织中lncRNA进行微阵列分析,总共检测到8 925 个差异表达的lncRNA,其中包括上调的4 313 个和下调的4 612 个。lncRNA与牙周炎之间存在密不可分的关系,两者发现联系时间脉络见图3,探究两者关系为探究牙周炎的发病机制及lncRNA在牙周炎的应用方面有着很大价值。"

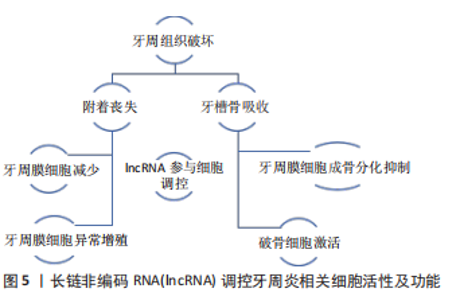
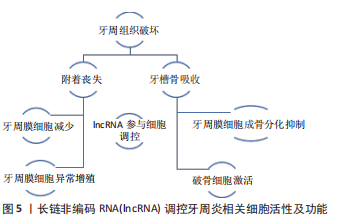
在急性炎症中破骨细胞被激活导致骨吸收,造成的牙槽骨丧失难以恢复,牙周微环境长期处在炎症环境中导致牙周膜细胞数量减少,牙周膜干细胞异常增殖,成骨分化能力受到抑制,使牙周组织很难再生[11]。lncRNA参与调控细胞生物活性的过程,在炎症过程中牙周膜干细胞及破骨细胞的生物活性及能力都受到影响,lncRNA参与着其中的调控机制。有研究发现同一种lncRNA对牙周膜干细胞及破骨细胞均发挥了调控作用。ZHANG等[12]发现通过敲除lncRNA DANCR可使 Jagged1蛋白减少从而导致力学诱导的牙周的破骨细胞形成和根吸收。WANG等[13]验证了lncRNA DANCR在牙周膜干细胞中上调可以抑制其成骨分化潜能,但调控机制并不明确,而此前在间充质干细胞中已被证实LncRNA DANCR可以通过调节叉盒转录因子1(forkhead box O1,FOXO1)的表达来抑制成骨分化[14],以此可推测其在牙周骨改建的调控机制。lncRNA在骨代谢疾病中表达异常发挥着作用,牙周炎作为骨代谢疾病的一种,lncRNA发挥着重要调控作用。见图5。"
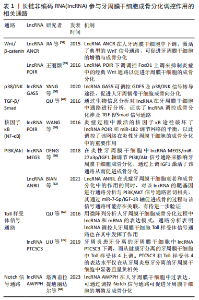
2.2.1 lncRNA与牙周炎中的免疫调控 LncRNA与免疫功能的调控密切相关,不仅在炎症被激活的过程中发挥重要作用,同时也是抑制炎症反应的重要参与者[15]。随着技术的进步及对lncRNA在免疫机制中研究的重视,近年来人们对于lncRNA在牙周炎中的调控机制有了更进一步的研究[12-40]。多种lncRNA在牙周炎免疫方面的调控机制被证明,ZHANG等[16]通过生物信息学分析系统地鉴定了牙周炎中与免疫相关的lncRNA,发现大多数相关lncRNA在免疫调节中表达扰动也与多种免疫通路途径相关联等等。人们通过体外实验证实了可通过调控lncRNA的表达水平来实现免疫的调控。 炎症免疫反应在牙周炎的发病机制中主要由免疫细胞介导,免疫细胞在牙周炎的发病机制目前并不明确。目前已有研究表明,对于B细胞及巨噬细胞,lncRNA在牙周炎中可调控其亚群的浸润、细胞活性和功能发挥。牙周炎疾病进展过程中,不同时期免疫细胞亚群浸润的比例会发生变化,人们通过生物信息学分析lncRNA在牙周炎中的表达及在牙周炎中浸润的免疫细胞亚群的比例,发现lncRNA FAM30A、lncRNA GUSBP11、lncRNA LINC00525的表达水平与牙周炎患者的浆细胞分数呈正相关,相关lncRNA上调时,浆细胞数量增加,T细胞数量会下调[17]。在基于牙周炎建立的免疫相关内源竞争性机制(ceRNA)网络中发现lncRNA MIAT与体液免疫中B细胞的活化、分化及激活可能有着密切联系[18]。牙周致病菌通过改变巨噬细胞不同表型使巨噬细胞在牙周炎进展过程中发挥着抗炎和促炎作用,lncRNA也参与了其中的调控且在调控巨噬细胞M2型中发挥了更大优势。在牙龈卟啉单胞菌刺激的巨噬细胞中lncRNA GAS5表达降低,抑制牙龈卟啉单胞菌产生的唾液酸酶可以减少lncRNA GAS5的抑制,在巨噬细胞中诱导更少的miR-21和更多的白细胞介素12来清除细菌[19]。 LncRNA参与调控牙周炎中相关炎性因子的表达从而参与炎性免疫过程。一方面,免疫应答反应在炎症刺激时快速诱导模式识别受体下游基因的表达[20],在牙周炎中其模式识别受体主要为Toll样受体(Toll-like receptor,TLRs)与NOD样受体(NOD like receptors,NLRs)。在慢性牙周炎中lncRNA MALAT1可以通过启动miR‐20a激活TLR4途径,增加脂多糖诱导的细胞因子的水平,作为miR‐20a的海绵,增加了TLR4水平和炎症因子的分泌参与炎症反应[21]。lncRNA PTCSC3的过表达可以通过抑制牙周膜干细胞(periodontal mesenchymal stem cells,PDLSCs)的增殖并下调TLR4的表达来改善牙周炎起到抗炎作用[22]。根据生物信息学分析与NLRP3介导的凋亡相关的lncRNA_1810058I24Rik, lncRNA_Gm12474和lncRNA_Gm41514在糖尿病相关的牙周炎中可进行调控[23]。另一方面,信号通路的激活在炎症中发挥重要作用,是lncRNA参与炎性免疫反应的桥梁,尤其是核因子κB途径。多项研究表明,lncRNA ANRIL、lncRNA POIR、lncRNA GAS5于牙周炎中在该通路的调控都有一定研究进展[24-26]。CHEN等[27]通过实验验证了在炎性牙周膜细胞中LncRNA FGD5-AS1下调,其上调可以通过使miR-142-3p下调,socs6上调,抑制核因子kB信号通路起到抗炎作用。 2.2.2 lncRNA与牙周炎相关的牙周膜细胞 牙周膜细胞包括了多种细胞,其中结缔组织细胞包括了成纤维细胞(也称为牙周韧带细胞,periodontal ligament cell,PDLC)、成骨细胞、破骨细胞以及牙周膜干细胞。炎性环境的存在会造成牙周膜细胞的凋亡、增殖及分化等方面均受到影响,破坏其正常功能,甚至脱离微环境后仍很难恢复[28]。lncRNA对于牙周膜细胞的细胞生物活性发挥着调控作用,现有研究来看,lncRNA对炎性环境的牙周膜细胞主要参与了促炎的调控。 牙周炎的炎症反应会促进牙周膜细胞的凋亡使其数量减少,同时又激发了牙周膜细胞的增殖能力使其异常增殖。多项研究证明了lncRNA参与了牙周炎中牙周膜细胞的凋亡促进。LncRNA NEAT1在牙周炎中表达上调,NEAT1负调节miR-200c-3p靶向TRAF6降低牙周膜细胞活力及炎症因子的分泌,促进细胞凋亡[29]。lncRNA MEG3在牙周炎中下调,通过miR-143-3p/AKT/IKK通路调控抑制牙周膜细胞的生存、促进凋亡和炎症反应[15-16]。lncRNA也参与调控牙周炎中的牙周膜细胞的增殖促进。CHEN等[32]发现LncRNA MALAT1在牙周炎中显著上调,其与FGF2呈正相关,促进牙周膜干细胞的增殖。LncRNA LOXL1-AS在牙周炎中下调也促进牙周炎影响的PDLSCs的增殖,并上调白细胞介素1β加重牙周炎[33]。LncRNA DCST1-AS1在牙周炎中表达被抑制,干扰了miR-21的表达,并降低了PLAP-1的表达,促牙周炎的牙周韧带细胞增殖[34]。 lncRNA在成骨分化过程中存在多种调控机制[35],炎性环境下参与牙周膜干细胞成骨分化抑制,尤其在基因转录前过程中进行修饰调控基因表达的过程中被体现,表现在lncRNA与Zeste 同 系 物 2 的 增 强 剂 (enhancer of zeste homolog 2,EZH2) 的协同作用,EZH2与牙周膜干细胞成骨分化的潜在机制仍有待探索。DENG等[36]发现lncRNA MEG3及EZH2的减少对成骨分化有负调节作用,后证实了此作用是EZH2是通过对 Wnt启动子区H3K27me3的影响,激活 Wnt/beta-catenin信号途径而完成的调节过程。LI等[37]最近发现,LncRNA SNHG1可以与EZH2的组蛋白甲基转移酶增强子结合,通过调控 Kruppel样因子2 (KLF2)启动子区的组蛋白甲酯化,从而抑制牙周膜干细胞成骨分化。目前来看,EZH2在癌症中的作用被认为是一个新的治疗靶点已被验证[38],与lncRNA相关的抑制剂也有望为牙周炎治疗进展实现突破。 牙周炎骨吸收过程以破骨细胞活性活跃和牙槽骨吸收显著为特征,已有研究证实lncRNA在这一过程中起调控作用[39],关于lncRNA对牙周炎中的破骨细胞相关研究较为有限。李俊辉等[40]发现LncRNA Nron在破骨细胞过表达时可抑制牙周炎疾病中牙槽骨的吸收来缓解牙周炎的进展。赵祥宇等[41]发现,LINC00511在牙周炎标本中呈高表达,它既能促进破骨细胞,又能抑制成骨细胞,因此,作者提出LINC00511可能是通过调节这两种细胞的数量,从而引起牙槽骨骨吸收的假说。根据最新研究,人们发现LncRNA MALAT1可通过ceRNA机制与miR-124竞争性结合调节NFATc1的表达,从而促进破骨细胞生成[42]。lncRNA在破骨细胞分化中调控机制的研究,为牙周炎的发病机制提供新的线索。 2.3 lncRNA在牙周炎的应用 2.3.1 lncRNA在牙周炎中的诊断及预后的应用 牙周炎初期症状不明显,不容易引起人们的重视,进展到晚期后,牙槽骨往往丧失过多造成牙松动甚至牙缺失等难以挽回的局面,故对于牙周炎的早期诊断是很有必要的。已有大量研究证实在癌症中lncRNA作为前瞻性生物标志物有一定诊断价值。但可能因lncRNA的调控机制存在组织特异性,lncRNA在牙周炎的外周血中虽有一定水平变化,但其变化与lncRNA在牙龈组织的水平变化并没有关联。GHOLAMI等[43]发现lncRNA ANRIL在患者外周血中的表达明显低于对照组,但其在血液中的水平与牙龈组织的水平并没有统计学意义,同时其在血液中及牙龈组织中表达水平均与年龄无关,不受年龄影响。若未来可证实lncRNA作为牙周炎的生物标志物的作用,对牙周炎的早期诊断将有很大价值。同时对于牙周炎的分型上也可能存在着一定作用,研究发现lncRNA-TNFRSF13C在牙周炎患者B淋巴细胞中显著高表达,其水平升高抑制了炎症刺激下的B细胞增殖,加剧了凋亡,并发现其在侵袭性牙周炎与慢性牙周炎中B细胞表达量情况不同[44],这可能将为其应用于牙周炎分型提供了一定依据。 牙周炎治疗后的复发一直是一个挑战性的问题,除了跟患者自身维护等问题外,人们发现lncRNA也在其中可能发挥作用。LncRNA MORT水平会影响牙周炎复发率,其上调会降低牙周炎复发率[45],LncRNA AWPPH的表达量可以通过血清预测牙周炎的复发[46]。由此看来,lncRNA是否有望成为牙周炎预后的标志来预测牙周炎复发情况值得进一步研究。 2.3.2 lncRNA在牙周炎的治疗中的应用 lncRNA与牙周炎之间关系的研究最终目的指向为牙周炎的治疗,对于牙周炎的治疗目前研究方向主要为控制炎症及牙周再生两方面。因此,从lncRNA在牙周炎症中所起免疫调控及牙周膜干细胞再生的调控进行论述,为lncRNA在牙周炎的治疗研究提供相关指向性思路。 (1) lncRNA与牙周炎的免疫治疗:牙周炎的炎症免疫机制目前并不明确,人们通过生物信息学分析筛选了多种lncRNA在牙周炎中呈现差异表达,并进行了 ceRNA的网络构建,部分已经有实验进行了验证,还有部分lncRNA仍需进一步探究,例如LNC-Coro2B-1、LNCMBL2-7、LNC-TRIM45-1、LNC-CHST10-2、LNC-TNP1-6、LINC00687、LBX2‐AS1、LINC01566等[45-48]。经前文论述,如今研究证实了多种lncRNA都参与了牙周炎炎症反应,且多起到了抗炎的作用。不仅是体外实验,在动物实验中也有研究证实其作用,例如:lncRNA SNHG5直接与核因子κBp65亚基结合抑制其易位来抑制核因子κB信号通路的激活,来调控炎症因子,抑制炎症[49];已证实在小鼠牙周炎模型中局部注射si-SNHG5可加重牙周破坏[50]。该研究为牙周炎治疗提供了潜在的治疗靶点并在动物实验中验证了局部注射lncRNA的作用,为临床应用提供了一定的依据,证明了可以通过调控lncRNA的表达水平来逆转lncRNA在牙周炎的作用起到抗炎作用,为将其作为牙周炎的治疗靶点提供了一定的科学依据。 (2) lncRNA与牙周再生:随着间充质干细胞在再生医学中研究逐步发展,人们开始着重将牙周膜干细胞应用于牙周治疗的研究。人们致力于通过体外牙周膜干细胞来实现恢复牙周炎带来的破坏,使严重牙周炎的治疗不只达到维持控制的程度。2004年SEO等[51]证实了牙周膜细胞中存在间充质干细胞并能实现体外增殖,可在免疫受损的大鼠的牙周中起修复作用。2008年LIU等[52]通过进行以小型猪为研究对象的动物实验,证明了移植自体牙周膜干细胞有助于小型猪实验性牙周炎的牙周组织修复,尤其可以生成骨/牙本质样矿化组织。牙周膜干细胞的细胞生物活性受到多方面影响,参与了其中调控的lncRNA进一步对其探究有望成为牙周炎的治疗靶点。 在炎症反应中对于牙周膜细胞异常增殖、细胞凋亡及成骨抑制和破骨激活方面前文已有论述,对于牙周膜干细胞异常增殖的调控,lncRNA有望成为牙周膜干细胞增殖的激活剂,可致力于改善炎症环境下牙周膜干细胞的存在数量。起促炎和起凋亡调控的lncRNA、使成骨抑制的lncRNA及破骨细胞激活的lncRNA,探究其作为lncRNA抑制剂来调控炎症发展,对减轻炎症反应控制组织破坏将有很大价值。 对于炎症已经控制的骨组织的恢复,lncRNA在牙周膜干细胞的研究进展为其提供了大量实验数据,并且发现不同lncRNA发挥作用存在着差异性。同一种lncRNA在健康及炎性牙周膜干细胞中均有正向调节成骨分化作用。XU等[53]发现了LncRNA TWIST1通过抑制TWIST1的表达来促进健康及炎性牙周膜干细胞的成骨分化。根据现有研究来看,lncRNA对牙周膜干细胞的调控机制主要还是通过内源性竞争机制的调控,贾搏[54]已经证实,lncRNA PCAT1能够通过这种机制,逆转miR-106a-5p对SMAD4和骨形态发生蛋白2的抑制,从而提高了牙周膜干细胞的成骨分化能力[55]。TU等[56]发现lncRNA CYTOR通过与miR-6512-3p竞争性结合,正向调节SOX11的表达,从而促进牙周膜干细胞的成骨分化。目前该机制的研究较多,还需通过生物信息学分析指导进一步构建调控网络来明确lncRNA在其中的机制并加以验证。 结合目前已有研究,lncRNA主要通过Wnt/β-catenin、MAPK、TGF-β/Smad、核因子kB、Notch、BMP-4及PI3K/AKT信号通路来调控成骨分化[57],牙周膜干细胞中lncRNA参与成骨分化调控作用的相关通路,见表1。"
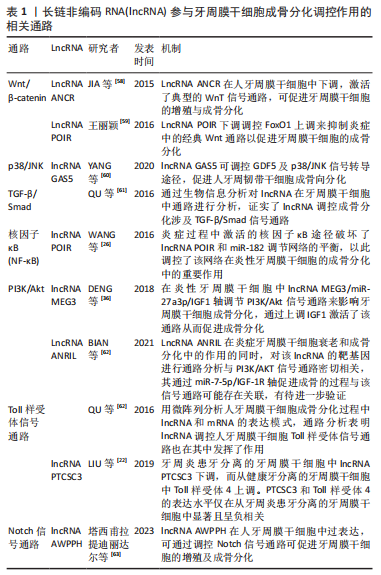

2.4 lncRNA参与牙周炎相关因素的调控 铁死亡是以铁依赖性致死性脂质过氧化为特征调控细胞死亡的因素之一,近年在炎症中发现其相关性,存在于牙周炎的病程发展中,牙周韧带细胞的铁死亡导致牙周炎的发展[64-65]。近期lncRNA在其中发挥的作用被实验证实,LINC00616作为竞争性内源性RNA,通过miR-370/TFRC轴促进牙周膜干细胞的铁死亡[66],通过生物信息学分析,在牙周炎铁死亡中的ceRNA网络被建立[67],lncRNA多个靶点被预测,相关研究较少且需进一步验证,该方面研究为lncRNA在牙周炎治疗提供了新思路。 自噬参与炎症和宿主免疫,自噬与牙周炎之间的相互作用已逐渐引起关注。自噬保护牙周膜干细胞免于凋亡,并促进炎症微环境中的血管生成,有助于消除牙周病原体感染,并调节牙周炎中的免疫炎症反应。有研究证实了牙周炎中牙周炎症激活自噬通量,lncRNA H19可以通过AKT途径介导自噬的激活[68],该研究的发现对lncRNA在牙周炎分子调控作用有了新的扩展,为牙周治疗靶点提供了新的思路方向。 在细胞代谢中,lncRNA可能也参与其中。lncRNA GACAT2通过与线粒体功能相关的丙酮酸激酶M1/2(PKM1/2)蛋白结合,在炎症环境下调节线粒体功能,为lncRNA在其中的调控方面提供了新的见解[69]。 牙周组织可在机械应力作用下发生变化,使牙槽骨的压力侧骨吸收、张力侧骨形成。正畸治疗便是应用该特性的常见手段,在健康牙周组织中正畸治疗机械应力的施加造成牙周组织重塑,lncRNA在该过程中发挥着作用,通过生物信息学分析lncRNA在其中的调控图谱被建立[70],之后经实验验证了lncRNA FER1L4通过AKT/FOXO3调节了牙周膜干细胞在压力应变下介导的自噬[71]。在持续压缩力作用下,牙周膜干细胞中lncRNA HHIP-AS1表达下调促进了成骨分化潜能,并抑制了牙周膜干细胞的迁移和趋化能力[72]。lncRNA SNHG8的下调导致了EZH2的表达降低,在表观遗传水平促进了机械力作用下牙周膜干细胞的成骨分化[73]。这些研究为调控在正畸治疗期间牙周组织的重塑提供了靶点,有望推进正畸加速牙齿移动的研究。 牙周炎患者因常出现牙移位影响美观,对正畸有一定诉求。已有研究证实了健康的牙周膜干细胞与处于炎症环境的牙周膜干细胞对于力学刺激会有不同的反应,尤其以12%静态牵张力为分界,可促进健康牙周膜干细胞成骨分化,抑制炎性牙周膜干细胞的成骨分化,lncRNA被发现在这一过程中也同样起着调控作用[74]。已有实验证实lncRNA NR034015、linc-01135及LINC00638三者的上调均可在这一力学刺激作用下实现促进炎性牙周膜干细胞的成骨分化[75-78]。同时通过生物信息学分析,人们发现多种lncRNA在炎性牙周膜干细胞受力学刺激中呈差异表达,为该方面进一步研究提供了更多的靶点[79],该领域研究的进展推进了通过调控lncRNA来改善牙周炎患者进行正畸治疗的研究。 牙周炎属于低氧性疾病的一种,炎症反应导致组织代谢加快,氧气需求量增加逐渐形成了组织低氧的环境,牙周炎造成的低氧环境对于牙周炎的发病进程起着重要作用[80]。lncRNA与低氧之间存在着密切联系,近年来lncRNA在牙周炎低氧方面的研究被推进。lncRNA多通过影响低氧诱导因子1α的表达来在牙周炎发挥作用。HIF1A-AS1、HIF1A-AS2及LncRNA 01126均被证明在缺氧时调控低氧诱导因子1α进而调控牙周膜干细胞的成骨分化[81-82]。在正畸牙移动时会发生缺氧和无菌性炎症等反应,LncRNA SNHG8在牙周膜细胞中表达显著降低,释放低氧诱导因子1α,激活下游核因子κB通路,在缺氧中发挥抗炎作用[83]。据现有研究lncRNA在低氧时可对牙周炎症及成骨分化方面都起着正向作用,但目前研究还较少,其进一步研究有望对牙周炎的治疗起到进一步推进作用。 氧化应激的作用也不容忽视,其会造成并加重.牙周组织的损伤,现有研究也证实了lncRNA也参与了其中的调控。LncRNA JHDM1D-AS1会在牙周膜干细胞受到氧化应激时下调从而抗细胞凋亡[84]。LncZFY-AS1在牙周炎中表达上调进一步加重了牙周炎炎症及细胞凋亡,而在牙周膜细胞中下调可增加细胞活力,抑制了炎症,减少了氧化应激减少细胞凋亡[85]。不同lncRNA在受到氧化应激的牙周膜细胞所产生的炎症反应及细胞活性起着作用。"

| [1] BRANNAN CI, DEES EC, INGRAM RS, et al. The product of the H19 gene may function as an RNA. Mol Cell Biol. 1990;10(1):28-36. [2] The FANTOM Consortium And The RIKEN Genome Exploration Research Group Phase I & II Team*. Analysis of the mouse transcriptome based on functional annotation of 60,770 full-length cDNAs. Nature. 2002;420(6915):563-573. [3] 黄蕾,王雅洁,陈实.非编码RNA编辑技术研究进展[J].中国细胞生物学学报,2015,37(7):1036-1045. [4] 李法君.长链非编码RNA及其生物学功能概述[J].生物学教学,2017,42(2):2-4. [5] 李朋飞.电离辐射应答长链非编码RNA的研究[D].兰州:中国科学院研究生院(近代物理研究所),2015. [6] 夏芳芳,胡明智,孙慧莹,等.LncRNA在自身免疫性疾病中的研究进展[J].中国免疫学杂志,2019,35(15):1907-1912. [7] SCHAEFER AS, RICHTER GM, GROESSNER-SCHREIBER B, et al. Identification of a shared genetic susceptibility locus for coronary heart disease and periodontitis. PLoS Genet. 2009;5(2):e1000378. [8] 屈茜,房付春,吴补领.长链非编码RNA在牙周炎和口腔肿瘤疾病中的作用[J].国际口腔医学杂志,2016,43(1):62-65. [9] BOCHENEK G, HÄSLER R, EL MOKHTARI NE, et al. The large non-coding RNA ANRIL, which is associated with atherosclerosis, periodontitis and several forms of cancer, regulates ADIPOR1, VAMP3 and C11ORF10. Hum Mol Genet. 2013;22(22):4516-4527. [10] ZOU Y, LI C, SHU F, et al. LncRNA expression signatures in periodontitis revealed by microarray: the potential role of lncRNA in periodontitis pathogenesis. J Cell Biochem. 2015;116(4):640-647. [11] 范琳媛,李红凌.长链非编码RNAs调控骨稳态研究进展[J].基础医学与临床,2020,40(1):115-119. [12] ZHANG X, ZHAO Y, ZHAO Z, et al. Knockdown of DANCR reduces osteoclastogenesis and root resorption induced by compression force via jagged1. Cell Cycle. 2019;18(15):1759-1769. [13] WANG Z, HUANG Y, TAN L. Downregulation of lncRNA DANCR promotes osteogenic differentiation of periodontal ligament stem cells. BMC Dev Biol. 2020;20(1):2. [14] TANG Z, GONG Z, SUN X. LncRNA DANCR involved osteolysis after total hip arthroplasty by regulating foxo1 expression to inhibit osteoblast differentiation. J Biomed Sci. 2018;25(1):4. [15] 郭东光,陈明艳,王丰,等.长链非编码RNA对免疫功能的调控作用研究进展[J].动物医学进展,2021,42(7):90-95. [16] ZHANG X, REN L, YAN X, et al. Identification of immune-related lncRNAs in periodontitis reveals regulation network of gene-lncRNA-pathway-immunocyte. Int Immunopharmacol. 2020;84:106600. [17] WU D, ZHOU P, CAO F, et al. Expression Profiling and Cell Type Classification Analysis in Periodontitis Reveal Dysregulation of Multiple lncRNAs in Plasma Cells. Front. Genet. 2020;11:382. [18] TANG H, YUAN S, CHEN T, et al. Development of an immune-related lncRNA-miRNA-mRNA network based on competing endogenous RNA in periodontitis. J Clin Periodontol. 2021;48(11):1470-1479. [19] YANG X, PAN Y, XU X, et al. Sialidase deficiency in porphyromonas gingivalis increases IL-12 secretion in stimulated macrophages through regulation of CR3, lncRNA GAS5 and miR-21. Front Cell Infect Mi. 2018;8:100. [20] 胡安妮,苏俭生.LncRNA参与固有免疫及其在牙周炎症反应中的研究进展[J].口腔颌面外科杂志,2021,31(1):52-55. [21] LI J, WANG M, SONG L, et al. LncRNA MALAT 1 regulates inflammatory cytokine production in lipopolysaccharide‐stimulated human gingival fibroblasts through sponging miR‐20a and activating TLR 4 pathway. J Periodont Res. 2020;55(2):182-190. [22] LIU W, ZHENG Y, CHEN B, et al. LncRNA papillary thyroid carcinoma susceptibility candidate 3 (PTCSC3) regulates the proliferation of human periodontal ligament stem cells and toll-like receptor 4 (TLR4) expression to improve periodontitis. BMC Oral Health. 2019;19(1):108. [23] ZHOU X, WANG Q, NIE L, et al.Metformin ameliorates the NLPP3 inflammasome mediated pyroptosis by inhibiting the expression of NEK7 in diabetic periodontitis. Arch Oral Biol. 2020;116:104763. [24] AARABI G, ZELLER T, HEYDECKE G, et al. Roles of the Chr.9p21.3 ANRIL Locus in Regulating Inflammation and Implications for Anti-Inflammatory Drug Target Identification. Front Cardiovasc Med. 2018;5:8. [25] YANG Q, LIU P, HAN Y, et al. Long noncoding RNA GAS5 alleviates the inflammatory response of human periodontal ligament stem cells by regulating the NF-κB signalling pathway. Eur J Orthodont. 2022;44(6):669-678. [26] WANG L, WU F, SONG Y, et al. Long noncoding RNA related to periodontitis interacts with miR-182 to upregulate osteogenic differentiation in periodontal mesenchymal stem cells of periodontitis patients. Cell Death Dis. 2016;7(8): e2327. [27] CHEN H, LAN Z, LI Q, et al. Abnormal expression of long noncoding RNA FGD5-AS1 affects the development of periodontitis through regulating miR-142-3p/SOCS6/NF-κB pathway. Artif Cell Nanomed B. 2019;47(1):2098-2106. [28] LIU N, SHI S, DENG M, et al. High levels of β-catenin signaling reduce osteogenic differentiation of stem cells in inflammatory microenvironments through inhibition of the noncanonical Wnt pathway. J Bone Miner Res. 2011;26(9): 2082-2095. [29] ZHANG L, LV H, CUI Y, et al. The role of long non-coding RNA (lncRNA) nuclear paraspeckle assembly transcript 1 (NEAT1) in chronic periodontitis progression. Bioengineered. 2022;13(2):2336-2345. [30] LIU Y, ZENG X, MIAO J, et al. Upregulation of long noncoding RNA MEG3 inhibits the osteogenic differentiation of periodontal ligament cells. J Cell Physiol. 2019; 234(4):4617-4626. [31] DONG Y, FENG S, DONG F. Maternally-Expressed Gene 3 (MEG3)/miR-143-3p Regulates Injury to Periodontal Ligament Cells by Mediating the AKT/Inhibitory κB Kinase (IKK) Pathway. Med Sci Monit. 2020;26:e922486. [32] CHEN P, HUANG Y, WANG Y, et al. MALAT1 overexpression promotes the proliferation of human periodontal ligament stem cells by upregulating fibroblast growth factor 2. Exp Ther Med. 2019;18(3):1627-1632. [33] RUAN D, WU C, ZHANG Y, et al. LncRNA LOXL1-AS1 inhibits proliferation of PDLSCs and downregulates IL-1β in periodontitis patients. J Periodontal Res. 2022;57(2):324-331. [34] WANG X, WANG Y. LncRNA DCST1-AS1 inhibits PDLCs’ proliferation in periodontitis and may bind with miR-21 precursor to upregulate PLAP-1. J Periodontal Res. 2021;56(2):256-264. [35] 胡琮佼,孙瑶.长链非编码RNA在干细胞成骨分化中作用机制的研究进展[J].口腔生物医学,2021,12(3):205-210. [36] DENG L, HONG H, ZHANG X, et al. Down-regulated lncRNA MEG3 promotes osteogenic differentiation of human dental follicle stem cells by epigenetically regulating Wnt pathway. Biochem Biophys Res Commun. 2018;503(3):2061-2067. [37] LI Z, GUO X, WU S. Epigenetic silencing of KLF2 by long non-coding RNA SNHG1 inhibits periodontal ligament stem cell osteogenesis differentiation. Stem Cell Res Ther. 2020;11(1):435. [38] DUAN R, DU W, GUO W. EZH2: a novel target for cancer treatment. J Hematol Oncol. 2020;13(1):104. [39] 冯志国,孙海飚,韩晓强.长链非编码RNA对骨相关细胞增殖、分化、凋亡的调控[J].中国组织工程研究,2022,26(1):112-118. [40] 李俊辉,蔡明详,孙瑶.长链非编码RNA Nron在牙周炎疾病中骨吸收的作用研究[C]//2019第九次全国口腔生物医学学术年会论文汇编. 中华口腔医学会口腔生物医学专业委员会,2019:24. [41] 赵祥宇,张桂荣,郭传波,等.在牙周炎样本中长链非编码RNA linc00511表达增高并促进破骨细胞增殖[J].中国组织工程研究,2019,23(33):5360-5365. [42] ZHANG C, PAN L, ZHANG H, et al.Osteoblasts-Derived Exosomal lncRNA-MALAT1 Promotes Osteoclastogenesis by Targeting the miR-124/NFATc1 Signaling Axis in Bone Marrow-Derived Macrophages. Int J Nanomedicine. 2023;18:781-795. [43] GHOLAMI L, GHAFOURI-FARD S, MIRZAJANI S, et al. The lncRNA ANRIL is down-regulated in peripheral blood of patients with periodontitis. Noncoding RNA Res. 2020;5(2):60-66. [44] 赖文.LncRNA-tnfrsf13c对b细胞功能的调节作用和机制初探[D]. 天津:天津医科大学,2020. [45] WANG Y, SUN Y, ZHENG P, et al. Long non-coding RNAs mortal obligate RNA transcript regulates the proliferation of human periodontal ligament stem cells and affects the recurrence of periodontitis. Arch Oral Biol. 2019;105:1-4. [46] WANG X, MA F, JIA P. LncRNA AWPPH overexpression predicts the recurrence of periodontitis. Biosci Rep. 2019;39(7):BSR20190636. [47] JIN SH, ZHOU RH, GUAN XY, et al. Identification of novel key lncRNAs involved in periodontitis by weighted gene co-expression network analysis. J Periodontal Res. 2020;55(1):96-106. [48] ZHOU H, CHEN D, XIE G, et al. LncRNA-mediated ceRNA network was identified as a crucial determinant of differential effects in periodontitis and periimplantitis by high-throughput sequencing. Clin Implant Dent Relat Res. 2020;22(3):424-450. [49] 李艳平,徐明.NLRP3炎性小体激活机制及小分子抑制剂研究进展[J].广东化工,2020,47(19):83-86. [50] HAN Y, HUANG Y, YANG Q, et al. Long non-coding RNA SNHG5 mediates periodontal inflammation through the NF-κB signalling pathway. J Clin Periodontol. 2022;49(10):1038-1051. [51] SEO BM, MIURA M, GRONTHOS S, et al. Investigation of multipotent postnatal stem cells from human periodontal ligament. The Lancet. 2004;364(9429):149-155. [52] LIU Y, ZHENG Y, DING G, et al. Periodontal ligament stem cell-mediated treatment for periodontitis in miniature swine. Stem Cells. 2008;26(4):1065-1073. [53] XU Y, QIN W, GUO D, et al. LncRNA-TWIST1 promoted osteogenic differentiation both in PPDLSCs and in hPDLSCs by inhibitingTWIST1 expression.Biomed Res Int. 2019;2019:8735952. [54] 贾搏.LncRNA-PCAT1对人牙周膜干细胞成骨分化调控机制的研究[D].广州:南方医科大学,2018. [55] 付秋月,兰兴明,徐溶蔚,等.不同信号通路对牙周膜干细胞成骨分化的影响[J].中国组织工程研究,2023,27(24):3910-3919. [56] TU S, CHEN Y, FENG Y, et al. lncRNA CYTOR Facilitates Osteogenic Differentiation of Human Periodontal Ligament Stem Cells by Modulating SOX11 via Sponging miR-6512-3p. Stem Cells Int. 2023;2023:5671809. [57] 施翔文,倪昊楠,李明军,等.长链非编码RNA在成骨分化相关信号通路中的调控作用[J].中国修复重建外科杂志,2022,36(4):479-486. [58] JIA Q, JIANG W, NI L.Down-regulated non-coding RNA (lncRNA-ANCR) promotes osteogenic differentiation of periodontal ligament stem cells. Arch Oral Biol. 2015;60(2):234-241. [59] 王丽颖.LncRNA对炎症条件下人牙周膜干细胞成骨分化调控作用的研究[D].西安:第四军医大学,2016. [60] YANG Q, HAN Y, LIU P, et al. Long noncoding RNA GAS5 alleviates the inflammatory response of human periodontal ligament stem cells by regulating the NF-κB signalling pathway. Eur J Orthodont. 2020;11:701. [61] QU Q, FANG F, WU B, et al. Potential role of long non-coding RNA in osteogenic differentiation of human periodontal ligament stem cells. J Periodontol. 2016; 87(7):e127-137. [62] BIAN M, YU Y, LI Y, et al. Upregulating the Expression of LncRNA ANRIL Promotes Osteogenesis via the miR-7-5p/IGF-1R Axis in the Inflamed Periodontal Ligament Stem Cells. Front Cell Dev Biol. 2021;9:604400. [63] 塔西甫拉提迪丽达尔,牛雅琪,阿布都克依木热依沙,等.长链非编码RNA AWPPH通过调控notch信号通路对人牙周膜细胞增殖和成骨向分化的影响[J].上海口腔医学,2023,32(1):23-27. [64] ZHAO Y, LI J, GUO W, et al. Periodontitis-level butyrate-induced ferroptosis in periodontal ligament fibroblasts by activation of ferritinophagy. Cell Death Discov. 2020;6(1):119. [65] MAO H, ZHAO Y, LI H, et al. Ferroptosis as an emerging target in inflammatory diseases. Prog Biophys Mol Biol. 2020;155:20-28 [66] WANG H, QIAO X, ZHANG C, et al. Long non-coding RNA LINC00616 promotes ferroptosis of periodontal ligament stem cells via the microRNA-370 / transferrin receptor axis.Bioengineered. 2022;13(5):13070-13081. [67] ZHANG C, XUE P, KE J, et al. Development of Ferroptosis-Associated ceRNA Network in Periodontitis. Int Dent J. 2023;73(2):186-194. [68] GUO R, HUANG Y, LIU H, et al.Long Non-Coding RNA H19 Participates in Periodontal Inflammation via Activation of Autophagy. J Inflamm Res. 2020;13: 635-646. [69] Li X, Tian BM, Deng DK, et al.LncRNA GACAT2 binds with protein PKM1/2 to regulate cell mitochondrial function and cementogenesis in an inflammatory environment. Bone Res. 2022;10(1):29. [70] Huang Y, Zhang Y, Li X, et al. The long non-coding RNA landscape of periodontal ligament stem cells subjected to compressive force. Eur J Orthod. 2019;41(4): 333-342. [71] Huang Y, Liu H, Guo R, et al. Long Non-coding RNA FER1L4 Mediates the Autophagy of Periodontal Ligament Stem Cells Under Orthodontic Compressive Force via AKT/FOXO3 Pathway. Front Cell Dev Biol. 2021;9:631181. [72] Qin Q, Yang H, Zhang C, et al.lncRNA HHIP-AS1 Promotes the Osteogenic Differentiation Potential and Inhibits the Migration Ability of Periodontal Ligament Stem Cells. Stem Cells Int. 2021;2021:5595580. [73] Zhang Z, He Q, Yang S, et al. Mechanical force-sensitive lncRNA SNHG8 inhibits osteogenic differentiation by regulating EZH2 in hPDLSCs. Cell Signal. 2022;93: 110285. [74] 刘佳.静态牵张力作用下健康和牙周病微环境来源PDLSCs生物学功能及LncRNA表达谱的研究[D].西安:第四军医大学,2016. [75] 孙唯夫,刘传宏,张校晨,等.静态牵张力通过下调linc01135/miR-106a-5p抑制PPDLSCs 成骨分化[J].临床口腔医学杂志,2022,38(4):195-199. [76] 邹宛桦,秦文,徐悦蓉,等.长链非编码RNA linc-01135对静态牵张力作用下人炎症牙周膜干细胞成骨分化的影响[J].实用口腔医学杂志,2018,34(2): 193-197. [77] 秦文.长链非编码RNA linc00638在牵张力作用下影响炎症来源牙周膜干细胞成骨分化作用的研究[D].西安:中国人民解放军空军军医大学,2019. [78] 邹宛桦,秦文,徐悦蓉,等.LncRNA nr_034015对静态牵张力作用下人炎症牙周膜干细胞成骨分化的影响[G]//2017年国际正畸大会暨第十六次全国口腔正畸学术会议论文汇编.中华口腔医学会口腔正畸专业委员会、中国国际科技交流中心,2017: 351-352. [79] LIU J, ZHAO Y, NIU Q, et al. Long Noncoding RNA Expression Profiles of Periodontal Ligament Stem Cells from the Periodontitis Microenvironment in Response to Static Mechanical Strain.Stem Cells Int. 2021;2021:6655526. [80] 温静瑜,和红兵,任晓斌,等.抗氧化剂在牙周炎治疗中的应用研究[J].口腔医学研究,2018,34(1):97-99. [81] CHEN D, WU L, LIU L, et al. Comparison of HIF1A‑AS1 and HIF1A‑AS2 in regulating HIF‑1α and the osteogenic differentiation of PDLCs under hypoxia. Int J Mol Med,. 2017;40(5):1529-1536. [82] ZHOU M, HU H, HAN Y, et al. Long non‐coding RNA 01126 promotes periodontitis pathogenesis of human periodontal ligament cells via miR‐518a‐5p/HIF‐1α/MAPK pathway. Cell Prolif. 2021;54(1):e12957. [83] WANG C, YANG Q, HAN Y, et al. A reduced level of the long non-coding RNA SNHG8 activates the NF-kappaB pathway by releasing functional HIF-1alpha in a hypoxic inflammatory microenvironment. Stem Cell Res Ther. 2022;13(1):229. [84] SHI B, SHAO B, YANG C, et al. Upregulation of JHDM1D-AS1 protects PDLSCs from H2O2-induced apoptosis by decreasing DNAJC10 via phosphorylation of eIF2α. Biochimie. 2019;165:48-56. [85] CHENG L, FAN Y, CHENG J, et al. Long non-coding RNA ZFY-AS1 represses periodontitis tissue inflammation and oxidative damage via modulating microRNA-129-5p/DEAD-Box helicase 3 X-linked axis. Bioengineered. 2022;13(5): 12691-12705. [86] SAYAD A, GHAFOURI-FARD S, SHAMS B, et al. Sex-specific up-regulation of p50-associated COX-2 extragenic RNA (PACER) lncRNA in periodontitis.Heliyon. 2020; 6(5):e03897. [87] LIU X, ZHOU Y. Downregulation of lncRNA ANRIL Inhibits Osteogenic Differentiation of Periodontal Ligament Cells via Sponging miR-7 through NF-κB Pathway. Anal Cell Pathol (Amst). 2021;2021:7890674. |
| [1] | Yu Weijie, Liu Aifeng, Chen Jixin, Guo Tianci, Jia Yizhen, Feng Huichuan, Yang Jialin. Advantages and application strategies of machine learning in diagnosis and treatment of lumbar disc herniation [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(9): 1426-1435. |
| [2] | Yang Yufang, Yang Zhishan, Duan Mianmian, Liu Yiheng, Tang Zhenglong, Wang Yu. Application and prospects of erythropoietin in bone tissue engineering [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(9): 1443-1449. |
| [3] | Qi Xue, Li Jiahui, Zhu Yuanfeng, Yu Lu, Wang Peng. Abnormal modification of alpha-synuclein and its mechanism in Parkinson’s disease [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(8): 1301-1306. |
| [4] | Huang Haoran, Fan Yinuo, Wei-Yang Wenxiang, Jiang Mengyu, Fang Hanjun, Wang Haibin, Chen Zhenqiu, Liu Yuhao, Zhou Chi. Urolithin A mediates p38/MAPK pathway to inhibit osteoclast activity [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(8): 1149-1154. |
| [5] | Liu Jianhong, Liao Shijie, Li Boxiang, Tang Shengping, Wei Zhendi, Ding Xiaofei. Extracellular vesicles carrying non-coding RNA regulate the activation of osteoclasts [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(7): 1076-1082. |
| [6] | Xu Rong, Wang Haojie, Geng Mengxiang, Meng Kai, Wang Hui, Zhang Keqin, Zhao Huijing. Research advance in preparation and functional modification of porous polytetrafluoroethylene artificial blood vessels [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(5): 759-765. |
| [7] | Yin Kaiwen, Li Yunfeng. Application of metal-organic frameworks in implant surface modification [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(5): 783-788. |
| [8] | Wei Yuanxun, Chen Feng, Lin Zonghan, Zhang Chi, Pan Chengzhen, Wei Zongbo. The mechanism of Notch signaling pathway in osteoporosis and its prevention and treatment with traditional Chinese medicine [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(4): 587-593. |
| [9] | Xing Hao, Meng Qingfeng, Chang Zhengqi. Mechanism of negative pressure wound therapy in the auxiliary treatment of bone and soft tissue infection [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(4): 621-626. |
| [10] | Bi Yujie, Ma Dujun, Peng Liping, Zhou Ziqiong, Zhao Jing, Zhu Houjun, Zhong Qiuhui, Yang Yuxin. Strategy and significance of Chinese medicine combined with medical hydrogel for disease treatment [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(3): 419-425. |
| [11] | Xie Peng, Zhang Jiang, Deng Xiaolei, Wei Bo, Hou Decai. A systematic review of mouse model construction for sarcopenia [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(2): 263-266. |
| [12] | Xie Heng, Gu Ye, Gu Yingchu, Wu Zerui, Fang Tao, Wang Qiufei, Peng Yuqin, Geng Dechun, Xu Yaozeng. Ferroptosis in bone diseases: therapeutic targets of osteoporosis [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(16): 2613-2618. |
| [13] | Pan Chengzhen, Chen Feng, Lin Zonghan, Mo Jian, Zhang Chi, Wei Yuanxun, Wei Zongbo. Mechanism by which terpenoid herbal monomers prevent osteoporosis by regulating nuclear factor-kappaB signaling pathway [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(14): 2234-2241. |
| [14] | Zhai Haoyan, Zhao Yuan, Fan Dengying, Liu Chunyan. The role of reactive oxygen species in periodontitis and periodontal tissue regeneration [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(14): 2254-2260. |
| [15] | Wang Xin, Huang Jinyong, Wubulikasimu · Mijiti, Xie Zengru. Regulation of Toll-like receptors on function of osteoblasts and osteoclasts [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(12): 1931-1936. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||