Chinese Journal of Tissue Engineering Research ›› 2024, Vol. 28 ›› Issue (9): 1443-1449.doi: 10.12307/2024.014
Previous Articles Next Articles
Application and prospects of erythropoietin in bone tissue engineering
Yang Yufang1, Yang Zhishan1, Duan Mianmian1, Liu Yiheng1, Tang Zhenglong1, 2, Wang Yu1, 2
- 1School of Stomatology, Guizhou Medical University, Guiyang 550004, Guizhou Province, China; 2Department of Oral and Maxillofacial Surgery, Affiliated Stomatological Hospital of Guizhou Medical University, Guiyang 550004, Guizhou Province, China
-
Received:2023-02-14Accepted:2023-03-23Online:2024-03-28Published:2023-07-26 -
Contact:Wang Yu, MD, PhD, Associate professor, School of Stomatology, Guizhou Medical University, Guiyang 550004, Guizhou Province, China; Department of Oral and Maxillofacial Surgery, Affiliated Stomatological Hospital of Guizhou Medical University, Guiyang 550004, Guizhou Province, China -
About author:Yang Yufang, Master candidate, School of Stomatology, Guizhou Medical University, Guiyang 550004, Guizhou Province, China -
Supported by:National Natural Science Foundation of China, No. 82160193 (to WY); a grant from Guizhou Provincial Department of Science and Technology, No. ZK[2022]384 (to WY)
CLC Number:
Cite this article
Yang Yufang, Yang Zhishan, Duan Mianmian, Liu Yiheng, Tang Zhenglong, Wang Yu. Application and prospects of erythropoietin in bone tissue engineering[J]. Chinese Journal of Tissue Engineering Research, 2024, 28(9): 1443-1449.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks

2.1 促红细胞生成素与骨代谢之间的关系 骨是一种动态器官,具有高度再生的潜能,生理性骨代谢和重建是一个持续终生的动态过程[22]。间充质干细胞是一种来源于中胚层的多能干细胞,从各种组织中分离出来,包括骨髓、子宫内膜、牙髓、经血和脂肪组织等,具有易获取、易培养、低免疫原性和易于转染外源基因并长期表达的特点,也具有向成骨细胞、破骨细胞、脂肪细胞、神经细胞和基质细胞分化的能力[23]。当缺损发生时,间充质干细胞被招募到缺陷区[24],通过成骨细胞和破骨细胞的耦合活动进行持续不断的重塑,用新骨取代旧骨,并修复骨缺损,以维持骨组织结构和功能的完整性,是骨组织再生的关键。 促红细胞生成素对成骨有着重要的促进作用,大量不同动物模型的体内研究都显示外源性促红细胞生成素的应用可以提高成骨效果,促进骨缺损的修复。在鼠的股骨缺损模型中,促红细胞生成素增加了新生骨的体积和生物力学性能[25-26],在鼠的颅骨缺损模型中也观察到了类似的结果[24]。无论是新生还是成年小鼠,全身应用剂量为6 000 U/kg的促红细胞生成素都可以诱导骨形成。在兔的脊柱融合模型中,每日应用250 U/kg 促红细胞生成素连续皮下注射,20 d后可以观察到明显的成骨[27]。在猪的颅骨缺损模型中,促红细胞生成素的治疗也可以明显增强骨愈合[28-29]。HOLSTEIN等[30]第一次报道将促红细胞生成素短时间应用于大鼠骨折时对骨折愈合的促进效果。目前研究认为,促红细胞生成素在骨折愈合中的作用主要包括增加骨的体积和矿化程度、加速骨折断端连接以及增强骨的生物力学性能[31-32]。 与上述促红细胞生成素的促进成骨作用相反,促红细胞生成素对骨代谢的影响还体现在破骨活动中。SINGBRANT等[33]观察到大剂量 (300 U/kg)的促红细胞生成素应用会导致骨小梁体积减少,并伴有骨的重建活动活跃,而用双膦酸盐抑制破骨细胞活性后,大剂量促红细胞生成素引起的骨量减少也受到了抑制,表明破骨细胞可能是造成这种作用的原因。此外,一些其他研究也观察到外源性促红细胞生成素的应用可能会引起类似的骨量减少的现象[34-35]。此外,在构建的促红细胞生成素过表达的转基因小鼠模型中,也观察到了骨吸收速率增加、成骨速率降低和骨量减少的现象[35-37]。有体外实验表明促红细胞生成素可以直接刺激破骨细胞分化为成熟的破骨细胞,破骨细胞的分化导致促红细胞生成素R的转录水平相应降低,说明促红细胞生成素R的表达仅限于不成熟的破骨细胞,而促红细胞生成素对破骨细胞的刺激作用可能与JAK2和PI3K信号通路有关[35,38]。"

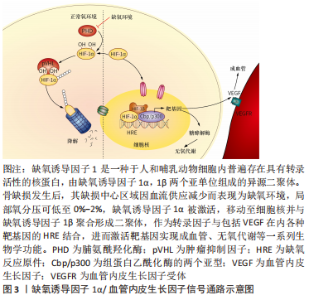
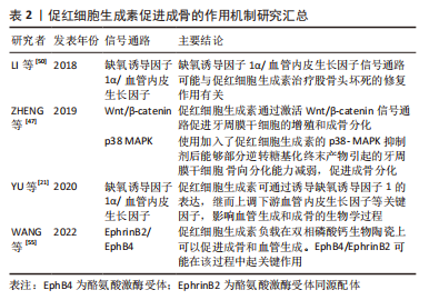
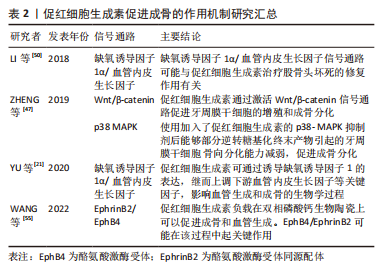
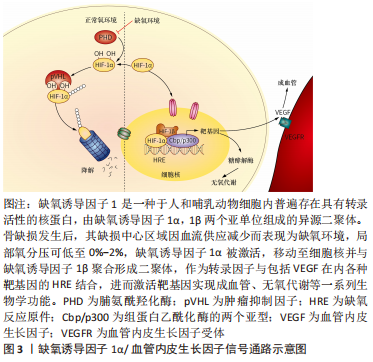
2.2 促红细胞生成素促进成骨的作用机制 有研究显示,促红细胞生成素受体在巨噬细胞及其分化形成的破骨细胞和成骨细胞表面均有RNA水平的基因表达[33,35]。此外,在成骨细胞和单核细胞系中分离出的细胞中也检测到了特异性的促红细胞生成素受体[35,39-41]。然而,SINGBRANT等[33]认为促红细胞生成素的特异性受体只存在于少数分化程度较低的细胞中,而在成熟的成骨和破骨细胞中没有表达。可以确定的是,促红细胞生成素R确实在成骨和单核细胞系的某个特定发育阶段出现了表达,为了验证这种表达和功能上的相关性,不同的学者分别使用浓度范围设定在10-100 U/mL的促红细胞生成素于体外成功诱导了人或啮齿类动物骨髓的成骨细胞及小鼠骨髓基质细胞(ST2)的成骨分化。这种成骨分化作用可能是由Wnt/β-catenin、缺氧诱导因子1α/血管内皮生长因子、p38 MAPK、EphrinB2/EphB4信号通路介导完成的[21,40-44]。 2.2.1 Wnt/β-catenin信号通路 Wnt是一类分泌型糖蛋白,在哺乳动物中至少有19种,是Wnt/β-catenin信号通路中的关键蛋白,可通过自分泌或旁分泌的方式与细胞膜受体结合,参与调控细胞增殖、分化和凋亡,在胚胎的发育和组织的再生中发挥作用。 有研究探讨了促红细胞生成素治疗骨髓增生异常综合征间充质干细胞中Wnt/β-catenin通路的作用[45],发现在促红细胞生成素与氯化锂联合治疗后可观察到类似经典Wnt信号激活后的成骨细胞分化过程,而且Wnt蛋白表达在促红细胞生成素处理的成骨细胞中显著上调。这表明促红细胞生成素可通过经典Wnt通路的激活促进骨髓增生异常综合征患者间充质干细胞的成骨向分化。牙周膜干细胞是牙周组织再生和修复的主要功能细胞,可分化为成骨细胞、脂肪细胞和成牙骨质细胞,它对牙骨质牙周膜复合体和牙槽骨的生理愈合至关重要[46]。ZHENG等[47]研究了促红细胞生成素对牙周膜干细胞增殖和成骨分化的最佳浓度,发现20 U/mL和50 U/mL 促红细胞生成素都以剂量和时间依赖的方式增加牙周膜干细胞的碱性磷酸酶活性,证实其对牙周膜干细胞的增殖和成骨分化都显示出积极作用。促红细胞生成素通过激活Wnt/β-catenin信号通路中的β-catenin蛋白及上调其靶基因Cyclin D1的表达调控成骨。在他们的研究中,促红细胞生成素诱导的β-catenin表达增加显著上调了Cyclin D1 和Runx2的蛋白水平,而β-catenin的敲除下调了这两种蛋白并抑制了骨矿化的形成。这些发现表明促红细胞生成素可以通过激活Wnt/β-catenin信号通路中的β-catenin和Cyclin D1刺激成骨标志物的表达。综上所述,促红细胞生成素促进干细胞成骨分化的潜在机制可能是激活Wnt/β-catenin信号通路。 2.2.2 缺氧诱导因子1α/血管内皮生长因子通路 促红细胞生成素促进骨缺损修复是一个成骨成血管协同的作用过程。缺氧诱导因子1可以调节心肌缺氧并激活内源性炎症反应,被认为是低氧损伤的关键调节因子[48]。随着学者们对缺氧诱导因子1研究的深入,发现缺氧诱导因子1是由α和β两个亚基组成的异源二聚体。人们对缺氧诱导因子1α参与介导促红细胞生成素的成骨作用进行了研究,研究结果显示,在缺氧条件下,缺氧诱导因子1被激活并导致促红细胞生成素水平升高[49-50]。有研究用明胶微球负载人重组促红细胞生成素在坏死的股骨头进行局部释放,发现缺氧诱导因子1α和血管内皮生长因子表达上调,缺氧诱导因子1α的激活还促进了间充质干细胞成骨分化,增加骨细胞增殖活性。这表明缺氧诱导因子1α/血管内皮生长因子信号通路可能参与了促红细胞生成素对股骨头坏死的修复作用,见图3。"
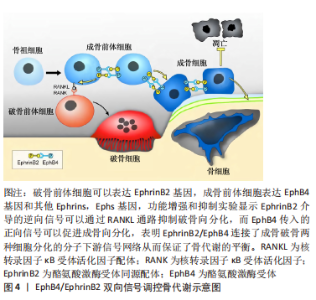
YU等[21]在缺氧条件下培养内皮祖细胞和ST2细胞,使用siRNA和缺氧诱导因子1抑制剂干扰缺氧诱导因子1,然后检测血管内皮生长因子和促红细胞生成素的变化。结果表明,在缺氧环境下,缺氧诱导因子1α/血管内皮生长因子通路的所有因子均上调;随着缺氧诱导因子1的抑制或干扰,血管内皮生长因子在蛋白质和mRNA水平上的表达均降低,而促红细胞生成素的mRNA表达从干预后6 h开始下降,从干预后12 h开始在蛋白质水平上发生显著变化。综上,促红细胞生成素可通过诱导缺氧诱导因子1的表达,继而上调下游血管内皮生长因子等关键因子,影响血管生成和成骨的生物学过程。 2.2.3 p38 MAPK信号通路 丝裂原活化蛋白激酶(mitogen-activited protein kinases,MAPK)信号通路是介导细胞外信号到细胞内反应的重要信号转导通路,与细胞的增殖、分化和凋亡等许多重要的生命活动密切相关,可被多种刺激如生长因子、神经递质、激素、细胞应激和细胞因子等所活化。p38是MAPKs家族的一员,可以由细胞因子和环境理化压力的刺激下被激活,参与多种生物学活动,如肿瘤发生、成骨、成软骨分化等。在参与间充质干细胞的成骨分化方面,已有的研究都提示其与成骨细胞活性密切相关,还与成骨细胞的其他分化标记物相关。大量文献报道,p38 MAPK在干细胞成骨分化中也发挥着关键作用,且能够通过多种途径调节骨代谢,是干细胞成骨效应中重要的效应感受器。丁月峰等[51]的研究中发现体外抑制p38信号通路(抑制p38的磷酸化)会抑制上颌突间充质细胞的增殖和成骨分化,提示p38可能参与了MAKA信号通路调控的颅颌面骨骼发育。ZHENG等[47]的研究证实,促红细胞生成素可以活化p38 MAPK信号通路,增加p38和GSK3β磷酸化,在使用p38 MAPK抑制剂后,p38及GSK3β磷酸化受到阻滞,成骨相关因子水平明显下降;加入促红细胞生成素后,能够部分逆转糖基化终末产物引起的牙周膜干细胞骨向分化能力减弱,促进成骨分化,说明p38 MAPK信号通路可能也参与了促红细胞生成素的促进成骨作用。 2.2.4 EphrinB2/EphB4信号通路 在骨重塑过程中,破骨细胞和成骨细胞之间可通过直接接触(如配体和受体结合),也能通过间接接触(如分泌旁分泌因子或转录因子与细胞或骨基质等相互作用)。近年来有研究表明,破骨细胞表面也存在相关因子能作用于成骨细胞,并调控成骨细胞的分化[52-53]。EphrinB2/EphB4信号通路见图4。"
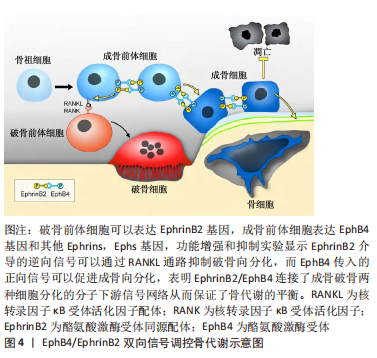
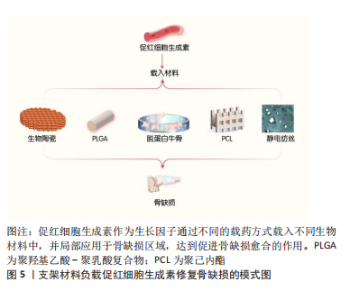
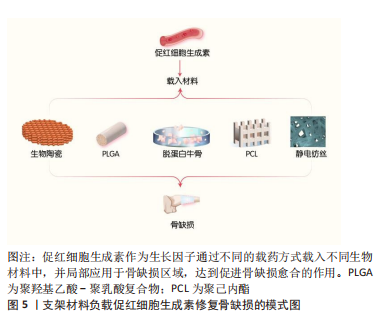
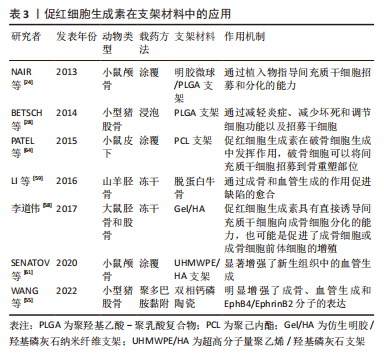
2.3 促红细胞生成素在骨组织工程中的应用 经典的骨组织工程包括种子细胞、支架材料和生长因子。促红细胞生成素作为在骨代谢过程中具有重要应用潜力和价值的生长因子,其在骨组织工程中的应用也逐渐受到不同研究者的关注[56-60]。 2.3.1 促红细胞生成素与支架材料 骨组织工程的支架材料可分为天然生物和人工合成两种。已有研究中,负载促红细胞生成素的人工合成支架材料包括聚己内酯(Polycaprolactone,PCL)、聚羟基乙酸-聚乳酸复合物(poly(lactic-co-glycolic acid),PLGA)、生物陶瓷、纳米纤维、脱蛋白牛骨(deproteinized bovine bone,DBB)和明胶微球等。天然生物支架材料包括胶原凝胶及壳聚糖等,促红细胞生成素与各种支架材料结合参与构建新型的组织工程骨,进而修复不同尺寸和部位的骨缺损,支架材料负载促红细胞生成素修复骨缺损的模式图,见图5。"
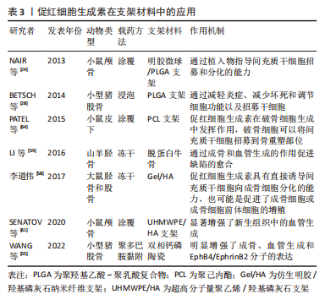
作为材料改性的基本方法,涂覆和浸泡是生物支架负载促红细胞生成素的传统方式,不同的研究者都通过涂覆或浸泡的方式构建了不同生物支架负载促红细胞生成素的新型组织工程骨并取得了良好的骨缺损修复效果[24,28,61-63]。然而,传统的涂覆或浸泡方式仍存在着促红细胞生成素的释放速度过快,无法实现缓释的缺点。为了解决这一问题,WANG等[55]利用聚多巴胺(polydopamine,pDA)的仿贻贝黏附特性将促红细胞生成素成功接枝在双相钙磷陶瓷(biphasic calcium phosphate,BCP)表面,通过材料表面的PDA涂层成功实现了促红细胞生成素在支架材料表面的缓释。顾中一[56]通过把促红细胞生成素引入到壳聚糖水凝胶体系中,利用壳聚糖水凝胶的特性阻止促红细胞生成素的突释。KARPOV等[57]成功将促红细胞生成素掺入静电纺丝支架中,实验结果表明静电纺丝明显改善了促红细胞生成素的释放方式,释放的时间显著延长。李道伟[58]尝试通过冻干的方法制备仿生明胶/羟基磷灰石(gelatin/hydroxyapatite,Gel/HA)纳米纤维支架,将促红细胞生成素直接与纤维支架复合,结果发现促红细胞生成素释放仍呈现明显的突释现象,仅有少量促红细胞生成素存留于支架内缓慢释放,尽管其对骨缺损修复仍有良好的效果,却未能实现促红细胞生成素的缓释。 2.3.2 促红细胞生成素在骨组织工程中的作用及潜在机制 (1)促红细胞生成素在骨组织工程中的促血管生成作用:作为促红细胞生成素的经典生物学作用,促血管生成是促红细胞生成素在其参与构建的新型组织工程骨中不可或缺的基本功能,多个研究者通过各种不同的生物支架及动物模型均证实了促红细胞生成素在骨组织工程中这一功能的存在。有研究建立山羊缺陷模型,将负载人重组促红细胞生成素的DBB支架填充于缺损处,与纯DBB支架相比,DBB/人重组促红细胞生成素组更明显地通过其成骨和血管生成的作用促进骨缺陷的愈合,其中血管内皮生长因子可能是促红细胞生成素介导的血管生成作用的重要下游信号分子[59]。有研究指出促红细胞生成素可以刺激骨髓内皮祖细胞迁移、聚集到血管形成部位,并分化为血管内皮细胞,血管内皮生长因子等促血管形成因子的分泌,从而促进血管形成和牙周组织再生[60]。有研究于2020年在小鼠颅骨缺损模型中应用促红细胞生成素参与构建的超高分子量聚乙烯/羟基磷灰石(ultra-high molecular weight polyethylene/hydroxyapatite,UHMWPE/HA)支架[61],发现新生骨组织中的血管生成明显增多,尽管该文作者并未深入阐述其分子生物学机制,其实验结果仍证实了促红细胞生成素通过血管生成促进骨缺损愈合的作用。该课题组团队在2022年的研究中也发现促红细胞生成素负载后的BCP陶瓷不仅对大鼠股骨缺损的修复效果更明显[55],其骨缺损区域的新生血管数量与BCP陶瓷相比也显著增多,免疫组织化学染色的结果提示促红细胞生成素的应用上调了EphrinB2和EphB4蛋白的表达,表明EphrinB2/EphB4可能是促红细胞生成素构建的组织工程骨血管生成作用的可能机制。在LI等[50]应用促红细胞生成素构建新型明胶微球的研究中,缺氧诱导因子1α/血管内皮生长因子信号通路也被证明参与了促红细胞生成素促进成骨成血管的过程。然而,Wnt/β-catenin及p38 MAPK等在促红细胞生成素促进成骨中发挥作用的信号通路却未出现在促红细胞生成素构建的新型组织工程骨促进骨缺损愈合的研究中,其在促红细胞生成素相关的骨组织工程中的具体机制尚需进一步证实。 (2)促红细胞生成素在骨组织工程中对间充质干细胞的募集和促成骨分化作用:以往的研究者除了关注促红细胞生成素经典的促血管生成作用外,也注意到了促红细胞生成素在骨组织工程中直接促进间充质干细胞募集和成骨分化的作用。有研究构建了负载促红细胞生成素的明胶微球/PLGA支架,将其植入小鼠颅骨,观察到新骨形成几乎完全(超过80%)覆盖了骨缺损区域,并发现在这一过程中促红细胞生成素促进了不同程度的间充质干细胞募集,并在间充质干细胞的成骨向分化中扮演了不可或缺的角色[24]。在顾中一[56]将促红细胞生成素引入壳聚糖水凝胶体系的研究中,牙周炎+促红细胞生成素组和牙周炎+载促红细胞生成素水凝胶组牙周组织再生明显,炎细胞浸润显著减轻,此作用与 促红细胞生成素促进间充质干细胞成骨向分化、抑制破骨细胞的功能有关。李道伟[58]的研究中也发现了类似的结果,促红细胞生成素能够显著促进间充质干细胞的成骨向分化。促红细胞生成素的这一生物学作用不仅局限于骨,在软骨中也有着类似的发现。BETSCH等[28]的研究中,将PLGA支架作为载体负载促红细胞生成素,在小型猪软骨缺损中获得了理想的成骨效果,结果显示促红细胞生成素在减轻炎症、减少坏死、调节细胞功能以及招募间充质干细胞方面均发挥了作用,从不同方面促进了软骨缺损的愈合过程。 2.3.3 促红细胞生成素与其他生长因子的共同作用 促红细胞生成素还可与其他生物因子共同作用构建新型组织工程骨。骨形态发生蛋白是转化生长因子超家族中的成员,能诱导间充质干细胞向成骨及软骨细胞分化,对其他骨组织工程种子细胞也有同样的诱导作用。SUN等[62]使用颅骨缺损模型确定了促红细胞生成素在骨形态发生蛋白2诱导的骨再生中的作用,结果显示对照组和促红细胞生成素治疗组没有明显的骨形成,尽管在缺损区域的中部观察到一些孤立的小骨岛;促红细胞生成素给药改善了骨形态发生蛋白2诱导的骨的质量,与单独骨形态发生蛋白2治疗相比,联合促红细胞生成素组形成的骨更接近天然颅骨,具有更高的骨体积分数和更低的骨髓分数。张广德[63]的实验利用骨形态发生蛋白9 促进脂肪来源干细胞成骨分化和促红细胞生成素促进脂肪来源干细胞增殖迁移和成骨的特点,将骨形态发生蛋白9和促红细胞生成素基因共转染脂肪来源干细胞,结果提示经促红细胞生成素基因转染后碱性磷酸酶活性及钙结节数均显著高于未经促红细胞生成素基因转染组,进一步验证了骨形态发生蛋白9 和促红细胞生成素基因在促进脂肪来源干细胞成骨分化方面具有协同作用。有研究检测了负载促红细胞生成素和骨形态发生蛋白2的新型PCL支架上的结合和释放动力学,通过在小鼠皮下植入分别负载骨形态发生蛋白2和负载骨形态发生蛋白2+促红细胞生成素的3D打印PCL支架,观察发现双蛋白负载组比单纯骨形态发生蛋白2组有更明显的骨生成[64]。以上结果表明,促红细胞生成素在与其他生物因子共同作用构建新型组织工程骨方面同样具有重要的研究价值。 上述研究具体成果,见表3。"
| [1] NAKAJIMA Y. Retinoic acid signaling in heart development. Genesis. 2019;57(7-8):e23300. [2] AWIDA Z, HIRAM-BAB S, BACHAR A, et al. Erythropoietin Receptor (EPOR) signaling in the osteoclast lineage contributes to epo-induced bone loss in mice. Int J Mol Sci. 2022;23(19):12051. [3] BAHLMANN FH. Erythropoietin regulates endothelial progenitor cells. Blood. 2004;103(3):921-926. [4] SATO T, TAKEDA N. The roles of HIF-1α signaling in cardiovascular diseases. J Cardiol. 2023;81(2):202-208. [5] LIPSIC E, SCHOEMAKER RG, VAN DER MEER P, et al. Protective effects of erythropoietin in cardiac ischemia: from bench to bedside. J Am Coll Cardiol. 2006;48(11):2161-2167. [6] PANKRATOVA S, KIRYUSHKO D, SONN K, et al. Neuroprotective properties of a novel, non-haematopoietic agonist of the erythropoietin receptor. Brain. 2010;133(Pt 8):2281-2294. [7] NAKANO M, SATOH K, FUKUMOTO Y, et al. Important role of erythropoietin receptor to promote VEGF expression and angiogenesis in peripheral ischemia in mice. Circ Res. 2007;100(5):662-669. [8] TSAI PT, OHAB JJ, KERTESZ N, et al. A critical role of erythropoietin receptor in neurogenesis and post-stroke recovery. J Neurosci. 2006; 26(4):1269-1274. [9] ELLIOTT S, BUSSE L, MCCAFFERY I, et al. Identification of a sensitive anti-erythropoietin receptor monoclonal antibody allows detection of low levels of EpoR in cells. J Immunol Methods. 2010;352(1-2): 126-139. [10] MAXWELL P, MELENDEZ-RODRÍGUEZ F, MATCHETT KB, et al. Novel antibodies directed against the human erythropoietin receptor: creating a basis for clinical implementation. Br J Haematol. 2015; 168(3):429-442. [11] WESTENBRINK BD, LIPSIC E, VAN DER MEER P, et al. Erythropoietin improves cardiac function through endothelial progenitor cell and vascular endothelial growth factor mediated neovascularization. Eur Heart J. 2007;28(16):2018-2027. [12] LIFSHITZ, TABAK G, GASSMANN M, et al. Macrophages as novel target cells for erythropoietin. Haematologica. 2010;95(11):1823-1831. [13] REX TS, WONG Y, KODALI K, et al. Neuroprotection of photoreceptors by direct delivery of erythropoietin to the retina of the retinal degeneration slow mouse. Exp Eye Res. 2009;89(5):735-740. [14] TOBALEM M, HARDER Y, REZAEIAN F, et al. Secondary burn progression decreased by erythropoietin. Crit Care Med. 2013;41(4):963-971. [15] NAKAMURA S, SHO M, KOYAMA F, et al. Erythropoietin attenuates intestinal inflammation and promotes tissue regeneration. Scand J Gastroenterol. 2015;50(9):1094-1102. [16] LIU QS, CHENG ZW, XIONG JG, et al. Erythropoietin pretreatment exerts anti-inflammatory effects in hepatic ischemia/reperfusion-injured rats via suppression of the TLR2/NF-κB pathway. Transplant Proc. 2015;47(2): 283-289. [17] GARCIA P, SPEIDEL V, SCHEUER C, et al. Low dose erythropoietin stimulates bone healing in mice. J Orthop Res. 2011;29(2):165-172. [18] 徐良,周凯.EPO对失血性休克合并内毒素血症兔TNF-α、IL-6、IL-10、MDA影响的研究[J]. 浙江中医药大学学报,2010;34(2):155-157. [19] KERTESZ N, WU J, CHEN TH, et al. The role of erythropoietin in regulating angiogenesis. Dev Biol. 2004;276(1):101-110. [20] WANG J, FU X, JIANG C, et al. Bone marrow mononuclear cell transplantation promotes therapeutic angiogenesis via upregulation of the VEGF-VEGFR2 signaling pathway in a rat model of vascular dementia. Behav Brain Res. 2014;265:171-180. [21] YU Y, MA L, ZHANG H, et al. EPO could be regulated by HIF-1 and promote osteogenesis and accelerate bone repair. Artif Cells Nanomed Biotechnol. 2020;48(1):206-217. [22] 李杜晨晖,田艾,唐正龙.骨生物支架材料诱导的血管生成[J].中国组织工程研究,2022,26(22):3602-3608. [23] TARI K, ATASHI A, KAVIANI S, et al. Erythropoietin induces production of hepatocyte growth factor from bone marrow mesenchymal stem cells in vitro. Biologicals. 2017;45:15-19. [24] NAIR AM, TSAI YT, SHAH KM, et al. The effect of erythropoietin on autologous stem cell-mediated bone regeneration. Biomaterials. 2013; 34(30):7364-7371. [25] WAN L, ZHANG F, HE Q, et al. EPO promotes bone repair through enhanced cartilaginous callus formation and angiogenesis. PLoS One. 2014;9(7):e102010. [26] HOLSTEIN JH, ORTH M, SCHEUER C, et al. Erythropoietin stimulates bone formation, cell proliferation, and angiogenesis in a femoral segmental defect model in mice. Bone. 2011;49(5):1037-1045. [27] RÖLFING JH, BENDTSEN M, JENSEN J, et al. Erythropoietin augments bone formation in a rabbit posterolateral spinal fusion model. J Orthop Res. 2012;30(7):1083-1088. [28] Betsch M, Thelen S, Santak L, et al. The role of erythropoietin and bone marrow concentrate in the treatment of osteochondral defects in mini-pigs. PLoS One. 2014;9(3):e92766. [29] RÖLFING JH, JENSEN J, JENSEN JN, et al. A single topical dose of erythropoietin applied on a collagen carrier enhances calvarial bone healing in pigs. Acta Orthop. 2014;85(2):201-209. [30] HOLSTEIN JH, MENGER MD, SCHEUER C, et al. Erythropoietin (EPO): EPO-receptor signaling improves early endochondral ossification and mechanical strength in fracture healing. Life Sci. 2007;80(10):893-900. [31] GARCI P, SPEIDEL V, SCHEUER C, et al. Low dose erythropoietin stimulates bone healing in mice. J Orthop Res. 2011;29(2):165-172. [32] MIHMANLI A, DOLANMAZ D, AVUNDUK MC, et al. Effects of recombinant human erythropoietin on mandibular distraction osteogenesis. J Oral Maxillofac Surg. 2009;67(11):2337-2343. [33] SINGBRANT S, RUSSELL MR, JOVIC T, et al. Erythropoietin couples erythropoiesis, B-lymphopoiesis, and bone homeostasis within the bone marrow microenvironment. Blood. 2011;117(21):5631-5642. [34] DESHET-UNGER N, HIRAM-BAB S, HAIM-OHANA Y, et al. Erythropoietin treatment in murine multiple myeloma: immune gain and bone loss. Sci Rep. 2016;6:30998. [35] HIRAM-BAB S, NEUMANN D, GABET Y. Erythropoietin in bone-Controversies and consensus. Cytokine. 2017;89:155-159. [36] OIKONOMIDOU PR, CASU C, YANG Z, et al. Polycythemia is associated with bone loss and reduced osteoblast activity in mice. Osteoporos Int. 2016;27(4):1559-1568. [37] RAUNER M, FRANKE K, MURRAY M, et al. Increased EPO levels are associated with bone loss in mice lacking PHD2 in EPO-producing cells. J Bone Miner Res. 2016;31(10):1877-1887. [38] SURESH S, DE CASTRO LF, DEY S, et al. Erythropoietin modulates bone marrow stromal cell differentiation. Bone Res. 2019;7:21. [39] JUNG Y, SONG J, SHIOZAWA Y, et al. Hematopoietic stem cells regulate mesenchymal stromal cell induction into osteoblasts thereby participating in the formation of the stem cell niche. Stem Cells. 2008; 26(8):2042-2051. [40] RÖLFING JH, BAATRUP A, STIEHLER M, et al. The osteogenic effect of erythropoietin on human mesenchymal stromal cells is dose-dependent and involves non-hematopoietic receptors and multiple intracellular signaling pathways. Stem Cell Rev Rep. 2014;10(1):69-78. [41] KIM J, JUNG Y, SUN H, et al. Erythropoietin mediated bone formation is regulated by mTOR signaling. J Cell Biochem. 2012;113(1):220-228. [42] LI C, SHI C, KIM J, et al. Erythropoietin promotes bone formation through EphrinB2/EphB4 signaling. J Dent Res. 2015;94(3):455-463. [43] RANKIN EB, WU C, KHATRI R, et al. The HIF signaling pathway in osteoblasts directly modulates erythropoiesis through the production of EPO. Cell. 2012;149(1):63-74. [44] TSIFTSOGLOU AS. Erythropoietin (EPO) as a key regulator of erythropoiesis, bone remodeling and endothelial transdifferentiation of multipotent mesenchymal stem cells (MSCs): implications in regenerative medicine. Cells. 2021;10(8):2140. [45] BALAIAN E, WOBUS M, WEIDNER H, et al. Erythropoietin inhibits osteoblast function in myelodysplastic syndromes via the canonical Wnt pathway. Haematologica. 2018;103(1):61-68. [46] WASHIO K, IWATA T, MIZUTANI M, et al. Assessment of cell sheets derived from human periodontal ligament cells: a pre-clinical study. Cell Tissue Res. 2010;341(3):397-404. [47] ZHENG DH, WANG XX, MA D, et al. Erythropoietin enhances osteogenic differentiation of human periodontal ligament stem cells via Wnt/β-catenin signaling pathway. Drug Des Devel Ther. 2019;13:2543-2552. [48] JU S, LIM L, WI K, et al. LRP5 Regulates HIF-1α Stability via Interaction with PHD2 in Ischemic Myocardium. Int J Mol Sci. 2021;22(12):6581 [49] SU J, LI Z, CUI S, et al. The Local HIF-2α/EPO pathway in the bone marrow is associated with excessive erythrocytosis and the increase in bone marrow microvessel density in chronic mountain sickness. High Alt Med Biol. 2015;16(4):318-330. [50] LI D, HU Q, TAN G, et al. Erythropoietin enhances bone repair effects via the hypoxia-inducible factor signal pathway in glucocorticoid-induced osteonecrosis of the femoral head. Am J Med Sci. 2018;355(6): 597-606. [51] 丁月峰, 王学娟, p38信号通路在牙周膜细胞成骨分化中的调控作用[J].口腔医学,2015,35(9):726-729. [52] KIM MH, CHO GW, HUH YM, et al. Transduction of human EPO into human bone marrow mesenchymal stromal cells synergistically enhances cell-protective and migratory effects. Mol Biol (Mosk). 2010; 44(4):656-663. [53] 李琛, EphrinB2/EphB4介导促红细胞生成素调控骨重塑的实验研究[D].长春:吉林大学,2014. [54] WANG Q, LIU Y, ZHAO Y, et al. Research progress on the expression and function of erythropoietin-producing hepatomocellular receptors and their receptor-interacting proteins in oral-related diseases. Hua Xi Kou Qiang Yi Xue Za Zhi. 2020;38(2):218-223. [55] WANG Y, WANG P, WU Q, et al. Loading of erythropoietin on biphasic calcium phosphate bioceramics promotes osteogenesis and angiogenesis by regulating EphB4/EphrinB2 molecules. J Mater Sci Mater Med. 2022;33(2):19. [56] 顾中一.载EPO壳聚糖水凝胶促牙周组织再生的研究[J].口腔生物医学,2017,8(3):127-131. [57] KARPOV TE, PELTEK OO, MUSLIMOV AR, et al. Development of optimized strategies for growth factor incorporation onto electrospun fibrous scaffolds to promote prolonged release. ACS Appl Mater Interfaces. 2020;12(5):5578-5592. [58] 李道伟.载EPO仿生Gel/HA纳米纤维促骨再生研究[J].口腔生物医学,2017,8(3):117-121. [59] LI D, DENG L, XIE X, et al. Evaluation of the osteogenesis and angiogenesis effects of erythropoietin and the efficacy of deproteinized bovine bone/recombinant human erythropoietin scaffold on bone defect repair. J Mater Sci Mater Med. 2016;27(6):101. [60] KIRKEBY A, TORUP L, BOCHSEN L, et al. High-dose erythropoietin alters platelet reactivity and bleeding time in rodents in contrast to the neuroprotective variant carbamyl-erythropoietin (CEPO). Thromb Haemost. 2008;99(4):720-728. [61] SENATOV F, AMANBEK G, ORLOVA P, et al. Biomimetic UHMWPE/HA scaffolds with rhBMP-2 and erythropoietin for reconstructive surgery. Mater Sci Eng C Mater Biol Appl. 2020;111:110750. [62] SUN H, JUNG Y, SHIOZAWA Y, et al. Erythropoietin modulates the structure of bone morphogenetic protein 2-engineered cranial bone. Tissue Eng Part A. 2012;18(19-20):2095-2105. [63] 张广德.重组腺病毒介导BMP-9及促红细胞生成素双基因共转染促进脂肪来源干细胞体外成骨的研究[J].中国修复重建外科杂志, 2016,30(3):272-278. [64] PATEL JJ, MODES JE, FLANAGAN CL, et al. Dual delivery of EPO and BMP2 from a novel modular poly-ɛ-caprolactone construct to increase the bone formation in prefabricated bone flaps. Tissue Eng Part C Methods. 2015;21(9):889-897. |
| [1] | Huang Haoran, Fan Yinuo, Wei-Yang Wenxiang, Jiang Mengyu, Fang Hanjun, Wang Haibin, Chen Zhenqiu, Liu Yuhao, Zhou Chi. Urolithin A mediates p38/MAPK pathway to inhibit osteoclast activity [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(8): 1149-1154. |
| [2] | Dai Yuexing, Zheng Liqin, Wu Minhui, Li Zhihong, Li Shaobin, Zheng Desheng, Lin Ziling. Effect of vessel number on computational fluid dynamics in vascular networks [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(8): 1206-1210. |
| [3] | Liu Jianhong, Liao Shijie, Li Boxiang, Tang Shengping, Wei Zhendi, Ding Xiaofei. Extracellular vesicles carrying non-coding RNA regulate the activation of osteoclasts [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(7): 1076-1082. |
| [4] | Wang Shanshan, Shu Qing, Tian Jun. Physical factors promote osteogenic differentiation of stem cells [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(7): 1083-1090. |
| [5] | Wang Wen, Zheng Pengpeng, Meng Haohao, Liu Hao, Yuan Changyong. Overexpression of Sema3A promotes osteogenic differentiation of dental pulp stem cells and MC3T3-E1 [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(7): 993-999. |
| [6] | Wei Yuanxun, Chen Feng, Lin Zonghan, Zhang Chi, Pan Chengzhen, Wei Zongbo. The mechanism of Notch signaling pathway in osteoporosis and its prevention and treatment with traditional Chinese medicine [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(4): 587-593. |
| [7] | Yang Yuqing, Chen Zhiyu. Role and application of early transient presence of M1 macrophages in bone tissue engineering [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(4): 594-601. |
| [8] | Zhou Shibo, Guan Jianbin, Yu Xing, Zhao He, Yang Yongdong, Liu Tao. Animal models of femoral bone defects: preparation status and characteristics [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(4): 633-638. |
| [9] | Dai Jing, Liu Shasha, Shen Mingjing. Exosome-loaded injectable hydrogel for repairing bone defects around implants [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(3): 347-354. |
| [10] | Zhu Zhiqi, Yuan Sijie, Zhang Zilin, Ji Shijie, Meng Mingsong, Yan Anming, Han Jing. Mechanism underlying the effect of Liuwei Dihuang Pill on osteolysis and osteogenesis induced by titanium particles [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(3): 392-397. |
| [11] | Gao Xueyu, Zhang Wentao, Sun Tianze, Zhang Jing, Li Zhonghai. Application of metal ions in bone tissue engineering [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(3): 439-444. |
| [12] | Chen Pinrui, Pei Xibo, Xue Yiyuan. Function and advantages of magnetically responsive hydrogel in bone tissue engineering [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(3): 452-457. |
| [13] | Long Zhirui, Huang Lei, Xiao Fang, Wang Lin, Wang Xiaobei. Characteristics of hydrogel microspheres in bone tissue engineering [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(3): 472-478. |
| [14] | Kong Xiangyu, Wang Xing, Pei Zhiwei, Chang Jiale, Li Siqin, Hao Ting, He Wanxiong, Zhang Baoxin, Jia Yanfei. Biological scaffold materials and printing technology for repairing bone defects [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(3): 479-485. |
| [15] | Xu Jing, Lyu Huixin, Bao Xin, Zhang Yi, Wang Yihan, Zhou Yanmin. Application of near infrared responsive hydrogels in tissue engineering [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(3): 486-492. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||