Chinese Journal of Tissue Engineering Research ›› 2024, Vol. 28 ›› Issue (3): 479-485.doi: 10.12307/2024.244
Previous Articles Next Articles
Biological scaffold materials and printing technology for repairing bone defects
Kong Xiangyu1, Wang Xing2, Pei Zhiwei1, Chang Jiale1, Li Siqin2, Hao Ting3, He Wanxiong1, Zhang Baoxin3, Jia Yanfei3
- 1Graduate School of Inner Mongolia Medical University, Hohhot 010000, Inner Mongolia Autonomous Region, China; 2Bayannur Hospital, Bayannur 015000, Inner Mongolia Autonomous Region, China; 3Second Affiliated Hospital of Inner Mongolia Medical University, Hohhot 010030, Inner Mongolia Autonomous Region, China
-
Received:2023-01-16Accepted:2023-03-02Online:2024-01-28Published:2023-07-10 -
Contact:Zhang Baoxin, Attending physician, Second Affiliated Hospital of Inner Mongolia Medical University, Hohhot 010030, Inner Mongolia Autonomous Region, China Jia Yanfei, Chief physician, Second Affiliated Hospital of Inner Mongolia Medical University, Hohhot 010030, Inner Mongolia Autonomous Region, China -
About author:Kong Xiangyu, Master candidate, Physician, Graduate School of Inner Mongolia Medical University, Hohhot 010000, Inner Mongolia Autonomous Region, China -
Supported by:Science and Technology Plan Project of Inner Mongolia Science and Technology Department, No. 2020GG0195 (to ZBX); Natural Science Foundation Project of Inner Mongolia Autonomous Region, No. 2019MS008158 (to ZBX); Technology Million Project (Joint) of Inner Mongolia Medical University, No. YKD2018KJBW(LH)002 (to ZBX); Science and Technology Plan Project of Inner Mongolia Science and Technology Department, No. 2021GG0174 (to ZBX)
CLC Number:
Cite this article
Kong Xiangyu, Wang Xing, Pei Zhiwei, Chang Jiale, Li Siqin, Hao Ting, He Wanxiong, Zhang Baoxin, Jia Yanfei. Biological scaffold materials and printing technology for repairing bone defects[J]. Chinese Journal of Tissue Engineering Research, 2024, 28(3): 479-485.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
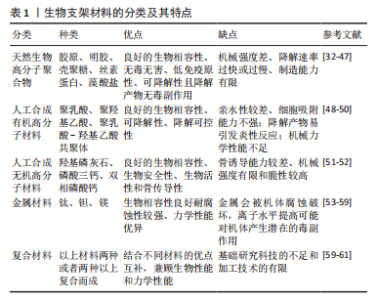
2.1 骨缺损的修复方式 由于创伤、感染、肿瘤、骨髓炎手术清创和各种先天性疾病导致的骨缺损问题在全球范围内威胁着患者的健康,同时对社会经济和临床工作带来深远的影响。目前临床上治疗修复骨缺损的主要方法包括骨移植、膜引导再生技术、基因治疗、骨组织工程技术等。 2.1.1 骨移植 骨移植根据移植骨的来源分为自体骨、异体骨和人工骨移植[11],而其中自体骨不仅是骨移植时作为骨替代物的首选材料,自体骨移植还是治疗骨缺损的主要选择[2-3]。自体骨具有骨诱导性、骨传导性与成骨性以及能尽早填补骨缺损且不会带来免疫反应等优点,对于骨源的选择大多数是松质骨和带血管的腓骨,松质骨主要选取自身的髂骨、股骨,其依靠空隙与受体血管之间的相互融合以及其优异的骨诱导、骨传导性能,在早期愈合发挥着重要作用[12]。殷渠东等[13]用松质骨包裹植骨技术治疗胫骨大段缺损,结果平均愈合时间6.1个月,愈合率达98%,优良率为80%,表明松质骨具有良好的诱导成骨作用。 异体骨移植不同于自体骨骨移植,其移植所用的骨材料不来自于自身,因此根据异体骨的来源将其分为同种异体骨移植和异种异体骨移植。同种异体骨大多数来自于他人尸体的骨组织经过处理制备而成,异种异体骨则是从动物骨组织中获得的。相较于自体骨而言,异体骨来源广泛,弥补了自体骨取材有限的缺陷,同时其良好的力学强度和支撑作用为骨缺损的修复提供了条件;另外,异体骨不需要从自身取材,因此缩短了手术时间,减少了对患者不必要的创伤,规避了一些不确定的风险[14]。胡小晓等[15]用冻干异体骨作为载体结合自体外周血干细胞治疗骨缺损患者,术后平均随访10个月时均在X射线片上显示骨折愈合良好,平均骨折愈合时间4-6个月,表明了使用自体外周血干细胞可以弥补冻干骨因灭活带来的成骨能力缺陷,冻干异体骨作为载体结合自体外周血干细胞具有良好的诱导性和成骨性。 人工骨移植即使用人工合成生物材料作为骨移植的原料,主要包括磷酸钙及其衍生物。由于人工骨修复材料来源丰富且与天然骨的无机成分非常相似,同时还具有良好的性能,因此很少出现生物安全性和组织相容性相关问题,所以作为骨的替代材料已被广泛应用于骨科、口腔颌面外科等领域[16]。人工骨还可作为载体与多种聚合物、生物因子、药物等形成复合物,诱导与骨生成相关的细胞增殖,促进间充质细胞的黏附和分化,也能促进血管生成,针对继发于感染的骨缺损提高其局部组织的药物浓度。 2.1.2 膜引导再生技术 MASQUELET于1986年提出了一种主要适用于长骨大段骨缺损的技术理念,称为膜引导再生技术(Mqsquelet技术)。该技术分为2个阶段,第一阶段是指在进行骨移植之前,首先应用骨水泥作为诱导剂填充到骨缺损的位置,诱导损缺部位生成诱导膜;第二阶段是切开诱导膜取出骨水泥并植入骨材料后缝合诱导膜,以此促进患者骨缺损的修复[17-19]。王有为[20]在研究中将64例下肢长骨感染性骨缺损患者分为2组,分别使用Masquelet技术与骨移植治疗,结果显示,术后3个月Masquelet技术治疗组患者的膝、踝关节评分均大于骨移植治疗组,表明Mqsquelet技术在治疗长骨大段感染性骨缺损方面有重要地位。 2.1.3 基因治疗 大量的研究表明,生长因子参与骨折的愈合过程,虽然它在体内的浓度很低,但却起着重要的作用,并且对骨折的愈合有着深远的影响[21]。但骨折断端生长因子的含量相当低,不足以发挥最大效能,因此,人为地使外源性生长因子在骨折端周围聚集来促进骨折的愈合具有重要意义[22]。目前在骨缺损治疗方面研究最多且最深入、效果最确切的成骨生长因子是骨形态发生蛋白2。GUAN等[23]的研究发现,被携带了骨形态发生蛋白2基因的慢病毒载体感染后,人尿源性干细胞高表达骨形态发生蛋白2基因,并且高表达成骨转录因子2和骨钙素,最后通过组织学验证这一体系可以促进新骨的形成。内源性骨形成蛋白有着较外源重组蛋白生物利用度高的优点,而且随着细胞生物学和分子生物学理论基础和实验技术的进步,应用基因治疗骨缺损正成为国际上研究的热点。 2.1.4 骨组织工程技术 骨组织工程研究主要集中在种子细胞、生长因子、生物支架这3个方面[24]。种子细胞为组织工程骨提供生物活性,间充质干细胞是目前应用最广泛的种子细胞,而其中骨髓间充质干细胞仍然是取材来源的首选,其具备了优秀的成骨及增殖能力,能够灵活适应微环境并且迅速分化为成骨及软骨细胞,避免了免疫排斥等问题[25]。生长因子为组织工程骨增加骨诱导及骨生成能力,促进成骨细胞的增殖及分化,提高细胞外基质的合成速度,以此来增强骨组织的再生修复能力。 骨组织工程技术作为治疗骨缺损的新兴技术,在促进成骨细胞增殖分化及骨形成能力方面有着独有的优势,然而却面临着血管化不足的挑战[26]。移植物的血管化和矿化是骨发育过程中的偶联过程,血管化在决定组织工程骨移植是否成功以及缺损能否修复方面具有重要意义。然而,新生血管生长缓慢,传统组织工程骨植入后需要较长时间才能实现血管化,往往因缺乏足够的营养和氧气供应而出现缺氧坏死的现象[27-28]。将组织工程骨植入宿主骨缺损处之前,于体外在其内部构建一个成熟的微血管网络,使其在植入体内后能快速地与宿主血管吻合,实现植入物早期充足的血液供应,这种技术称为预血管化。黄孟全等[29]将多孔β-磷酸三钙组织工程骨与内皮祖细胞和骨髓间充质干细胞共培养使其预血管化,将其植入骨缺损模型兔体内4周后的血管数量、血管直径及面积分数均优于对照组,表明组织工程骨经过预血管化后可加快其在骨缺损修复的早期的血管化进程。 2.2 生物支架材料和打印技术在骨缺损修复中的应用 2.2.1 生物支架材料的理想特性 生物支架在骨组织工程中充当着重要的角色,因此构建生物支架为中心环节,理想的生物支架需满足诸多特性[24,30]:良好的机械性能和弹性,可以在植入早期提供足够的支撑力和抗剪切力,否则会导致支架塌陷或断裂;具有骨诱导、骨传导能力,促进成骨细胞的增殖分化,使新生骨组织沿支架逐渐长入,保证连续性骨痂的生成[31];具有良好的生物相容性,避免发生严重的免疫排斥反应;具有可降解性,使新生的组织逐步代替降解的生物支架,且保证二者的动态平衡;具有良好的孔隙率,利于细胞黏附;可持续的抗菌作用,通过缓释的抗生素与缺损部位直接接触,在感染性骨缺损的治疗中起到关键作用。根据支架材料来源的不同,分为天然生物高分子聚合物、人工合成有机高分子材料、人工合成无机高分子材料、金属材料、复合材料,见表1。"
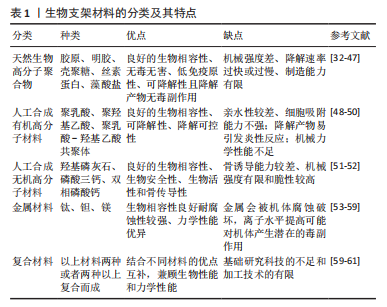
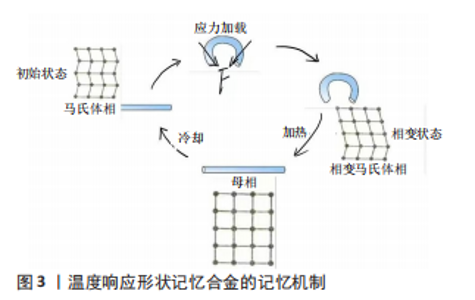
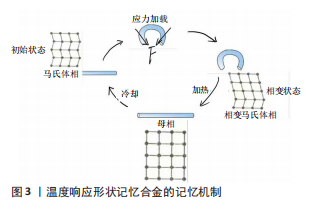
2.2.2 天然生物高分子聚合物 胶原:作为来自于人体的天然生物材料,具有良好的生物相容性及成骨诱导性,并且无毒无害、无致癌性,能够被人体吸收而实现降解。将胶原作为生物支架的材料则有利于促进细胞的黏附、生长增殖和分化,可以充分地发挥其低抗原性,诱导骨组织再生修复[32]。与无机材料联合应用制备支架,明胶能够锁住钙质,增加支架的韧性,其良好的骨诱导能力弥补无机材料在该方面的缺陷[33]。ZHOU等[34]通过将胶原/羟基磷灰石复合纤维与细胞共培养发现,该复合纤维不仅无体外细胞毒性,而且还有利于细胞的增殖及黏附。 明胶:具有优秀的生物相容性和可降解性,而且其极易凝胶化,易于成型,故被作为载药生物支架的选用材料。赵少华等[35]通过冻干法制备载双氯芬酸钠的明胶多孔支架,体外及体内实验结果表明,载双氯芬酸钠明胶多孔支架具有合适的孔径、孔隙率、细胞相容性和良好抗炎性能,可缓解植入部位的炎症反应,促进体内软骨再生。明胶降解速度相对较快,一般不单纯使用明胶作为支架材料,多与其他材料联合使用。常思佳等[36]通过将溶剂浇铸/粒子沥滤法制备的明胶-羟基磷灰石-磷酸三钙支架与明胶支架进行对比,发现明胶-羟基磷灰石-磷酸三钙支架的微观表征与天然骨结构相似,具有良好的抗压性,不易变形,并且具有显著的骨诱导性,可促进人牙髓干细胞的增殖和分化。 壳聚糖:广泛存在于细胞外基质中,是连接胶原纤维的主要成分之一,故其可为细胞增殖和细胞外基质生成提供微环境,具有促进成骨的潜力[37-38]。壳聚糖不仅具有良好的组织相容性、安全性、低抗原性等优点,而且还具有抗细菌和真菌的特性,可以抑制细菌、真菌、病毒的繁殖,常常作为抗菌材料联合其他材料用于治疗感染性骨缺损。李扬等[39]将壳聚糖乙酸填充到多孔生物玻璃支架中合成生物玻璃/壳聚糖多孔支架,与生物玻璃支架进行对比,分别接种小鼠胚胎成纤维细胞、与金黄色葡萄球菌及表皮葡萄球菌共培养,结果显示,生物玻璃/壳聚糖多孔支架不仅具有良好的体外生物相容性,而且还在抗感染方面有不俗的表现,具有成为新型预防及治疗骨关节感染骨修复材料的潜力。由于单纯的壳聚糖机械性能弱、水溶性较差、生物降解率较低,通常将壳聚糖作为支架涂层或者通过化学修饰做改性处理亦或者制备成可注射水凝胶使用,充分发挥其优点,扬长避短。YANG等[40]通过将季铵化处理的壳聚糖3D打印到聚丙交酯乙交酯共聚物和羟基磷灰石形成一种具有抗感染和骨修复双重功能的复合支架,将其植入到甲氧西林敏感金黄色葡萄球菌感染的股骨干缺损和股骨髁缺损模型中,结果表明该支架在两种感染骨缺损模型中均表现出优异的抗感染和骨修复能力,证实了此种支架具有抗菌和成骨的双重功能。 丝素蛋白:作为天然生物材料,不仅具有良好的生物相容性和可降解性,还具有优异的机械强度,能够承载较强的拉力,常常作为三维支架及无纺网等的材料。此外,丝素蛋白在体内的降解速度与骨缺损的修复周期相匹配,因此在作为骨缺损修复材料上展现出巨大优势[41-42]。 藻酸盐:具有良好的生物相容性、机械性能和生物可降解性,并且无毒副作用[43]。性能优良的藻酸盐在医学领域具有多处用途,例如其可以水凝胶的形式充当细胞外基质,为新生细胞组织提供机械支撑和生存空间;还可作为药物的载体,保护药物在生理环境下的活性,同时调节药物释放,延长药物在病灶部位的作用时间,起到药物缓释控释的作用[44]。练胜[45]通过构建藻酸盐凝胶细胞微球与双相磷酸钙陶瓷复合支架,并进行体内外实验评估其在骨缺损修复中的效果,结果显示,藻酸盐凝胶细胞微球与双相磷酸钙陶瓷复合支架可以促进新骨组织生长,并且在一定程度上修复了新西兰大耳兔尺骨缺损。 天然生物材料具有多种共同特性,如良好的生物相容性、无毒无害、低免疫原性、可降解性且降解产物无毒副作用,因此其可作为组织工程支架材料的优选,但也普遍存在机械强度差、降解速率过快或过慢、制造能力有限等缺点[46]。由于单一的材料总是存在不可避免的缺点,很难满足组织工程三维支架材料的要求,因此,将两种或两种以上具有互补特性的天然生物或人工合成高分子材料,按一定比例和方式复合,构造出能够满足结构与性能需求的三维支架复合材料,最终形成组织工程骨完成骨缺损的修复[47]。 2.2.3 人工合成高分子材料 人工合成有机高分子材料:近年来随着人工合成有机高分子材料的不断发展,聚乳酸类高分子聚合物及其衍生物在骨缺损修复中应用广泛,已经成为组织工程支架材料的重要组成部分[48],其中以聚乳酸、聚羟基乙酸以及二者共聚体即聚乳酸-羟基乙酸共聚体的应用最为广泛[49]。由于聚乳酸类高分子聚合物良好的生物相容性、可降解性、降解可控性等,可用于组织工程支架材料,但在实际运用过程中发现其亲水性较差、对细胞的吸附能力不强;其降解产物会引起降解速率的激增,并且容易引发机体出现炎性反应;机械力学性能不足及制备共聚物过程中残余的有机溶剂对细胞和周围组织的毒性作用等缺陷[50],限制了聚乳酸-羟基乙酸共聚体材料在骨缺损修复中的应用。 人工合成无机高分子材料:骨组织是一种双相组合材料,一相是以钙磷为主的无机质,一相是以胶原和其他基质构成的有机质。磷酸钙人工骨与天然骨无机组分非常相似,目前研究得较多也相对较理想的磷酸钙材料主要有3种:羟基磷灰石、磷酸三钙、羟基磷灰石/磷酸三钙复合而成的双相磷酸钙。磷酸钙与人体成分相似,因此具有良好的生物相容性、生物安全性、生物活性和骨传导性,在植入骨缺损处后安全且无不良反应,不引起免疫排斥反应,并且对受体组织具有亲和性,但较差的骨诱导能力及有限的机械强度和较高的脆性仍是该材料最突出的缺点,在其单独应用时仅能用于非负重区域,因此,需要与其他材料复合使用应用于骨缺损修复[51]。石永新等[52]采用3D打印技术制备聚磷酸钙/淫羊藿苷复合骨支架,并植入大白兔股骨髁骨缺损内,同时经股静脉注入骨髓间充质干细胞,通过X射线片观察复合骨支架及周围骨痂形成情况,结果显示淫羊藿苷弥补了传统磷酸钙在骨诱导能力方面的缺陷,3D打印技术制备的聚磷酸钙/淫羊藿苷骨支架可诱导骨髓间充质干细胞向成骨细胞分化,并且在骨缺损治疗中具有较好效果。 2.2.4 金属材料 金属支架材料具有良好的生物相容性、较强的耐腐蚀性、优异的力学性能,因此主要用于需要机械支撑的部位,如负重的长骨(股骨、胫骨等)和椎骨的骨缺损,能够有效避免植入物与皮质骨间极低的骨内应力变和骨吸收,从而促进骨向植入物内生长,增强骨组织与植入物的结合强度[53]。金属植入物的主要问题是生理环境的腐蚀会改变材料的理化性质,使移植物出现松动与损坏,并且金属离子水平的提高会对机体产生潜在的毒副作用。 根据金属材料的降解特性分为可降解金属支架材料和不可降解金属支架材料。目前,不可降解材料研究最多且应用最广泛的主要是钛和钽,可降解金属支架材料主要是镁。芮敏等[54]通过将3D打印技术制备的多孔钛合金支架植入兔桡骨缺损部位研究其缺损修复的能力,术后第12周的X射线图像显示,该组桡骨缺损处两侧断端均与钛支架形成骨性连接,而对照组桡骨缺损未修复,断端及邻近尺侧有少量新骨生成, 髓腔已封闭,表明3D打印技术制备的多孔钛合金支架具有良好的生物相容性和骨传导性。相比于钛,金属钽具有更高的惰性,其表面形成的氧化膜即使在强酸环境中也可维持较好的抗腐蚀性能,但也由于其是一种不能提供生长因子的惰性材料,因此需要表面改性或者复合其他材料增加其骨诱导能力[55]。张倩等[56]将转化生长因子β1与多孔钽颗粒复合制备生物活性多孔钽修复材料,并将此植入到比格犬的下颌骨缺损模型中,发现转化生长因子β1可以弥补钽金属在骨诱导方面的缺陷,使生物活性多孔钽具有高促骨活性,加速骨缺损区域的早期成骨及成血管进程,加快多孔钽与周围骨组织的早期生物性结合,缩短愈合时间。镁是人体中不可缺少的矿质元素之一,作为可降解金属支架材料在体内可逐渐降解生成镁离子,并被周围肌体组织吸收或通过体液排出体外[57]。镁支架不仅具有良好的生物相容性,而且其弹性模量与人骨非常接近,可以有效减少应力屏蔽效应;另外,镁可以诱导骨生成并在支架堆积,其降解速率与骨生成速度相匹配,可在早期提供生物力学支撑,后续降解部分逐步由新生骨代替[58-59]。 2.2.5 复合材料 当前,由于单一材料在生物和理化性质方面各具的优势及局限性,尚没有一种生物材料单独应用能有效模拟骨组织,满足骨组织工程的全部要求,因此,由属于相同或不同类别的两种或两种以上的基底制成的复合材料支架成为研究热点[59]。多种生物材料之间互补复合,可有效结合各种材料的优势,在提供良好的力学强度同时促进骨再生。比如,天然高分子聚合物虽然具备良好的生物相容性及可降解性,但是存在机械性能不强和骨诱导能力弱等缺陷,如果单独使用则会影响骨缺损修复的效果。刘星纲等[60]构建多孔β-磷酸三钙/胶原支架用于修复兔下颌牙槽骨缺损,结果显示β-磷酸三钙可提供良好的力学性能,胶原良好的生物相容性也使得术后伤口未见明显炎症反应、组织切片观察未见明显的排异反应,表明该支架具有良好的降解性能并可有效成骨。李欢欢[61]采用胶原自组装和矿化协同进行的方法制备出掺锶胶原支架和掺银胶原支架,通过体外和体内实验证明了掺锶胶原支架材料具有良好的生物相容性,可调节局部免疫微环境,利于诱导骨组织再生;另外,掺银胶原支架具备优异的抗菌性能。 2.3 打印技术在骨缺损修复中的应用 骨组织工程属于未来骨修复的主要发展方向,而支架材料是组织工程骨的中心环节。理想的支架需模拟细胞外基质的三维结构,具有合适的孔隙率,若支架孔隙率过高,会导致其力学性能下降;反之,孔隙率过低则不利于新骨生长,使植入体内的支架无法达到预期效果[62-63]。如何制备同时具有良好的力学性能和生物性能的支架,是支架结构设计中的一个难点。 2.3.1 3D打印技术在骨修复中的应用 3D打印技术能将数字信号转化为物理实体,其利用骨缺损病变部位的CT/MRI成像数据用于计算机三维设计,后将设计图纸传送到3D打印机,使原料供给装置送出粉末,经加工平台滚筒铺陈为薄原料,喷嘴喷出黏结剂,用层层粉末黏成精确制作的个性化3D生物材料支架,能够与骨缺失部位的完美匹配,微观结构也与正常骨组织高度相似[57,64]。 3D打印技术制备生物支架独特的优势在于:能够满足骨修复对支架机械强度的要求,还能对孔隙进行调节及构建复杂的空间结构[65]。在3D打印支架制备的过程中,打印参数对支架影响尤为重要,优化打印参数可以制备出拥有适合的孔隙率、良好生物相容性及足够的比表面积的3D打印生物支架,其为骨细胞提供了合适的微环境,促进了成骨细胞的增殖、分化以及细胞外基质在三维多孔结构内的均匀分布,为成骨细胞提供营养;另外,方便细胞营养液的输送和代谢产物的排放[66-67]。3D打印支架可调控的孔隙结构使其在骨组织工程中备受青睐,支架孔隙结构的优劣主要受孔隙形状、孔径大小、孔隙率、表面粗糙度、孔隙内部的连通性等因素的影响[68]。孔隙形状及孔径的大小对细胞生长、黏附、转移以及物质传递的速率都有影响[69]。TANG等[70]发现不同孔隙形状和孔径的单元组合可以改变支架的弹性模量增强其力学性能,多个研究比较方形和圆形单元结构支架的力学特性,结果表明方形多孔结构边缘尖锐,会产生高的集中应力,弹性模量较低,并且在降解过程中与骨组织的生长会发生干涉,不利于骨细胞发育,相比而言圆形单元结构在力学性能和降解性能上更加优良。多项研究表明,最适合骨组织生长、利于骨缺损修复的孔径直径范围是200-350 μm[71]。HUNG等[72]对孔径在150-200,250-300,300-350 μm范围的普通支架进行研究,结果显示孔径约为200 μm的支架具有最高的强度,对于普通支架,孔径越小结构越致密,支架的机械强度越大。孔隙率是指空隙体积与支架总体积的比值,孔隙率影响骨相关细胞的移动、局部pH值稳定性和新血管的形成[73]。孔隙率越大越有利于营养物质流动,为组织填充提供空间,但孔隙率太高会导致比表面积减少,不利于细胞黏附,同时支架力学性能也会降低;而孔隙率太低会阻碍细胞向内生长,因此,孔隙率过高或过低都不利于骨组织的修复生长。支架表面的粗糙度对不同细胞的形态和增殖有直接影响,增大表面粗糙度可改善细胞的黏附和增殖,进一步提高骨传导性,促进新骨的形成[73-74]。利用3D打印技术可制造任意复杂形状、按照实际需求复合不同种类生物材料的支架, 在满足个性化的同时还可精确控制支架的孔径大小、孔径形状、孔隙率等关键参数,有利于细胞增殖和组织再生,从而弥补传统支架存在的缺陷[75]。 2.3.2 4D打印技术在骨组织工程的应用 2014年,麻省理工大学首次展示了4D打印技术[76]。4D生物打印源于3D生物打印,本质上也是一种三维打印技术,“时间”是其中包含的第四维度。4D打印可以弥补3D打印假定打印对象是无生命的和静态的,并且只考虑其初始条件的局限性,通过模拟自然组织再生中复杂的三维结构、微观结构和微环境,制造各种三维设计的生物活性结构,响应内在或/和外部刺激,从而引起组织构象的动态变化,满足组织再生的需求[77]。 打印支架的形状和功能能随时间的变化而变化,是4D生物打印的两种主要策略[78],这些特性对于支架能够适应并长期维持内环境稳态和促进生物结构的合成更新尤为重要。在过去的许多年里,3D打印技术将生物支架与细胞和生长因子构建组织工程骨治疗骨缺损的研究得到了众多成果,然而仍有许多问题有待解决,如大型不规则骨组织修复的个性化需求,一系列4D打印策略的提出,4D打印产物的形状转换特征有望解决当前骨组织工程的挑战[79-80]。各种刺激响应性形状恢复聚合物,作为骨组织工程的合适支架和可注射水凝胶已被广泛研究[81]。 用于4D打印的智能材料是实现支架形状和功能动态变化的根本,刺激响应生物材料为影响物体的控制形状转换提供了更精细的策略[82]。形状记忆合金属于智能聚合物,由于物理或化学交联,它可以“记住”永久的形状,这使得它们可以暂时变形,并在外部刺激下回到原来的形状[83],如图3。形状记忆合金属于固态智能材料,细胞只能接种在材料表面,而不能均匀地分散在材料内部,因此,负载细胞的形状记忆水凝胶被开发出来,其可以实现结构和功能的可逆和依序变化[84-86]。智能水凝胶的典型形状记忆行为是通过聚合物网络内亲水链段的可逆水化实现的,从而形成临时交联形成或裂解。智能材料结合4D打印所制备的生物支架动态变化是由内/外部刺激控制的,因此根据刺激类型将其分为物理、化学和生物响应性刺激响应材料。"

在生物打印智能材料的结构中,实现材料变形最常用的物理刺激是温度,目前已有热响应性可注射多糖水凝胶被研发,在骨组织工程中充当载体角色,与种子细胞、生长因子或人工合成高分子聚合物进行复合[87- 88]。4D打印结构的动态形变特征不仅可以满足不同个体骨缺损修复的个性化需求,还可以配合骨生成和支架降解的动态平衡,因此越来越多的研究将4D打印支架应用于骨缺损[89-90]。SENATOV等[91]以聚乳酸和羟基磷灰石为材料打印出一种具有形状记忆功能的多孔骨支架,对其热学性能、力学性能、形状记忆效应进行分析发现,该支架的形状记忆恢复率高达98%,可作为自体植入物用于修复较小的骨缺损。董学明[92]基于形状记忆聚乳酸材料,成功通过4D打印技术分别制备了聚乳酸/Fe3O4和聚乳酸/Fe3O4/羟基磷灰石形状记忆多孔支架,以及聚乳酸/Fe3O4/羟基磷灰石/阿仑膦酸钠和聚乳酸/Fe3O4/羟基磷灰石/阿仑膦酸钠-胶原/地塞米松载药形状记忆多孔支架,体内、外实验结果表明,多孔支架均具有良好的热力学性能、药物释放行为、形状记忆性能,且固定率和回复率均在98%以上,可实现大尺寸变形;制备的多孔支架均能提高骨髓间充质干细胞的增殖数量;4D打印制备的新型载药形状记忆多孔支架,将药物缓控释和快速释放体系与生物支架良好地结合起来,可以有效促进骨修复。ARONSSON等[93]以可生物降解的水基形状记忆聚氨酯作为主要成分制备了可作为骨组织工程定制化骨替代物的打印支架,由于其不仅具有生物降解性和形状记忆性能,还具有良好的成骨性能,因此常应用于微创外科手术。目前4D生物打印的相关研究为将来其在组织工程中应用提供了依据,4D生物打印技术与智能材料共同发展、互相结合为将来骨缺损的高效修复提供了可能,同时可展示了4D生物打印在骨组织工程的巨大潜力[89-90]。 2.4 骨缺损修复的挑战 推动生物支架材料和生物打印技术的发展,被众多研究人员认为是将来高效解决骨缺损修复问题的主要方向。近年来,随着组织工程技术的成熟及对骨再生机制的深入了解,智能材料结合打印技术制备仿生支架引起人们的关注,组织工程技术通过仿生学原理模仿天然骨的成分及结构特征,成为目前骨缺损修复的前沿课题。不同的生物材料及治疗方式在骨缺损修复上仍面临许多挑战以待解决。 自体骨移植具有取材于自身的独特优势,临床应用广泛,被誉为骨缺损修复的 “金标准”,但也存在相关并发症(增加创伤、供区疼痛血肿、切口感染等),同时也受到“供量”不足的影响。同种异体骨来源充足、结构类似自体骨、排斥反应低等优点成为骨缺损修复的备选材料之一,但存在疾病交叉感染的风险,如果彻底灭活消毒处理又会影响其生物性能,成骨能力下降,如何在有效降低抗原性的前提下尽可能地保留材料理化性质和组织细胞活性,是当前所面临的问题以及研究的重点。人工合成材料可通过控制加工时的关键参数使其具备可控的形状、孔隙率和降解速度,因此在骨缺损修复中具有个性化的优势,然而,材料种类众多,单一材料性能有限,如何优化材料功能和结构,探索发现新的材料,以达到提高材料的组织相容性、生物活性、力学性能及可降解性,是骨修复材料的发展方向。 生物支架的打印技术在应用中同样面临挑战,3D打印直接将材料与细胞、生长因子等混合打印,如何使细胞或生长因子保持稳定、不失去活性却是一个难题;此外,有时在修复骨和软骨的缺损时,需要整合的细胞类型不止一种,因此,3D 生物打印过程中如何满足不同类型细胞和组织的同时生长和分化的需求也是一个问题。4D打印技术作为新兴技术,它的出现可能推动组织工程的发展达到一个新的高度,但是目前仍处于起步阶段,面临着更多的挑战:面对人体多种复杂刺激信号,单一刺激响应智能材料无法做出多种反应;简单的形状转换无法满足人体应用的复杂需求;打印制备的支架形态反复变化时无法维持其力学性能。"

| [1] EL-RASHIDY AA, ROETHER JA, HARHAUS L, et al. Regenerating bone with bioactive glass scaffolds: A review of in vivo studies in bone defect models. Acta Biomater. 2017;62:1-28. [2] KARALASHVILI L, KAKABADZE A, UHRYN M, et al. Bone grafts for reconstruction of bone defects (REVIEW). Georgian Med News. 2018;282: 44-49. [3] BALDWIN P, LI DJ, AUSTON DA, et al. Autograft, Allograft, and Bone Graft Substitutes: Clinical Evidence and Indications for Use in the Setting of Orthopaedic Trauma Surgery. J Orthop Trauma. 2019;33(4):203-213. [4] HOLZAPFEL BM, RUDERT M, HUTMACHER DW.[Scaffold-based Bone Tissue Engineering]. Der Orthopade. 2017;46(8):701-710. [5] CUNNIFFE GM, DÍAZ-PAYNO PJ, RAMEY JS, et al. Growth plate extracellular matrix-derived scaffolds for large bone defect healing. Eur Cell Mater. 2017;33:130-142. [6] WUBNEH A, TSEKOURA EK, AYRANCI C, et al. Current state of fabrication technologies and materials for bone tissue engineering. Acta Biomater. 2018;80:1-30. [7] FENG Y, ZHU S, MEI D, et al. Application of 3D Printing Technology in Bone Tissue Engineering: A Review. Curr Drug Deliv. 2021;18(7):102-111. [8] SHAKIBANIA S, GHAZANFARI L, RAEEZADEH-SARMAZDEH M, et al. Medical application of biomimetic 4D printing. Drug Dev Ind Pharm. 2021;47(4): 521-534. [9] CLEGG JR, WAGNER AM, SHIN SR, et al. Modular Fabrication of Intelligent Material-Tissue Interfaces for Bioinspired and Biomimetic Devices. Prog Mater Sci. 2019;106:100589. [10] GHILAN A, CHIRIAC AP, NITA LE, et al.Trends in 3D Printing Processes for Biomedical Field:Opportunities and Challenges. J Polym Environ. 2020; 28(5):1345-1367. [11] LI BL, LIU L, ZHAO WB, et al. Bottleneck and development trend of bone xenograft for the treatment of bone defect. Zhongguo Gu Shang. 2015; 28(12):1166-1170. [12] KIM JK, YOON JO, BAEK H. Corticocancellous bone graft vs cancellous bone graft for the management of unstable scaphoid nonunion. Orthop Traumatol Surg Res. 2018;104(1):115-120. [13] 殷渠东,顾三军,芮永军,等.松质骨包裹植骨技术治疗长骨节段性骨缺损[J].中华创伤骨科杂志,2017,19(9):775-781. [14] SHARIFI M, KHERADMANDI R, SALEHI M, et al. Criteria, Challenges, and Opportunities for Acellularized Allogeneic/Xenogeneic Bone Grafts in Bone Repairing. ACS Biomater Sci Eng. 2022;8(8):3199-3219. [15] 胡小晓,叶剑平,蒋志勇,等.微创方法结合自体外周血干细胞及同种异体冻干骨载体治疗四肢骨干术后骨不愈合[J].中国骨与关节损伤杂志,2015,30(5):536-537. [16] 李忠杰,李绍波.磷酸钙人工骨修复骨缺损的研究进展[J].生物骨科材料与临床研究,2021,18(4): 87-91. [17] 贾乐,葛建华.Masquelet技术修复骨缺损应用及研究进展[J].西南医科大学学报,2020,43(4):421-424. [18] KLEIN C, MONET M, BARBIER V, et al. The Masquelet technique: Current concepts, animal models, and perspectives. J Tissue Eng Regen Med. 2020; 14(9):1349-1359. [19] ALFORD AI, NICOLAOU D, HAKE M, et al. Masquelet’s induced membrane technique: Review of current concepts and future directions. J Orthop Res. 2021;39(4):707-718. [20] 王有为.Masquelet技术与骨移植治疗感染性骨缺损的临床效果分析[J].中外医学研究,2022,20(11):151-154. [21] 黄旋平,谢庆条,江献芳,等.慢病毒载体介导的基因治疗在骨缺损修复中的研究进展[J].中国矫形外科杂志,2014,22(14):1284-1287. [22] 刘亚军,张先启,官建中.骨折愈合的基因治疗进展[J].医学综述,2015, 21(10):1796-1799. [23] GUAN J, ZHANG J, ZHU Z, et al. Bone morphogenetic protein 2gene transduction enhances the osteogenic potential of human urine-derived stem cells. Stem Cell Res Ther. 2015;6(1):5. [24] BAKHSHANDEH B, ZARRINTAJ P, OFTADEH MO, et al. Tissue engineering; strategies, tissues, and biomaterials. Biotechnol Genet Eng Rev. 2017;33(2): 144-172. [25] 周思佳,姜文学,尤佳.骨缺损修复材料:现状与需求和未来[J].中国组织工程研究与临床康复,2018,22(14):2251-2258. [26] ATLAS Y, GORIN C, NOVAIS A, et al. Microvascular maturation by mesenchymal stem cells in vitro improves blood perfusion in implanted tissue constructs. Biomaterials. 2021;268:120594. [27] NULTY J, FREEMAN FE, BROWE DC, et al. 3D bioprinting of prevascularised implants for the repair of critically-sized bone defects. Acta Biomater. 2021; 126:154-169. [28] FILIPOWSKA J, TOMASZEWSKI KA, NIEDŹWIEDZKI Ł, et al. The role of vasculature in bone development, regeneration and proper systemic functioning. Angiogenesis. 2017;20(3): 291-302. [29] 黄孟全,樊简,马子扬,等.预血管化多孔β-磷酸三钙组织工程骨的构建及其生物学效应评价[J].中国修复重建外科杂志,2022,36(5):625-632. [30] GAO Q, ZHU X, XIANG J, et al. [Strategies to choose scaffold materials for tissue engineering]. Sheng Wu Gong Cheng Xue Bao. 2016;32(2): 172-184. [31] FU M, WANG F, LIN G. Design and research of bone repair scaffold based on two-way fluid-structure interaction. Comput Methods Programs Biomed. 2021;204:106055. [32] CHEN FM, LIU XH. Advancing biomaterials of human origin for tissue engineering. Prog Polym Sci. 2016;53:86-168. [33] CHEN G, LV Y, DONG C, et al. Effect of internal structure of collagen/hydroxyapatite scaffold on the osteogenic differentiation of mesenchymal stem cells. Curr Stem Cell Res Ther. 2015;10(2):99-108. [34] ZHOU YY, YAO HC, WANG JS, et al. Greener synthesis of electrospun collagen/hydroxyapatite composite fibers with an excellent microstructure for bone tissue engineering. Int J Nanomedicine. 2015;10:3203-3215. [35] 赵少华,菅炎鹏, 王一公,等.具有抗炎作用的载双氯芬酸钠明胶多孔支架促进体内软骨再生研究[J].中国修复重建外科杂志,2023,37(1):91-100. [36] 常思佳,杨柳,李冉.明胶-羟基磷灰石-磷酸三钙支架对hDPSCs的成骨刺激作用[J].上海口腔医学,2020,29(5):492-498. [37] ZANG SQ, ZHU L, LUO KF, et al. Chitosan composite scaffold combined with bone marrow-derived mesenchymal stem cells for bone regeneration: in vitro and in vivo evaluation. Oncotarget. 2017;8(67):110890. [38] 崔升,袁美玉,付俊杰,等.抗菌用壳聚糖及其金属粒子复合材料研究进展[J].精细化工,2021,38(9):1757-1764+1778. [39] 李扬,刘怡卓,沈超,等.生物玻璃/壳聚糖三维多孔支架的抗感染性能和生物相容性研究[J].生物骨科材料与临床研究,2020,17(2):49-54. [40] YANG Y, CHU LY, YANG SB, et al. Dual-functional 3D-printed composite scaffold for inhibiting bacterial infection and promoting bone regeneration in infected bone defect models. Acta Biomater. 2018;79:265-275. [41] 陈亮.丝素蛋白支架在骨组织工程中的应用进展[J].中华骨科杂志, 2016,14(36): 932-937. [42] 贾明鲲,闫景龙.生物可降解丝素蛋白在骨科中的应用与进展[J].北京生物医学工程,2021,40(6):629-634. [43] ZHANG HT, CHENG JQ, AO Q. Preparation of Alginate-Based Biomaterials and Their Applications in Biomedicine. Mar Drugs. 2021;19(5):264-264. [44] 张汉波,张睿凌,王汉虎,等.藻酸盐水凝胶的研究进展[J].药学与临床研究,2022,30(4):347-351+358. [45] 练胜.藻酸盐凝胶细胞微球与双相磷酸钙陶瓷复合修复骨缺损的研究[D].南昌:南昌大学,2021. [46] 耿丽鑫,甘洪全,王茜,等.国产多孔钽对成骨细胞生物相容性及其相关成骨基因表达的影响[J].第三军医大学学报,2014,36(11):1163-1167. [47] 吴海啸,张超,GORYAEVA GL,等.β-TCP/α-CSH复合材料骨支架在骨缺损治疗中的应用研究进展[J].山东医药,2016,56(32):104-106. [48] HIEP TN, KHON H, HAI ND, et al. Biocompatibility of PCL/PLGA-BCP porous scaffold for bone tissue engineering applications. J Biomater Sci Polym Ed. 2017;28(9):864-878. [49] MOATAZ AE, KIM KH, PARK JW, et al. Hydrolytic degradation of polylactic acid (PLA) and its composites. Renew Sustain Energy Rev. 2017;79:1346-1352. [50] 李雪雯,刘尧,李波.生物支架材料在骨组织工程中的应用[J].中国医科大学学报,2019,48(11):1024-1028. [51] CASTRO AG, POLINI A, AZAMI Z, et al. Incorporation of PLLA micro-fillers for mechanical reinforcement of calcium-phosphate cement. J Mech Behav Biomed. 2017;71:286-294. [52] 石永新,逄增金,羊明智,等.3D打印技术制备聚磷酸钙/淫羊藿苷骨支架诱导骨髓间充质干细胞成骨分化治疗骨缺损[J].中国组织工程研究,2019,23(21):3309-3315. [53] 张焕超,吕玉强,王茜,等.金属材料修复临界性骨缺损的实验研究进展[J].安徽医药,2019,23(7):1273-1276. [54] 芮敏,郑欣,张云庆,等.3D打印多孔钛合金支架修复兔桡骨骨缺损[J].中国组织工程研究,2019,23(18):2789-2793. [55] 彭琳晶,干耀恺,姚怡飞.多孔钽植入物在骨缺损中的应用进展[J].材料工程,2022,50(11):1-13. [56] 张倩,节云峰,朱璨,等.生物活性多孔钽骨修复材料促骨生长的实验研究[J].第三军医大学学报,2016,38(11):1245-1250. [57] 党莹,李月,李瑞玉,等.骨组织工程支架材料在骨缺损修复及3D打印技术中的应用[J].中国组织工程研究,2017,21(14):2266-2273. [58] 郑健茂,毛学理,凌均棨.镁基支架及其在动物骨缺损修复中的应用[J].国际口腔医学杂志,2015,42(6):720-723. [59] 廖欣宇,王福科,王国梁.骨组织工程支架的进展与挑战[J].中国组织工程研究,2021,25(28):4553-4560. [60] 刘星纲,邓旭亮,邹超,等.多孔β-磷酸三钙/胶原支架修复兔下颌牙槽骨缺损的实验研究[J].北京口腔医学,2014,22(1):1-4. [61] 刘欢欢.基于胶原自组装/矿化协同策略制备掺杂生物活性元素的骨组织工程胶原支架[D].天津:天津医科大学,2020. [62] LEE K, SILVA EA, MOONEY DJ. Growth factor delivery-based tissue engineering:general approaches and a review of recent developments. J R Soc Interface. 2011;8(55):153-170. [63] 陈泽驹,冯少龙,刘桂宏,等.基于骨组织工程的骨再生策略[J].中国医药生物技术,2022,17(5):440-444. [64] 燕朋程,王东.3D打印在组织工程骨预制及其骨缺损修复的作用探讨[J].临床医药文献电子杂志,2019,6(12):188. [65] BOSE S, VAHABZADEH S, BANDYOPADHYAY A. Bone tissue engineering using 3D printing. Mater Today. 2013;16(12):496-504. [66] 赵静一, 禹娜娜, 邓平平.骨组织工程支架内微管孔结构的研究现状[J].机床与液压,2011,39(6):113-116. [67] 张旭婧.3D同轴打印组织工程骨支架成型工艺与实验研究[D].乌鲁木齐:新疆大学,2017. [68] REZANIA N, ASADI-EYDIVAND M, ABOLFATHI N, et al. Three-dimensional printing of polycaprolactone/hydroxyapatite bone tissue engineering scaffolds mechanical properties and biological behavior. J Mater Sci Mater Med. 2022;33(3):31. [69] ENTEZARI A, ROOHANI I, LI G, et al. Architectural Design of 3D Printed Scaffolds Controls the Volume and Functionality of Newly Formed Bone. Adv Healthc Mater. 2019;8(1):e1801353. [70] TANG MS, ABDUL KADIR AZ, NGADIMAN NHA. Simulation analysis of different bone scaffold porous structures for fused deposition modelling fabrication process. IOP Conf Ser Mater Sci Eng. 2020;788(1):012023. [71] MURPHY CM, HAUGH MG, O’BRIEN FJ. The effect of mean pore size on cell attachment, proliferation and migration in collagen–glycosaminoglycan scaffolds for bone tissue engineering. Biomaterials. 2009;31(3):461-466. [72] HUNG KS, CHEN MS, LAN WC, et al.Three-Dimensional Printing of a Hybrid Bioceramic and Biopolymer Porous Scaffold for Promoting Bone Regeneration Potential. Materials (Basel). 2022;15(5):1971-1971. [73] 张伟蒙,汪杰,胡晶.3D打印骨组织支架孔隙结构对支架性能影响的研究进展[J].中国塑料,2022,36(12):155-166. [74] MANGIRDAS M, SIMA R, LAURYNAS L, et al. 3D Microporous Scaffolds Manufactured via Combination of Fused Filament Fabrication and Direct Laser Writing Ablation. Micromachines. 2014;5(4):839-858. [75] 吕超凡,朱莉娅,李客楼,等.3D打印在软骨组织损伤修复中的应用进展[J].南京师范大学学报(工程技术版),2017,17(1):12-17. [76] WAN Z, ZHANG P, LIU Y, et al. Four-dimensional bioprinting:Current developments and applications in bone tissue engineering. Acta Biomater. 2020;101:26-42. [77] ZHANG X, YANG Y, YANG Z, et al. Four-Dimensional Printing and Shape Memory Materials in Bone Tissue Engineering. Int J Mol Sci. 2023;24(1):814. [78] WAN Z, ZHANG P, LIU Y, et al. Four-dimensional bioprinting: Current developments and applications in bone tissue engineering. Acta Biomater. 2020;101:26-42. [79] WANG C, YUE H, LIU J, et al. Advanced reconfigurable scaffolds fabricated by 4D printing for treating critical-size bone defects of irregular shapes. Biofabrication. 2020;12(4):045025. [80] CHEN X, HAN S, WU W, et al. Harnessing 4D Printing Bioscaffolds for Advanced Orthopedics. Small. 2022;18(36):e2106824. [81] QASIM M, CHAE DS, LEE NY. Advancements and frontiers in nano-based 3D and 4D scaffolds for bone and cartilage tissue engineering. Int J Nanomedicine. 2019;14:4333-4351. [82] SU M, SONG Y. Printable Smart Materials and Devices: Strategies and Applications. Chem Rev. 2022;122(5):5144-5164. [83] HOLMAN H, KAVARANA MN, RAJAB TK. Smart materials in cardiovascular implants: Shape memory alloys and shape memory polymers. Artificial organs. 2021;45(5):454-463. [84] WU SD, HSU SH. 4D bioprintable self-healing hydrogel with shape memory and cryopreserving properties. Biofabrication. 2021;13(4).doi: 10.1088/1758-5090/ac2789. [85] ZHANG Y, DESAI MS, WANG T, et al. Elastin-Based Thermoresponsive Shape-Memory Hydrogels. Biomacromolecules. 2020;21(3):1149-1156. [86] YING G, JIANG N, PARRA C, et al. Bioprinted Injectable Hierarchically Porous Gelatin Methacryloyl Hydrogel Constructs with Shape-Memory Properties. Adv Funct Mater. 2020;30(46):2003740. [87] 刘若锦,王丽,刘华,等.4D打印用水凝胶在植入性医疗器械领域的研究进展[J].中国医疗器械杂志,2021,45(5):524-529. [88] GRAHAM S, MARINA PF, BLENCOWE A. Thermoresponsive polysaccharides and their thermoreversible physical hydrogel networks. Carbohydr Polym. 2019;207:143-159. [89] 关健,贾燕飞,张葆鑫,等.4D生物打印在组织工程的应用[J].中国组织工程研究,2022,26(3):446-455. [90] 党竞医,朱东泽,刘鑫成,等.4D打印技术的医学应用与展望[J].解放军医学杂志,2021,46(6):598-602. [91] SENATOV FS, NIAZA KV, ZADOROZHNYY MY, et al. Mechanical properties and shape memory effect of 3D-printed PLA-based porous scaffolds. J Mech Behav Biomed Mater. 2016;57:139-148. [92] 董学明.4D打印载药形状记忆多孔聚乳酸复合支架用于骨组织修复[D].哈尔滨:哈尔滨商业大学,2020. [93] ARONSSON C, JURY M, NAEIMIPOUR S, et al. Dynamic peptide-folding mediated biofunctionalization and modulation of hydrogels for 4D bioprinting. Biofabrication. 2020;12(3):035031. |
| [1] | Dai Jing, Liu Shasha, Shen Mingjing. Exosome-loaded injectable hydrogel for repairing bone defects around implants [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(3): 347-354. |
| [2] | Gu Mingxi, Wang Changcheng, Tian Fengde, An Ning, Hao Ruihu, Guo Lin. Preparation and in vitro evaluation of a three-dimensional porous cartilage scaffold made of silk fibroin/gelatin/chitosan [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(3): 366-372. |
| [3] | Wang Xinmin, Yan Wenkai, Song Yahui, Liu Fei. Leukocyte- and platelet-rich fibrin with autologous hamstring tendon for traumatic patella dislocation [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(3): 404-410. |
| [4] | Bi Yujie, Ma Dujun, Peng Liping, Zhou Ziqiong, Zhao Jing, Zhu Houjun, Zhong Qiuhui, Yang Yuxin. Strategy and significance of Chinese medicine combined with medical hydrogel for disease treatment [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(3): 419-425. |
| [5] | Wang Xinyi, Xie Xianrui, Chen Yujie, Wang Xiaoyu, Xu Xiaoqing, Shen Yihong, Mo Xiumei. Electrospun nanofiber scaffolds for soft and hard tissue regeneration [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(3): 426-432. |
| [6] | Gao Xueyu, Zhang Wentao, Sun Tianze, Zhang Jing, Li Zhonghai. Application of metal ions in bone tissue engineering [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(3): 439-444. |
| [7] | Yang Jie, Hu Haolei, Li Shuo, Yue Wei, Xu Tao, Li Yi. Application of bio-inks for 3D printing in tissue repair and regenerative medicine [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(3): 445-451. |
| [8] | Chen Pinrui, Pei Xibo, Xue Yiyuan. Function and advantages of magnetically responsive hydrogel in bone tissue engineering [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(3): 452-457. |
| [9] | Chen Junyan, Meng Qingqi, Li Siming. Cartilage targeting function in the drug delivery system by intra-articular injection for the treatment of osteoarthritis [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(3): 458-463. |
| [10] | Long Zhirui, Huang Lei, Xiao Fang, Wang Lin, Wang Xiaobei. Characteristics of hydrogel microspheres in bone tissue engineering [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(3): 472-478. |
| [11] | Xu Jing, Lyu Huixin, Bao Xin, Zhang Yi, Wang Yihan, Zhou Yanmin. Application of near infrared responsive hydrogels in tissue engineering [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(3): 486-492. |
| [12] | Fan Yongjing, Wang Shu, Jin Wulong. Characteristics, advantages and application of osteogenic differentiation of jaw bone marrow mesenchymal stem cells [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(1): 100-106. |
| [13] | Sun Kexin, Zeng Jinshi, Li Jia, Jiang Haiyue, Liu Xia. Mechanical stimulation enhances matrix formation of three-dimensional bioprinted cartilage constructs [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(在线): 1-7. |
| [14] | He Wanyu, Cheng Leping. Strategies and advance on stem cell transplantation for repair of spinal cord injury [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(在线): 1-7. |
| [15] | Wen Xinghua, Ding Huanwen, Cheng Kai, Yan Xiaonan, Peng Yuanhao, Wang Yuning, Liu Kang, Zhang Huiwu. Three-dimensional finite element model analysis of intramedullary nailing fixation design for large femoral defects in Beagle dogs [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(9): 1371-1376. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||