Chinese Journal of Tissue Engineering Research ›› 2024, Vol. 28 ›› Issue (3): 439-444.doi: 10.12307/2023.972
Previous Articles Next Articles
Application of metal ions in bone tissue engineering
Gao Xueyu1, 2, Zhang Wentao2, Sun Tianze2, Zhang Jing2, Li Zhonghai2
- 1Qilu Medical University, Zibo 255300, Shandong Province, China; 2Department of Orthopedics, First Affiliated Hospital of Dalian Medical University, Dalian 116011, Liaoning Province, China
-
Received:2022-11-23Accepted:2023-01-13Online:2024-01-28Published:2023-07-10 -
Contact:Li Zhonghai, MD, Professor, Chief physician, Department of Orthopedics, First Affiliated Hospital of Dalian Medical University, Dalian 116011, Liaoning Province, China -
About author:Gao Xueyu, Qilu Medical University, Zibo 255300, Shandong Province, China; Department of Orthopedics, First Affiliated Hospital of Dalian Medical University, Dalian 116011, Liaoning Province, China -
Supported by:Dalian Science and Technology Innovation Fund Application Foundation Project, No. 2022JJ12SN045 (to LZH)
CLC Number:
Cite this article
Gao Xueyu, Zhang Wentao, Sun Tianze, Zhang Jing, Li Zhonghai. Application of metal ions in bone tissue engineering[J]. Chinese Journal of Tissue Engineering Research, 2024, 28(3): 439-444.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
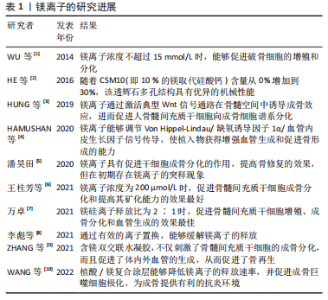
2.1 镁 镁元素参与骨组织形成、骨代谢和骨矿物结晶等生理过程,可促进细胞成骨分化与骨矿化,有利于骨缺损部位的修复;缺乏镁离子会加快骨量丢失,不利于骨的修复与再生。与其他金属植入物相比,镁合金和多孔镁的机械性能更接近天然骨,但镁合金的降解速度较快,降解过程中会产生较多氢气,且低浓度的镁离子具有促进破骨细胞分化的作用,因此,镁离子的作用在骨组织工程中具有比较大的争议。 WU等[1]研究了镁离子浓度对人破骨细胞的影响,实验发现,当镁离子浓度不超过15 mmol/L时,能够促进破骨细胞的增殖和分化;镁离子浓度大于15 mmol/L时,随着浓度的增加抑制破骨细胞的增殖和分化。HE等[2]通过镁取代硅灰石,利用3D打印技术开发了基于透辉石的多孔生物陶瓷复合材料,实验结果表明,随着CSM10(即10%的镁取代硅酸钙)含量从0%增加到30%,新型CSM10增强的透辉石多孔结构具有优异的机械性能。HUNG等[3]的研究发现,镁离子通过激活典型Wnt信号通路在骨髓空间中诱导成骨效应,进而促进人骨髓间充质干细胞向成骨细胞谱系分化。HAMUSHAN等[4]通过实验发现,高纯度镁植入物具有良好的力学性能,进一步测试发现其释放的镁离子能够调节Von Hippel-Lindau/缺氧诱导因子1α/血管内皮生长因子信号传导,使植入物获得增强血管生成和促进骨形成的能力。潘昊田[5]通过Pickering乳液法制备了负载MgO纳米颗粒的甲基丙烯酸酐化明胶-co-聚乙二醇大孔复合水凝胶,实验结果表明该水凝胶支架可调控细胞增殖和成骨分化等行为,而镁离子的释放具有显著促进干细胞成骨分化的作用,提高骨修复的效果,但在该支架的离子释放行为实验中发现,初期存在镁离子的突释现象。王桂芳等[6]通过对照实验发现,当镁离子浓度不超过400 μmol/L时,不会影响骨髓间充质干细胞的增殖,并且可以促进骨髓间充质干细胞成骨分化和提高其矿化能力,此外,该促进效果在镁离子浓度为200 μmol/L时最好。万卓[7]制备出镁硅离子共释放微球,研究发现该微球具有促进骨髓间充质干细胞增殖和成骨分化的作用,还能促进血管生成;并测定出镁硅离子释放比为2∶1时,该微球促进骨再生的效果最佳。李彪等[8]制备出含镁脱细胞牛骨基质,检测结果显示镁离子未对牛骨基质的微观结构、力学性能产生明显影响,而且通过有效的离子置换能够缓解镁离子的释放。ZHANG等[9]制备出一种能够稳定降解的含镁双交联水凝胶,实验结果表明镁离子的引入不仅刺激了骨髓间充质干细胞的成骨分化,而且促进了体内外血管的生成,从而促进了骨再生。WANG等[10]将植酸/镁离子复合物涂覆在聚醚醚酮纤维上,该复合物优化了聚醚醚酮纤维的表面性能,并有效降低了镁离子的释放速率;此外,具有植酸/镁复合涂层的聚醚醚酮纤维能通过刺激抗炎细胞因子的产生,促进成骨巨噬细胞极化,为成骨提供了有利的抗炎环境。 在修复材料中,掺入镁离子可以提高材料的骨修复性能,但低浓度的镁离子能促进破骨细胞的分化,因此限制了镁离子在骨组织工程中的应用(表1)。镁合金多孔支架虽然拥有很多优势,但其过快的降解速率仍然是一个亟待解决的问题。目前镁离子促进骨再生已得到广泛认可,而其对破骨细胞的作用机制和促进血管生成的途径尚不完全明确,缺少大量实验佐证,还需进一步研究。"
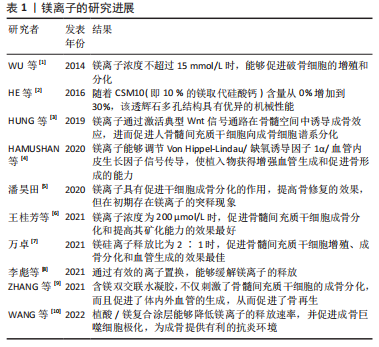
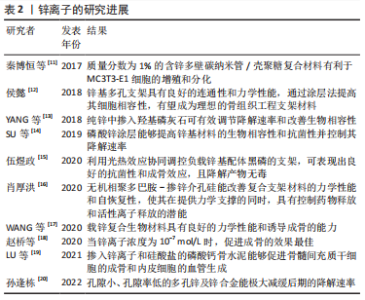
2.2 锌 锌元素是维持人体正常工作、转运所必需的微量元素,对人的生长和发育起着重要调节作用。锌离子具有促进成骨细胞生成、提高成骨细胞活性和增强组织矿化的能力。与镁合金相比,锌合金更易加工且降解性能更好,降解时无气体产生,是一种理想的生物活性支架材料。 秦博恒等[11]将MC3T3-E1细胞接种于含锌离子的多壁碳纳米管/壳聚糖复合材料表面,经过培养检测发现,质量分数为1%的含锌复合材料更有利于MC3T3-E1细胞的增殖分化。侯懿[12]通过研究发现,锌基多孔支架具有良好的连通性和力学性能,但该支架在10%浓度的浸提液中展现出较高的细胞毒性,通过涂层法提高其细胞相容性,锌基多孔支架有望成为更为理想的骨组织工程支架材料。YANG等[13]的研究发现,纯锌中掺入羟基磷灰石可有效调节降解速率和改善生物相容性,细胞实验表明,与纯锌相比,掺锌羟基磷灰石复合材料的细胞相容性显著提高;体内实验表明,羟基磷灰石的加入可延长植入时间,提高成骨性能。SU等[14]采用简单的化学转化法在锌基材料上制备了磷酸锌涂层,磷酸锌涂层能够调控含锌生物材料的降解速率,并显著改善了含锌生物材料的血液相容性、细胞相容性和抗菌性能。伍煜政[15]制备出稳定性良好的锌基配体黑磷并将其负载在支架表面,利用其光热效应协同调控,该支架表现出良好的抗菌性和成骨效应,且降解产物无毒,在骨组织工程中具有一定的应用价值。肖厚洪[16]通过紫外光自由基聚合法和原位释放法制备了海藻酸-聚乙二醇二丙烯酸酯-聚多巴胺-掺锌介孔硅(SA-PEGDA-PDA-MSN-Zn)水凝胶-介孔硅复合支架材料,研究表明无机相PDA-MSN-Zn的加入改善了该复合支架材料力学性能和自恢复性,使其在提供力学支撑的同时,具有控制药物释放和活性离子释放的潜能。WANG等[17]通过动物实验发现,载锌复合生物材料具有良好的力学性能和诱导成骨的能力,然而,需要进一步确定锌离子浓度以实现更好的骨再生。赵桥等[18]通过研究发现,锌离子能促进骨髓间充质干细胞的增殖和成骨分化,并且可以通过诱导碱性磷酸酶表达来促进组织矿化;当锌离子浓度为10-7 mol/L时其促进成骨的效果最佳。LU等[19]将锌离子和硅酸盐共掺入磷酸钙骨水泥中,能提高磷酸钙骨水泥的机械性能,为免疫细胞提供合适的微环境,并且能够促进骨髓间充质干细胞的成骨和内皮细胞的血管生成。孙逢栋[20]采用渗流铸造法制备出不同孔径大小、不同孔隙率的多孔锌及锌合金,通过浸泡实验证明孔隙小、孔隙率低的多孔锌及锌合金能极大减缓后期的降解速率,该发现对控制锌基支架稳定释放锌离子起到了一定的帮助。 锌离子可以提高骨组织工程材料的生物相容性和抗菌性,能促进骨髓间充质干细胞成骨分化和内皮细胞血管生成。锌合金作为可降解医用金属材料,具有适中的降解速率,释放低浓度的锌离子促进成骨,将锌合金用于骨组织工程,有望成为骨缺损修复的一种新途径(表2)。但锌及锌合金的力学性能较差,质地较软难以塑型,因此在临床的应用中受到限制[21-23]。锌离子在应用研究中存在许多问题,锌离子在细胞内的作用机制缺少实验验证,锌基支架植入体内后生物相容性、降解行为以及骨修复性能还需进一步的研究。"
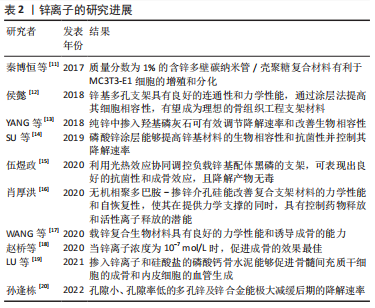
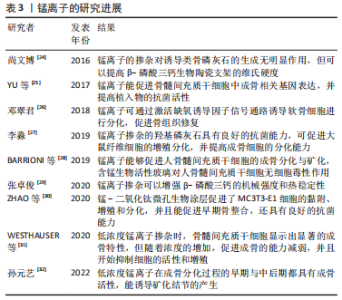
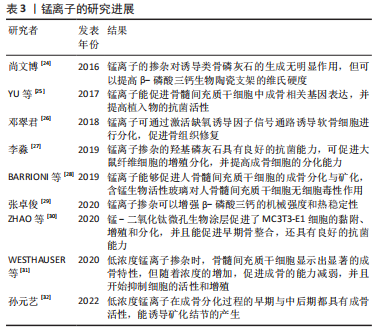
2.3 锰 锰元素是人体正常生理活动中必不可少的微量元素,与多种生理功能有关,是人体内多种酶的辅助因子,能维持正常的代谢过程,还能刺激免疫细胞增殖,增强人体的免疫力。锰离子具有良好的生物相容性,能够促进硫酸软骨素的合成,发挥促进软骨细胞外基质合成的作用。研究表明,将锰离子掺入生物材料,能够改善材料的力学性能并赋予其一定的抗菌性,同时锰离子还能够改善材料的耐腐蚀性,增强其降解性能,提高材料的生物相容性,进一步提升生物材料诱导成骨的活性。与镁离子、锌离子和锶离子等近些年研究较多的金属离子相比,锰离子是骨组织工程材料研究领域中的后起之秀。 尚文博[24]采用溶胶-凝胶法成功制备了锰掺杂的β-磷酸三钙材料,并采用致孔剂法制备了多孔支架,结果表明锰离子的掺杂对诱导类骨磷灰石的生成无明显作用,但可以提高β-磷酸三钙生物陶瓷支架的维氏硬度。YU等[25]将大鼠骨髓间充质干细胞置于含锰离子的植入物表面进行培养,通过观察发现,大鼠骨髓间充质干细胞的成骨相关基因表达和胶原沉积率增加;与不含锰离子的植入物相比,含锰离子的植入物抗菌活性更强。邓翠君[26]采用化学沉淀法制备了锰离子掺杂的β-磷酸三钙材料,并利用3D打印技术制备了骨-软骨一体化支架,体内植入实验结果表明,锰离子可通过激活缺氧诱导因子信号通路诱导软骨细胞进行分化,促进骨组织修复。李淼[27]通过水热法制备锰离子掺杂的羟基磷灰石,研究发现,这种材料对金黄色葡萄球菌和大肠杆菌有90%以上的抗菌能力,可以促进大鼠纤维细胞的增殖分化,并提高成骨细胞的分化能力。BARRIONI等[28]用摩尔比4.4%的氧化锰代替58S生物活性玻璃中的氧化钙,研究发现含锰生物活性玻璃对人骨髓间充质干细胞无细胞毒性作用,并能持续释放锰离子,从中释放的锰离子能够促进人骨髓间充质干细胞的成骨分化与矿化,锰离子掺入为获得具有优异骨再生性能的材料提供了帮助。张卓俊[29]采用氯化锰作为锰源制备了锰离子掺杂β-磷酸三钙的材料,通过检测表明锰离子掺杂会使材料粉体颗粒之间黏结作用加强,出现烧结颈,该现象证明了锰离子掺杂的助烧结作用;随着锰离子掺杂浓度的提高,β-磷酸三钙生成温度会降低,证明锰离子掺杂可以增强β-磷酸三钙的热稳定性。ZHAO等[30]制备出锰-二氧化钛微孔生物涂层,实验发现该涂层促进了MC3T3-E1细胞的黏附、增殖和分化,并且能促进早期骨整合;经过初步研究发现,该涂层可以在体外抑制大肠杆菌的生长,显示出可靠的抗菌能力。WESTHAUSER等[31通过研究不同浓度的锰掺杂介孔生物活性玻璃纳米颗粒,结果显示,低浓度锰离子掺杂时,骨髓间充质干细胞显示出显著的成骨特性,但随着浓度的增加,纳米颗粒促进成骨的能力减弱,并且开始抑制细胞的活性和增殖。孙元艺[32]通过低温沉积3D打印技术制备出聚乳酸/二氧化锰复合支架,测试发现复合支架降解产物的主要成分——低浓度锰离子,在成骨分化过程的早期与中后期都具有成骨活性,能诱导矿化结节的产生。 锰离子促进成骨的机制和在人体内的代谢途径尚未达成共识,且其在材料中的应用比例带来的一系列问题还未解决。相应浓度的锰离子具有促进成骨的作用,但有研究显示人体摄入过量的锰离子会损伤神经系统[33-35]。近年来,将锰离子应用于骨组织工程的研究相对较少,锰离子的作用机制和功能缺少大量实验验证,其临床应用还需进一步探索(表3)。"

2.4 锶 锶是人体的必需微量元素,是骨组织的重要组成成分。锶离子能够促进成骨细胞的增殖分化,抑制破骨细胞的活性,并具有促进骨缺损部位血管再生的作用。锶不仅拥有良好的生物学性能,还能够改善骨组织工程材料的理化性能。有研究表明,在生物活性材料中掺入锶离子能使材料的机械强度更接近骨组织,显著提高了生物活性材料在骨缺损处的稳定性,保证了材料的修复效果。 王成健[36]将氧化锶掺入羟基磷灰石,经研究发现该复合材料的力学性能优于羟基磷灰石,且无细胞毒性,还能对成骨细胞的增殖分化起到促进作用,通过实验确定了含锶量3%-7%的复合材料具有最优的性能。GAO等[37]将聚γ-谷氨酸和锶盐掺入基于α-磷酸三钙的磷酸钙骨水泥中,检测结果表明,含有质量分数8.9%γ-谷氨酸的掺锶磷酸钙骨水泥比纯磷酸钙骨水泥具有更好的细胞相容性和机械抗压强度。由于锶具有促进成骨细胞增殖、抑制破骨细胞分化的作用,RIEDEL等[38]通过研究进一步发现,用含锶药物治疗骨质疏松症能有效改善骨的微观结构和力学特性。张文等[39]通过实验发现,巨噬细胞极化能促进骨髓间充质干细胞的成骨分化,在骨组织修复中发挥了巨大作用,并且确定了摩尔比10%掺锶量的微纳米生物活性玻璃对巨噬细胞极化的促进效果最好。ZHANG等[40]以尼龙筛为模板,成功地复制了锶离子掺杂生物陶瓷的有序微观形貌,结果表明,锶离子的掺杂可促进骨髓间充质干细胞的细胞黏附、碱性磷酸酶活性和成骨分化。NARUPHONTJIRAKUL等[41]通过实验发现,球形含锶生物活性纳米颗粒能刺激骨髓间充质干细胞沿成骨途径分化,并加速矿化的早期、中期和晚期;含锶生物活性纳米颗粒具有促进骨再生或治疗骨质疏松等病症的潜力,因为它们能够通过颗粒局部降解持续向细胞释放促进成骨的锶离子。LINO等[42]通过体内外实验发现,含1%锶离子的聚ε-己内酯和富马酸聚二异丙酯的增容共混物能释放少量锶离子,因此不会对心血管造成不良影响,并且对巨噬细胞没有细胞毒性,能显著增加骨组织再生并改善纤维桥接,同时不会诱导局部炎症反应。YE等[43]成功制备了长期释放锶离子的新型锶-氧化石墨烯纳米复合材料增强型胶原支架,实验发现该结构显著增强了支架的理化与机械性能,为成骨提供了良好的微环境,并显著促进了大鼠颅骨缺损模型体内血管化骨再生。赵德路等[44]通过增加锶离子的浓度来观察携锶离子光交联海藻酸盐水凝胶支架的性能变化,结果发现锶离子能够提高支架的机械性能,并且有利于MC3T3-E1细胞在支架表面的黏附和伸展。SUN等[45]的研究发现,锶能通过降低诱导破骨细胞分化的核因子κB受体活化因子配体的水平,从而直接抑制破骨细胞的分化;进一步研究发现,锶还能增强MC3T3-E1细胞中的低密度脂蛋白受体相关蛋白6/β-连环蛋白/骨保护素信号通路,间接抑制核因子κB受体活化因子配体诱导的破骨细胞分化。刘欢欢[46]通过实验发现,在胶原支架中掺入锶能够促进骨髓间充质干细胞增殖分化,并且可以通过调控巨噬细胞极化来调节机体免疫反应,进而促进骨再生,该支架有望做为免疫调节材料用于治疗骨缺损。 锶离子在骨组织工程中的各种实验研究已经取得重大突破,已有含锶药物用于治疗骨质疏松,但锶的最佳摄入量还有待研究(表4)。目前,锶离子的成骨机制尚无公认的理论,相应理论还处于实验验证阶段,需要大量基础实验进一步说明。"

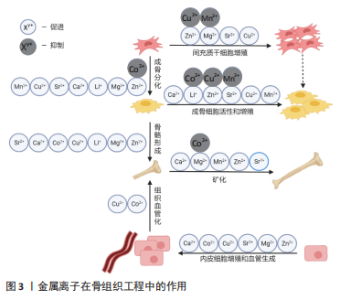
WANG等[49]制造出生物玻璃-铜支架,实验发现该支架使铜离子的释放更加稳定,促进血管生成的效果更好。施孟超[50]制备出含铜介孔氧化硅纳米球材料,实验发现该材料能够刺激巨噬细胞分泌炎症因子,将产生的炎症因子用于培养骨髓间充质干细胞,并能促进骨髓间充质干细胞中成骨基因的表达,提高其矿化水平,抑制破骨细胞分化,该材料有望成为一种免疫调节材料促进成骨。ZHOU等[51]将铜离子引入介孔生物活性玻璃中,激活缺氧诱导因子1α,诱导内皮生长因子表达,刺激人脐静脉内皮细胞的迁移,为早期血管形成提供了正反馈回路;同时,还引发了组织再生巨噬细胞亚型,促进血管形成和血管生成基因表达。刘静[52]制备出含铜介孔生物活性玻璃/海藻酸钠复合抗菌骨组织工程支架,经实验发现该支架具有较好的抗菌性能、生物活性和体外矿化能力,同时对MC3T3-E1细胞的增殖表现出明显的促进作用。LI等[53]通过检测不同细胞系和细菌在不同浓度铜离子中的反应发现,人脐静脉内皮细胞、MC3T3-E1细胞和大鼠骨髓间充质干细胞的铜离子IC50值分别接近327.9,134.6,0.7 μmol/L;此外,铜离子的有效抑菌阈值浓度为37 μmol/L,当铜离子浓度超过阈值时抗菌活性会显著增加。王新等[54]对海藻酸盐进行铜离子光双交联,经过实验发现,通过调控铜离子的浓度能够增强光交联海藻酸盐水凝胶的机械强度,并且MC3T3-E1细胞能在支架中存活,受铜离子的影响,MC3T3-E1细胞早期的黏附性和伸展性得到提高。铙其强[56]使用聚多巴胺螯合铜离子修饰聚己内酯/β-磷酸三钙,体外抗菌实验表明,铜离子增强聚己内酯/β-磷酸三钙支架材料的抗菌性能,其能够有效抑制大肠杆菌和金黄色葡萄球菌,但在一定程度上会抑制细胞的增殖与活性。董西玲等[57]通过制备聚多巴胺修饰聚己内酯电纺膜载铜涂层,实验发现载铜电纺膜具有良好的细胞相容性与抗菌性,并且具有促进细胞成骨的能力。NOORI等[58]通过实验发现,当铜离子浓度为100 μmol/L时,抑制骨髓间充质干细胞的成骨分化,补充L-精氨酸在一定程度上能减轻该抑制作用,并可以协同促进内皮细胞增殖和血管生成。 随着研究的深入,人们对铜离子成骨机制和血管生成机制的认知已具雏形,但实验发现铜离子的释放难以控制,会导致不规则交联和产生细胞毒性,因此限制了铜离子在骨组织工程中的应用。铜离子的作用机制还需要进一步完善,增强其释放的可控性,掺铜骨组织工程材料有望进一步应用于临床。 2.6 其他金属 除了以上几种金属离子,还有一些金属离子也被应用于骨组织工程材料中,例如:钙(Ca)、锂(Li)、钴(Co)等。 钙离子是骨的主要组成成分,能够促进骨髓间充质干细胞分化形成成骨细胞[59],并进一步促进成骨细胞增殖分化[60],同时抑制破骨细胞的形成。KUMAGAI等[61]通过实验证明,β-磷酸三钙能有效促进血管的生成,这与其中钙离子的释放有关。另有实验证明,钙离子可以通过促进释放生长因子来调节成骨[62]。血凝块形成是骨损伤最初和最重要的阶段,血凝块能调节随后的骨形成和骨重塑过程[63],钙离子在凝血过程在发挥了重要作用,钙离子有通过调控血凝块结构来治疗骨缺损的潜力。 锂离子通常作为情绪稳定剂用于治疗双相障碍,但其在骨组织工程领域也具有一定的应用价值。WANG等[64]的研究发现,锂离子可促进成骨细胞分化和体内新骨形成。黄廷贲[65]通过体内外实验证明,锂离子能通过β-catenin/核因子KB受体活化因子配体/破骨细胞抑制因子信号通路促进骨髓间充质干细胞的成骨分化,抑制破骨前体细胞增殖,进而加速新骨的形成,为锂离子在骨组织工程中的应用提供了理论依据。但锂离子促进成骨的作用机制仍存在争议,其最适用量也有待进一步研究。 钴是人体内一种必需微量元素,能够促进血管生成。李俊刚[66]的研究发现,含钴支架能显著促进体内新骨生成和血管形成,其对大鼠颅骨缺损骨修复的能力显著优于无钴支架。实验证明,将钴离子应用于骨组织工程材料中具有成本低、稳定性好、安全性高等优点;但钴的掺杂对生物材料的结构、理化性能及细胞毒性都有一定影响,有研究显示钴离子会抑制骨髓间充质干细胞的成骨分化,同时降低骨组织矿化的能力[67]。总的来说,钴离子是一种前途较广的掺杂剂。 2.7 不同金属离子间的相互作用 随着研究的不断深入,单一的金属离子的掺入已无法满足骨组织工程材料的需求,因此,出现了含2种或2种以上金属离子的生物活性材料,不同金属离子掺杂其中相互作用,提高了材料的成骨性能和抗菌性能,改善了某些单一金属离子降解不可控的缺点。此外,由于自身功能不同,不同离子掺杂可以使生物活性材料同时具有多种功能,有利于骨组织修复。 刘菲菲[68]构建了电纺聚乳酸基掺锶羟基磷灰石和铜的复合材料,通过测试发现该复合材料具有较高稳定性,能够促进骨髓间充质干细胞分化为成骨细胞,且抗菌性良好。钡离子通常以化合物的形式作为显影剂,刘香笈[69]将钡离子和镁离子共同掺入羟基磷灰石,实验发现该羟基磷灰石具有良好的生物相容性,在促进成骨细胞增殖分化的同时又展现出良好的影像学功能。OKUZU等[70]开发了一种同时释放锶离子和银离子的钛金属植入物,实验显示该植入物没有表现出细胞毒性,但表现出了明显的抗菌性,并且具有促进细胞成骨的能力。陈思奇[71]制备出掺镁、铜的硅酸钙生物陶瓷与羟基磷灰石复合支架,通过对照实验发现,镁、铜的加入促进了成骨细胞的增殖,使复合支架获得更强的骨修复能力。YEDEK?I等[72]采用微波辐射法合成硼、锶离子和镁离子多重掺杂的羟基磷灰石,研究表明该多掺杂羟基磷灰石能促进成骨细胞增殖;并且随着烧结温度的升高,样品机械强度增加,促进细胞的成骨分化的能力也随之增强。张畅[73]通过体外实验发现,低锰含量的镁锰合金对骨髓间充质干细胞无细胞毒性,并且能够促进骨髓间充质干细胞向成骨细胞谱系分化,当镁锰合金浓度比为1∶4时促进成骨效果最好。任浩征[74]在多孔锌支架上掺入铜离子和银离子,与纯锌支架相比,该支架抗菌能力得到提升,并且具有良好的力学性能;在体外实验时该支架出现较弱的细胞毒性,但在体内实验时其生物相容性良好,能促进成骨。 由此可见,不同金属离子掺杂的骨组织工程材料弥补了单一金属由于自身性质所造成的不足,同时也提高了原有支架材料的性能。虽然多金属掺杂材料在治疗骨缺损方面具有很大的潜力,但在骨组织工程领域的研究才刚刚开始。不同金属离子的相互作用机制、协同作用效果、最适掺杂浓度等一系列问题层出不穷,需要通过大量研究来验证和探索(图3)。"
| [1] WU L, LUTHRINGER BJ, FEYERABEND F, et al. Effects of extracellular magnesium on the differentiation and function of human osteoclasts. Acta Biomater. 2014;10(6):2843-2854. [2] HE D, ZHUANG C, XU S, et al. 3D printing of Mg-substituted wollastonite reinforcing diopside porous bioceramics with enhanced mechanical and biological performances. Bioact Mater. 2016;1(1):85-92. [3] HUNG CC, CHAYA A, LIU K, et al. The role of magnesium ions in bone regeneration involves the canonical Wnt signaling pathway. Acta Biomater. 2019;98:246-255. [4] HAMUSHAN M, CAI W, ZHANG Y, et al. High-purity magnesium pin enhances bone consolidation in distraction osteogenesis model through activation of the VHL/HIF-1α/VEGF signaling. J Biomater Appl. 2020;35(2):224-236. [5] 潘昊田.负载Mg元素的GelMA大孔水凝胶支架构建及其骨组织工程的应用研究[D].广州:华南理工大学,2020. [6] 王桂芳,吕凯歌.镁离子激活自噬促进大鼠骨髓间充质干细胞成骨分化的体外实验观察[J].口腔颌面外科杂志,2021,31(4):212-220. [7] 万卓.镁硅离子共释放可注射微球促成骨成血管协同效应的研究[D].北京:北京化工大学,2021. [8] 李彪,李齐宏,胡先同,等.含镁脱细胞牛骨基质的制备与性能评估[J].军事医学, 2021,45(1):40-44+49. [9] ZHANG X, HUANG P, JIANG G, et al. A novel magnesium ion-incorporating dual-crosslinked hydrogel to improve bone scaffold-mediated osteogenesis and angiogenesis. Mater Sci Eng C Mater Biol Appl. 2021;121:111868. [10] WANG F, SUN P, XIE E, et al. Phytic acid/magnesium ion complex coating on PEEK fiber woven fabric as an artificial ligament with anti-fibrogenesis and osteogenesis for ligament-bone healing. Biomater Adv. 2022;140:213079. [11] 秦博恒,杨犇,何东宁.载锌多壁碳纳米管/壳聚糖复合材料成骨性能的研究[J].口腔医学研究,2017,33(7):725-728. [12] 侯懿.骨组织工程用锌基多孔支架及其表面生物活性涂层的制备与表征[D].上海:上海交通大学,2018. [13] YANG H, QU X, LIN W, et al. In vitro and in vivo studies on zinc-hydroxyapatite composites as novel biodegradable metal matrix composite for orthopedic applications. Acta Biomater. 2018;71:200-214. [14] SU Y, WANG K, GAO J, et al. Enhanced cytocompatibility and antibacterial property of zinc phosphate coating on biodegradable zinc materials. Acta Biomater. 2019;98:174-185. [15] 伍煜政.锌基配体黑磷修饰骨组织工程支架及其光热抗菌与促成骨性能研究[D].北京:中国科学院大学,2020. [16] 肖厚洪.离子掺杂介孔硅改性水凝胶材料的研究及其性能表征[D].广州:暨南大学,2020. [17] WANG C, LIU J, LIU Y, et al. Study on osteogenesis of zinc-loaded carbon nanotubes/chitosan composite biomaterials in rat skull defects. J Mater Sci Mater Med. 2020; 31(2):15. [18] 赵桥,杨飞,张成栋,等.锌离子浓度可影响兔骨髓间充质干细胞的增殖与成骨分化[J].中国组织工程研究,2020,24(19):2985-2990. [19] LU T, ZHANG J, YUAN X, et al. Enhanced osteogenesis and angiogenesis of calcium phosphate cement incorporated with zinc silicate by synergy effect of zinc and silicon ions. Mater Sci Eng C Mater Biol Appl. 2021;131:112490. [20] 孙逢栋.锌基多孔骨组织工程支架的制备与表征[D].天津:天津理工大学, 2022. [21] RAZAVI M, HUANG Y. Assessment of magnesium-based biomaterials:from bench to clinic. Biomater Sci. 2019;7(6):2241-2263. [22] BEKMURZAYEVA A, DUNCANSON WJ, AZEVEDO HS, et al. Surface modification of stainless steel for biomedical applications:Revisiting a century-old material. Mater Sci Eng C Mater Biol Appl. 2018;93:1073-1089. [23] KIRADZHIYSKA DD, MANTCHEVA RD. Overview of Biocompatible Materials and Their Use in Medicine. Folia Med (Plovdiv). 2019;61(1):34-40. [24] 尚文博.锰掺杂β-磷酸三钙多孔仿骨材料性能研究[D].长春:吉林大学,2016. [25] YU L, TIAN Y, QIAO Y, et al. Mn-containing titanium surface with favorable osteogenic and antimicrobial functions synthesized by PIII&D. Colloids Surf B Biointerfaces. 2017; 152:376-384. [26] 邓翠君.骨-软骨复杂组织修复生物活性无机材料的制备及性能研究[D].上海:中国科学院上海硅酸盐研究所,2018. [27] 李淼.微量元素掺杂羟基磷灰石的制备及生物学效应研究[D].上海:上海师范大学,2019. [28] BARRIONI BR, NORRIS E, LI S, et al. Osteogenic potential of sol-gel bioactive glasses containing manganese. J Mater Sci Mater Med. 2019;30(7):86. [29] 张卓俊.离子掺杂β-磷酸三钙材料制备及3D支架性能研究[D].哈尔滨:哈尔滨工业大学,2020. [30] ZHAO QM, SUN YY, WU CS, et al. Enhanced osteogenic activity and antibacterial ability of manganese-titanium dioxide microporous coating on titanium surfaces. Nanotoxicology. 2020;14(3):289-309. [31] WESTHAUSER F, WILKESMANN S, NAWAZ Q, et al. Osteogenic properties of manganese-doped mesoporous bioactive glass nanoparticles. J Biomed Mater Res A. 2020;108(9):1806-1815. [32] 孙元艺.锰复合骨修复支架的3D打印及其性能评估[D].北京:中国科学院大学(中国科学院深圳先进技术研究院),2022. [33] HREHA J, WEY A, CUNNINGHAM C, et al. Local manganese chloride treatment accelerates fracture healing in a rat model. J Orthop Res. 2015;33(1):122-130. [34] LI L, YANG X. The Essential Element Manganese,Oxidative Stress,and Metabolic Diseases:Links and Interactions. Oxid Med Cell Longev. 2018;2018:7580707. [35] 郭书含,宋平平,陈曾曾,等.人骨髓间充质干细胞脑内移植治疗锰中毒模型的可行性[J].中国组织工程研究,2018,22(9):1402-1406. [36] 王成健.多孔SrO/HA生物复合陶瓷骨修复材料的制备及体外生物相容性研究[D].昆明:昆明理工大学,2016. [37] GAO C, LIU H, LUO ZP, et al. Modification of calcium phosphate cement with poly(γ-glutamic acid)and its strontium salt for kyphoplasty application. Mater Sci Eng C Mater Biol Appl. 2017;80:352-361. [38] RIEDEL C, ZIMMERMANN EA, ZUSTIN J, et al. The incorporation of fluoride and strontium in hydroxyapatite affects the composition,structure,and mechanical properties of human cortical bone. J Biomed Mater Res A. 2017;105(2):433-442. [39] 张文,黄德球,郭周义,等.掺锶生物活性玻璃通过调控巨噬细胞极化促进成骨[J].激光生物学报,2018,27(3):232-239. [40] ZHANG X, LI H, LIN C, et al. Synergetic topography and chemistry cues guiding osteogenic differentiation in bone marrow stromal cells through ERK1/2 and p38 MAPK signaling pathway. Biomater Sci. 2018;6(2):418-430. [41] NARUPHONTJIRAKUL P, TSIGKOU O, LI S, et al. Human mesenchymal stem cells differentiate into an osteogenic lineage in presence of strontium containing bioactive glass nanoparticles. Acta Biomater. 2019;90:373-392. [42] LINO AB, MCCARTHY AD, FERNÁNDEZ JM. Evaluation of Strontium-Containing PCL-PDIPF Scaffolds for Bone Tissue Engineering:In Vitro and In Vivo Studies. Ann Biomed Eng. 2019;47(3):902-912. [43] YE H, ZHU J, DENG D, et al. Enhanced osteogenesis and angiogenesis by PCL/chitosan/Sr-doped calcium phosphate electrospun nanocomposite membrane for guided bone regeneration. J Biomater Sci Polym Ed. 2019;30(16):1505-1522. [44] 赵德路,铁朝荣,王新,等.复合锶离子光交联海藻酸盐水凝胶支架的机械和生物学性能[J].中国组织工程研究,2019,23(18):2880-2887. [45] SUN T, LI Z, ZHONG X, et al. Strontium inhibits osteoclastogenesis by enhancing LRP6 and β-catenin-mediated OPG targeted by miR-181d-5p. J Cell Commun Signal. 2019;13(1):85-97. [46] 刘欢欢.基于胶原自组装/矿化协同策略制备掺杂生物活性元素的骨组织工程胶原支架[D].天津:天津医科大学,2020. [47] SHI M, CHEN Z, FARNAGHI S, et al. Copper-doped mesoporous silica nanospheres,a promising immunomodulatory agent for inducing osteogenesis. Acta Biomater. 2016; 30:334-344. [48] ALI A, ERSHAD M, VYAS VK, et al. Studies on effect of CuO addition on mechanical properties and in vitro cytocompatibility in 1393 bioactive glass scaffold. Mater Sci Eng C Mater Biol Appl. 2018;93:341-355. [49] Wang H,Zhao S,Xiao W, et al.Influence of Cu doping in borosilicate bioactive glass and the properties of its derived scaffolds.Mater Sci Eng C Mater Biol Appl. 2016;58: 194-203. [50] 施孟超.多功能介孔生物活性材料用于骨组织工程的研究[D].中国科学院大学, 2017. [51] Zhou Y,Han S,Xiao L,et al.Accelerated host angiogenesis and immune responses by ion release from mesoporous bioactive glass.J Mater Chem B. 2018; 6(20):3274-3284. [52] 刘静.基于超低温挤出沉积技术的含铜介孔生物活性玻璃/海藻酸钠复合骨组织工程支架的研究[D].武汉:华中科技大学,2019. [53] LI K, XIA C, QIAO Y, et al. Dose-response relationships between copper and its biocompatibility/antibacterial activities. J Trace Elem Med Biol. 2019;55:127-135. [54] 王新,铁朝荣,尹苗,等.铜离子光双交联海藻酸盐水凝胶支架材料的性能研究[J].临床口腔医学杂志,2020,36(2):84-88. [55] LIN Z, CAO Y, ZOU J, et al. Improved osteogenesis and angiogenesis of a novel copper ions doped calcium phosphate cement. Mater Sci Eng C Mater Biol Appl. 2020;114: 111032. [56] 铙其强.PDA负载金属离子修饰PCL/β-TCP支架表面用于骨组织工程[D].南昌:南昌大学,2021. [57] 董西玲,惠敏,曹飞,等.聚多巴胺修饰聚己内酯电纺膜载铜涂层的制备及抗菌和细胞性能评价[J].中国组织工程研究,2022,26(27):4272-4278. [58] NOORI A, HOSEINPOUR M, KOLIVAND S, et al. Synergy effects of copper and L-arginine on osteogenic,angiogenic,and antibacterial activities. Tissue Cell. 2022;77:101849. [59] YANG Y, XIAO Y. Biomaterials Regulating Bone Hematoma for Osteogenesis. Adv Healthc Mater. 2020:e2000726. doi: 10.1002/adhm.202000726. [60] 雷群,林东,黄文秀,等.钙离子对人成骨细胞迁移与成骨分化的影响[J].华西口腔医学杂志,2018,36(6):602-608. [61] KUMAGAI H, MAKIHARA T, FUNAYAMA T, et al. Angiogenesis and new bone formation in novel unidirectional porous beta-tricalcium phosphate:a histological study. J Artif Organs. 2019;22(4):294-299. [62] GARNER AL, FRELINGER AL 3RD, GERRITS AJ, et al. Using extracellular calcium concentration and electric pulse conditions to tune platelet-rich plasma growth factor release and clotting. Med Hypotheses. 2019;125:100-105. [63] WANG X, ZHANG Y, JI W, et al. Categorising bone defect hematomas-Enhance early bone healing. Med Hypotheses. 2018;113:77-80. [64] WANG L, ZHANG K, HAO Y, et al. Osteoblast/bone-tissue responses to porous surface of polyetheretherketone-nanoporous lithium-doped magnesium silicate blends’integration with polyetheretherketone. Int J Nanomedicine. 2019;14:4975-4989. [65] 黄廷贲.掺锂种植体表面调控β-catenin/RANKL/OPG信号轴在种植体骨结合形成中的作用及机制[D].杭州:浙江大学,2019. [66] 李俊刚.3D打印掺钴生物陶瓷支架介导成骨-成血管偶联促进骨修复的作用研究[D].福州:福建医科大学,2021. [67] 蒋昇源,李丹,姜建浩,等.假体无菌性松动过程中Co2+对成骨前体细胞的生物学反应[J].中国组织工程研究,2021,25(21):3292-3299. [68] 刘菲菲.金属纳米粒子增强的抗菌聚乳酸基复合纤维的构建及其性能研究[D].乌鲁木齐:新疆师范大学,2021. [69] 刘香笈.一种Ba/Mg共掺杂羟基磷灰石的合成与其复合材料在骨修复中的研究[D].长春:吉林大学,2021. [70] OKUZU Y, FUJIBAYASHI S, YAMAGUCHI S, et al. In vitro study of antibacterial and osteogenic activity of titanium metal releasing strontium and silver ions. J Biomater Appl. 2021;35(6):670-680. [71] 陈思奇.掺杂Cu/Mg的硅酸钙生物陶瓷与纳米羟基磷灰石复合多孔支架对成骨影响[D].泸州:西南医科大学,2021. [72] YEDEKÇI B, TEZCANER A, ALSHEMARY AZ, et al. Synthesis and sintering of B,Sr,Mg multi-doped hydroxyapatites:Structural,mechanical and biological characterization. J Mech Behav Biomed Mater. 2021;115:104230. [73] 张畅.含锰镁合金的生物学活性及其成骨能力初探[D].遵义:遵义医科大学,2022. [74] 任浩征.可降解Zn基多孔骨修复支架材料的制备与性能研究[D].天津:天津理工大学,2022. |
| [1] | Dai Jing, Liu Shasha, Shen Mingjing. Exosome-loaded injectable hydrogel for repairing bone defects around implants [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(3): 347-354. |
| [2] | Yang Jie, Hu Haolei, Li Shuo, Yue Wei, Xu Tao, Li Yi. Application of bio-inks for 3D printing in tissue repair and regenerative medicine [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(3): 445-451. |
| [3] | Chen Pinrui, Pei Xibo, Xue Yiyuan. Function and advantages of magnetically responsive hydrogel in bone tissue engineering [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(3): 452-457. |
| [4] | Chen Junyan, Meng Qingqi, Li Siming. Cartilage targeting function in the drug delivery system by intra-articular injection for the treatment of osteoarthritis [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(3): 458-463. |
| [5] | Long Zhirui, Huang Lei, Xiao Fang, Wang Lin, Wang Xiaobei. Characteristics of hydrogel microspheres in bone tissue engineering [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(3): 472-478. |
| [6] | Kong Xiangyu, Wang Xing, Pei Zhiwei, Chang Jiale, Li Siqin, Hao Ting, He Wanxiong, Zhang Baoxin, Jia Yanfei. Biological scaffold materials and printing technology for repairing bone defects [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(3): 479-485. |
| [7] | Xu Jing, Lyu Huixin, Bao Xin, Zhang Yi, Wang Yihan, Zhou Yanmin. Application of near infrared responsive hydrogels in tissue engineering [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(3): 486-492. |
| [8] | He Wanyu, Cheng Leping. Strategies and advance on stem cell transplantation for repair of spinal cord injury [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(在线): 1-7. |
| [9] | Wen Xinghua, Ding Huanwen, Cheng Kai, Yan Xiaonan, Peng Yuanhao, Wang Yuning, Liu Kang, Zhang Huiwu. Three-dimensional finite element model analysis of intramedullary nailing fixation design for large femoral defects in Beagle dogs [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(9): 1371-1376. |
| [10] | Xu Cong, Zhao He, Sun Yan. Regeneration of facial nerve injury repaired by biomaterial nerve conduits [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1089-1095. |
| [11] | Chen Shisong, Liu Xiaohong, Xu Zhiyun. Current status and prospects of bioprosthetic heart valves [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1096-1102. |
| [12] | Tang Haotian, Liao Rongdong, Tian Jing. Application and design of piezoelectric materials for bone defect repair [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1117-1125. |
| [13] | Xu Yan, Li Ping, Lai Chunhua, Zhu Peijun, Yang Shuo, Xu Shulan. Piezoelectric materials for vascularized bone regeneration [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1126-1132. |
| [14] | Zhang Min, Zhang Xiaoming, Liu Tongbin. Application potential of naringin in bone tissue regeneration [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(5): 787-792. |
| [15] | Xiong Wei, Yuan Lingmei, Qian Guowen, Huang Jinyang, Pan Bin, Guo Ling, Zeng Zhikui. Value of a critical bone defect animal model in evaluating osteogenic efficacy of bone tissue engineering scaffold [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(35): 5714-5720. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||