Chinese Journal of Tissue Engineering Research ›› 2023, Vol. 27 ›› Issue (35): 5714-5720.doi: 10.12307/2023.852
Previous Articles Next Articles
Value of a critical bone defect animal model in evaluating osteogenic efficacy of bone tissue engineering scaffold
Xiong Wei1, Yuan Lingmei2, Qian Guowen3, Huang Jinyang1, Pan Bin1, Guo Ling1, Zeng Zhikui2, 4
- 1Jiangxi University of Chinese Medicine, Nanchang 330004, Jiangxi Province, China; 2Affiliated Hospital of Jiangxi University of Chinese Medicine, Nanchang 330006, Jiangxi Province, China; 3Jiangxi University of Science and Technology, Nanchang 330013, Jiangxi Province, China; 4National Engineering Research Center for Manufacturing Technology of Traditional Chinese Medicine Solid Preparations, Jiangxi University of Chinese Medicine, Nanchang 330004, Jiangxi Province, China
-
Received:2022-10-31Accepted:2023-01-10Online:2023-12-18Published:2023-06-05 -
Contact:Zeng Zhikui, MD, Doctoral supervisor, Jiangxi University of Chinese Medicine, Nanchang 330004, Jiangxi Province, China; Affiliated Hospital of Jiangxi University of Chinese Medicine, Nanchang 330006, Jiangxi Province, China -
About author:Xiong Wei, MD, Doctoral supervisor, Jiangxi University of Chinese Medicine, Nanchang 330004, Jiangxi Province, China -
Supported by:the National Natural Science Foundation of China, No. 81960880 (to ZZK); Scientific Research Innovation Team Project of Jiangxi University of Chinese Medicine, No. CXTD22009; a grant from Jiangxi Clinical Medical Center, No. 20212BCG74004
CLC Number:
Cite this article
Xiong Wei, Yuan Lingmei, Qian Guowen, Huang Jinyang, Pan Bin, Guo Ling, Zeng Zhikui. Value of a critical bone defect animal model in evaluating osteogenic efficacy of bone tissue engineering scaffold[J]. Chinese Journal of Tissue Engineering Research, 2023, 27(35): 5714-5720.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks

2.1 临界骨缺损的定义与治疗 临界骨缺损,是指由外源性创伤(交通事故、高处坠落等)或内源性损伤(如骨感染和骨肿瘤和先天性疾病等)引起的骨缺损,缺损范围超过机体自行修复的阈值,若不进行外界干预,骨缺损无法完成自我修复。目前文献对临界骨缺损的定义尚未统一,1986年,临界骨缺损由SCHMITZ等[8]首次提出,其研究表明在无外界干预的条件下,骨缺损存在一个无法自愈的临界值。MAUFFREY等[9]将临界骨缺损定义为缺损尺寸> 2 cm或超过骨周径50%的骨缺损。然而,考虑到实验动物与人类在体型、骨骼大小上的差异,人体的临界骨缺损定义无法直接应用于实验动物,因此有学者提出动物模型中的临界骨缺损是动物特定骨骼的最小骨缺口,该缺口在整个实验阶段无法自愈,或在动物的一生中骨再生率低于10%的骨缺损[10]。 目前,针对临界骨缺损的修复方案中,自体/异体骨移植虽已在世界范围内的骨科手术中得到了广泛应用[11-12],但存在自体骨供区疼痛、潜在感染风险和异体骨免疫排斥等缺点,极大地限制了其临床疗效[13-14]。为攻克临界骨缺损这一医学难题,学者们相继提出了牵张成骨(Ilizarov)、诱导膜(Masquelet)及骨组织工程技术等诸多新方案,其中尤以新兴的骨组织工程技术最为耀眼,有望从根本上突破临界骨缺损修复中的瓶颈问题。但骨组织工程材料绝大多数属于植入类医疗器械,在正式进入临床研究阶段时,需要完成临床前研究,对其生物相容性、有效性以及安全性在内诸多性能展开系统评估研究,其中大部分研究需要在动物体内进行。因此,合适的动物实验模型对骨组织工程支架未来进入临床应用,帮助临床医生解决现有临界骨缺损难题具有重要价值。 2.2 临界骨缺损动物模型 由于目前对各动物的临界骨缺损定义尚未明确,导致在选择实验动物进行临界骨缺损造模研究时,除了遵循骨缺损范围仅靠动物自身无法愈合的原则外,具体骨缺损长度大小标准不一,同时选用的骨骼部位不同,将导致截取的骨缺损大小也存在明显差异[15-16]。因此文章列举常用的临界骨缺损动物模型,对各模型的优缺点进行综述。 2.2.1 小鼠 小鼠作为应用范围最广的小动物模型实验动物,具有生长周期短、价格低廉、来源广泛及容易饲养等优点[17],同时小鼠自身抗感染能力较强,围术期易于管理,故在临床应用前的基础研究中发挥重要作用。由于啮齿动物基因与人类基因组区域基因排列顺序基本相同,具有高度的基因同源性[18],因此在生物学、心理学、行为学及动物遗传学方面均与人类相似,通过小鼠模型可模拟大量人类疾病症状[19]。GUO等[20]在小鼠颅骨临界骨缺损模型中评估了骨形态发生蛋白2(bone morphogenetic proteins-2,BMP-2)、血管内皮生长因子(vascular endothelial growth factor,VEGF)共表达细胞薄片修复临界颅骨缺损的成骨效能,结果表明骨形态发生蛋白2和血管内皮生长因子共表达细胞薄片诱导的体内成骨效果优于骨形态发生蛋白2或血管内皮生长因子单独诱导。TAZAWA等[21]研究发现在修复小鼠股骨骨缺损时,适宜浓度的生长因子可有效促进新骨形成,增加骨体积与骨矿物质含量。 但小鼠模型亦存在一定的局限性:①小鼠有限的骨容量、快速的皮质骨重塑及继发性骨形成,导致应用小鼠建立临界骨缺损修复模型时,仅可作为人工骨材料的生物相容性、短期修复效果评估及骨修复分子机制等初步研究,不宜做长期骨修复效果评价。②人体骨结构中含有哈佛氏系统,小鼠的骨骼为原始的骨系统不具备该结构,故其骨骼重建过程与人体存在差异,因此不宜用于针对哈佛氏系统的成骨研究。③小鼠骨骼体积小,质薄且脆,操作难度大,其造模手术要求术者具备一定的显微外科手术操作基础,同时其皮质骨组成与人类存在一定的差异性(如羟脯氨酸和蛋白质含量)。 2.2.2 大鼠 大鼠亦是小动物模型的常用实验动物,相比小鼠,在行为学、生理学、遗传学和认知行为等方面,大鼠与人类更加接近,如大鼠的遗传基因组有27.5亿对,相较小鼠的26亿对更接近人类基因组的29亿对,且大鼠心率相对较慢约为300次/min,虽与人类正常心率60-100次/min仍存在差别,但对比小鼠近600 次/min的心率,仍具有显著优势[22]。同时与小鼠相比,大鼠体型较大,成年大鼠的体质量是成年小鼠的8-10倍,其生理特征更适合疾病研究,优异的模拟疾病能力使大鼠成为理想实验动物。在过去一个世纪中,大鼠一直是首选啮齿类实验动物,广泛用于生物医学研究。直到20世纪80年代末,随着基因敲除技术与ES细胞基因打靶技术的陆续出现[23-24],才使得小鼠逐渐取代大鼠在医学动物实验中的地位。 大鼠骨缺损模型中常用造模部位为股骨或下颌骨,选用股骨作为造模部位时,因不同学者在模型中实施的骨修复方案不同和所用大鼠体型不一等因素,所建立的大鼠股骨骨缺损临界值也存在差别,数值多为4-10 mm[25-27]。DRéNO等[28]在大鼠下颌骨癌症放疗模型中将高辐射环境下的大鼠下颌骨临界骨缺损数值确定为3 mm。MIGUEZ等[29]在利用橙皮苷对小鼠胚胎成骨细胞前体细胞(MC3T3-E1)进行干预时发现,橙皮苷不仅促进MC3T3-E1细胞成骨分化,还可在组织矿化中发挥积极作用,并且通过大鼠下颌骨骨缺损动物实验进一步进行橙皮苷对体内、外骨再生的作用机制研究。ZHANG等[30]利用3D打印支架构建双重载药系统,借助支架负载白藜芦醇和雷奈酸锶用于骨缺损部位,发现植入物释放的两种药物可对骨髓间充质干细胞的成骨分化产生协同促进作用,诱导血管生成和抑制破骨细胞活性,促进骨缺损修复。 由于大鼠来源广泛,容易饲养及造模成本低等优点,而骨骼大小亦适合建立临界骨缺损模型,造模部位以股骨和颅骨多见,同时造模的可操作性和重复性强,故通常被认为是评估骨组织再生的首选实验动物模型之一。在实际基础研究中被广泛应用,其缺点是相比大动物,骨骼偏小,难以完全模型人体骨修复过程。 2.2.3 兔 在动物模型中,兔的应用历史十分悠久,其中新西兰大白兔是骨缺损模型最常用的实验动物之一[31]。新西兰大白兔性格温顺,来源广泛,容易饲养,还具有较强的手术耐受和伤口抗感染能力。田彬等[32]观察不同尺寸兔颅骨圆形骨缺损在不同时间段的骨愈合情况,发现在12 周的观察期内,直径为 4 mm的骨缺损可以自行修复,而直径大于5 mm时,骨缺损虽表现出愈合趋势但未达到临床愈合要求,故将直径≥5 mm 的圆形骨缺损设置为临界骨缺损参考值。徐石庄等[33]采用兔股骨髁制备直径为5,6,7 mm,深度10 mm的圆形骨缺损模型,发现直径5 mm的实验组在实验周期内可自行愈合,而6 mm、7 mm的骨缺损难于修复,故作者将直径6 mm、深度10 mm认定为兔股骨髁临界骨缺损值。LIU等[34]发现骨膜的覆盖情况直接影响兔肋骨骨缺损的临界值,当骨膜覆盖良好时其可为骨髓间充质干细胞提供一个有利的增殖分化环境,调节成骨潜能,而没有骨膜的骨骼则愈合能力较差,并总结兔肋骨临界骨缺损参考值有骨膜覆盖情况下为5 cm,而无骨膜则为2 cm。 因兔骨干中段骨密度以及骨韧性与人体相仿,故在研究人体肌肉组织和骨骼疾病时亦常选用兔作为实验动物。相比大鼠、小鼠等啮齿动物,兔的体型更大,在进行大段骨缺损时更加方便操作且造模成本也可控,造模部位多集中于股骨髁和前臂。但是,与人类下肢负重主要为膝、踝关节不同,兔的后肢基本处于完全弯曲的状态,与人体截然相反。因此,由于不同的力学性能,在进行实验时,需注意实验结果和人体的差异性。此外,兔的代谢活性和骨缺损区干细胞密度均比人类高,导致其骨缺损模型中有更多的细胞参与骨缺损修复,修复率可能更高,同时相比大型动物骨骼尺寸偏小也是其主要缺点。 2.2.4 犬 一直以来,在测试人工骨材料成骨效能时,多选用骨骼发育成熟的大型动物。虽然犬骨与人骨在微观结构和修复重建方面存在差距,但犬骨在骨组织的密度、质量和有机/无机成分方面却与人类非常相似。从实际情况考虑,在漫长的研究期间,犬类具有易于饲养、容易接近等优势。LEE等[35]利用犬下颌骨临界骨缺损模型检验3D打印PCL复合支架的成骨效能,发现该复合支架虽表现出较强的骨修复作用,但与生长因子的负载量密切相关,未来在临床应用前仍需解决复合支架如何负载大剂量生长因子的问题。KAWAI等[36]在犬颅骨临界骨缺损模型中研究了磷酸八钙/胶原蛋白的骨再生特性,发现该复合材料在大型骨缺损动物模型中具有优异的成骨效能,该实验可作为磷酸八钙/胶原蛋白治疗人体骨缺损的临床前实验。还有研究突破传统造模方案,设计出一类三壁犬牙槽骨临界骨缺损模型,用以评估各类生物材料的成骨效能与作用机制[37]。 虽然犬已被用于骨组织再生研究几十年,但基于长期以来犬类在人类社会充当伴侣动物和“人类忠实伙伴”的角色,在医学研究中使用犬类作为实验动物时,受到动物福利与科研伦理的关注也是超乎想象的,因此在实际应用中考虑到来自社会伦理的挑战,犬类在动物模型特别是骨缺损模型中的使用正在逐渐减少。目前的共识认为在骨科动物实验研究中,如果可以用绵羊等作为替代实验动物,无特殊情况下将不使用犬进行实验。 2.2.5 猪 在进行临界骨缺损骨修复效果评估研究中,猪因具有与人类相似的骨解剖结构、骨形态学、骨内代谢、血液供应、骨愈合速率、矿物质浓度及矿化率和骨横截面,更重要的是猪骨存在与人骨相似的板层骨,因此被视为人类骨再生修复研究中最具代表性的模型动物。猪的关节缺损模型已被应用于工程化的人工关节置换研究,用以评估人工关节对骨、软骨、韧带及周围软组织的影响[38]。 MOEST等[39]利用标准化钛管植入猪额骨建立单壁临界骨缺损模型,在钛管内植入脱矿牛骨矿物质填充材料可确保其处于受保护的环境,有效避免了材料的微运动及软组织的侵袭,有利于骨缺损的重塑。JOHNSON等[40]设计出一类可用于临床前研究的猪颅骨临界缺损模型,在临界骨缺损部位填充羟基磷灰石/磷酸三钙支架与骨髓间充质干细胞,证实了该联合疗法的生物安全性,同时新生骨与自然骨的骨质相当,并可形成一个光滑颅面,符合功能和美学要求。 然而,猪的股骨与胫骨长度较人体更短,在进行大尺寸人工骨修复性能评估时,存在着一定的局限性。且猪作为实验动物存在着饲料昂贵、场地环境要求高、群养时好斗、难以驯服等缺点。常见的商品猪常由于体质量增长较快和体质量太大难以满足骨科研究需求,为克服上述劣势,研究人员致力于培育出体型较小的小型猪及微型猪作为实验用猪[41]。 2.2.6 绵羊 在大型哺乳动物中,绵羊的药理反应与人最相近,并且绵羊性格温顺,成年绵羊的体质量、大小、骨骼尺寸亦与成年男性相接近。同时绵羊的骨骼有机/无机物组成和骨再生重塑能力与人相仿,在绵羊的行走过程中,其后肢的负载接近人类下肢负载的一半,可更加真实地模拟人工骨材料在人体内进行骨缺损修复的力学环境。6-7岁以上的绵羊可为人类的临床研究提供强有力的替代品,它们具有与人体非常相似的骨矿物质组成、宏/微观结构、重塑能力以及生物力学[42]。此外,雌性绵羊还具有与人类女性相似的自发性排卵、激素分泌的生理现象,因此绵羊模型的骨组织对激素刺激更加敏感,是一种极具潜力的研究女性骨质疏松动物模型[43]。 CROVACE等[44]利用绵羊胫骨临界骨缺损模型对比钛合金支架与羟基磷灰石支架的成骨效能,研究发现由于钛合金在生物力学及骨导电性方面的优势,与羟基磷灰石材料相比,钛合金支架可更有效地修复骨缺损,有利于长期骨整合。牙本质是一种骨样矿化组织,具有与骨骼相似的化学成分,是一种可开发的骨移植材料,KABIR等[45]在羊髂骨临界骨缺损模型中检验了牙本质材料的骨修复性能,发现其不仅具有优异的成骨效能,且生物吸收率与缺损区新骨生成率基本一致。HETTWER等[46]运用综合影像技术分析多种材料在绵羊股骨临界骨缺损模型中成骨效果,因不同材料的属性与成骨机制差异,部分材料存在特有的影像学和组织学特征,综合影像技术的应用有助于帮助研究人员更好地观察与理解体内成骨过程。 关于临界大小骨缺损动物模型的相关研究进展见表1。"


综上所述,在进行动物实验模型选择时,首先须考虑生理和病理上与人类的相似性、造模的可操作性及在相对短的周期内能观察到造模后实验动物的差异性[15]。进行临界骨缺损实验造模时,理论上犬、猪、羊等大中体型动物往往具有优势,一则大中型动物与人类有着类似的骨代谢机制,更能模仿人体骨愈合微环境,再者大中型动物骨骼更加粗壮坚硬,可降低骨缺损造模操作难度,故大动物模型是评估骨重建方法非常有用的临床前模型[16]。然而大中型动物存在成本过高、购买及饲养均需投入大量人力和物力等问题,故较难以进行大数量造模。况且实验动物体型越大,自我恢复速度越慢,实验周期越长,不利于研究者进行骨缺损断端骨痂生长情况的观察,所以临界骨缺损实验模型动物选择中大型动物并不常见。而小动物模型如大鼠、兔等因获取容易、成本低、伦理接受程度高,经常被用于各种在体骨再生研究的评估。各种类动物骨缺损模型的优缺点见表2。"

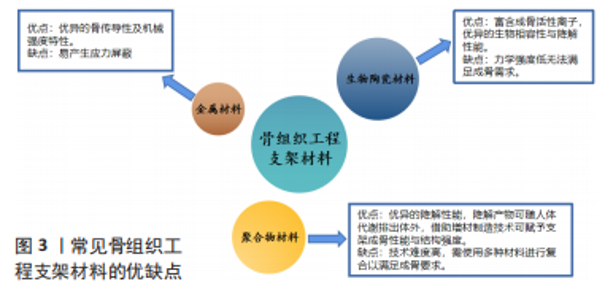
2.3 骨组织工程支架在骨缺损动物模型中的应用 始于20世纪80年代的骨组织工程学,作为组织工程学的重要分支,是一个独立的研究领域,致力于研发出与人体骨组织成分、结构和功能相似的人工材料。理想的骨组织工程支架应具备种子细胞、生物支架和生长因子3大要素[47],将支架复合种子细胞植入到骨缺损部位,随着支架在体内的降解,支架中的种子细胞与生长因子逐渐释放,从而诱导骨髓间充质干细胞成骨分化,并通过加快新生骨组织血管化,促进骨组织矿化,最终实现修复骨缺损的目的。 支架材料作为骨组织工程支架设计与制备的关键因素,将直接决定其在临床应用的潜力。目前常见的支架材料包括聚合物材料、金属材料及生物陶瓷材料等,在实际应用中其性能各有优势[48-51],见图3。"
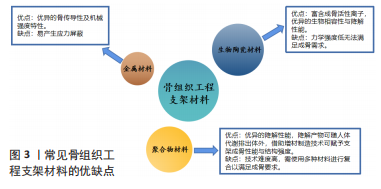
然而,骨组织工程支架作为植入型医疗器械,属于第三类医疗器械中的植入物产品,在进入临床应用前,根据相关法律法规要求,需进行大量动物实验及临床前研究,以评估支架在人体的生物相容性及生物安全性[52]。因此,选择合适的骨缺损动物模型尤为重要。 能准确模拟人体成骨过程是选择骨缺损动物模型的首要原则。骨来源于胚胎时期的间充质,其发生过程有两种方式,即膜内成骨和软骨内成骨。膜内成骨是间充质细胞直接分化成原始结缔组织膜,而后在膜内形成骨组织,如头颅的扁平骨、下颌骨、上颌骨、锁骨和膝盖骨均属膜内成骨。软骨成骨是由间充质先分化成软骨,再把软骨组织逐渐破坏,而后形成骨组织,随后被重塑成骨骼,通过此过程形成了股骨、胫骨和肱骨等长骨。故在评估骨组织工程支架成骨效能时,应注意骨缺损部位成骨机制的区别。 评价骨组织工程支架膜内成骨机制的临界性骨缺损动物模型,通常有大鼠与兔的颅骨骨缺损模型和犬与猪的下颌骨骨缺损模型等。CAO等[53]借助大鼠颅骨临界性骨缺损模型评估了一种基于聚乳酸-羟基乙酸/β-磷酸三钙 (lactic-co-glycolic acid/β-calcium phosphate,PLGA/β-TCP)的中药支架的成骨效能,通过在支架上负载中药提取物葛根素(Puerarin)作为生长因子的替代物构建了中药复合支架,发现此支架可通过刺激血管内皮生长因子和骨形态发生蛋白2的表达,诱导血管生成和募集骨髓间充质干细胞,从而促进血管生成和骨缺损重建。SUVARNAPATHAKI等[54]在大鼠颅骨临界骨缺损模型中测试了新型产氧支架的潜在成骨效能,该支架可在骨重塑早期为组织提供一个可控的氧气输送系统,通过氧气的逐渐释放,为骨细胞提供适宜的成骨微环境,研究表明含氧支架表现出良好的成骨活性和细胞相容性。YAN等[55]在小猎犬牙槽骨骨缺损动物模型中应用氟化处理的镁合金植入物修复骨缺损,发现镁合金材料在体内展现出良好的生物相容性,且不会增加感染风险,同时镁具有骨诱导的潜力,未来可作为理想的口腔移植物。DEWEY等[56]采用猪下颌骨临界(直径25 mm,厚10 mm)骨缺损模型,评估了矿化胶原/聚乙内酯复合材料的成骨效能,研究发现利用聚乙内酯网格可有效改善矿化胶原支架的机械性能,而此拟合材料可有效避免植入支架的微运动和由此产生的成纤维化,有利于网格支架成骨。 评估软骨内成骨机制的临界性骨缺损动物模型主要集中于大鼠、兔、羊与猪的股骨或胫骨骨缺损模型等。DEBAUN 等[57]在SD大鼠诱导膜模型中,通过将聚乙内酯/β-磷酸三钙(PCL/β-TCP)支架与诱导膜相结合,展现出较好的成骨效能,植入12周后的X射线片显示骨缺损区基本修复。ZWINGENBERGER等[58]利用大鼠股骨临界骨缺损模型评估壳聚糖材料支架成骨效能,研究结果显示壳聚糖材料支架组骨缺损区未能完全修复,相比矿化胶原和同种异松质骨支架,壳聚糖材料支架的机械稳定性和骨传导性仍有待提高。第46届井上春成奖获得者ISHIKAWA团队将碳酸磷灰石蜂窝支架植入大鼠股骨5 mm骨缺损区,术后8周骨缺损区通过软骨内成骨,12周后碳酸磷灰石支架逐渐降解并被新生骨组织替代,局部完成骨修复[59],该研究表明单独的碳酸磷灰石支架骨修复效果与细胞复合骨组织工程支架效果相当,但具有低成本和高安全性的优点。 POBLOTH等[60]运用三维(3D)增材制造策略,定制出钛植入物(Ti网支架),该支架的柔韧性以及优异的生物力学性能有利于临界骨缺损的骨修复,应用于绵羊胫骨4 cm骨缺损模型中,通过降低支架的机械强度,减少骨再生区域的应力遮蔽效应,启动内源性骨再生,增加新骨生成量。TEOTIA等[61]运用3D打印技术生产出含高比例的生物活性陶瓷的(碳酸三甲基酯)多孔三维复合支架,通过兔长骨和颅骨大段骨缺损双模型进行成骨效能评估,发现多孔复合支架模拟了骨骼的微孔结构,仿生结构可加速骨形成,促进长骨和颅骨临界骨缺损的骨愈合。段钢等[62]借助3D打印技术制备β-磷酸三钙仿生骨支架,其具有与实验动物相仿的骨小梁结构,并且整体形貌与兔股骨解剖形态相似,在兔骨缺损模型中表现出良好的成骨活性和生物力学性能。 文章总结了应用在临界骨缺损动物模型中进行骨修复的骨组织工程支架研究概况,见表3。"
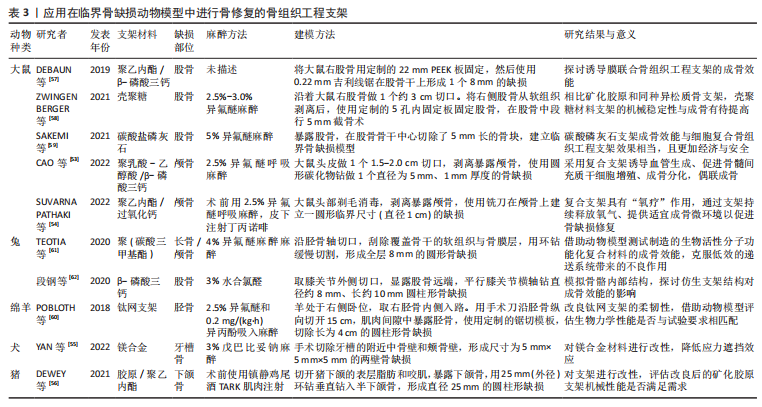

用以评估骨组织工程支架成骨效能的临界骨缺损动物模型具有多样性,但各动物模型对实验室场地、环境与经费预算的要求存在明显差异性。因受制于实验场地、环境与经费,目前实际用于评估骨组织工程支架成骨效能的实验动物模型多集中在大鼠与兔骨缺损模型。通常研究者先借助小动物模型如(大鼠模型)与中等体型动物模型(如兔模型)完成主要实验内容,获得理想实验数据与结果之后,在正式进入临床应用前,还需选用大动物模型(如羊模型或猴模型)进行相关的性能和生物安全性检测。故目前使用大鼠与兔临界骨缺损模型评估骨组织工程支架的成骨效能,在环境要求、实验操作、大规模造模与实验成本等方面具有一定的优势,后期可通过大动物骨缺损模型完善相关实验研究,以满足支架临床前应用的评估。"

| [1] NORRIS B L, VANDERKARR M, SPARKS C, et al. Treatments, cost and healthcare utilization of patients with segmental bone defects. Injury. 2021;52(10):2935-2940. [2] DAHL MT, MORRISON S. Segmental bone defects and the history of bone transport. J Orthop Trauma. 2021;35(Suppl 4):S1-S7. [3] SCHMIDT AH. Autologous bone graft: Is it still the gold standard? Injury. 2021;52 Suppl 2:S18-S22. [4] MASQUELET A. The induced membrane technique. Orthop Traumatol Surg Res. 2020;106(5):785-787.. [5] VALTANEN RS, YANG YP, GURTNER GC, et al. Synthetic and bone tissue engineering graft substitutes: what is the future? Injury. 2021;52 Suppl 2:S72-S77. [6] 王海波,杨新明,张瑛,等.大段骨缺损修复的组织工程学研究进展[J].中华生物医学工程杂志,2013,19(1):73-76. [7] 周思睿,邓江.修复临界及超临界骨缺损的组织工程材料研究进展[J].山东医药,2016,56(48):103-105. [8] SCHMITZ J, HOLLINGER J. The Critical size defect as an experimental model for craniomandibulofacial nonunions. Clin Orthop Related Res. 1986;205:299-308. [9] MAUFFREY C, BARLOW BT, SMITH W. Management of segmental bone defects. J Am Acad Orthop Surg. 2015;23(3):143-153. [10] HOLLINGER JO, KLEINSCHMIDT JC. The critical size defect as an experimental model to test bone repair materials. J Craniofac Surg. 1990;1(1):60-68. [11] BHARADWAZ A, JAYASURIYA AC. Recent trends in the application of widely used natural and synthetic polymer nanocomposites in bone tissue regeneration. Mater Sci Eng C Mater Biol Appl. 2020;110:110698. [12] GUGALA Z, GOGOLEWSKI S. Regeneration of segmental diaphyseal defects in sheep tibiae using resorbable polymeric membranes: a preliminary study. J Orthop Trauma. 1999;13(3):187-195. [13] KOLK A, HANDSCHEL J, DRESCHER W, et al. Current trends and future perspectives of bone substitute materials-from space holders to innovative biomaterials. J Craniomaxillofac Surg. 2012;40(8):706-718. [14] HOBURG A, KESHLAF S, SCHMIDT T, et al. Fractionation of high-dose electron beam irradiation of BPTB grafts provides significantly improved viscoelastic and structural properties compared to standard gamma irradiation. Knee surgery, sports traumatology, arthroscopy: official journal of the ESSKA. 2011;19:1955-1961. [15] 陈胡贵,覃建国,李理,等.大动物节段性骨缺损模型的研究进展[J].北京生物医学工程,2021,40(2):203-208. [16] RHINELANDER FW, PHILLIPS RS, STEEL WM, et al. Microangiography in bone healing. II. Displaced closed fractures. J Bone Joint Surg Am. 1968;50(4):643-662. [17] 李福兵,徐永清,潘兴华,等.小鼠胫骨中段1/3不同缺损直径单层骨皮质缺损模型比较研究[J].中国修复重建外科杂志,2012,26(10):1218-1222. [18] HUANG S, XU L, SUN Y, et al. An improved protocol for isolation and culture of mesenchymal stem cells from mouse bone marrow. J Orthop Translat. 2015;3(1):26-33. [19] AWADEEN MA, AL-BELASY FA, AMEEN LE, et al. Early therapeutic effect of platelet-rich fibrin combined with allogeneic bone marrow-derived stem cells on rats’ critical-sized mandibular defects. World J Stem Cells. 2020;12(1):55-69. [20] GUO T, YUAN X, LI X, et al. Bone regeneration of mouse critical-sized calvarial defects with human mesenchymal stem cell sheets co-expressing BMP2 and VEGF. Lab Anim Res. 2013;29(4):196-203. [21] TAZAWA R, UCHIDA K, MINEHARA H, et al. Poly(POG)n loaded with recombinant human bone morphogenetic protein-2 accelerates new bone formation in a critical-sized bone defect mouse model. J Orthop Surg Res. 2020;15:471. [22] MEEK S, MASHIMO T, BURDON T. From engineering to editing the rat genome. Mamm Genome. 2017;28(7-8):302-314. [23] 王昕.基因编辑技术创新构建大鼠药物代谢模型及其应用[J].中国药理学与毒理学杂志,2019,33(10):814. [24] 孙筱品,董玉梅,汪海燕,等.Neuritin条件性基因打靶载体的构建和同源重组胚胎干细胞克隆鉴定[J].动物医学进展,2019,40(4):16-21. [25] LIU F, FERREIRA E, PORTER RM, et al. Rapid and reliable healing of critical size bone defects with genetically modified sheep muscle. Eur Cell Mater. 2015;30:118-130: 130-131. [26] 曾志奎,黄枫,黄培镇,等.大鼠股骨Masquelet诱导膜实验模型的建立[J].山东医药,2017,57(48):1-4. [27] 马云飞.医用硫酸钙介导的Masquelet技术修复SD大鼠大段骨缺损的实验研究[D].广州:南方医科大学,2017. [28] DRENO M, BLERY P, GUICHEUX J, et al. Development of a rat model of mandibular irradiation sequelae for preclinical studies of bone repair. Tissue Eng Part C Methods. 2020;26(8):447-455. [29] MIGUEZ PA, TUIN SA, ROBINSON AG, et al. Hesperidin promotes osteogenesis and modulates collagen matrix organization and mineralization in vitro and in vivo. Int J Mol Sci. 2021;22(6):3223. [30] ZHANG W, SHI W, WU S, et al. 3D printed composite scaffolds with dual small molecule delivery for mandibular bone regeneration. Biofabrication. 2020,12(3):35020. [31] MANJU V, ANITHA A, MENON D, et al. Nanofibrous yarn reinforced HA-gelatin composite scaffolds promote bone formation in critical sized alveolar defects in rabbit model. Biomed Mater. 2018;13(6):65011. [32] 田彬,胡磊,江青松,等.兔颅顶骨临界骨缺损模型的构建[J].北京口腔医学, 2022,30(2):88-92. [33] 徐石庄,王进,潘文振,等.兔股骨髁临界性骨缺损动物模型制备及临界骨缺损值[J].中国组织工程研究,2020,24(20):3191-3195. [34] LIU F, CHEN K, HOU L, et al. Determining the critical size of a rabbit rib segmental bone defect model. Regen Biomater. 2016;3(5):323-328. [35] LEE JS, PARK TH, RYU JY, et al. Osteogenesis of 3D-Printed PCL/TCP/bdECM scaffold using adipose-derived stem cells aggregates: an experimental study in the canine mandible. Int J Mol Sci. 2021;22(11):5409. [36] KAWAI T, MATSUI K, IIBUCHI S, et al. Reconstruction of critical-sized bone defect in dog skull by octacalcium phosphate combined with collagen. Clin Implant Dent Relat Res. 2011;13(2):112-123. [37] ALVIRA-GONZALEZ J, SANCHEZ-GARCES MA, CAIRO JR, et al. Assessment of bone regeneration using adipose-derived stem cells in critical-size alveolar ridge defects: an experimental study in a dog model. Int J Oral Maxillofac Implants. 2016;31(1):196-203. [38] LUNNEY JK, Van GOOR A, WALKER KE, et al. Importance of the pig as a human biomedical model. Sci Transl Med. 2021;13(621):d5758. [39] MOEST T, SCHLEGEL KA, KESTING M, et al. A new standardized critical size bone defect model in the pig forehead for comparative testing of bone regeneration materials. Clin Oral Investig. 2020;24(5):1651-1661. [40] JOHNSON ZM, YUAN Y, LI X, et al. Mesenchymal stem cells and three-dimensional-osteoconductive scaffold regenerate calvarial bone in critical size defects in swine. Stem Cells Transl Med. 2021;10(8):1170-1183. [41] LI Y, CHEN SK, LI L, et al. Bone defect animal models for testing efficacy of bone substitute biomaterials. J Orthop Translat. 2015;3(3):95-104. [42] REICHERT JC, SAIFZADEH S, WULLSCHLEGER ME, et al. The challenge of establishing preclinical models for segmental bone defect research. Biomaterials. 2009,30(12):2149-2163. [43] GOODMAN R, INSKEEP K. Chapter 44. Neuroendocrine Control of the Ovarian Cycle of the Sheep. 2006:2389-2447. [44] CROVACE AM, LACITIGNOLA L, FORLEO DM, et al. 3D biomimetic porous titanium (Ti(6)Al(4)V ELI) scaffolds for large bone critical defect reconstruction: an experimental study in sheep. Animals (Basel). 2020;10(8):1389. [45] KABIR M A, MURATA M, SHAKYA M, et al. Bio-absorption of human dentin-derived biomaterial in sheep critical-size iliac defects. Materials (Basel). 2021;14(1):223. [46] HETTWER W, HORSTMANN PF, BISCHOFF S, et al. Establishment and effects of allograft and synthetic bone graft substitute treatment of a critical size metaphyseal bone defect model in the sheep femur. APMIS. 2019;127(2):53-63. [47] 孙东东,孙明林,高丽兰.生长因子在软骨组织工程中的研究进展[J].中华骨科杂志,2019,39(10):645-652. [48] RAINA DB, MATUSZEWSKI LM, VATER C, et al. A facile one-stage treatment of critical bone defects using a calcium sulfate/hydroxyapatite biomaterial providing spatiotemporal delivery of bone morphogenic protein-2 and zoledronic acid. Sci Adv. 2020;6(48):eabc1779. [49] WEI X, ZHOU W, TANG Z, et al. Magnesium surface-activated 3D printed porous PEEK scaffolds for in vivo osseointegration by promoting angiogenesis and osteogenesis. Bioact Mater. 2023;20:16-28. [50] KIM DS, LEE JK, KIM JH, et al. Advanced PLGA hybrid scaffold with a bioactive PDRN/BMP2 nanocomplex for angiogenesis and bone regeneration using human fetal MSCs. Sci Adv. 2021;7(50):j1083. [51] SHUAI C, YANG W, FENG P, et al. Accelerated degradation of HAP/PLLA bone scaffold by PGA blending facilitates bioactivity and osteoconductivity. Bioact Mater. 2021;6(2):490-502. [52] 邢晓敏,邓蕊.第三类医疗器械临床试验伦理问题案例探讨[J].中国新药与临床杂志,2018,37(8):467-471. [53] CAO H, LI L, LI L, et al. New use for old drug: local delivery of puerarin facilitates critical-size defect repair in rats by promoting angiogenesis and osteogenesis. J Orthop Translat. 2022;36:52-63. [54] SUVARNAPATHAKI S, WU X, ZHANG T, et al. Oxygen generating scaffolds regenerate critical size bone defects. Bioact Mater. 2022;13:64-81. [55] YAN ZY, ZHU JH, LIU GQ, et al. Feasibility and efficacy of a degradable magnesium-alloy GBR membrane for bone augmentation in a distal bone-defect model in beagle dogs. Bioinorg Chem Appl. 2022;2022:4941635. [56] DEWEY MJ, MILNER DJ, WEISGERBER D, et al. Repair of critical-size porcine craniofacial bone defects using a collagen-polycaprolactone composite biomaterial. Biofabrication. 2021;14(1):10. [57] DEBAUN MR, STAHL AM, DAOUD AI, et al. Preclinical induced membrane model to evaluate synthetic implants for healing critical bone defects without autograft. J Orthop Res. 2019;37(1):60-68. [58] ZWINGENBERGER B, VATER C, BELL RL, et al. Treatment of critical-size femoral bone defects with chitosan scaffolds produced by a novel process from textile engineering. Biomedicines. 2021;9(8):1015. [59] SAKEMI Y, HAYASHI K, TSUCHIYA A, et al. Reconstruction of critical-size segmental defects in rat femurs using carbonate apatite honeycomb scaffolds. J Biomed Mater Res A. 2021;109(9):1613-1622. [60] POBLOTH AM, CHECA S, RAZI H, et al. Mechanobiologically optimized 3D titanium-mesh scaffolds enhance bone regeneration in critical segmental defects in sheep. Sci Transl Med. 2018;10(423):eaam8828. [61] TEOTIA AK, DIENEL K, QAYOOM I, et al. Improved bone regeneration in rabbit bone defects using 3d printed composite scaffolds functionalized with osteoinductive factors. ACS Appl Mater Interfaces. 2020;12(43):48340-48356. [62] 段钢,陈宏亮,郭开今,等.3D打印β-磷酸三钙仿生骨支架修复兔股骨髁骨缺损[J]. 骨科临床与研究杂志,2020,5(4):243-250. |
| [1] | Yang Yufang, Yang Zhishan, Duan Mianmian, Liu Yiheng, Tang Zhenglong, Wang Yu. Application and prospects of erythropoietin in bone tissue engineering [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(9): 1443-1449. |
| [2] | Chen Kaijia, Liu Jingyun, Cao Ning, Sun Jianbo, Zhou Yan, Mei Jianguo, Ren Qiang. Application and prospect of tissue engineering in treatment of osteonecrosis of the femoral head [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(9): 1450-1456. |
| [3] | Yu Weijie, Liu Aifeng, Chen Jixin, Guo Tianci, Jia Yizhen, Feng Huichuan, Yang Jialin. Advantages and application strategies of machine learning in diagnosis and treatment of lumbar disc herniation [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(9): 1426-1435. |
| [4] | Lin Zeyu, Xu Lin. Research progress in gout-induced bone destruction mechanism [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(8): 1295-1300. |
| [5] | Dai Yuexing, Zheng Liqin, Wu Minhui, Li Zhihong, Li Shaobin, Zheng Desheng, Lin Ziling. Effect of vessel number on computational fluid dynamics in vascular networks [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(8): 1206-1210. |
| [6] | Li Rui, Zhang Guihong, Wang Tao, Fan Ping. Effect of ginseng polysaccharide on the expression of prostaglandin E2/6-keto-prostaglandin 1alpha in traumatic osteoarthritis model rats [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(8): 1235-1240. |
| [7] | Zhou Chao, Yu Guangyu, Fan Jiaqi, Yu Chunmei, Wu Min, Chen Shibei. Establishment and validation of embryo high-quality prediction models based on the third-day 340 nm absorbance embryo culture [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(7): 1050-1056. |
| [8] | Wang Shanshan, Shu Qing, Tian Jun. Physical factors promote osteogenic differentiation of stem cells [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(7): 1083-1090. |
| [9] | Ma Shuwei, He Sheng, Han Bing, Zhang Liaoyun. Exosomes derived from mesenchymal stem cells in treatment of animals with acute liver failure: a meta-analysis [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(7): 1137-1142. |
| [10] | Zhang Kefan, Shi Hui. Research status and application prospect of cytokine therapy for osteoarthritis [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(6): 961-967. |
| [11] | Hu Zhixing, Li Qun, Yang Chao, Wang Xiaoxiao, Fang Luochangting, Hou Wuqiong, Lin Na, Chen Weiheng, Liu Chunfang, Lin Ya. Network meta-analysis of the modeling effects of different factors on rabbit models of steroid-induced osteonecrosis of femoral head [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(6): 976-984. |
| [12] | Wang Jianchun, Yang Shuqing, Su Xin, Wang Hongyuan. Different contents of B2O3 affect mechanical properties and bioactivity of bioactive glass scaffolds [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(5): 712-716. |
| [13] | Lan Weiwei, Yu Yaodong, Huang Di, Chen Weiyi. In vitro degradation behavior of Mg-Zn-Ca alloys [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(5): 717-723. |
| [14] | Zhou Xiaowen, Fu Zuchang, Huang Fei, Ai Jianguo, Zhao Feng. Bone defect blocked by bone cement segmental filling in single-plane tibial bone transport [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(5): 736-740. |
| [15] | Zhang Yihai, Shang Peng, Ma Benyuan, Hou Guanghui, Cui Lunxu, Song Wanzhen, Qi Dexuan, Liu Yancheng. Structural design and mechanical property analysis of trabecular scaffold of triply periodic minimal surface with a radial gradient [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(5): 741-746. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||