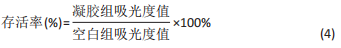1.1 设计 水凝胶支架的制备与表征,实验数据采用单因素方差分析。
1.2 时间及地点 实验于2021年9月至2022年5月在汕头大学海洋生物技术重点实验室H407完成。
1.3 材料
1.3.1 细胞 小鼠脐带间充质干细胞购于上海烜雅生物科技有限公司。
1.3.2 试剂 壳聚糖(西安普瑞斯生物工程有限公司,中国);盐酸(优级纯,西陇化工股份有限公司,中国);双氰胺(山东华特威生物科技有限公司,中国);无水乙醇(分析纯,西陇科学股份有限公司,中国);乙酸(分析纯,西陇科学股份有限公司,中国);β-甘油磷酸钠(Sigma-Aldrich公司,美国);鱼胶原蛋白、CCK-8、4%组织固定液、溶菌酶、4%鸡红细胞悬液(北京索莱宝科技有限公司,中国);碳酸氢钠(分析纯、广东光华科技股份有限公司,中国);1×PBS缓冲液(Biosharp,中国);DMEM培养基(赛默飞世尔生物化学制品有限公司,北京);胎牛血清(Zeta Life,美国);青霉素-链霉素、0.25% 胰蛋白酶、Calcein/PI细胞活性与细胞毒性检测试剂盒(Beyotime,中国);二甲基亚砜(MP Biomedicals,LLC,美国);生理盐水注射液(广东科伦药业有限公司,中国);脐带间充质干细胞完全培养基(Peocell,中国)。
1.3.3 仪器 37 ℃恒温水浴锅、磁力搅拌水浴锅(上海坤诚科学仪器有限公司,中国);SHZ-D(Ⅲ)循环水式多用真空泵(郑州特尔仪器设备有限公司,中国);扫描电子显微镜(泰思肯有限公司,中国);电子天平(Sartorius,德国);冷冻干燥机(青岛永合创信电子科技有限公司,中国);24孔板、细胞培养皿、冻存管、离心管、一次性细胞培养皿、6孔板、24孔板、96孔板、0.22 μm滤膜(Biofil,中国);多功能微孔板检测仪(Biotek,美国);3-5 N离心机(湖南恒诺仪器设备有限公司,中国);CO2无菌培养箱(Thermo,美国);光学显微镜(宁波舜宇仪器有限公司,中国)。
1.4 实验方案
1.4.1 壳聚糖的改性 4 g壳聚糖溶于100 mL 0.2 mol/L盐酸,50 ℃水浴加热搅拌1 h,待壳聚糖溶解后加入3 g双氰胺和50 mL去离子水的混合溶液,并在90 ℃下搅拌1 h,同时向液体中滴加2 mL 0.1 mol/L盐酸调节pH值(反应开始时和反应结束前30 min加入,共2次,每次2 mL)。反应结束后静置冷却至室温,加入无水乙醇析出絮状沉淀,减压抽滤,无水乙醇洗涤。将产品冻干,研磨,得到CGH粉末。反应式见图1[32]。
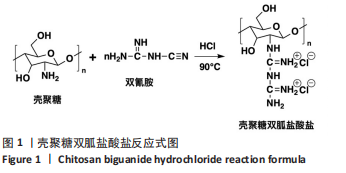
1.4.2 复合水凝胶的制备
(1)原料准备:①2%壳聚糖:2 g壳聚糖溶于100 mL 0.1 mol/L乙酸;②2%CGH:2 g CGH溶于100 mL去离子水;③50% β-甘油磷酸钠:17.714 g β-甘油磷酸钠,用去离子水定容至25 mL;④0.5%鱼胶原蛋白:0.25 g鱼胶原蛋白溶于50 mL去离子水;⑤2%碳酸氢钠:2 g碳酸氢钠溶于100 mL去离子水。
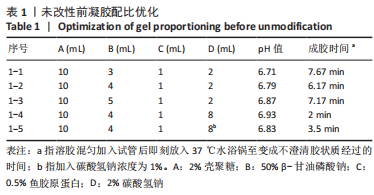
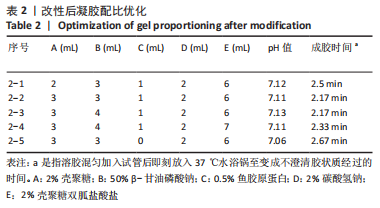
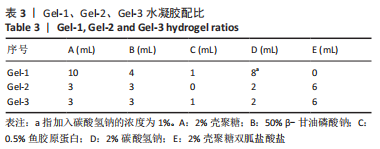
(2)水凝胶配比优化:用上述原料尝试配制水凝胶,成胶温度设定为37 ℃。以水凝胶成胶时间、成胶效果、pH值范围为标准,探究符合条件的水凝胶配比。为了对比壳聚糖改性后对水凝胶的影响,遵循制备标准,利用未改性的壳聚糖制备水凝胶,以及再添加CGH制备水凝胶,对它们进行理化性质的表征。
1.4.3 小鼠脐带间充质干细胞的培养
(1)脐带间充质干细胞的复苏:将购置的脐带间充质干细胞于37 ℃水浴解冻后将其转移至离心管,1 200 r/min离心3 min,弃上清,加入1 mL 基本培养基(90% DMEM培养基,体积分数为10%胎牛血清,1%青霉素-链霉素)轻轻悬浮脐带间充质干细胞,转移到一次性细胞培养皿,加入4 mL基本培养基,放入CO2无菌培养箱培养。
(2)脐带间充质干细胞的换液:将一次性培养皿中的培养基倒出,用1 mL PBS洗两三次,再加入5 mL基本培养基,每2 d换液1次。
(3)脐带间充质干细胞的传代:脐带间充质干细胞铺满整个培养皿底部80%以上即可传代。将一次性培养皿中的培养基倒出,用1 mL PBS洗两三次,加入1 mL 0.25%胰蛋白酶消化,在CO2无菌培养箱温育2 min,轻拍培养皿壁且显微镜观察脐带间充质干细胞从培养皿底部消化下来,加入1 mL基本培养基(至少与加入酶体体积一致)终止消化,消化液全部转移至离心管,1 200 r/min离心3 min,弃上清,加入3 mL基本培养基轻轻悬浮脐带间充质干细胞,均分到3个一次性培养皿中,每个培养皿加入4 mL基本培养基继续培养,脐带间充质干细胞代数不超过10代。
(4)脐带间充质干细胞的冻存:为保证细胞活力和提高实验容错率,对部分脐带间充质干细胞(第2代)进行冻存。将一次性培养皿中的培养基倒出,用1 mL PBS洗两三次,加入1 mL 0.25% 胰蛋白酶消化,在CO2无菌培养箱温育2 min,轻拍培养皿壁且显微镜观察脐带间充质干细胞从培养皿底部消化下来,加入1 mL基本培养基(至少与加入酶体体积一致)终止消化,消化液全部转移至离心管,1 200 r/min离心3 min,弃上清,加入2 mL冻存液(1 mL二甲基亚砜+9 mL基本培养基),轻轻悬浮细胞,全部溶液转移到冻存管中并于-80 ℃冰箱冻存。
1.4.4 表征与测试
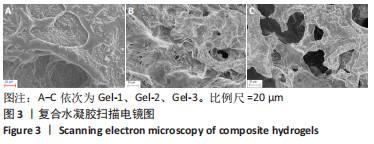
(1)扫描电子显微镜观察冻干水凝胶的横截面形貌以及孔径大小及分布:先将水凝胶样品冷冻干燥48 h后得到干燥凝胶样品,用液氮淬断干燥凝胶样品,表面真空喷金20 min以提高导电率,扫描电镜观察,电压10 kV。
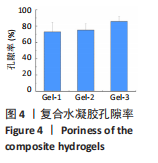
(2)复合水凝胶孔隙率和溶胀比测定:称取适量水凝胶干品记其质量m0和体积v,浸泡于50 mL无水乙醇中,使液体充分进入凝胶孔隙,用滤纸吸干表面的乙醇,记录凝胶质量m,重复3次平行实验,以公式(1)计算孔隙率:

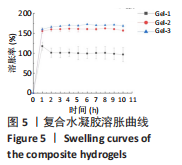
称取适量水凝胶干品记其质量m0,将样品浸泡在PBS中,按1 h为时间间隔取出,用滤纸轻轻吸干表面的水,并立即称质量mt,重复3次平行实验,以此进行10 h时间长度的质量。由公式(2)计算溶胀比:

(3)复合水凝胶体外降解性能测定:将水凝胶冻干称质量记作m0,利用2% 溶菌酶对水凝胶冻干样进行降解,每
3 d更换1次降解液,分别在1,3,5,7,11,15 d取出样品冻干称质量记作mn,重复3次平行实验,利用公式(3)计算降解率:

(4)复合水凝胶毒性测定:选取表征综合性能最好的水凝胶,制备并称取0.4 g水凝胶于10 mL 基本培养基中浸泡24 h,将浸提液过滤后得到0.04 g/mL的原液,将其稀释至
0.02 g/mL作为母液,再将母液稀释10倍、100倍得到稀释液。
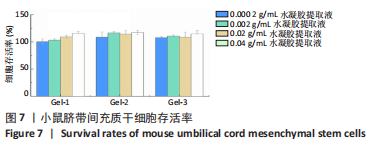
将培养至第3代的脐带间充质干细胞用0.25%胰蛋白酶消化,将细胞浓度调整为1×109 L-1,用基本培养基悬浮后接种到96孔板,每孔加100 μL脐带间充质干细胞悬液,过夜培养,待细胞贴壁后,PBS洗2次,每孔加入100 μL梯度稀释的稀释液,以每孔加入100 μL基本培养基为对照,培养24 h
后加入CCK-8,每孔10 μL,孵育48 h后在酶标仪450 nm
处测吸光度值,每组重复5次平行实验,以公式(4)计算脐带间充质干细胞的存活率。
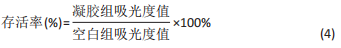
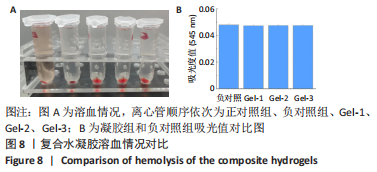
(5)复合水凝胶溶血性能测定:先将4%鸡红细胞悬液用生理盐水稀释得到2%鸡红细胞悬液。制备表征综合性能最好的水凝胶,取0.1 g凝胶于6 mL生理盐水中,37 ℃浸泡24 h,然后取2 mL凝胶提取液,向其中加入100 μL 2%鸡红细胞悬液,以2 mL生理盐水中加入100 μL 2%鸡红细胞悬液做负对照,2 mL去离子水中加入100 μL 2%鸡红细胞悬液做正对照,37 ℃孵育1 h,8 000 r/min离心5 min,取上清,每组重复5次平行实验,在酶标仪545 nm处测凝胶组和负对照组的吸光度值,比对凝胶组和负对照组的吸光度值分析其溶血性能。
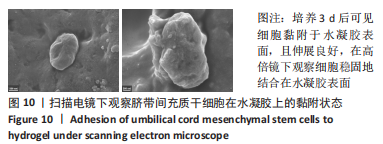
(6)脐带间充质干细胞黏附效应测定:将表征综合性能最好的水凝胶原料过0.22 μm滤膜除菌后配制水凝胶前体液,在6孔板中加入3 mL水凝胶前体液,放入37 ℃培养箱成胶。将第3代脐带间充质干细胞用0.25%胰蛋白酶消化,将细胞浓度调整为1×109 L-1,用完全培养基重悬。水凝胶成胶后在6孔板每孔加入1 mL细胞悬液和4 mL脐带间充质干细胞完全培养基,培养2 d后吸出3 mL旧培养基,再加入3 mL新培养基,培养3 d后吸出全部培养基,加入4%组织固定液固定30 min,然后进行乙醇梯度脱水(体积分数为10%,30%,50%,70%,85%,90%,100%),冻干后置于扫描电镜下观察。
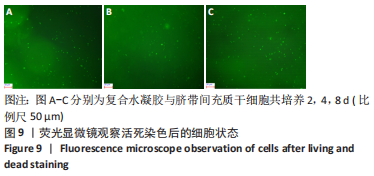
(7)复合水凝胶与脐带间充质干细胞共培养后活死细胞染色:将配制表征综合性能最好的水凝胶原料用0.22 μm滤膜除菌后配制水凝胶前体液,用水凝胶前体液悬浮第3代脐带间充质干细胞后接种到24孔板中,每孔500 μL,然后将24孔板放入37 ℃培养箱成胶,成胶后每孔加入2 mL 脐带间充质干细胞完全培养基,在培养的第2,4,8天进行活死细胞染色。
1.5 主要观察指标 水凝胶的形态、孔隙率、溶胀性能、降解性以及溶血情况。水凝胶的细胞毒性、细胞存活情况、细胞黏附效应。