1.1 设计 动物体内实验和细胞学体外实验,组间比较采用单因素方差分析。
1.2 时间及地点 实验于2018年12月至2020年7月在西安市儿童医院中心实验室完成。
1.3 材料
1.3.1 实验动物 无特定病原体级新生雌性SD大鼠40只,体质量5-10 g,购自西安交通大学实验动物中心,许可证号:SCXK(陕)2017-0007。实验方案经西安市儿童医院动物实验伦理委员会批准,批准号为XACH2017-0135。实验过程遵循了国际兽医学编辑协会《关于动物伦理与福利的作者指南共识》和本地及国家法规。
1.3.2 试剂及仪器 淫羊藿苷购自西安康诺化工有限公司;丙基硫氧嘧啶购自美国MCE公司;锂盐购自MCE公司;DMEM培养液、胎牛血清购自美国Hyclone公司;青霉素-链霉素、0.25%胰蛋白酶/EDTA消化液购自美国Sigma公司;Trizol试剂盒购自美国Sigma公司;转染试剂Lipofectamine®3000购自美国Sigma公司;PROP成对同源1蛋白(prop paired end homology 1 protein,ROP1)、LIM同源框4(LIM homeobox 4,LHX4)及HESX1等一抗及相应二抗购自美国Santa Cruz公司;实时荧光定量PCR试剂盒购自美国Millipore公司;RNA提取试剂盒购自美国Millipore公司;反转录试剂盒购自美国Millipore公司;蛋白提取试剂盒购自美国Millipore公司;ELISA试剂盒购自美国Millipore公司;引物合成由上海生工合成;CCK-8试剂盒购自美国Millipore公司;miR-17-5p模拟物(mimic)、miR-17-5p抑制剂(inhibitor)、模拟物阴性对照(NC mimic)、抑制剂阴性对照(NC inhibitor)由上海生工合成。
高通量实时荧光定量PCR仪(Roche公司,瑞士);Western blot系统(北京六一仪器厂DYY-7C);台式低温高速离心机(日本KUBOTA公司);细胞培养箱(上海力申科学仪器公司);凝胶成像分析仪(广州瑞丰实验设备有限公司);双荧光素酶报告基因检测系统(Promega,美国)。
1.4 方法
1.4.1 动物体内实验
(1)甲状腺功能减退大鼠模型建立及分组:按随机数字表法将40只新生雌性SD大鼠随机选取32只,每日灌服丙基硫氧嘧啶1.5 mg/kg制备模型,连续给药10 d;其余8只大鼠纳入对照组,每日用等量生理盐水灌胃。大鼠头颈部皮下注射促甲状腺激素释放激素后促甲状腺激素无明显变化则建模成功。
将建模成功的大鼠随机分为模型组及75,150,300 mg/kg淫羊藿苷组,每组8只。75,150,300 mg/kg淫羊藿苷组分别给予75,150,300 mg/kg淫羊藿苷灌胃,1次/d,连续给药10 d;模型组给予等体积的生理盐水。
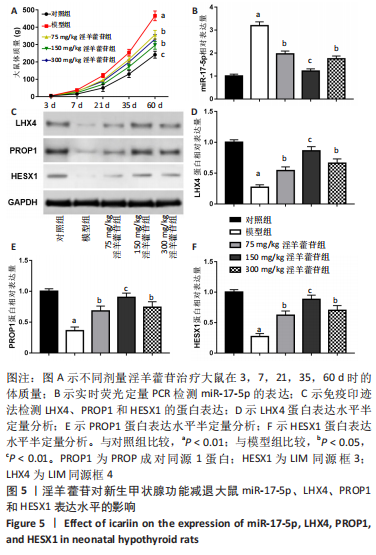
(2)取材:5组大鼠均在实验终止后24 h用相同处理办法取材。大鼠眼眶放血后腹腔注射35 mg/kg戊巴比妥钠麻醉断颈处死,取大鼠脑垂体组织,用预冷的PBS冲洗掉多余血液,将采集的脑垂体组织样本剪碎并在加有组织裂解液的研钵中充分研磨,过滤,PBS冲洗3次,用组织匀浆器匀浆至无明显肉眼可见固体。将组织匀浆吸入预冷的无菌离心管中,于4 ℃,10 000 r/min条件下离心5 min,取离心后的上清得到组织总蛋白,应用Western blotting检测LHX4、PROP1和HESX1蛋白的表达水平。
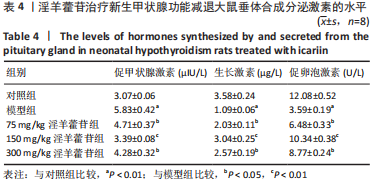
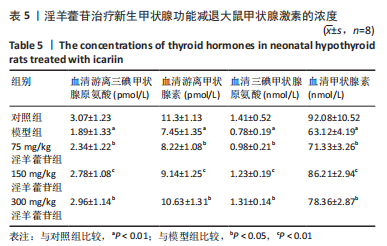
各组大鼠静脉采血离心获得血清,用ELISA法检测血清中生长激素、促卵泡激素和促甲状腺激素的分泌水平。

1.4.2 细胞体外实验
(1)细胞培养
大鼠垂体前叶原代细胞培养:新生雌性SD大鼠眼眶放血后腹腔注射35 mg/kg戊巴比妥钠麻醉断颈处死,在无菌条件下摘除垂体前叶组织,将其剪切成0.2-0.5 mm3的碎块,加入4 mL无菌胰蛋白酶液(浓度为25%),37 ℃恒温水浴30 min,然后加入含体积分数10%胎牛血清的DMEM培养液2 mL以终止消化。将滤液1 500 r/min离心10 min,使用5 mL DMEM培养液重悬细胞。细胞计数后按6.0×108 L-1的浓度接种于24孔培养板中培养,每孔1 mL。
大鼠甲状腺组织单细胞悬液的制备及细胞的原代培养:新生雌性SD大鼠(购自西安交通大学动物实验中心)眼眶放血后,腹腔注射35 mg/kg戊巴比妥钠麻醉断颈处死,PBS洗涤以充分显露甲状腺组织。将甲状腺组织浸泡于含1 g/LⅠ型胶原酶的组织消化液中于37℃消化2 h。消化后的组织液经Ficoll分离得甲状腺单个核细胞,用RPMI 1640培养基洗2遍,然后调整细胞浓度至2×108 L-1后于6孔板中接种,每3 d半量换液1次。为了探索甲状腺激素对垂体前叶细胞合成分泌激素的影响,采用Transwell系统将大鼠甲状腺细胞与垂体前叶细胞共培养。将1×104个垂体前叶细胞接种在腔室的底板中,并将3×104个甲状腺细胞接种在上腔室中。共培养48 h后,加入30 μmol/L锂盐处理细胞24 h。随后收集垂体前叶细胞,用于后续实验。
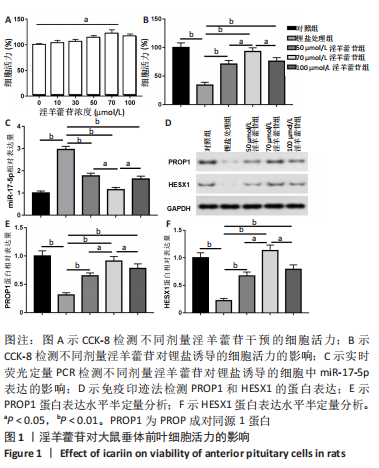
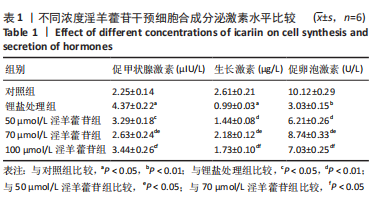
淫羊藿苷处理大鼠垂体前叶细胞:分别使用不同剂量(0,10,30,50,70,100 μmol/L)淫羊藿苷处理大鼠垂体前叶细胞24 h,收获细胞检测细胞活力,评估淫羊藿苷对垂体前叶细胞的毒性剂量。随后使用50,70,100 μmol/L的淫羊藿苷处理锂盐诱导的垂体前叶细胞24 h,收获细胞检测实验指标。
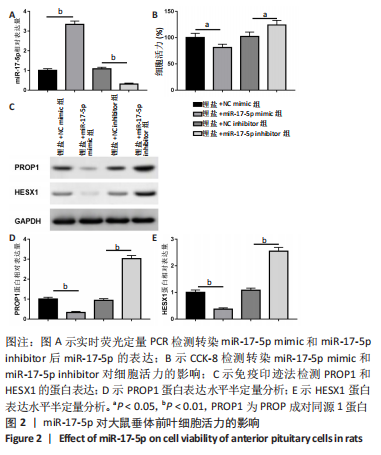
(2)载体构建及转染:根据GenBank(https://www.ncbi.nlm.nih.gov/genbank/GenBank)中LHX4基因序列,采用Oligo 6.0软件设计引物,并交由上海生工合成。将测序正确的LHX4基因克隆到pcDNA-3.1载体中,构建pcDNA-LHX4表达载体。采用siDESIEN软件设计引物,BLAST对比序列同源性,靶向LHX4基因的siRNA序列由上海生工合成。分别使用miR-17-5p模拟物(mimic)、miR-17-5p抑制剂(inhibitor)、模拟物阴性对照(NC mimic)、抑制剂阴性对照(NC inhibitor)转染锂盐处理前和处理后的大鼠垂体前叶细胞,或使用pcDNA-LHX4过表达载体、LHX4 siRNA、pcDNA3.1空载体、NC-siRNA转染锂盐处理后的大鼠垂体前叶细胞,所有转染均使用Lipofectamine®3000根据制造商的说明进行。
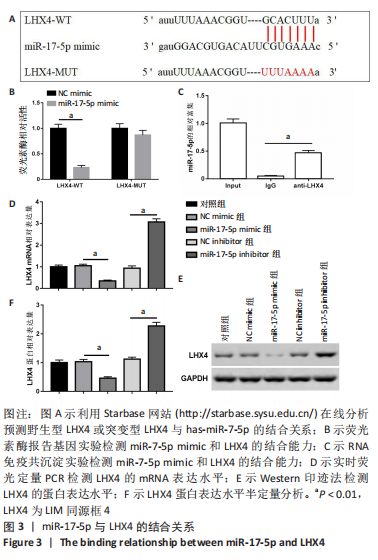
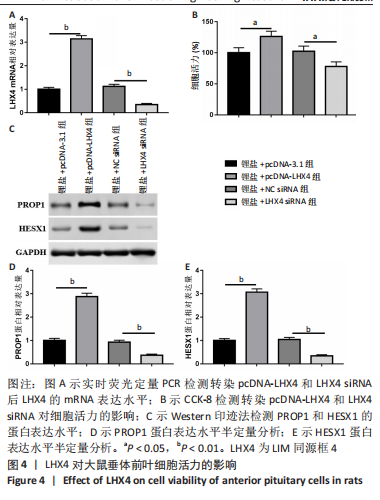
(3)实时荧光定量PCR:检测LHX4的mRNA水平和miR-17-5p的表达,按照TRIZOL试剂盒说明书提取各组垂体前叶细胞总RNA。Superscript III反转录酶用于合成cDNA模板。用SYBR ExScript qPCR试剂盒在以下条件下进行:95 ℃预变性2 min,94 ℃变性15 s,55 ℃退火25 s,在72 ℃延伸15 s,进行35个循环。PCR产物经1%琼脂糖凝胶电泳检测。
实时荧光定量PCR引物序列如下:GAPDH上游5′‐GAC TCA TGA CCA CAG TCC ATG C‐3′, 下游5′‐AGA GGC AGG GAT GAT GTT CTG‐3′;U6上游5′‐CTC GCT TCG GCA GCA CA‐3′,下游5′‐AAC GCT TCA CGA ATT TGC GT‐3′;miR-17-5p上游5′‐CGG CGG CAA AGT GCT TAC AG‐3′, 下游5′‐GTG CAG GGT CCG AGG T‐3′;LHX4上游5′‐AGC GAC TCA CCT GTC AAG TG‐3′,下游5′‐TAT CTC TGG GCC AGG CTT CT‐3′。依据2-ΔΔCt法计算各样本相对表达量。
(4) Western印迹法检测蛋白表达:检测LHX4、PROP1和HESX1的蛋白表达。将各组大鼠垂体前叶细胞按照每孔1×105的浓度接种于6孔板,24 h后换液,进行无血清培养基培养。采用BCA法进行蛋白定量,各取15 μL样品进行SDS-PAGE,再将蛋白转移至膜上,5%脱脂奶粉室温封闭1 h,加入一抗:鼠抗LHX4(1∶1 000,ab50790)、兔抗PROP1(1∶500,ab172084)、鼠抗HESX1(1∶500,ab67728)和兔抗GAPDH(1∶2 500,ab9485),4 ℃孵育过夜。加入辣根过氧化物酶标记的山羊抗兔二抗(1∶1 000,ab150077)或山羊抗鼠二抗(1∶2 000,ab6728)37 ℃孵育45 min,用ECL液显影,使用化学发光试剂盒在化学发光系统检测,随后结果采用Image-Pro Plus 6软件(Media Cybernetics)分析,以待测蛋白与内参照GAPDH的灰度值比值作为蛋白的相对表达量。
(5)CCK-8实验检测细胞活力:将各组大鼠垂体前叶细胞按照每孔1×105的浓度接种于96孔板中,用含体积分数10%胎牛血清的DMEM培养基制成单细胞悬液,置于37 ℃、体积分数5%CO2的条件下培养。每组设5个复孔,待细胞长至80%融合时,于转染后48 h加入20 μL CCK-8溶液。培养24 h,于酶标仪450 nm处检测吸光度(A)值。取5孔A值的平均数,按照下列公式计算细胞相对活力:细胞相对活力(%)=处理组A/对照组A×100%。
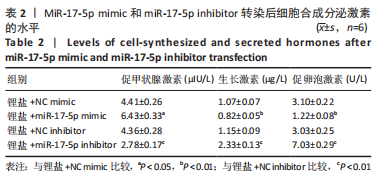
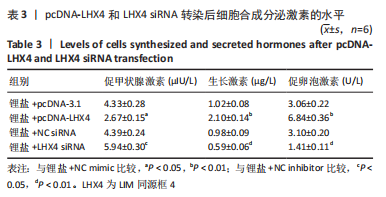
(6)激素水平检测:根据制造商的说明,通过ELISA试剂盒(Thermo Fisher Scientific,Waltham,MA,USA)测定大鼠垂体前叶细胞、甲状腺功能减退大鼠血清中促卵泡激素、生长激素和促甲状腺激素水平。
(7)生物信息学分析及双荧光素酶报告基因实验:利用PITA(https://genie.weizmann.ac.il/pubs/mir07/mir07_data.html)数据库预测miR-17-5p的靶基因。设计合成含有LHX4 3’UTR野生型(LHX4-Wt)或突变型(LHX4-Mut)片段的pmirGLO双荧光素酶报告基因质粒。将上述质粒与miR-17-5p mimic或NC mimic共转染至HEK-293T细胞中,48 h后采用双荧光素酶报告基因检测系统检测荧光素酶活性。
(8)RNA结合蛋白免疫沉淀实验检验miR-17-5p和LHX4的结合:使用RNA结合蛋白免疫沉淀裂解缓冲液裂解大鼠垂体前叶细胞,并将100 μL裂解物与含有磁珠的缓冲液一起温育,所述磁珠与LHX4抗体(1∶20)或对照正常兔免疫球蛋白(IgG,1∶200)共同孵育。IgG作为阴性对照。然后将蛋白酶K缓冲液添加到样品中以消化蛋白质。最后,用Trizol试剂盒从珠子中分离结合的RNA,并用实时荧光定量PCR测定纯化的RNA。
1.5 主要观察指标
细胞检测指标:①细胞活力;②miR-17-5p表达水平;③LHX4、PROP1和HESX1蛋白表达水平;④生长激素、促卵泡激素和促甲状腺激素的分泌水平。
动物实验检测指标:①大鼠体质量;②大鼠脑垂体中miR-17-5p表达水平;③大鼠脑垂体中LHX4、PROP1和HESX1蛋白表达水平;④大鼠血清中生长激素、促卵泡激素和促甲状腺激素的分泌水平。
1.6 统计学分析 文章统计学方法已经西安市儿童医院生物统计学专家审核。数据均采用SPSS 20.0统计软件进行统计学分析,呈正态分布的计量资料以x±s表示。采用ANOVA方差分析、Dunnett-t法比较总体和总体中两样本均数之间的差异。以P < 0.05为差异有显著性意义。