中国组织工程研究 ›› 2021, Vol. 25 ›› Issue (14): 2148-2153.doi: 10.3969/j.issn.2095-4344.3517
• 脊柱组织构建 spinal tissue construction • 上一篇 下一篇
通督活血汤含药血清可抑制椎间盘纤维环细胞的焦亡
吴子健1,胡昭端1,周晓红1,李 佳1,李柏村2,蔡国伟2,彭 锐1
- 1湖北中医药大学,湖北省武汉市 430065;2华中科技大学同济医学院附属协和医院针灸科,湖北省武汉市 430020
Tongdu Huoxue Decoction-medicated serum inhibits pyroptosis in annulus fibrosus cells of the intervertebral disc
Wu Zijian1, Hu Zhaoduan1, Zhou Xiaohong1, Li Jia1, Li Bocun2, Cai Guowei2, Peng Rui1
- 1Hubei University of Traditional Chinese Medicine, Wuhan 430065, Hubei Province, China; 2Department of Acupuncture, Wuhan Union Hospital of China, Tongji Medical College, Huazhong University of Science and Technology, Wuhan 430020, Hubei Province, China
摘要:  文题释义:
文题释义:
细胞焦亡:是一种不同于细胞凋亡和细胞坏死的另一种程序性死亡方式,它由炎症性半胱氨酸蛋白酶(如Caspase-1/4/5/11)介导,可在胞质内产生炎症小体,进而活化炎症递质(如白细胞介素1β、白细胞介素18)并破坏细胞膜形成孔洞,导致细胞逐渐膨胀破裂,炎性物质渗出而激发强烈的炎症反应,因与炎症反应密切相关,所以又称之为炎症性死亡。
中药含药血清:是指经动物灌胃给予中药及制剂,经胃肠道吸收后进入机体血液循环,在一定时间内采集血液,此时分离所得的血清必定含有一定量的该药物成分,其血药浓度反映了机体的真实血药浓度,将此血清加入到体外细胞培养体系,观察其药理作用的一种体外实验方法。
背景:腰椎间盘退变是腰椎间盘突出症的主要病理改变,与椎间盘纤维环细胞的程序性死亡密切相关。既往临床研究表明,通督活血汤治疗腰椎间盘突出症疗效显著,其是否通过抑制椎间盘纤维环细胞焦亡起作用值得深入研究。
目的:通过观察通督活血汤含药血清对脂多糖/ATP诱导的椎间盘纤维环细胞焦亡的影响,探讨通督活血汤治疗腰椎间盘突出症的可能作用机制。
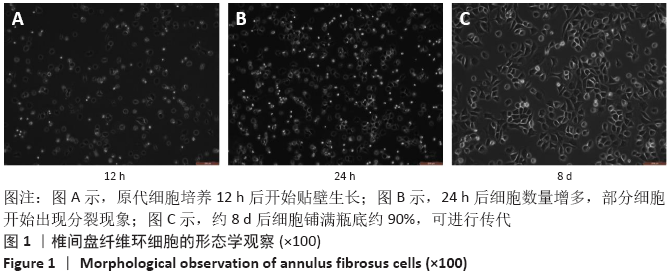
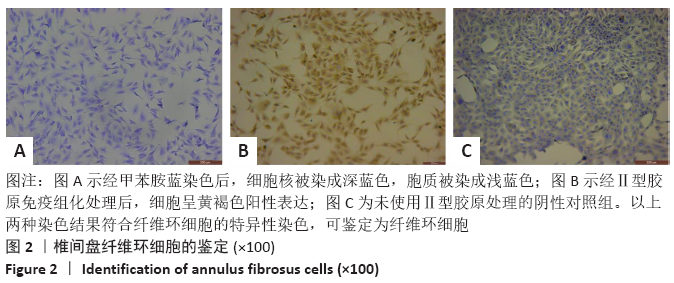
方法:将36只10周龄SD大鼠以通督活血汤灌胃,连续灌胃7 d后腹主动脉取血,制备含药血清。提取4周龄SD大鼠的腰椎间盘,采用机械-酶消化法提取椎间盘纤维环细胞,培养至第2代后采用甲苯胺蓝染色法和Ⅱ型胶原免疫组化染色法进行鉴定。之后将第2代细胞随机分为空白组、模型组、含药血清低、中、高剂量组,除空白组外,其余4组予脂多糖/ATP制造细胞焦亡模型,成模后低、中、高剂量含药血清组分别予5%,10%,20%通督活血汤含药血清干预,空白组不采取任何干预措施。采用MTT法摸索含药血清干预椎间盘纤维环细胞焦亡的最佳干预浓度和最佳干预时间;采用流式细胞术Annexin V FIFT/PI双染测定细胞焦亡率;采用ELISA法检测各组细胞上清液的白细胞介素1β、白细胞介素18的表达量;采用qRT-PCR检测各组半胱氨酸蛋白酶1、Gasdermin D(GSDMD)、NOD样受体蛋白3基因的表达量;采用Western Blot法检测各组半胱氨酸蛋白酶1、GSDMD、NOD样受体蛋白3蛋白的表达量。
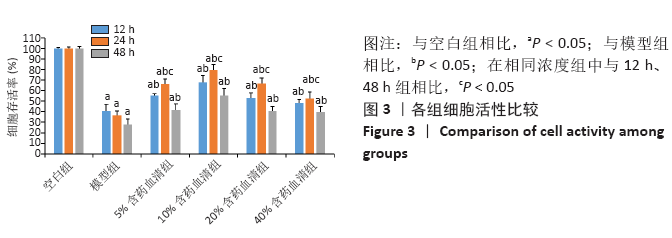
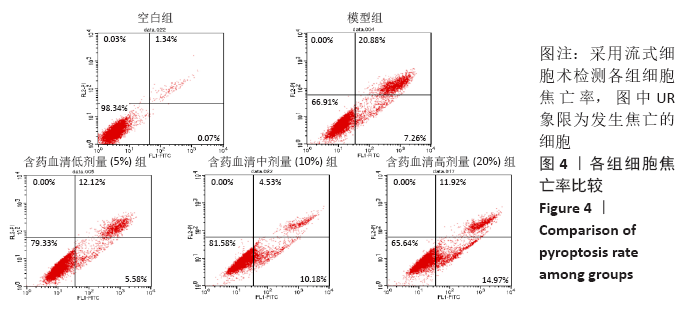
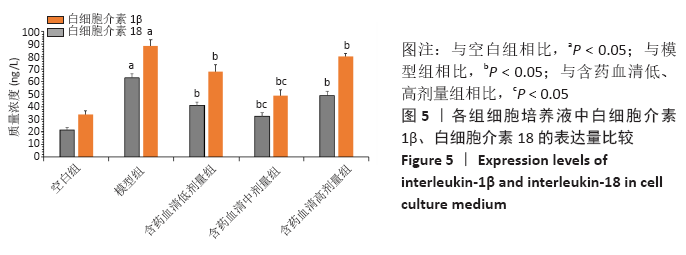
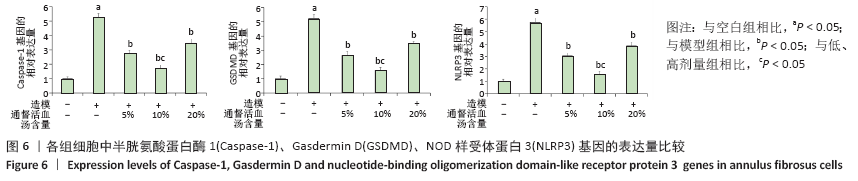
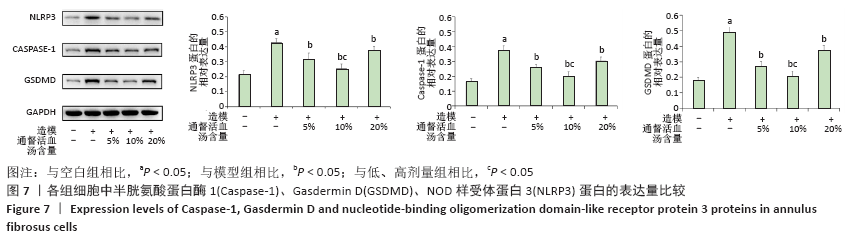
结果与结论:①MTT结果示:通督活血汤含药血清干预椎间盘纤维环细胞焦亡的最佳干预浓度为10%,最佳干预时间为24 h;②流式细胞术结果示:与空白组相比,其他4组细胞焦亡比率明显增加;与模型组相比,含药血清各剂量组细胞焦亡比率明显下降;与低、高剂量组相比,中剂量组细胞焦亡比率明显下降;③ELISA、qRT-PCR、Western Blot结果示:与空白组相比,其他4组白细胞介素1β、白细胞介素18的表达量、半胱氨酸蛋白酶1、GSDMD、NOD样受体蛋白3的基因及蛋白表达量均显著升高;与模型组相比,含药血清各剂量组均显著降低;各剂量组组间比较,中剂量组表达量显著低于低、高剂量组;以上差异均有显著性意义(P < 0.05);④提示通督活血汤含药血清可有效缓解脂多糖/ATP诱导的椎间盘纤维环细胞发生焦亡,减轻炎症反应;中剂量组在延缓细胞焦亡、减轻炎症反应方面疗效最佳。
https://orcid.org/000-0003-1568-9202(吴子健)
中国组织工程研究杂志出版内容重点:组织构建;骨细胞;软骨细胞;细胞培养;成纤维细胞;血管内皮细胞;骨质疏松;组织工程
中图分类号: