中国组织工程研究 ›› 2017, Vol. 21 ›› Issue (26): 4228-4233.doi: 10.3969/j.issn.2095-4344.2017.26.022
• 生物材料临床实践 clinical practice of biomaterials • 上一篇 下一篇
基于CT灌注评价早期钛网修补颅骨缺损对脑血流量及神经功能康复的影响:随机对照临床试验
庄亚瑟,方志成,刘伯毅,陈 黎,俞旦峰
- 十堰市太和医院(湖北医药学院附属医院)重症医学科,湖北省十堰市 442000
Effects of early skull repair with titanium mesh on cerebral blood flow and neurological recovery: a randomized controlled clinical trial based on CT perfusion evaluation
Zhuang Ya-se, Fang Zhi-cheng, Liu Bo-yi, Chen Li, Yu Dan-feng
- Department of Critical Care Medicine, Taihe Hopsital (Affiliated Hospital of Hubei University of Medicine), Shiyan 442000, Hubei Province, China
摘要:
文章快速阅读:
.jpg)
文题释义:
CT 灌注技术:是CT检查的附加功能,是通过螺旋CT仪器来实现的一项技术,它基于核医学的放射性示踪剂稀释和中心容积定律原理,具有多参数、扫描迅速、设备普及等优点。
CT 灌注评价脑血流量:借助CT灌注技术观测对比剂在颅脑的浓度及分布是否随时间变化的情况,评估脑组织血液动力学情况。首先静脉注射对比剂,当其通过脑组织和血管时,扫描选定区域获得密度曲线,时间-密度曲线反映的是测定区域中对比剂浓度和时间的相关性,间接反映脑组织血液灌注量。
背景:创伤性脑损伤后去骨瓣减压治疗形成了颅骨缺损,目前公认最合适的颅骨修补人工材料为金属钛网,其生物相容性良好,在临床上获得了广泛应用,但脑损伤后颅骨缺损修复的时机仍存在争议。
目的:采用CT 灌注技术比较早期、晚期钛网修补颅骨缺损前后患者的脑组织血流灌注变化以及神经功能康复情况。
方法:试验为单中心、前瞻性、观察性临床试验,在中国湖北省,湖北医药学院附属太和医院完成。选取2013年1月至2016年1月收治的颅脑损伤后去骨瓣减压患者86例,均采用钛网进行颅骨修复,随机分为2组,试验组40例行早期颅骨修补(去骨瓣减压术后1-3个月),对照组46例行晚期颅骨修补(去骨瓣减压术后6-12个月)。颅骨修补术前3 d和术后第10天,应用CT灌注技术观察脑组织血液灌注量变化;术后30 d评价日常活动能力Barthel 指数。试验于2017年7月12日在北美临床试验中心注册(NCT03222297)。试验方案经十堰市太和医院伦理委员会批准,批准号为2012第(08)号。临床试验研究的实施符合《赫尔辛基宣言》和医院对人体研究的相关伦理要求。参与试验的患病个体及其家属为自愿参加,均对试验过程完全知情同意,在充分了解治疗方案的前提下签署“知情同意书”。
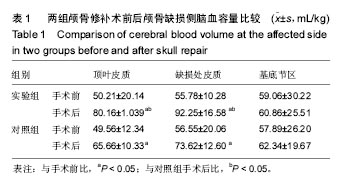
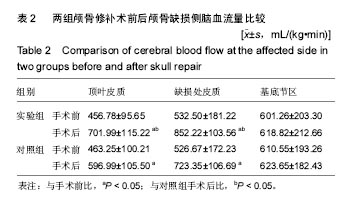
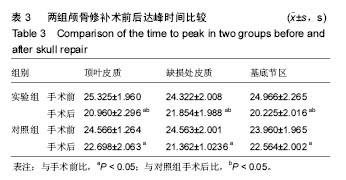
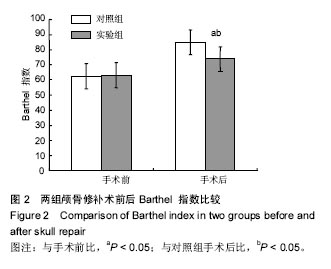
结果与结论:①两组患者颅骨修补后缺损侧顶叶皮质、缺损处皮质的脑血容量和脑血流量均高于颅骨修补前(P < 0.05),达峰时间则低于颅骨修补前(P < 0.05);颅骨修补后试验组的缺损侧顶叶皮质、缺损处皮质的脑血容量和脑血流量均高于对照组(P < 0.05),达峰时间则低于对照组(P < 0.05);②颅骨修补术后30 d试验组的Barthel 指数得分高于对照组(P < 0.05);③说明早期行颅骨缺损修补,对改善患侧脑组织灌注情况有利,进而对患侧神经功能的恢复有意义,而CT灌注观测脑血流动力学的变化安全有效。
中图分类号:
.jpg)
.jpg)