• 器官移植动物模型 organ transplantation and animal model • 上一篇 下一篇
SD大鼠股骨骨折合并脊髓损伤模型的构建
王海龙,盛伟斌,徐 韬,郭海龙
- 新疆医科大学第一附属医院,新疆维吾尔自治区乌鲁木齐市 830054
Preparation of a femoral fracture model combined with spinal cord injury in Sprague-Dawley rats
Wang Hai-long, Sheng Wei-bin, Xu Tao, Guo Hai-long
- The First Affiliated Hospital of Xinjiang Medical University, Urumqi 830054, Xinjiang Uygur Autonomous Region, China
摘要:
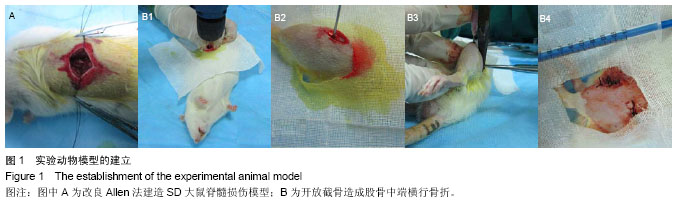
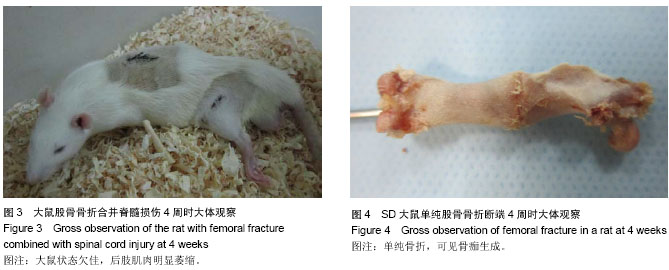
背景:骨折合并脊髓损伤的动物模型创伤大,造模后存活率较低,而改良Allen法和股骨开放截骨法制作动物模型时操作简单,不需要特殊器械,建模时间及出血较少,适用于骨折合并脊髓损伤动物模型的制作。 目的:建立一种既能成功维持长时间存活,并符合临床特征,又简便易行的实验动物模型。 方法:将48只SD雄性大鼠随机数字表法均分为单纯股骨骨折组和股骨骨折合并脊髓损伤组,通过双侧小切口开放截骨造成股骨中端横行骨折并植入内固定建立股骨骨折模型,改良Allen法自制打击装置造成大鼠T10段脊髓急性挫伤性损伤,两种方法融合制造股骨骨折合并脊髓损伤模型,观察大鼠制模成功后不同时间点大体情况及4周后骨折断端愈合情况。 结果与结论:建模后骨折合并脊髓损伤动物模型均成活,双下肢感觉及运动功能丧失,但可利用双上肢缓慢匍匐向前移动,前3 d进食少,活动少,夜间采用尾端悬吊后,骨折患肢未出现缺血坏死,到达第4周时,单纯股骨骨折组死亡1只,股骨骨折合并脊髓损伤组共死亡4只,成活率为83.33%,髓腔内固定未见脱出,两组骨折断端均有连续骨痂生成,从体积上来看,股骨骨折合并脊髓损伤组骨痂组织明显大于单纯股骨骨折组。证实将改良Allen法与小切口股骨外侧开放截骨法结合后,简单易行,可以成功制作股骨骨折合并脊髓损伤动物模型并成活至第4周。
中图分类号: