中国组织工程研究 ›› 2013, Vol. 17 ›› Issue (37): 6628-6635.doi: 10.3969/j.issn.2095-4344.2013.37.014
• 组织构建实验造模 experimental modeling in tissue construction • 上一篇 下一篇
以关节不稳建立的大鼠骨关节炎模型
张荣凯1,杨禄坤2,叶志强3,吴兆亚1,赵 庆1,蔡道章4
- 中山大学附属第五医院,1骨外科, 2麻醉科,广东省珠海市 519000;3中山大学附属第三医院急诊科,广东省广州市 510630;4南方医科大学附属第三医院关节外科,广东省广州市 510630
Establishing a rat osteoarthritis model based on knee joint instability
Zhang Rong-Kai1, Yang Lu-kun2, Ye Zhi-qiang3, Wu Zhao-ya1, Zhao Qing1, Cai Dao-zhang4
- 1Department of Orthopedics, 2Department of Anesthesiology, the Fifth Affiliated Hospital of Sun Yat-sen University, Zhuhai 519000, Guangdong Province, China; 3Department of Emergency, the Third Affiliated Hospital of Sun Yat-sen University, Guangzhou 510630, Guangdong Province, China; 4Department of Orthopedics, the Third Affiliated Hospital of Southern Medical University, Guangzhou 510630, Guangdong Province, China
摘要:
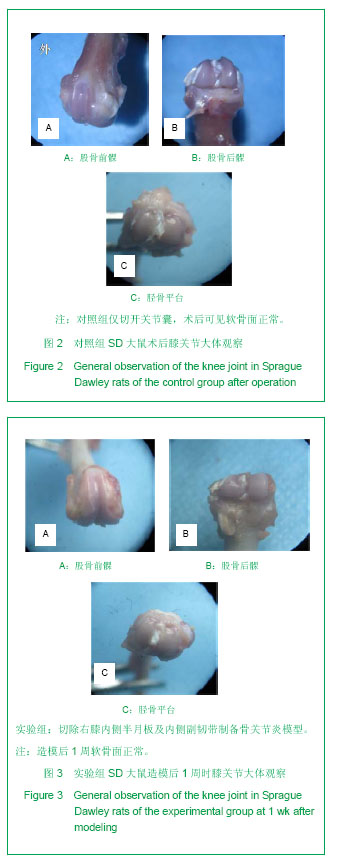
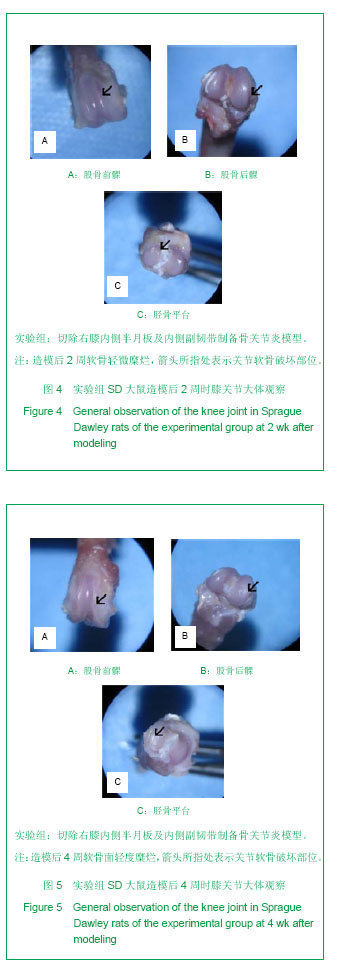
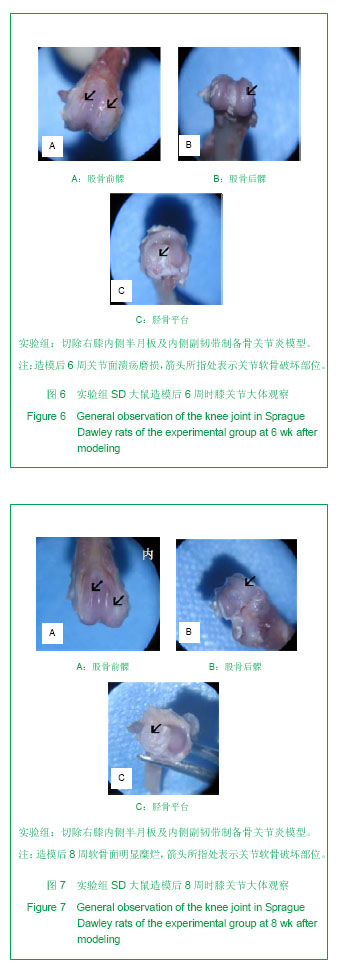
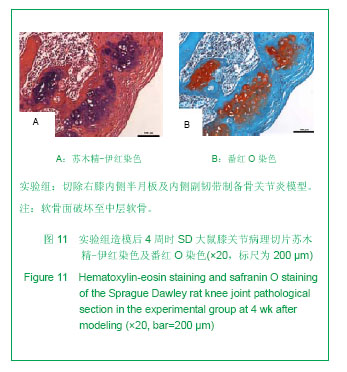
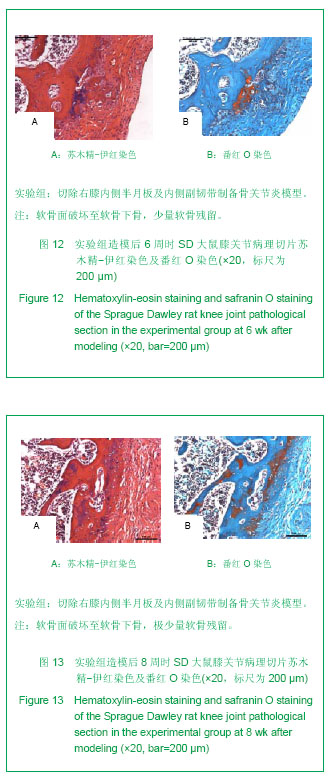
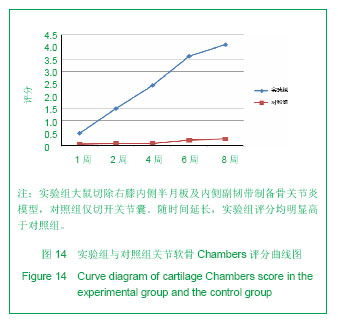
背景:骨性关节炎是一种复杂的多病因退变性关节疾病。早期进行骨性关节炎的防治尤其重要。但获取足量的适合研究的早期骨性关节炎的人类骨标本十分困难。 目的:观察关节不稳方法建立骨关节炎模型大鼠的关节软骨组织学变化。 方法:10周龄雄性SD大鼠随机分为2组:实验组切除右膝内侧半月板及内侧副韧带,对照组仅切开关节囊。于术后1,2,4,6,8周取右膝关节标本,行病理组织学检查分析大鼠骨关节炎病程的变化情况。 结果与结论:①术后2,4,6,8周,实验组关节软骨退变程度呈现轻度糜烂、溃疡磨损、严重磨损、骨赘形成等病理变化。②术后1,2,4,6,8周,实验组关节软骨评分均明显高于对照组(P < 0.05)。结果显示该实验采用内侧副韧带切断+内侧半月板切除方法成功建立了大鼠膝关节骨关节炎模型,且造模后4周内的病理、形态学改变类似于人类早期膝关节骨关节炎表现,是研究早期骨关节炎的理想模型。
中图分类号:



.jpg)
.jpg)