1.1 设计 材料的表征与体外细胞相容性实验,半定量数据采用one-way或two-way ANOVA及Turkey’s分析。
1.2 时间及地点 实验于2022年1-9月在苏州大学骨科研究所完成。
1.3 材料
1.3.1 实验动物 1只8周龄雄性SD大鼠,体质量约250 g,用于提取骨髓间充质干细胞,购自苏州昭衍研究中心有限公司,许可证号:SCXK(苏)2018-0006。4只6周龄雌性C57小鼠,体质量(15±2) g,用于提取骨髓巨噬细胞,购自苏州昭衍研究中心有限公司,许可证号:SCXK(苏)2018-0006。实验经苏州大学伦理委员会审批(批准号:SUDA20211123A01)。
1.3.2 主要材料与试剂 聚乳酸(济南怠罡生物科技有限公司);鼠尾Ⅰ型胶原(美国Sigma-Aldrich公司);二氯甲烷(江苏强盛功能化学股份有限公司);N,N-二甲基酰胺(上海强顺化学试剂有限公司);无水乙醇(国药集团上海化学试剂有限公司);10×PBS(美国Hyclone公司);α-MEM 培养基 (美国Gibco公司);CCK-8试剂盒(上海科艾博生物公司);活/死染色试剂盒(美国Invitrogen公司);整合素β1一抗(美国Novus Biologicals公司);兔抗大鼠F4/80-AF594抗体、小鼠抗大鼠CD206-AF488抗体、小鼠抗大鼠iNOS-AF488抗体(英国Abcam公司);鬼笔环肽(美国 Cytoskeleton公司);DAPI(英国Abcam公司)。
1.3.3 主要仪器 静电纺丝高压电源(天津东文高压电源有限公司);磁力加热搅拌仪(德国IKA公司);精密电子分析天平(上海天平仪器厂);扫描电子显微镜(日本日立公司);傅立叶红外光谱仪(美国Nicolet公司);力学测试机(上海衡仪精密仪器有限公司);细胞培养箱(美国Thermo公司);超净工作台(苏州净化设备厂);正置显微镜(美国蔡司公司);酶标仪(美国伯腾仪器有限公司);水接触角测试仪(上海程斯智能科技有限公司)。
1.4 实验方法
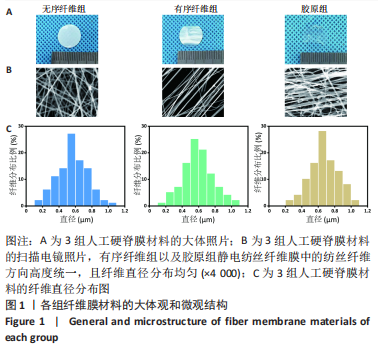
1.4.1 聚乳酸静电纺丝膜的制备 首先,将0.5 g的固体聚乳酸与4 g二氯甲烷溶液共同搅拌2 h,使固体的聚乳酸充分溶解,再加入2 g N,N-二甲基酰胺搅拌1 h,从而得到静电纺丝液。然后,将电纺液加入10 mL针筒内,针头采用特制的钝头钢针(内径为9 mm),再把高压电源的正极和负极分别连接在钢针和接收装置上,电压调整为12-15 kV,接收距离为15 cm。最后,使用滚筒型纺丝接收装置可获得无序的聚乳酸静电纺丝膜(无序纤维组),使用两根平行电极棒收集装置可获得有序定向的聚乳酸静电纺丝膜(有序纤维组)。
1.4.2 胶原溶液的制备 胶原蛋白运输和保存时为冻干后的固体形态,按照WU等[30]的方法将其配制成浓度合适的胶原溶液。首先用天平称取3 mg冻干后的胶原蛋白,然后加入1 mL浓度为0.1 mol/L的乙酸,使用磁力搅拌器充分搅拌均匀,得到质量浓度为3 mg/mL的胶原溶液,使用前放在4 ℃冰箱保存。
1.4.3 干细胞工程化双面异性人工硬脊膜的制备 首先,用体积分数75%乙醇浸泡上述方法得到有序聚乳酸静电纺丝膜1 h,并用无菌PBS冲洗3次备用。然后吸取1 000 µL配置好的胶原蛋白溶液加入EP管中,并用0.5 mol/L的NAOH溶液调节溶液pH值至7.0,全程冰上操作。接着把调至中性的胶原蛋白溶液滴加至聚乳酸静电纺丝膜表面,放入37 ℃恒温干燥箱中,使胶原蛋白在合适的条件下进行自组装。半小时后取出样品,并用无菌PBS冲洗3次,得到了一面为胶原蛋白、一面为单纯的有序聚乳酸静电纺丝纤维的双面异性静电纺丝膜(胶原组)。最后,在含有胶原蛋白的内表面进行骨髓间充质干细胞的培养,将内表面朝上放置于24孔板中,每个孔中加入1×105个骨髓间充质干细胞,然后加入1 mL α-MEM培养基,置于细胞培养箱中培养3 d,使细胞黏附于胶原蛋白表面,得到干细胞工程化的两面异性人工硬脊膜(干细胞组)。
1.4.4 人工硬脊膜的表征
扫描电镜分析:为了观察无序纤维组、有序纤维组、胶原组纤维膜的表面形貌,将3组纤维膜通过导电胶固定在载物台上,并用离子溅射仪在材料表面喷金45 s,然后移至扫描电镜下观察材料的微观结构。
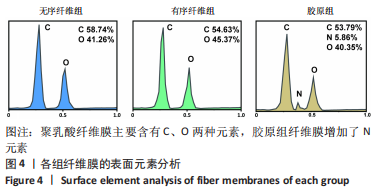
电镜能谱分析:使用上述方法进行喷金后移至扫描电镜下观察,通过能谱仪进行材料微区元素种类与含量的分析。
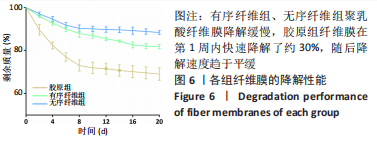
降解性能测试:将3组纤维膜分别取相同的质量(2 g),然后分别放入50 mL离心管中,并加入30 mL PBS,放置于37 ℃的恒温摇床中,每天更换离心管中的PBS。在固定时间点冻干并称质量,计算每个时间点的降解率,最后绘制降解曲线。
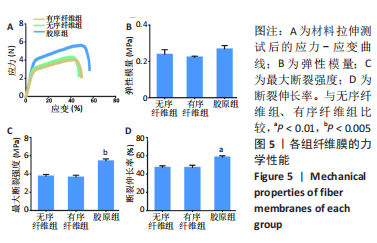
力学测试:通过力学拉伸测试来评估3组纤维膜的力学性能。首先通过压模法将3组材料压成15.0 mm×3.0 mm×0.1 mm (长×宽×厚)的大小,然后使用力学拉伸测试机以10 mm/min的拉伸速度测量材料的应力-应变数据(力学传感器为50 N),最后计算纤维膜的弹性模量、断裂强度、断裂伸长率。
水接触角测试:将3组纤维膜收集于圆形载玻片的表面,使其表面均匀平整,通过测量水滴在材料表面10 s后的水接触角来评估纤维膜的表面亲/疏水性能。
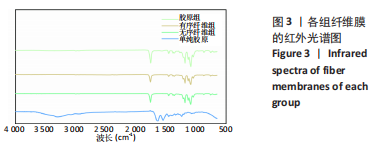
拉曼红外光谱分析:将3组纤维膜剪裁成1 cm×1 cm大小,直接放置于红外光谱仪中测试,而单纯的胶原蛋白则需加入适当的溴化钾在研钵中研磨成粉末,通过“压片法”压制成直径1 cm大小的薄片,再进行测试。每个样品在4 cm-1的分辨率下扫描128次,扫描范围为400-4 000 cm-1。
1.4.5 人工硬脊膜与骨髓间充质干细胞共培养
骨髓间充质干细胞的分离与培养:按照课题组之前采用的方法提取骨髓间充质干细胞[31]。取1只SD大鼠,腹腔注射2%戊巴比妥钠(40 mg/kg)后断颈处死,分离双侧股骨和胫骨,无菌条件下剪去长骨两端,用5 mL注射器吸取α-MEM培养基冲洗骨髓腔,将冲洗液以1 200 r/min离心5 min,重悬后放置于细胞培养箱中,得到原代骨髓间充质干细胞。通过流式细胞术对所提纯骨髓间充质干细胞表型进行相关检测,所提取细胞表面高表达CD29和CD90,低表达CD34和CD45。取传代至P4-P6代的细胞用于后续实验。
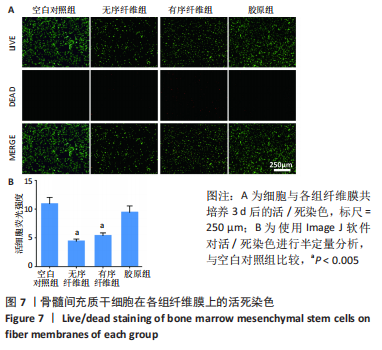
活/死染色:将无序纤维组、有序纤维组、胶原组纤维膜放置于24孔板中,以空白的细胞爬片为空白对照组;将骨髓间充质干细胞以1×105/孔的密度分别接种于各组材料表面,置于细胞培养箱中培养3 d后取出,用PBS冲洗3次后,每个孔加入300 µL 活/死细胞染液,37 ℃孵化1 h后吸出染液,用PBS冲洗3次,最后用正置荧光显微镜观察,并通过Image J软件进行荧光强度半定量,用Graphpad Prism软件进行统计分析。
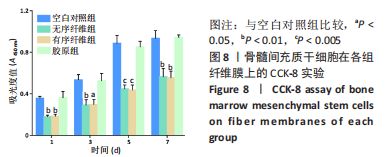
CCK-8实验:将无序纤维组、有序纤维组、胶原组纤维膜放置于24孔板中,以空白的细胞爬片为空白对照组;将骨髓间充质干细胞以5×104/孔的密度分别接种于各组材料表面,在第1,3,5,7天分别吸出培养基,以PBS冲洗3次后,加入CCK-8与培养基的共混液(CCK-8试剂∶培养基= 1∶9),将其再次放入细胞培养箱中,2 h后将每个孔的上清液吸至96孔板中,通过酶标仪测试每个孔的吸光度,来比较每组的细胞增殖活性。最终数据用Graphpad Prism软件进行统计分析。
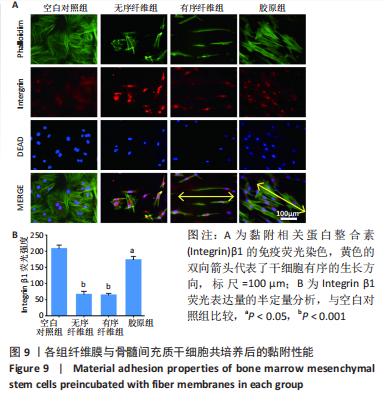
黏附实验:将无序纤维组、有序纤维组、胶原组纤维膜放置于24孔板中,以空白的细胞爬片为空白对照组;将间充质干细胞以5×104/孔的密度分别接种于各组材料表面,置于细胞培养箱中培养3 d后取出,用PBS冲洗3次后,加入40 g/L多聚甲醛固定细胞5 min;再次用PBS冲洗3次,加入0.5%的Triton溶液进行破膜;最后加入5%牛血清白蛋白在4 ℃冰箱进行封闭过夜,以避免非特异性染色;用PBS冲洗3次,加入抗整合素β1的一抗在4 ℃孵育过夜,再分别用对应的二抗在室温下染色;最后,肌动蛋白和细胞核分别用鬼笔环肽和DAPI染色。取出样本在正置荧光显微镜下观察。用Image J软件对平均荧光强度进行半定量。
1.4.6 人工硬脊膜与骨髓巨噬细胞共培养
骨髓巨噬细胞的分离与培养:按照BAI等[32]的方法提取骨髓巨噬细胞。取4只C57小鼠,腹腔注射2%戊巴比妥钠(40 mg/kg)后断颈处死,分离双侧股骨和胫骨,用上述同样的方法冲洗骨髓腔,然后向冲洗液中加入红细胞裂解液,裂解2 min后以1 200 r/min钟的速度离心重悬,继续培养于α-MEM培养基中,12 h后收集上层悬浮细胞,再次离心重悬并转移至6孔板中,加入2 mL含有30 µg/mL集落刺激因子的α-MEM培养基,使其贴壁生长3 d后得到骨髓巨噬细胞,用于后续细胞实验。
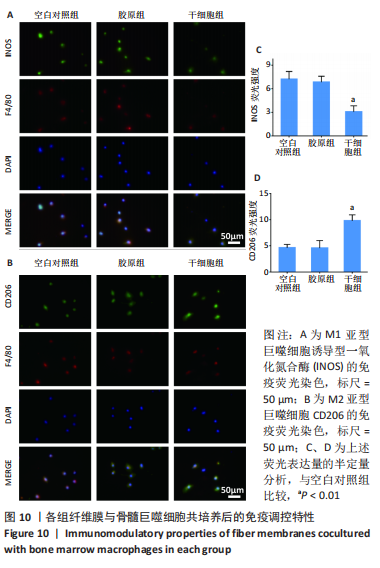
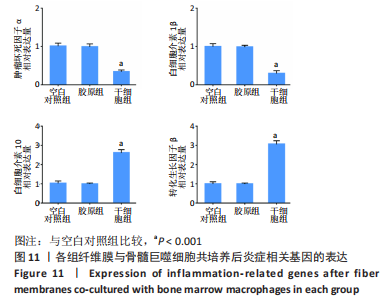
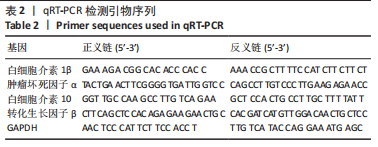
免疫调节实验:以空白的细胞爬片为空白对照组,将胶原组和干细胞组纤维膜分别和100 ng/mL脂多糖诱导3 d后的骨髓巨噬细胞通过24孔Transwell板进行共培养,上室加入1×104个骨髓巨噬细胞,下室分别加入空白细胞爬片以及两组材料,然后每个孔内加入1 mL的α-MEM培养基,培养3 d,以模拟人工硬脊膜对硬脊膜破损局部炎症微环境的影响。①培养3 d后,按照上述方法先用抗F4/80的一抗标记骨髓巨噬细胞,再分别用抗诱导型一氧化氮合酶(M1型)的一抗和抗CD206(M2型)的一抗分别标记不同亚型的巨噬细胞,用对应的二抗在室温下染色。最后,用DAPI给细胞核染色,取出样本,在正置荧光显微镜下观察。用Image J软件对平均荧光强度进行半定量分析。②培养3 d后,通过qRT-PCR技术来评估炎症基因的表达水平:将共培养的骨髓巨噬细胞进行裂解,提取RNA并反转录获取cDNA,以GAPDH作为内参基因,反应条件:95 ℃ 30 s,95 ℃ 5 s,60 ℃ 30 s,重复40个循环。聚合酶链反应扩增引物由Genewiz设计,详见表2。最终数据用Graphpad Prism软件进行统计分析。
1.5 主要观察指标 各组人工硬脊膜的理化性能、生物活性及免疫调节特性。
1.6 统计学分析 所有实验数据以x±s形式表示。采用Origin 9.1或GraphPad Prism 7.0软件进行统计学分析及绘制图片。通过one-way或two-way ANOVA以及Turkey’s分析,P < 0.05表示差异有显著性意义。该文统计学方法已经苏州大学生物统计学专家审核。