2.1 创伤性中枢神经系统损伤的病理 创伤性中枢神经系统损伤包括了创伤性脑损伤和脊髓损伤[14],在病理阶段上均可分为机械外力直接作用于损伤局部导致神经、血管等实质组织受损的原发性损伤和损伤局部微环境改变引起一系列级联反应而导致幸存神经组织再次受损的继发性损伤。
大脑的解剖结构异常精密,具有极其庞杂的神经、血管网络,细胞类型多种多样,如神经元细胞、星形胶质细胞、少突胶质细胞、小胶质细胞以及这些细胞的多种亚型。因其解剖结构的复杂,创伤性脑损伤后的病理机制同样非常复杂,目前对此知之甚少。总的来讲,创伤性脑损伤的病理阶段可分为原发性损伤和继发性损伤[15]。原发性损伤是指头部最初遭受到的机械打击所导致的损伤,可能是开放性、穿透性损伤,也可能是闭合性损伤[16];损伤可以是局灶性的,也可以是弥漫性的,导致广泛的轴突损伤。创伤可能会导致神经元、星形胶质细胞和少突胶质细胞受损甚至死亡,也可能会发生血管破裂、轴突切断/脱髓鞘。原发性损伤后损伤局部的微环境随时间推移发生一系列变化,血脑屏障功能丧失,血管破损血液连同外周免疫细胞渗入脑实质,造成炎症环境,组织水肿导致颅内压升高进而压迫动脉,脑血流量因此减少最终导致脑缺血,神经递质过度释放导致兴奋性毒性,Ca2+、Na+、K+失衡、乳酸和自由基堆积、ATP亏空及大量细胞因子释放等一系列复杂的级联反应导致幸存神经组织持续受损,损伤区域扩大,最终导致不可逆的后遗症发生甚至死亡[16-18]。
脊髓损伤的病理与创伤性脑损伤病理类似,原发性损伤同样涉及损伤局部神经组织和血管受损、一系列神经细胞损伤或死亡[19]。继发性损伤涉及组织水肿、神经炎症、兴奋性毒性、ATP亏空、Na+、K+失衡、Ca2+过载、自由基堆积、乳酸堆积及能量摄取障碍等一系列病理级联反应[20],最终导致神经元持续死亡、轴突脱髓鞘、脊髓空洞形成等病理改变[21]。
2.2 脂肪间充质干细胞外泌体治疗创伤性脑损伤 脂肪间充质干细胞外泌体在大鼠创伤性脑损伤后通过多条信号通路发挥调控小胶质细胞/巨噬细胞表型、抑制神经炎症、抑制神经元凋亡、促进神经再生的作用。
2.2.1 脂肪间充质干细胞外泌体调控小胶质细胞/巨噬细胞表型 创伤性脑损伤后,神经炎症作为对各种刺激和有害分子的反应,被认为是继发性损伤的关键机制。小胶质细胞/巨噬细胞属于中枢神经系统固有免疫细胞,约以1次/h的频率与神经元突触直接接触监测中枢神经系统状态,当发生感染、创伤时,小胶质细胞/巨噬细胞被迅速激活介导炎症反应。原发性脑损伤后细胞破裂,细胞碎片作为抗原激活小胶质细胞/巨噬细胞,使其从高度分枝样静息状态的M0表型活化为阿米巴样促炎状态的M1表型,分泌白细胞介素6及肿瘤坏死因子α等大量炎症因子,对邻近区域的神经元细胞、其他神经胶质细胞造成进一步损伤,在炎症后期,小胶质细胞/巨噬细胞活化为抑制炎症状态的M2表型,发挥组织修复作用。因此,抑制M1型小胶质细胞/巨噬细胞活化,促进M2型小胶质细胞/巨噬细胞表达可能是减轻神经炎症、发挥神经保护作用的有效方法。已有多项研究证实脂肪间充质干细胞外泌体在抑制小胶质细胞/巨噬细胞活化,调控小胶质细胞/巨噬细胞表型中发挥重要作用[22-24]。
在一项细胞实验中,FENG等[25]将脂肪间充质干细胞外泌体与脂多糖刺激的小鼠小胶质细胞系BV2细胞共培养,再将BV2细胞上清液与人神经母细胞瘤细胞株SH-SY5Y细胞共培养,研究证明脂肪间充质干细胞外泌体可以通过抑制核转录因子kB和MAPK信号通路的激活来抑制BV2细胞的活化,从而减弱肿瘤坏死因子α、白细胞介素6、白细胞介素1β、诱导型一氧化氮合酶和Cox2等炎症因子的基因表达和蛋白分泌,并保护神经细胞免受活化的BV2细胞所分泌的炎症因子损伤。对于未经受脂多糖干预的BV2细胞而言,外泌体的预处理未使其炎症因子的基因转录和蛋白质分泌增加,这证明脂肪间充质干细胞外泌体可能仅在活化的BV2细胞中起作用,这或许意味着更少的不良作用;该研究的局限之处在于关于巨噬细胞极化的信号通路还有很多,如Notch、JAK/STAT和TLRs信号通路[26],该研究只验证了核转录因子kB和MAPK信号通路,在未来的研究中可进一步探索其他信号机制,而且该研究只是细胞实验,尚未得到临床转化。在一项动物实验研究中,CHEN等[27]给创伤性脑损伤大鼠侧脑室局部显微注射人脂肪间充质干细胞外泌体,发现人脂肪间充质干细胞外泌体能促进创伤性脑损伤大鼠功能恢复、抑制损伤区神经炎症、减少神经元凋亡以及促进神经元细胞和星形胶质细胞再生。
有研究发现,人脂肪间充质干细胞外泌体主要是被损伤区域中的小胶质细胞/巨噬细胞吸收,并显著抑制了M1型小胶质细胞/巨噬细胞促炎细胞因子的形成,促进了M2型小胶质细 胞/巨噬细胞抑炎细胞因子的表达。在体外研究中,研究者发现用人脂肪间充质干细胞外泌体预处理抑制了脂多糖刺激下M1型小胶质细胞的阿米巴样形态改变。分子水平研究发现核转录因子kB通路和MAPK信号通路在小胶质细胞/巨噬细胞由M0型向M1型诱导的过程中被激活,人脂肪间充质干细胞外泌体抑制了这2条通路。总之,人脂肪间充质干细胞外泌体通过抑制核转录因子kB、MAPK信号通路来调控小胶质细胞活化和表型以及炎症介质的释放,发挥神经保护作用。
尽管脂肪间充质干细胞外泌体调控小胶质细胞/巨噬细胞表型的能力已经得到了验证,但它进入小胶质细胞/巨噬细胞的具体途径目前仍不明晰,对该问题的进一步探索或许有助于增强小胶质细胞/巨噬细胞摄取脂肪间充质干细胞外泌体的能力,使脂肪间充质干细胞外泌体特异性靶向小胶质细胞/巨噬细胞,提高用药效率和治疗精度。目前的重点主要是脂肪间充质干细胞外泌体和小胶质细胞/巨噬细胞表型之间的关系,但脂肪间充质干细胞外泌体对小胶质细胞/巨噬细胞的吞噬能力的影响、对神经元和其他神经胶质细胞的影响仍需进一步研究。此外,有研究表明脂肪间充质干细胞外泌体对小胶质细胞/巨噬细胞表型的调节能力与其所来源的脂肪间充质干细胞状态密切相关。炎症因子的预处理可激活脂肪间充质干细胞并诱导具有抑制M1表型、促进M2表型能力的外泌体释放,这意味着脂肪间充质干细胞外泌体调节小胶质细胞/巨噬细胞分化的能力不是组成性的,而是来自炎症微环境的激活。因此,在促炎环境下培养的脂肪间充质干细胞外泌体可能会对神经炎症有更好的抑制作用,这为脂肪间充质干细胞外泌体的标准化制备提供了一种思路。关于脂肪间充质干细胞外泌体的给药时间也需要进一步研究,过早的给药可能不利于损伤区域死亡细胞碎片的清除和降解,过迟的给药可能又会导致炎症因子大量释放,对损伤周围的神经元及其他胶质细胞造成严重的继发性伤害。
2.2.2 脂肪间充质干细胞外泌体中肺腺癌转移相关转录本1 (metastasis associated in lung denocarcinoma transcript 1,MALAT1)的神经保护作用 脂肪间充质干细胞外泌体治疗创伤性脑损伤在细胞实验和动物实验中已被证实疗效确切,进一步深入研究外泌体的具体生物成分在创伤性脑损伤治疗中的作用将对提高外泌体的临床应用效率大有裨益,也是精准医学思想的体现。皮下脂肪间充质干细胞主要应用于再生医学,MALAT1属于长链非编码RNA,在皮下脂肪间充质干细胞外泌体中表达较高,可通过多靶点、多通路发挥创伤性脑损伤的治疗作用,具有巨大的应用潜力。
神经营养受体酪氨酸激酶 3 (NRTK3)也称为原肌球蛋白受体激酶C(TrkC),神经元和神经胶质细胞中的TrkC水平受选择性剪接调节,产生2种剪接变体:全长受体(TrkC_FL)和缺乏激酶结构域的截短受体(TrkC_T1)。截短受体通过 TrkC 显着抑制NT3的信号传导。TrkC作为膜结合受体,与神经营养因子NT3结合后,会发生自身磷酸化,然后进一步磷酸化丝裂原活化蛋白激酶 (MAPK aka ERK)途径的成员。有研究表明NT3-TrkC 通路的激活可减轻神经损伤、增强神经修复。
MOSS等[28]向创伤性脑损伤模型小鼠鼻内途径递送人脂肪间充质干细胞外泌体,证明了人脂肪间充质干细胞外泌体经鼻内途径给药后可被大脑损伤区神经元细胞和小胶质细胞摄取,以MALAT1依赖方式调节神经元和小胶质细胞TrkC_FL表达,改善神经元线粒体功能,调控炎症基因降低炎症因子白细胞介素β水平,激活NT3-TrkC通路、MAPK通路并促进神经恢复。在其他类似研究中,侧脑室给药的外泌体绝大多数都被小胶质细胞摄取,该研究发现外泌体主要被同侧海马齿状回的IBA1+小胶质细胞和MAP2+神经元摄取,这可能是因为给药方式不同导致的,意味着不同的给药方式或许可以调控外泌体在损伤区内不同类型细胞中的分布,也意味着建立统一、规范的给药途径的重要性。此外,该研究还发现有无MALAT1的外泌体在脑内细胞中分布基本一致,意味着MALAT1与外泌体在脑内细胞中的分布无关;含有MALAT1的外泌体可降低损伤区的炎症标志物,但没有MALAT1的外泌体也能降低损伤区的炎症标志物,作用没前者明显,这意味着外泌体中发挥抗炎作用的生物成分可能有很多,MALAT1在其中非常重要。值得注意的是,研究者发现从远期(创伤性脑损伤 后 7 周)来看,假手术组、创伤性脑损伤组、无MALAT1外泌体组和有MALAT1外泌体组的TrkC_FL表达无显著性差异。这意味着MALAT1在创伤性脑损伤慢性期可能对NT3-TrkC-MAPK途径没有益处,提示MALAT1应当在损伤早期应用。
PATEL等[29]将含有或缺失MALAT1的人脂肪间充质干细胞外泌体静脉内给予受轻度皮质冲击后的大鼠,接受含有MALAT1的人脂肪间充质干细胞外泌体治疗的大鼠运动功能显著恢复,脑皮质损伤减少,用缺乏MALAT1的外泌体或缺乏外泌体的培养基处理显示出有限的运动恢复效果;体内成像显示外泌体在给药1 h后主要被脾脏和大脑摄取;基因测序表明,MALAT1调节大脑和脾脏中mRNA与ncRNA的表达,参与炎症反应、细胞凋亡和细胞存活、MAPK通路的信号转导和基因转录。值得注意的是,该研究通过静脉给药的方式使得一部分外泌体进入脾脏,这可能意味着外泌体的过滤和消除,但还可能意味着免疫相互作用。作为免疫器官,脾脏是外周巨噬细胞和单核细胞的来源之一,损伤后脾脏释放免疫细胞从而浸润到损伤区,阻断炎性单核细胞进入大脑损伤区,可以起到抑制神经炎症、减少皮质损伤和改善认知的作用。外泌体进入脾脏后可能会抑制这些免疫细胞释放到循环中,减少通过被破坏掉的血脑屏障的炎性细胞数量,降低外周免疫细胞引起的继发性损伤,因此脾脏同样也可能是人脂肪间充质干细胞外泌体治疗创伤性脑损伤的靶器官。
以往研究认为,通过靠近创伤性脑损伤损伤区给药(如侧脑室或鼻内给药)可提高药物递送效率,发挥更好的治疗效果,但这种给药方式可能会降低药物对其他靶器官的治疗作用,进而降低综合治疗效果。有研究表明,交替剪接的蛋白激酶Ⅱ(PKCδII)通过HT22神经元细胞中的B细胞淋巴瘤2基因(Bcl2)增强神经元存活。EL BASSIT等[30]在细胞实验中证明脂肪间充质干细胞外泌体中MALAT1募集富含丝氨酸-精氨酸的剪接因子2(SRSF2),使得激酶可以有效地磷酸化SRSF2,促进PKCδII的可变剪接从而增加神经元存活率。此外,研究者还发现用胰岛素处理脂肪间充质干细胞外泌体后可以显著增加MALAT1 和 SRSF2 的关联,提高HT22 细胞损伤后的存活和增殖,但并未揭示这种增强的机制,未来可进一步研究胰岛素如何增强MALAT1 和 SRSF2的关联。
脂肪间充质干细胞外泌体中的MALAT1在创伤性脑损伤领域以大脑和脾脏为靶器官,在神经元细胞和小胶质细胞中发挥作用,通过介导炎症反应、氧化应激、NT3-TrkC信号通路、MAPK信号通路和SRSF2-PKCδII-Bcl2信号通路发挥抑制神经炎症和神经细胞凋亡、增强神经元存活和增殖的作用。目前对于MALAT1的研究全部集中在细胞研究和动物研究,虽然取得了乐观的结果,但对临床试验是否有效并不可知,距离临床转化仍有很长的路要走。此综述的几项动物实验中,模型大鼠的脑损伤程度也不一致,有的仅对大鼠进行了轻度的皮质冲击,这导致目前对脂肪间充质干细胞外泌体治疗中重度创伤性脑损伤的研究还很不充分。
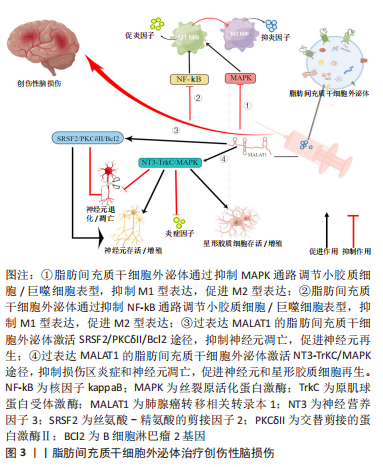
一些动物实验中MALAT1的给药途径包括了侧脑室、鼻内及静脉给药等,侧脑室给药和鼻内给药可能会提高药物靶向损伤区的效率,静脉给药虽然会被机体的一部分脏器截留,但同时也意味着药物靶向了更多的器官,尤其是与免疫相关的脾脏,这或许会提高药物的综合疗效,因此具体哪种给药方式最佳目前并无定论。MALAT1的给药时间也是需要明确的一个问题,早期给药似乎可以发挥更好的作用,MALAT1在创伤性脑损伤晚期可能对NT3-TrkC途径没有益处,但这需要进一步的验证。此外,该综述中对MALAT1的研究都是通过含有MALAT1的外泌体和不含有MALAT1的外泌体进行对比的,如果从外泌体中分离出MALAT1单独给药,它还能否发挥同外泌体中其他成分一起给药的作用并不可知。因此,应当进一步研究MALAT1单独给药的作用。然而,还有研究发现高血糖环境下LncRNA MALAT1通过激活miR-7641/TPR轴促进脑微血管内皮细胞凋亡,从而加剧脑小血管疾病引起的神经损伤[31]。创伤性脑损伤本身就包括了大脑的血管损伤,这意味着MALAT1的应用可能具有一定的风险,或许会加重创伤性脑损伤患者的脑血管损伤,尤其是对糖尿病患者而言。脂肪间充质干细胞外泌体治疗创伤性脑损伤机制见图3。
脂肪间充质干细胞外泌体治疗创伤性脑损伤相关实验研究汇总,见表1。

2.3 脂肪间充质干细胞外泌体治疗脊髓损伤 脂肪间充质干细胞外泌体在大鼠脊髓损伤中通过多条信号通路发挥调控小胶质细胞/巨噬细胞表型、抑制神经炎症、抑制神经元凋亡、促进神经再生的作用。
2.3.1 脂肪间充质干细胞外泌体调控小胶质细胞/巨噬细胞表型 与创伤性脑损伤相似,脊髓损伤后神经炎症是继发性损伤的关键机制。对小胶质细胞/巨噬细胞表型的调控有利于抑制神经炎症、改善脊髓损伤区微环境、促进神经修复。脂肪间充质干细胞外泌体及其生物成分在脊髓损伤后小胶质细胞/巨噬细胞表型的调控中发挥了有利的作用。
SUNG等[32]将人硬膜外脂肪间充质干细胞外泌体通过静脉注射到脊髓损伤模型大鼠中,改善了脊髓损伤大鼠的运动功能。Iba-1也称为同种异体移植物炎症因子,是一种在小胶质细胞/巨噬细胞中特异表达的基因。外泌体治疗可降低脊髓损伤后升高的Iba-1表达水平,抑制小胶质细胞/巨噬细胞的形态转变为阿米巴样(M1促炎型),抑制脊髓损伤后促炎因子白细胞介素1β、白细胞介素2和肿瘤坏死因子α的水平,提高抗炎因子白细胞介素10和白细胞介素13的水平。RNA测序揭示了外泌体给药后免疫反应和炎症反应相关基因表达发生变化。总之,该实验证明人硬膜外脂肪间充质干细胞外泌体可以抑制小胶质细胞/巨噬细胞的M1表型,改变免疫反应和炎症反应相关基因,调节促炎因子和抗炎因子水平,抑制神经炎症,促进脊髓损伤大鼠功能恢复。值得注意的一点是,高外泌体组大鼠在接受治疗的28 d后,平均体质量较对照组、损伤组、低外泌体组明显增加,这可能意味着人硬膜外脂肪间充质干细胞外泌体会带来肥胖不良反应。
陈浩贤等[33]发现,脂肪间充质干细胞外泌体可以抑制脊髓损伤大鼠损伤组织中M1型小胶质细胞/巨噬细胞标志物白细胞介素1β、白细胞介素6、诱异型一氧化氮合酶等促炎因子的表达,促进M2型小胶质细胞/巨噬细胞标志物白细胞介素4、白细胞介素10及Arg-1等抗炎因子的表达,并下调和胶质瘢痕形成密切相关的胶质纤维酸性蛋白、Vimentin蛋白水平。研究证明脂肪间充质干细胞外泌体通过调节小胶质细胞/巨噬细胞表型、抑制胶质瘢痕形成来改善脊髓损伤大鼠的运动能力。SHAO等[34]研究了脂肪间充质干细胞在缺氧状态下分泌的外泌体对脊髓损伤的治疗效果,高通量测序显示LncGm37494在缺氧外泌体中的表达明显高于正常外泌体,LncGm37494过表达下调miR-130b-3p的表达进而上调PPARγ的表达,从而使小胶质细胞由M1型极化至M2型。来自过表达脂肪间充质干细胞的lncGm37494的外泌体显示出与缺氧状态下培养的脂肪间充质干细胞外泌体相似的治疗效果。该研究证明缺氧状态下培养的脂肪间充质干细胞外泌体比正常培养的脂肪间充质干细胞外泌体在将小胶质细胞/巨噬细胞从M1型极化为M2型、抑制炎症因子表达以及促进功能恢复方面更为有效,可能是过表达的LncGm37494通过miR-130b-3p/PPARγ途径发挥作用。该研究在大鼠脊髓损伤模型建立后立即由尾静脉给药,治疗窗口短,在临床中几乎不存在给脊髓损伤患者在损伤后立即给药的条件,在未来研究中应进一步延长治疗窗口,增加临床应用可能。
脂肪间充质干细胞外泌体在脊髓损伤后调控小胶质细胞/巨噬细胞表型,下调促炎因子表达、上调抗炎因子表达,改善损伤区炎症微环境,减少瘢痕组织,为神经修复和再生提供可能,并改善脊髓损伤大鼠的运动功能。需要注意的是脂肪间充质干细胞外泌体还可能存在肥胖等不良反应,但这需要进一步验证。目前开展的几项研究都是临床前研究,且治疗窗口短,与临床实际不符,在未来的研究中应将治疗窗口延长至24-48 h,为临床转化做准备。除了lncGm37494之外,脂肪间充质干细胞外泌体中还有哪些生物成分参与了小胶质细胞/巨噬细胞的极化,以及脂肪间充质干细胞外泌体下调胶质纤维酸性蛋白阳性+星形胶质细胞的分子机制也是未来需要研究的内容。
2.3.2 脂肪间充质干细胞外泌体抑制神经元炎症和凋亡 神经元凋亡是脊髓损伤后的主要病理事件,抑制神经元凋亡对脊髓损伤的恢复至关重要。脂肪间充质干细胞外泌体中含有丰富的生物成分,可通过多通路来抑制脊髓损伤后神经元的炎症和凋亡。
HUANG等[35]发现低氧条件下miR-511–3p过表达的脂肪间充质干细胞外囊泡下调了脂多糖损伤的PC12细胞中凋亡相关基因Bax、Caspase3表达水平,上调了抗凋亡基因Bcl-2的表达,抑制TRAF6从而减少炎症相关因子诱导型一氧化氮合酶、环氧合酶2、 肿瘤坏死因子α、白细胞介素6和白细胞介素1β的表达,缓解脂多糖诱导的PC12细胞凋亡和炎症。鞘氨醇-1-磷酸(tyrosine protein kinase C,TrkC)/S1P受体3(S1PR3)可能是脊髓损伤临床治疗的一个有希望的靶点,研究发现S1P可诱导核转录因子κB p65的磷酸化和核转录因子κB核转位的激活,从而促进炎症反应[36]。脂多糖处理显著增加S1PR3浓度,但miR-511–3p治疗减弱了这种作用,将miR-511-3p模拟物静脉注射到脊髓损伤模型大鼠中,损伤组织炎症减轻并且大鼠神经功能部分恢复。
因此,脂肪间充质干细胞来源的过表达miR-511–3p的外囊泡通过TRAF6和S1P/核转录因子κB途径减轻神经炎症、抑制神经元凋亡、促进神经功能恢复。LIANG等[37]在体外建立神经元氧-葡萄糖剥夺和再灌注模型,以模拟脊髓损伤后的缺氧环境。研究发现缺氧条件下脂肪间充质干细胞外泌体显著减少了神经元凋亡。在大鼠脊髓损伤模型中发现脂肪间充质干细胞外泌体可以显著减少损伤部位的空洞体积,促进大鼠后肢的功能恢复。通过RNA测序分析及免疫荧光和蛋白质印迹检测,证明脂肪间充质干细胞外泌体中miR-499a-5p通过靶向JNK3调节JNK3/c-jun凋亡信号通路。该研究表明缺氧条件下脂肪间充质干细胞外泌体通过递送miR-499a-5p抑制JNK3/c-jun凋亡信号通路,从而减少脊髓损伤后神经元凋亡。需要注意的是,缺氧条件下脂肪间充质干细胞外泌体中表达量改变的生物成分很多,不能排除其他生物成分同样对神经元起到抗凋亡作用。
脂肪间充质干细胞外泌体向损伤区递送miR-511-3p、miR-499a-5p等生物成分,通过TRAF6信号通路、S1P/S1PR3/核转录因子κB信号通路和JNK3/c-jun凋亡信号通路发挥抗神经元炎症和凋亡的作用,并促进神经元增殖和存活。但已开展的实验以细胞实验为主,在动物或者临床试验中,脂肪间充质干细胞外泌体及其生物活性成分在复杂的体内环境中,能否如同细胞实验一样顺利被神经元细胞摄取从而发挥抗凋亡作用或直接被其他类型细胞摄取从而发挥有利或有害作用并不得知。进一步开展动物实验并逐步向临床试验过渡是接下来应关注的方向。
2.3.3 脂肪间充质干细胞外泌体促进神经修复再生 脊髓损伤后神经有效再生并促进功能恢复是治疗的终极目标,过表达miR-133b的脂肪间充质干细胞外泌体可通过多个途径发挥神经再生作用。Ren等[38]研究发现miR-133b转染脂肪间充质干细胞后,干细胞所分泌的外泌体中miR-133b显著上升。脊髓损伤后,脊髓组织中的RhoA显著增高,富集miR-133b的脂肪间充质干细胞外泌体降低了损伤组织中RhoA的水平,促进损伤部位轴突再生[39]。此外,富集miR-133b的脂肪间充质干细胞外泌体还显著提高了损伤脊髓中促神经再生相关蛋白的水平,包括了神经丝(NF)、生长相关蛋白43(GAP43)、胶质纤维酸性蛋白(GFAP)和髓鞘碱性蛋白(MBP)。cAMP-CREB-BDNF信号通路具有促进轴突再生、修复受损神经细胞、恢复神经功能的作用[40],过表达miR-133b的脂肪间充质干细胞外泌体提高了磷酸化CREB(p-CREB)的水平,可能是通过cAMP-CREB-BDNF通路促进了神经再生,但这需要进一步验证。需要注意的是,该实验并未从行为学角度去评价脊髓损伤大鼠的功能恢复,过表达miR-133b的脂肪间充质干细胞外泌体的具体治疗效果如何并不可知。此外,过表达miR-133b的脂肪间充质干细胞外泌体还提高了磷酸化STAT3(p-STAT3)的水平,但以往研究表明,STAT3磷酸化水平增加不利于神经修复,抑制p-STAT3水平可以起到神经保护作用[41],这似乎暗示过表达miR-133b的脂肪间充质干细胞外泌体在神经保护中具有双面性。调节性T细胞(Treg)可分泌白细胞介素10抑制炎性反应和神经元损伤。叉头盒蛋白3(FOXP3)是Treg细胞的标志蛋白,FOXP3下调会抑制Treg表达,进而导致神经元的炎性损伤。也有研究发现,抑制miR-133b的表达可上调FOXP3蛋白,减弱黑质的炎症反应,抑制神经元凋亡,发挥神经保护功能[42]。因此,miR-133b在神经再生中具体扮演什么角色还有待进一步研究。
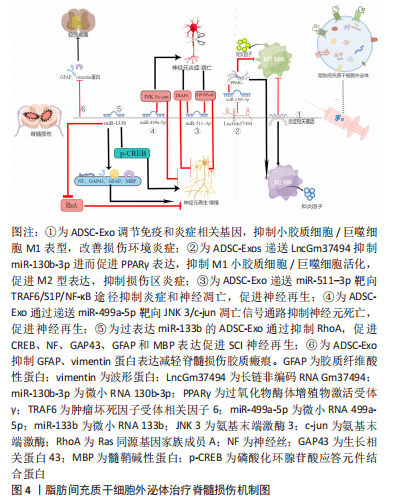
脂肪间充质干细胞外泌体治疗脊髓损伤,相关研究结果汇总见表2。肪间充质干细胞外泌体治疗脊髓损伤机制见图4。