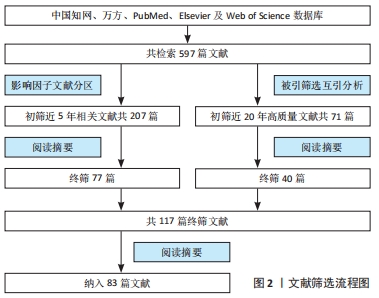
2.1 纳入文献基本情况 共检索到文献597篇,经上述标准进行文献筛选,最终共引用83篇文献,其中英文文献79篇,中文文献4篇,详见图2。
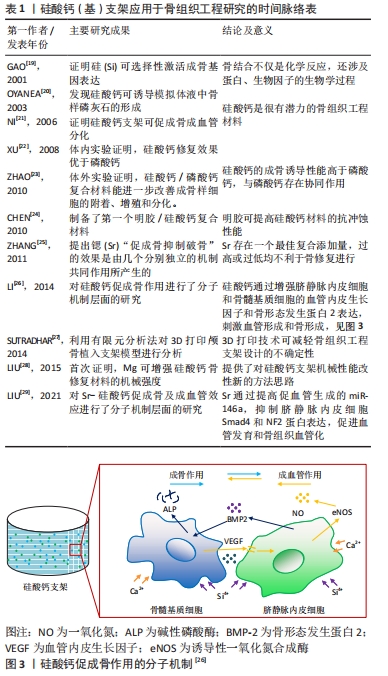
2.2 硅酸钙(基)支架应用于骨组织工程的研究发展历程 21世纪初,大量实验结果表明,硅酸钙材料具有一定的骨诱导效应,可促进骨缺损处的成骨成血管分化,修复效果与磷酸钙等材料存在显著性差异。但随着研究的进一步进行,研究者们发现单相硅酸钙材料用于骨缺损修复时存在多方面的弊端,如机械性能差、降解速度快和成骨性能不稳定等,临床效益欠佳。所以大量对硅酸钙支架进行优化处理的研究开始开展[19-29],通过结构改良、组成改性和表面涂层等多种手段,旨在充分利用硅酸钙材料自身生物优势的同时,对其不利于骨缺损修复的性能进行优化,以期在未来作为有效的骨组织工程材料修复大范围骨缺损,见表1,图3。
2.3 3D打印技术对硅酸钙(基)支架的应用优化 通过计算机辅助设计,可精准控制3D打印植入支架的外形、孔隙率、孔径大小和孔的连通性等参数[30],这些结构特征对早期负荷和新骨再生有着重要影响[31]。

2.3.1 3D打印硅酸钙(基)支架对应力分布的影响 骨的修复过程本质上是骨组织对机械力学刺激的一个适应性过程。硅酸钙(基)植入支架与周围骨组织弹性模量相差过大会产生应力遮蔽效应,导致周围骨组织缺乏有效的动态应力刺激[32],使成骨细胞活力显著降低,此时新骨生长速度慢、生长无序和机械强度低,甚至可能引起骨质疏松等病理改变,不利于骨修复的进行。由于材料的弹性模量和孔隙率、孔径大小成反比,故利用3D打印技术精确控制硅酸钙(基)植入支架的孔隙率,可以使硅酸钙(基)植入支架与支架周围骨组织的弹性模量尽可能地一致,以利于骨组织与修复支架之间的应力传递,从而有效刺激骨组织的修复再生[33],3D打印多孔硅酸钙(基)支架与传统硅酸钙(基)支架的比较[34-35],见表2。

另一方面,在骨适应性中还存在效力递减现象,即随着骨承载时间的增加,骨形成效应逐渐减缓,骨细胞对力学负荷的敏感性下降[36],这也不利于骨缺损处的修复。3D打印多孔硅酸钙(基)支架由于其个性化精准植入的特点,使被修复骨在支架植入早期即可部分行使功能,与卧床静养或者人为辅助进行的负荷加载模式相比,3D打印多孔硅酸钙(基)支架使新骨在沿着多孔结构生长的过程中,与生理活动范围内的周期性负荷频率和应变速率相适应,有利于新骨在形成过程中保持较高的力学敏感度。
综上,通过3D打印技术制备的个性化多孔硅酸钙(基)支架在骨修复的过程中,不仅能够保证有效的应力刺激,还能给予适当的力学加载间歇期,使新骨在沿着硅酸钙(基)支架孔隙生长的过程中即可完成对生理负荷刺激的适应过程,这将更有利于新骨形成[37]。
2.3.2 3D打印硅酸钙(基)支架对成骨成血管的影响 生物降解性、孔隙率以及相互连通的孔隙度是影响3D打印支架中细胞增殖的关键特征。支架的可降解性为发展中的细胞外基质留下扩展的空间;支架合适的孔隙率可促进骨质沿孔隙向内扩展,同时保证植入支架的稳定性[38-39];相互连通的孔隙度用于血管形成,营养、废物和氧气的运输,能够帮助指导细胞沿支架迁移。通过3D打印技术构建的三维大孔相互连接的空间结构能够改善体液的渗透和骨相关细胞的生长,同时增大支架表面积[40],极大地促进骨组织和血管的生成以及营养物质和代谢副产物的转运。
如图4所示,在3D打印技术应用于硅酸钙(基)支架制备时,有效的孔隙连通度和合适的孔径大小将更有利于细胞在硅酸钙(基)支架上的黏附、生长和增殖,综合实验数据表明,最佳的孔径大小为300-600 μm[38,41-42]。较大的孔径有利于细胞生长/增殖,其原因有2个:①较大孔径的支架具有更多的开放空间供细胞生长;②较大孔径的支架具有较高的培养基扩散性。初始较大孔径的硅酸钙(基)支架拥有较少的孔隙阻塞,更有利于氧气和养分的供应[43],但是大孔径的硅酸钙(基)支架具有较高的渗透性,因为细胞悬液在渗透支架时阻力较小,所以平均流体速度较高,使得细胞没有足够的时间与支架完成表面附着,降低细胞黏附效率。
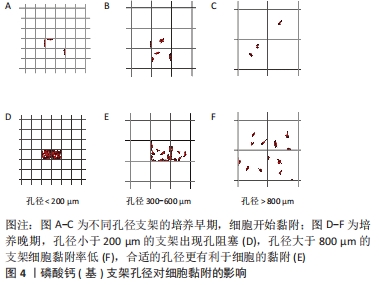
较小的孔径有利于细胞黏附,因为降低支架的渗透性可提高播种效率,若对不同孔径大小的支架进行对比研究,可以发现在体外培养的早期,孔径越小的支架上细胞数量明显更高[44]。但是,当细胞培养到后期,孔径过小的硅酸钙(基)支架上会出现孔堵塞,这会影响营养物质及代谢废物的转运[45],这时,即使硅酸钙(基)支架上已经形成了完全覆盖的细胞外基质层,由于缺乏营养和氧气供应,仍会导致硅酸钙(基)支架内的细胞死亡[41],因此过小的孔径对硅酸钙(基)支架内的细胞生长也无益。细胞在不同孔径的硅酸钙(基)支架上随时间变化的黏附生长趋势,见图5。
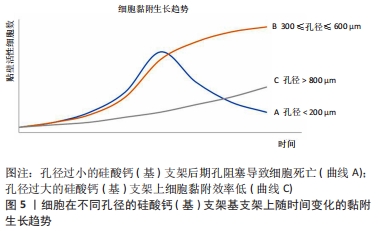
上述综合分析结果为后续研究人员设计3D打印硅酸钙(基)植入支架的孔隙参数提供了参考和思路,可以考虑设计分级梯度孔径的硅酸钙(基)支架,即在支架外部设计大孔径以保证营养和氧气供应、避免孔阻塞,在支架内部设计小孔径以降低通透性,从而增加初始细胞附着。
2.3.3 利用3D打印技术构建硅酸钙(基)药物缓释支架 3D打印技术还可用于辅助构建硅酸钙(基)网状缓释系统,通过在3D打印技术构建的缓释支架上加载药物[46],也可对硅酸钙(基)支架成骨性能进行优化改性。纳米硅酸盐的高表面积和带电特性能够将药物蛋白质固定在3D打印结构内,使药物在网络支架降解期间缓慢释放[47-48]。P2X和P2Y嘌呤能受体能够引导干细胞向骨细胞分化,HIELSCHER等[49]成功地在玻璃陶瓷支架上加载P2配体使其在间充质干细胞分化过程中持续释放,以调节干细胞向骨组织的分化。基于以上,文章可以进一步推测,利用3D打印技术在硅酸钙(基)支架上构建缓释系统是理论可行的,可以根据特定需要,在3D打印硅酸钙(基)支架上加载各种药物,如低分子量化合物(如抗生素)、高分子量化合物(如蛋白质和生长因子)和离子,使其在一段时间内持续稳定地释放,改善硅酸钙(基)植入支架在细胞分化、成骨诱导或抗菌抗炎等方面的性质。
2.4 通过材料复合对硅酸钙支架的优化改性
硅酸钙支架的快速降解会引起局部环境下pH值的快速增加,释放过量的硅离子,导致细胞毒性,降低支架早期稳定性,因此,一般并不推荐使用单相硅酸钙支架[40]。目前常用Si-Ca化合物[50],见表3。多种复合材料在化学组成和物理性质方面,对硅酸钙支架上述随时间变化的特征有着显著影响,通过对支架的机械性能、成骨诱导性能、成血管诱导性能等的优化改性,达到有效促进骨缺损修复效率的目的,故硅酸钙(基)复合材料支架的研究备受关注。

2.4.1 机械性能优化 利用金属元素改进硅酸钙支架机械性能是一种被广泛认可的手段,常用的有锶(Sr)和镁(Mg)。Sr可以增加硅酸钙支架的降解速率,而且Sr在增加硅酸钙支架降解速率的同时不会降低硅酸钙支架的机械强度[51],文章推测这一现象的产生是因为在一定范围内,硅酸钙支架上的新骨形成量与Sr呈剂量依赖性,支架上形成的新骨弥补了支架降解对机械性能的影响。所以在Sr/硅酸钙复合支架的研究上,确定合适的Sr添加量,使新骨形成速率与支架降解速率相匹配是一个重要方向。Mg是也一种常用的金属类改性复合剂,Ca2+和Mg2+在晶体空间结构上具有相似的配位多面体,所以Mg2+进入硅酸钙结构时,将取代Ca2+的位置,置换成更稳定的晶相[52],硅酸钙支架的Mg含量越高机械强度越高[53],通过控制镁的取代比,可以调节硅酸钙支架的动态机械强度、生物活性离子释放和生物降解性能。然而一方面,Mg掺杂虽然可以增加物理性能,但会抑制钙离子释放,降低支架的生物活性[54];另一方面,相较于硅酸钙支架,掺Mg的硅酸钙支架有更疏松的多孔结构,支架的致密性和Mg取代比成反比,即Mg取代比越大,支架降解越快[55],复合支架最终的强度取决于以上机制的综合影响。多个研究表明,当Mg取代10%-20%mol的Ca时,所得到的生物陶瓷有较佳的机械强度[56-58] ,由于不同Mg取代比的硅酸钙支架的机械强度和降解速率不同,所以在Mg的应用研究上,可以考虑通过调节Mg取代比,使硅酸钙支架与各种病理条件下的原位骨再生情况相匹配。
使用高分子聚合物(如聚己内酯和聚乳酸等)与硅酸钙组织工程骨支架复合,是改善其力学性能、提高支架杨氏模量的另一思路。聚己内酯/硅酸钙复合支架的抗压强度与人体松质骨(2-12 MPa)一致[59],有利于骨内支架-松质骨界面的应力传递,但聚己内酯的疏水性和较差的生物活性降低了细胞黏附和生长的效率,导致组织的再生率有限[60]。聚乳酸的亲水性明显优于聚己内酯,而且两相大孔聚乳酸结构的力学性能与也松质骨相匹配[61-62],所以聚乳酸对于硅酸钙支架来说,也许有着更佳的优化效应。
2.4.2 成骨诱导性能优化 近几年有很多关于通过复合金属离子,提升硅酸钙支架成骨诱导活性的研究。Sr离子以剂量依赖性的方式抑制破骨细胞形成[63],掺Sr的支架有更高的碱性磷酸酶活性,并可以发现更多的Runx-2阳性细胞[64-65],所以适当的Sr离子浓度可以刺激成骨细胞增殖分化,促进骨矿化,抑制破骨细胞活性。Sr的促成骨机制可以概括为:①抑制水解酶;②激活RAS/MAPK信号转导通路;③促进人去分化脂肪细胞;④拮抗M1型巨噬细胞(ΦM1)的促炎作用,促进M2型巨噬细胞(ΦM2)极化(免疫调节)[66]。但是,Sr离子的存在会阻碍Si离子的释放[64],而且对破骨细胞过强的抑制可能对骨骼重塑和组织再生产生负面影响[67],因此Sr的复合添加量并不是越高越好,最佳的Sr添加量应综合考虑各方面因素的影响。除Sr之外,Mg亦可从诱导羟基磷灰石沉积和成骨基因表达两方面促进硅酸钙支架的成骨诱导活性。与硅酸钙支架相比,Mg/硅酸钙复合支架具有更大的比表面积和孔容,在体外具有良好的骨样羟基磷灰石沉淀能力,可促进钙沉积和矿化结节的形成,这种磷灰石层的形成是材料与骨骼结合的先决条件[7];Mg/硅酸钙复合支架还能提高碱性磷酸酶的活性和骨钙素蛋白表达,促进成骨分化标志物的表达[68]。近些年,一些稀土金属在成骨诱导上的潜力也逐渐得到重视。如La可通过激活骨髓间充质干细胞成骨分化的关键途径——转化生长因子β通路,促进支架成骨[69];掺Gd的硅酸钙支架可显著上调碱性磷酸酶、Runx-2和Ⅰ型胶原等成骨相关基因的表达,加速细胞外基质沉积[70]。虽然目前针对稀土金属的相关研究并不多,但其在生物医学领域的应用潜力不容忽视。表4列举了骨组织工程中有应用前景的金属离子的应用情况。

有机分子复合改性是改善硅酸钙支架骨诱导性能的另一可行思路。明胶/硅酸钙复合支架是用于骨修复和再生的有前途的骨移植材料,明胶分子亲水且带有负电荷,可以和水分子作用形成氢键[74],所以与硅酸钙支架相比,明胶/硅酸钙复合支架更有利于成骨细胞的黏附和生长,氢键的存在使明胶/硅酸钙复合支架的抗冲蚀性能得到提高,为矿化基质的沉积提供了一个稳定的环境。有机分子影响硅酸钙支架成骨效应的机制多种多样,如多巴胺通过增强细胞黏附标志物和整合素的表达[75],促进成骨细胞黏附和细胞外基质的分泌;姜黄素和骨形态发生蛋白2则通过促进骨样磷灰石层的形成,增强硅酸钙支架的成骨效应[76-77]。由于有机分子种类基数大、化学结构多变,故其优化硅酸钙支架成骨性能的作用机制各不相同,难以总结出普遍适用的规律,但是相应的,有机分子复合对硅酸钙支架性能优化的潜力也是巨大的。
2.4.3 成血管诱导性能优化 植入支架的血管化是新骨形成、生存和行使功能必不可少的一步,诸多物质均可对硅酸钙支架的成血管活性产生影响,如干扰素γ、石墨烯和重组人骨形态发生蛋白2等。石墨烯能够诱导骨髓间充质干细胞向成骨谱系分化[78],并能诱导生长因子分泌的增强,如成纤维细胞生长因子和肝细胞生长因子[79],这2种因子都是血管生成的关键,能够促进石墨烯复合硅酸钙支架的血管生成[80]。重组人骨形态发生蛋白2可通过刺激血管内皮生长因子35-37的内源性表达间接促进血管生成[81],但是LI等[82]的实验显示,复合重组人骨形态发生蛋白2的硅酸钙支架的新生血管数量仅略多于硅酸钙组,提示在促血管生成上,重组人骨形态发生蛋白2虽有一定促进作用,但起主要作用的可能仍是Si离子。虽然硅酸钙本身具有一定的成血管效应,硅酸钙支架在降解过程中释放的Si能够诱导巨噬细胞M2极化[83],使组织工程骨血管化,但其效能难以满足新骨再生的需求,所以探索优化硅酸钙支架成血管性能的方案是有必要的。