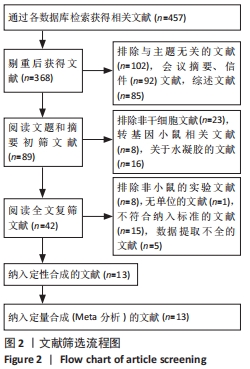
2.1 文献检索结果 共检索出457篇文献,最终纳入13篇文献进入结果分析,见图2。
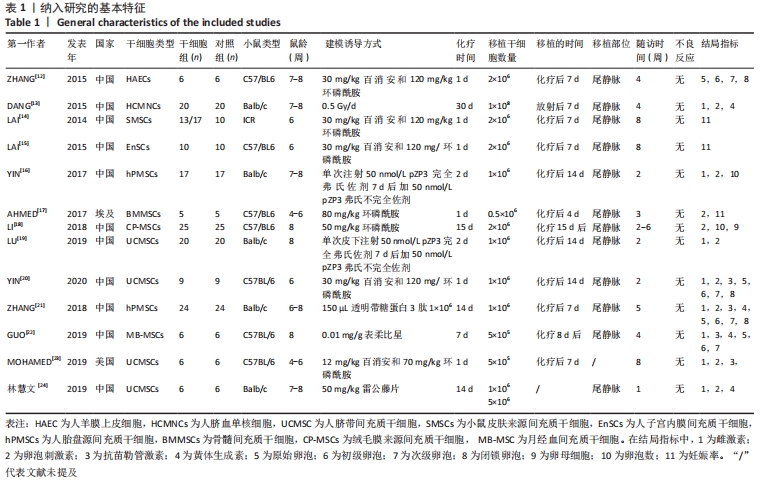
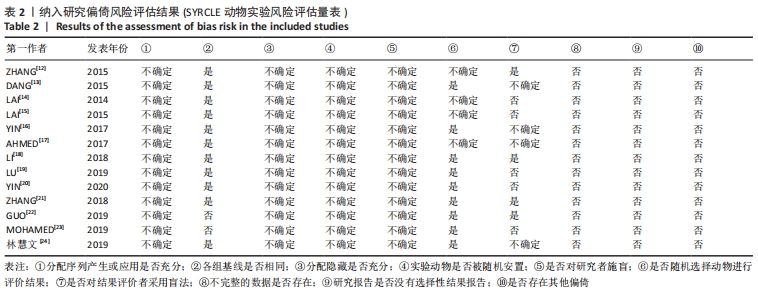
2.2 纳入文献的基本特征以及质量评价 共纳入13篇文献[12-24],共348只小鼠,干细胞组的小鼠184只,对照组的小鼠164只。在干细胞类型方面,其中4篇是脐带间充质干细胞[19-20,23-24],2篇是人胎盘源间充质干细胞[16, 22],1篇是人羊膜上皮细胞[12],1篇是人脐血单核细胞[13],1篇是皮肤来源的间充质干细胞[14],1篇是人子宫内膜间充质干细胞[15],1篇是骨髓来源的间充质干细胞[17],1篇是绒毛膜来源间充质干细胞[18],1篇是人月经血间充质干细胞[23]。共包括7个研究对象为C57BL/6的雌性小鼠[12, 15,17-18,20,22-23],5个研究对象为BALB/c的雌性小鼠[13,16,19,21,24],1个研究对照为ICR的雌性小鼠[14]。纳入研究的基线特征见表1。根据SYRCLE动物实验偏倚风险评估工具进行质量评价纳入研究,总体为中等质量研究,见表2。
2.3 Meta分析结果
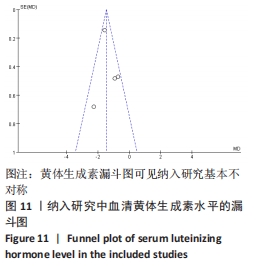
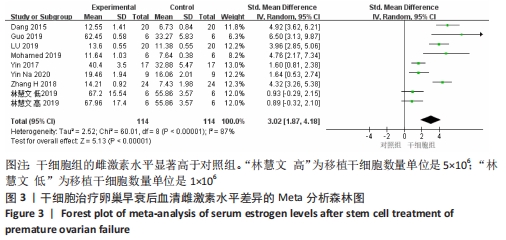
2.3.1 各组血清雌激素水平差异 共8篇文献报道了诱导小鼠卵巢早衰后干细胞对雌激素的修复能力的影响[13,16,19-24]。其中1篇研究包括脐带间充质干细胞高浓度和脐带间充质干细胞低浓度的2个研究[24],因此对雌激素的分析包括了9个研究[13,16,19-24]。由于各研究结果之间存在异质性(I2 > 50%),采用随机效应模型,结果提示,干细胞组的雌激素水平显著高于对照组(SMD=3.02,95%CI:1.87-4.18,P < 0.000 01),见图3。
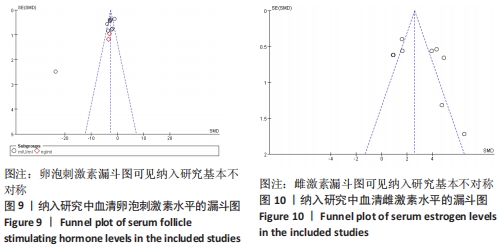
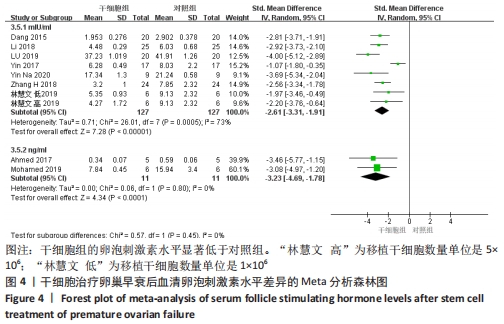
2.3.2 各组血清卵泡刺激素水平差异 共9篇文献报道了诱导小鼠卵巢早衰后干细胞对卵泡刺激素修复能力的影响[13,16-21,23-24]。因其中1篇研究包括脐带间充质干细胞高浓度和脐带间充质干细胞低浓度的2个剂量水平的研究[24],因此对卵泡刺激素的分析包括了10个研究,共纳入干细胞组138只小鼠,对照组138小鼠。基于单位mIU/mL亚组的各研究结果之间存在异质性(I2 > 50%),因此采用随机效应模型进行Meta分析。结果提示,干细胞组的卵泡刺激素水平显著低于对照组(SMD=-2.61,95%CI:-3.31至-1.91,P < 0.000 01)。单位ng/mL亚组各研究结果不存在异质性(I2 < 50%),结果提示,干细胞组的卵泡刺激素水平同样显著低于对照组(SMD=-3.23,95%CI:-4.69至-1.78,P < 0.00 01),见图4。
2.3.3 各组血清抗苗勒管激素水平差异 共4篇文献报道了诱导小鼠卵巢早衰后干细胞对抗苗勒管激素改善能力的影响[20-23]。单位ng/mL亚组的各研究结果之间存在异质性(I2 > 50%),因此采用随机效应模型进行Meta分析。结果提示,干细胞组抗苗勒管激素水平明显高于对照组(SMD=4.77,95%CI:0.95-8.59,P=0.01)。单位pg/mL亚组的各研究结果之间存在异质性(I2 > 50%),因此采用随机效应模型进行Meta分析,结果提示,干细胞组抗苗勒管激素水平同样高于对照组(SMD=4.94,95%CI:0.91-8.97,P=0.02),见图5。

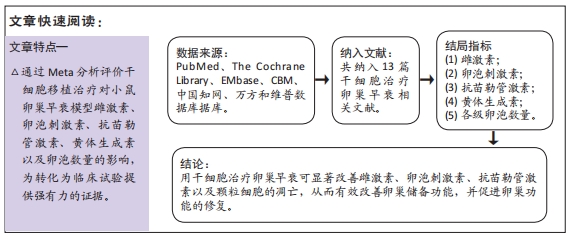
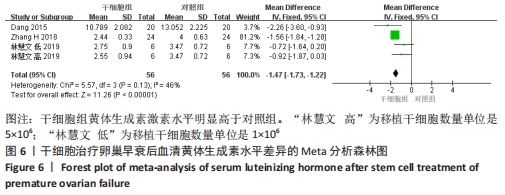
2.3.4 各组黄体生成素水平差异 共3篇文献报道诱导小鼠卵巢早衰后干细胞对黄体生成素能力的影响[13,21,24]。其中1篇研究包括脐带间充质干细胞高浓度和脐带间充质干细胞低浓度的2个剂量水平的研究[24],因此对黄体生成素的分析包括了4个研究。各研究结果之间组内没有异质性(I2 < 50%),采用固定效应模型。结果提示,干细胞组黄体生成素激素水平明显高于对照组(MD=-1.47,95%CI:-1.73至-1.22,P < 0.000 01),见图6。
2.3.5 各组各级卵泡比较差异 根据不同类型的卵泡进行亚组分析。
原始卵泡:共纳入4篇文献报道干细胞治疗对小鼠卵巢早衰原始卵泡的影响[12,20-22]。各研究存在明显的异质性(I2 > 50%),故选择随机效应模型。结果提示两组比较差异有显著性意义(SMD=2.33,95%CI:0.55-4.11,P= 0.01),见图7。
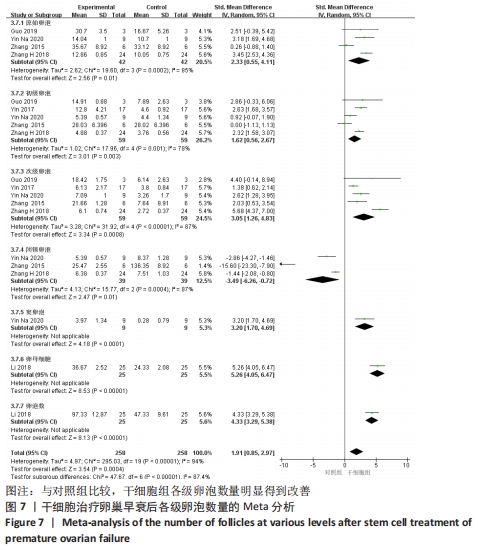
初级卵泡:共纳入5篇文献报道干细胞治疗对小鼠卵巢早衰初级卵泡的影响[12,16,20-22]。各研究间有存在异质性(I2 > 50%)。采用随机效应模型,结果提示两组比较差异有显著性意义(SMD=1.62,95%CI:0.56-2.67,P=0.003),见图7。
次级卵泡:共纳入5篇文献报道干细胞治疗对小鼠卵巢早衰次级卵泡的影响[12,16,20-22]。干细胞组59只小鼠,对照组59只小鼠。各组研究间存在异质性(I2 > 50%),采用随机效应模型。结果提示两组比较差异有显著性意义(SMD=3.05,95%CI:1.26-4.83,P= 0.000 8),见图7。
闭锁卵泡:共纳入3篇文献报道干细胞治疗对小鼠卵巢早衰闭锁卵泡的影响[12,20-21]。各研究间存在异质性(I2 > 50%),采用随机效应模型,结果提示两组比较差异有显著性意义(SMD=-3.49,95%CI:-6.26至-0.72,P=0.01),见图7。
窦卵泡:纳入1篇文献报道干细胞治疗对小鼠卵巢早衰对窦卵泡的影响[20]。因单篇研究无异质性,结果提示两组比较差异有显著性意义(SMD=3.20,95%CI:1.70-4.69,P < 0.000 1),见图7。
卵母细胞:纳入1篇研究报道干细胞治疗对小鼠卵巢早衰卵母细胞的影响[18]。干细胞组25只小鼠,对照组25只小鼠。因单篇研究无异质性,结果提示两组比较差异有显著性意义(SMD=5.26,95%CI:4.05-6.47,P < 0.000 01),见图7。
卵泡数:纳入1篇文献报道干细胞治疗对小鼠卵巢早衰对卵泡数量的影响[18]。因单篇研究无异质性,结果提示两组比较差异有显著性意义(SMD=4.33,95%CI:3.29-5.38,P < 0.000 01),见图7。
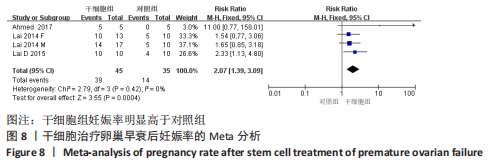
2.3.6 各组妊娠率差异 共纳入3篇研究干细胞治疗对小鼠卵巢早衰妊娠率的影响[14-15,17]。干细胞组小鼠45只,对照小鼠35只。其中1篇研究包括雌性皮肤间充质干细胞移植和雄性皮肤间充质干细胞2个干细胞类型的研究[14],因此对妊娠率的分析包括了4个研究。各研究间不存在异质性(I2=0%),选择固定效应模型。两组差异有显著性意义(RR=2.07,95%CI:1.39-3.09,P=0.000 4),见图8。
2.3.7 不同时间各级卵泡数目的亚组Meta分析结果 根据干细胞移植后≤ 2周、干细胞移植后2-4周和干细胞移植后> 4周的3个结局指标进行卵泡数目亚组Meta分析。
原始卵泡:基于不同时间段,与对照组相比,干细胞组移植后≤ 2周(MD=3.34,95%CI:2.42-4.26,P < 0.000 01)与干细胞组移植后> 4周(MD=2.81,95%CI:2.36-3.26,P < 0.000 01)均高于对照组。而移植后2-4周干细胞组与对照组比较差异无显著性意义(MD=8.87,95%CI:-2.33-20.06,P=0.12),见表3。
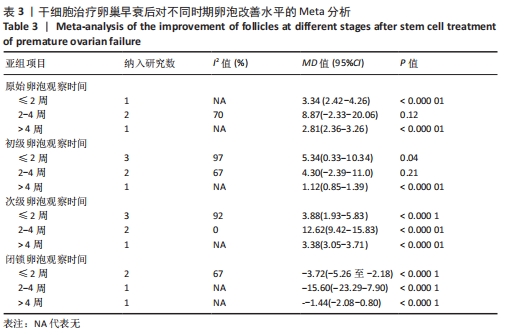
初级卵泡:基于不同时间段,与对照组相比,干细胞组移植后≤ 2周(MD=5.34,95%CI:0.33-10.34,P=0.04)与移植后> 4周(MD=1.12,95%CI:0.85-1.39,P < 0.000 01)均高于对照组。而移植后2-4周干细胞组与对照组比较差异无显著性意义(MD=4.30,95%CI:-2.39-11.0,P=0.21),见表3。
次级卵泡:基于不同时间段,与对照组相比,干细胞组移植后≤2周(MD=3.88,95%CI:1.93-5.83,P < 0.001)、移植后2-4周(MD=12.62,95%CI:9.42-15.83,P < 0.000 01)、移植后> 4周(MD=3.38,95%CI:3.05-3.71,P < 0.000 01)均高于对照组,见表3。
闭锁卵泡:基于不同时间段,与对照组相比,在移植后≤ 2周(MD=-3.72,95%CI:-5.26至-2.18,P < 0.000 1)、移植后2-4周(MD=-15,95%CI:-23.29至-7.90,P < 0.000 1)、移植后> 4周(MD=-1.44,95%CI:-2.08至-0.80,P < 0.000 1)均高于对照组,见表3。
2.3.8 不同细胞来源、细胞剂量、动物模型建立方式的亚组Meta分析结果
干细胞类型:基于不同来源的干细胞,与对照组相比,干细胞组人脐血单个核细胞组的雌激素水平明显升高(MD=4.92,95%CI:3.62-6.21,P < 0.000 01)、
干细胞组人脐带间充质干细胞组的雌激素水平明显升高(MD=2.26,95%CI:0.85-3.67,P=0.002)、干细胞组人经血间充质干细胞组的雌激素水平明显升高(MD=6.5,95%CI:3.13-9.87,P=0.000 2)、干细胞组人胎盘间充质干细胞组的雌激素水平明显升高(MD=2.93,95%CI:0.27-6.60,P=0.03)均高于对照组,见表4。
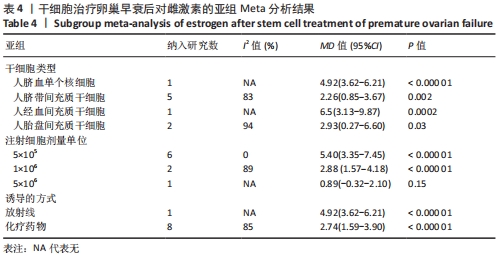
注射细胞剂量:基于不同注射细胞剂量,与对照组相比,干细胞组注射剂量5×105 (MD=5.40,95%CI:3.35-7.45,P < 0.000 01)与注射剂量1×106 (MD=2.88,95%CI:1.57-4.18,P < 0.000 01)均高于对照组。而注射剂量5×106干细胞组与对照组比较差异无显著性意义(MD=0.89,95%CI:-0.32-2.10,P=0.15),见表4。
诱导方式:基于不同诱导方式,与对照组相比,干细胞组放射线(MD=4.92,95%CI:3.62-6.21,P < 0.000 01)与化疗药物(MD=2.74,95%CI:1.59-3.90,P < 0.000 01)均高于对照组,见表4。
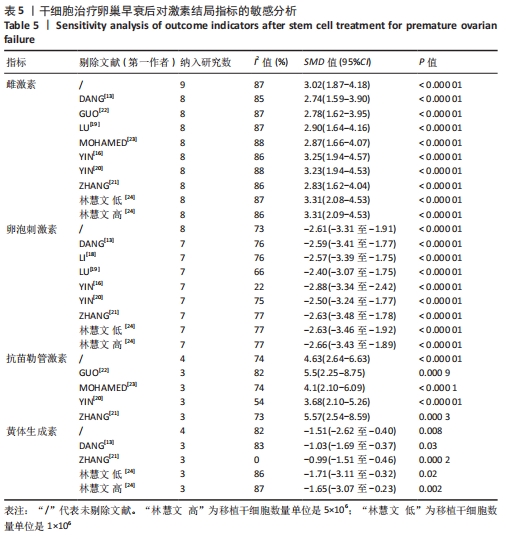
2.4 敏感性分析结果 通过逐篇剔除每项研究后,对4个结局指标血清雌激素、卵泡刺激素、抗苗勒管激素和黄体生成素水平分别进行敏感性分析显示,在雌激素结局指标中逐篇剔除每项研究,较总体异质性没有明显降低,结果稳定;在卵泡刺激素结局指标中,剔除YIN 等[16]的研究后异质性降低(I2=22%,P < 0.000 01);在抗苗勒管激素结局指标中,剔除MOHAMED等[23]的研究后异质性降低(I2=54%,P < 0.000 01);在黄体生成素结局指标中,剔除ZHANG等 [21]的研究后异质性降低(I2=0%,P < 0.000 2),见表5;据以上分析现在异质性来源不确切,不同的干细胞类型、放化疗药物、放化疗时间、取血清的时机等都可能是异质性来源,需要更大的样本量加以证实。
2.5 发表偏倚分析 根据干细胞治疗卵巢早衰的卵泡刺激素、雌激素及黄体生成素水平绘制漏斗图,可见都存在漏斗图不对称,说明可能存在发表偏倚,见图9-11。