Chinese Journal of Tissue Engineering Research ›› 2023, Vol. 27 ›› Issue (1): 83-90.doi: 10.12307/2022.972
Previous Articles Next Articles
Application and progress of small extracellular vesicles in periodontal and pulp regeneration
Liu Runyuan, Dong Ming, Han Wenqing, Dong Juhong, Niu Weidong
- Department of Dentistry and Endodontics, School of Stomatology, Dalian Medical University, Dalian 116041, Liaoning Province, China
-
Received:2021-11-22Accepted:2022-01-29Online:2023-01-08Published:2022-06-06 -
Contact:Niu Weidong, MD, Professor, Doctoral supervisor, Department of Dentistry and Endodontics, School of Stomatology, Dalian Medical University, Dalian 116041, Liaoning Province, China -
About author:Liu Runyuan, Master candidate, Department of Dentistry and Endodontics, School of Stomatology, Dalian Medical University, Dalian 116041, Liaoning Province, China -
Supported by:the Basic Research Program of Natural Science of Liaoning Provincial Education Department, No. LZ2019038 (to NWD); General Project of Education Department of Liaoning Province, No. LJKZ0841 (to DM); Science and Technology Planning Project of Liaoning Province, No. 2021JH2/10300027 (to NWD)
CLC Number:
Cite this article
Liu Runyuan, Dong Ming, Han Wenqing, Dong Juhong, Niu Weidong. Application and progress of small extracellular vesicles in periodontal and pulp regeneration[J]. Chinese Journal of Tissue Engineering Research, 2023, 27(1): 83-90.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
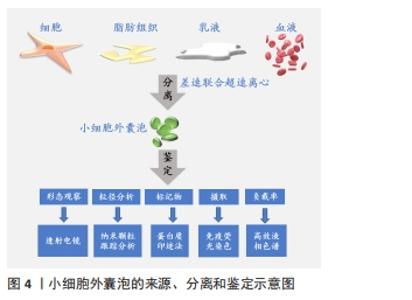
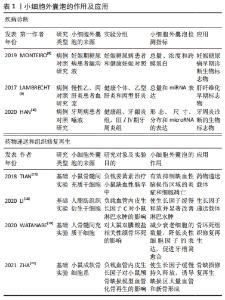
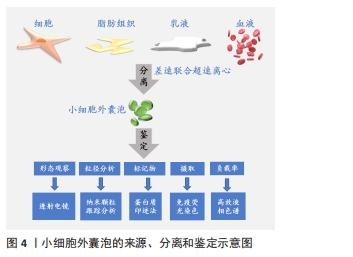
2.1.1 小细胞外囊泡的来源 小细胞外囊泡来源广泛,可由各种细胞在一定条件下释放,存在于胞浆中,还广泛分布于血液、乳液、唾液和脂肪组织中[5]。通过超高速差速离心的方式获取,其分离与鉴定见图4,在透射电镜下观察发现它是一种形似杯状的脂质双分子层膜性纳米级囊泡,内含蛋白质、脂质、miRNA和许多其他非编码RNA。小细胞外囊泡主要包括细胞内体途径来源的外泌体,以依赖运输所需的内体分选复合物(endosomal sorting complex required for transport,ESCRT)的方式,形成腔内小泡和多囊体,通过ESCRT-Ⅲ参与蛋白去泛素化并驱动囊泡分离,与质膜融合形成外泌体并释放到细胞外;其次还有胞膜出芽形成的微囊泡,由ESCRT机制中的关键因子TSG101、VPS4、GTPase ARF6和PLD2调控,促进肌动蛋白细胞骨架解聚,触发胞膜上的囊泡释放,使小细胞外囊泡在胞膜上直接出芽;此外,还包括细胞凋亡产生的凋亡小体以及肿瘤细胞出芽形成的癌小体等[6]。"
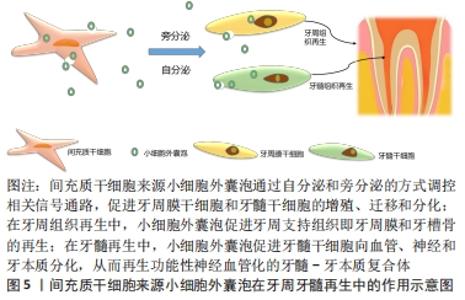
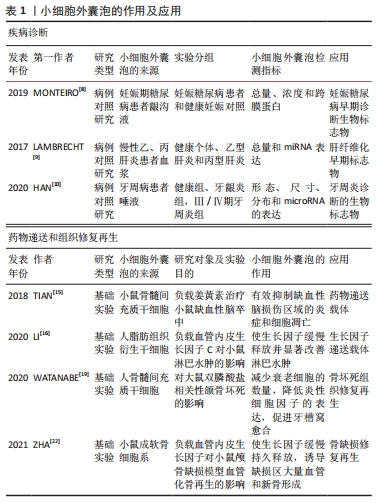
2.1.2 小细胞外囊泡的作用和应用 (1)疾病诊断的生物标志物:因小细胞外囊泡广泛存在于各种体液中,携带多种胞内遗传物质,在细胞旁分泌过程中发挥重要作用,可调节机体免疫应答反应,参与疾病进程,为疾病诊断提供多项参数,提高疾病诊断的敏感性[7]。在疾病发展中,小细胞外囊泡内部的蛋白质、RNA和脂质含量会发生变化,在“液体活组织检查”中容易获取,可作为诊断疾病的生物标志物。MONTEIRO等[8]在妊娠期糖尿病患者和健康妊娠对照者的龈沟液中分离和鉴定小细胞外囊泡,发现糖尿病患者龈沟液中小细胞外囊泡的总量更大,平均浓度更高,对小细胞外囊泡进行量化,可用于妊娠早期疾病的筛查。LAMBRECHT等[9]收集健康人群和慢性肝病患者的血浆,提取血浆中的小细胞外囊泡,通过qRT-PCR分析小细胞外囊泡中miRNA的表达,发现miRNA-200b和miRNA-122在乙型和丙型肝炎患者早期纤维化期间显著上调,说明小细胞外囊泡中的miRNA 可作为肝纤维化早期阶段的诊断标志物。HAN等[10]在牙周炎患者唾液的小细胞外囊泡中,发现hsa-miR-140-5p、hsa-miR-146a-5p和hsa-miR-628-5p这3种miRNA的表达高于健康牙周组织受试者,提示小细胞外囊泡可以作为牙周炎疾病早期诊断的生物标志物。 (2)提高疾病治疗的靶向性:目前,传统的药物递送载体包括脂质体和聚合物两种类型,从而递送抗癌药、抗真菌药和止痛药等不同分子大小的药物[11],但这种合成纳米颗粒再进入血液循环后,往往面临着毒性和网状内皮系统或单核吞噬细胞系统快速清除的问题[12]。而小细胞外囊泡可以穿过血脑屏障,通过一系列表面黏附蛋白和特定的配体如整合素、CD11b和CD18结合,易被细胞摄取而不发生免疫排异反应,提高治疗的靶向性[13],是临床上理想的天然纳米级药物递送载体[14],可负载难溶性中药,增加药物在体内的生物活性,从而提高药物的应用效率,如TIAN等[15]将姜黄素负载入小细胞外囊泡中,通过特殊方式修饰以结合c(RGDyk)肽和荧光,从而增加与反应性脑血管中整合素avβ3的亲和力,提高其靶向性,比单纯的姜黄素能更有效地抑制炎症和脑部损伤区域细胞的凋亡,可作为治疗缺血性脑血管病的有效方法。此外,小细胞外囊泡不仅能够负载小分子药物,还可以负载生长因子,LI等[16]发现血管内皮生长因子C可促进淋巴管内皮细胞的分化,从而促进淋巴管的形成,但其不稳定性、降解性、给药效率低和滞留时间短限制了其药效,利用电穿孔/超声波的方式使小细胞外囊泡负载血管内皮生长因子C,可将血管内皮生长因子C有效地转运到靶细胞促进淋巴管的形成,加入支架海藻酸钠水凝胶对其进行缓释,延长负载血管内皮生长因子C的小细胞外囊泡的作用时间,改善小鼠淋巴水肿,为疾病治疗提供了一种新的策略。 (3)促进组织修复和再生:因小细胞外囊泡具有广泛的来源和强大的生物学功能,还普遍应用于组织的修复与再生以及疫苗开发等领域[17],已在心脏、肺、肾和脑等组织和器官中得到验证[18]。WATANABE等[19]通过建立大鼠双膦酸盐相关性颌骨坏死模型,研究间充质干细胞来源小细胞外囊泡对双膦酸盐相关性颌骨坏死的预防和治疗作用,发现小细胞外囊泡可减少衰老细胞数量,下调衰老相关基因p21、pRB和炎性细胞因子的表达,增加干细胞标志物Bmi1和Hmga2以及血管内皮生长因子的表达,防止干细胞、成骨细胞和成纤维细胞衰老以及慢性炎症的扩散,促进血管和骨再生,从而有效预防双膦酸盐相关性颌骨坏死的发生和发展。脂肪干细胞来源小细胞外囊泡可被人脐静脉内皮细胞和成纤维细胞迅速摄取,并在体外和体内显著促进细胞增殖、迁移和血管生成,使细胞周期蛋白D1、D2、A1和A2等细胞增殖标志物以及生长因子(血管内皮生长因子A、血小板衍生生长因子A、表皮细胞生长因子、成纤维细胞生长因子2)的基因表达上调,还可刺激细胞中AKT和ERK信号通路,增加上皮再生、胶原沉积和新血管形成,加速软组织的损伤愈合[20]。SHI等[21]建立大鼠肌腱缺损模型,将骨髓间充质干细胞来源小细胞外囊泡植入缺损部位,4周后,与肌腱基质形成和肌腱分化相关的基因(Ⅰ型胶原α1和腱调节蛋白)表达显著上调,CD146阳性肌腱干细胞和抗炎巨噬细胞数量明显增加,凋亡细胞和促炎巨噬细胞数量减少,肌腱胶原纤维排列规则和致密,说明骨髓间充质干细胞来源小细胞外囊泡可通过抑制炎症和凋亡,增加肌腱干细胞的比例来促进肌腱愈合。ZHA等[22]分离小鼠成软骨细胞中的小细胞外囊泡,用电穿孔的方式包裹血管内皮生长因子质粒,并与3D打印的多孔骨支架结合,体外研究发现小细胞外囊泡可诱导骨髓间充质干细胞成骨分化,控制释放血管内皮生长因子并促进血管系统的重建,将其植入大鼠桡骨缺损模型,可诱导大量的血管化骨再生。此外,小细胞外囊泡还可促进颌面骨、牙周、牙髓组织和颞下颌关节的再生,促进颌面部皮肤伤口愈合等[4]。虽然,天然小细胞外囊泡具有多种潜力,能够模拟间充质干细胞的功能促进牙周和牙髓干细胞的再生,见图5,但其作用机制和应用还有待进一步总结和研究。 "
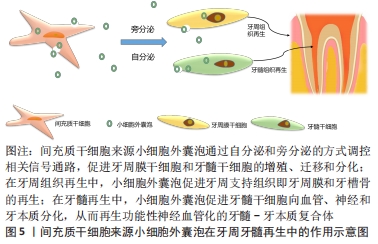

牙周组织缺损的常规手术治疗方法因无法激活牙周组织再生所必须的细胞间通讯,显示出一定的局限性,而牙周膜干细胞可分化为牙周软组织和牙槽骨,是牙周组织再生最合适的干细胞来源[23]。目前研究表明,牙周膜干细胞来源小细胞外囊泡可作为主要的细胞间媒介,传递信息并刺激受伤组织自愈[24],已成为一种免疫原性低、安全性高的无细胞治疗方法,有望替代牙周膜干细胞,在牙周组织修复再生中发挥重要的作用,已被应用于牙周慢性炎症的调控、牙周膜和牙槽骨的再生中 [25-26]。 2.2.1 小细胞外囊泡参与牙周炎症的调控 牙周炎是由细菌感染引起的一种炎症性疾病,表现为持续牙周支持组织的破坏和牙齿脱落,慢性炎症环境可能会影响牙周膜干细胞的免疫调节功能,小细胞外囊泡已被证明在不同组织中具有抗炎和免疫抑制作用,通过超高速离心方式分离牙周膜干细胞中的小细胞外囊泡,发现其可竞争结合Toll样受体4信号通路的靶点,抑制炎性小体NF-κB 的表达和脂多糖的活性,还可以增加Akt 及其下游基因 GSK3β(Ser 9)的磷酸化,通过激活PI3K/Akt信号通路抑制NF-κB的活性,从而抑制牙周炎的慢性炎症[27]。骨髓干细胞来源小细胞外囊泡可通过OPG-RANKL-RANK信号通路影响巨噬细胞的极化和转化生长因子β1的表达,将M1型巨噬细胞转化为M2型,从而调节炎症反应,抑制牙周炎的发展和牙周组织的免疫损伤,利用水凝胶负载骨髓间充质干细胞来源小细胞外囊泡,注射到实验性大鼠牙周炎模型内,可见牙槽骨的丢失、炎性浸润和胶原破坏明显减少[28]。用牙龈卟啉单胞菌脂多糖刺激牙周膜干细胞后,牙周膜干细胞来源小细胞外囊泡中miR-155-5p 表达显著降低,小细胞外囊泡被CD4+ T细胞摄取,miR-155-5p可以在CD4+ T细胞中负调节其下游靶分子Sirtuin-1,而Sirtuin-1可以有效抑制Th17细胞,同时使Treg细胞的活性及功能得以恢复,调节Th17/Treg细胞的平衡,有利于牙周组织炎症与宿主免疫调节达到稳态[29]。此外,间充质干细胞和免疫细胞分泌的小细胞外囊泡可进行双向的信息交换,间充质干细胞来源小细胞外囊泡可下调促炎细胞因子肿瘤坏死因子α的表达,抑制免疫细胞的增殖,减少氧化应激和纤维化,而免疫细胞也可以通过它们的小细胞外囊泡影响间充质干细胞的生物学功能和再生潜力[30]。 2.2.2 小细胞外囊泡促进牙周膜再生 牙周膜纤维可将牙根表面的牙骨质与牙槽骨连接起来,并将牙齿固定在牙槽窝中,缓冲和减弱咬合应力,可有效保护牙齿免受创伤。原有的引导性组织再生方法容易形成结合上皮而非牙周膜,虽然牙周袋变浅但结合不牢固,患者预后较差,因此在牙周组织再生中,形成定向的牙周膜纤维仍然是一个严峻且重要的挑战。研究发现,在慢性牙周炎的炎症微环境下,牙周膜干细胞来源小细胞外囊泡可通过抑制miR-17-5p使血管内皮生长因子A的表达上调,促进牙周组织中血管的再生[31]。CHEW等[32]将间充质干细胞来源小细胞外囊泡与胶原海绵结合应用于大鼠牙周缺损模型中,发现间充质干细胞来源小细胞外囊泡通过激活AKT和ERK信号通路以及调控牙周膜细胞增殖、迁移和凋亡相关因子:胰岛素样生长因子、碱性成纤维细胞生长因子和BCL-2的表达,形成横跨根面和新生骨的功能性牙周膜纤维。MOHAMMED等[33]将脂肪干细胞来源小细胞外囊泡注射到大鼠结扎诱导的牙周袋中,组织学结果显示在大鼠牙槽骨缺损位置形成了新的组织,类似附着于牙骨质和牙槽骨的健康牙周膜纤维,此外,脂肪干细胞来源小细胞外囊泡具有抗炎和免疫调节活性,可以促进多种细胞的生物学功能以及血管生成来诱导组织再生,对牙周炎的治疗效果比单纯脂肪干细胞更好,显示出更大面积的新组织形成。 2.2.3 小细胞外囊泡在牙槽骨再生中的作用 牙周炎会导致牙槽骨的丧失,患者本身的特异性以及环境因素加剧了牙槽骨缺损修复的难度。在过去的几十年里,人们一直致力于探寻牙槽骨缺损的骨再生治疗方法,临床上治疗该问题的主要方法是自体或异体骨移植和引导性组织再生,被称为“黄金疗法”,然而自体骨移植物不能为具有较大缺损的患者提供足够的骨量;异体骨充填使得超过30%的患者患有骨折、骨缺损和感染等并发症;引导性组织再生对患者的要求较高,且治疗效果不稳定[34]。因此需要寻找一种更加可行的方法弥补传统治疗方式的缺陷,基于干细胞的牙周组织再生应运而生,而干细胞分泌的小细胞外囊泡同样具有强大的骨组织再生特性,且其安全性较高,有望用于牙槽骨缺损的再生治疗。 (1)小细胞外囊泡在骨缺损再生治疗中的作用机制:牙槽骨的再生取决于骨吸收和骨形成之间的动态平衡,因此,成骨细胞和破骨细胞之间的相互作用至关重要。研究发现小细胞外囊泡结合支架和生长因子后可同时调控成骨细胞和破骨细胞的功能,促进骨缺损修复[35]。 在骨形成方面,小细胞外囊泡可作为仿生工具直接诱导间充质干细胞和其他原始干细胞转化为成骨细胞谱系,促进成骨细胞增殖,增加成骨细胞分化相关miRNA的表达,抑制Axin1激活的Wnt信号,诱导成骨分化和骨再生[36]。高通量 miRNA 测序显示,间充质干细胞经成骨诱导后分泌的小细胞外囊泡中有41 种 miRNA 差异表达,这些miRNA可参与骨的发育和分化,如破骨细胞分化和MAPK信号通路,其中hsa-miR-2110 和hsa-miR-328-3p是小细胞外囊泡中最重要的成骨调控 miRNA[37]。 NARAYANAN等[38]研究发现,人骨髓间充质干细胞分泌的小细胞外囊泡可上调骨形成相关基因骨钙素、人侏儒相关转录因子2、成骨细胞特异性转录因子和骨桥蛋白的表达,在体内和体外均能加速诱导人骨髓间充质干细胞特异性成骨分化,并提高成骨细胞的矿化能力,通过特异性启动子研究发现小细胞外囊泡的mRNA可翻译成控制人骨髓间充质干细胞命运的功能蛋白,在人骨髓间充质干细胞谱系分化调控中可能优于细胞外基质。CUI等[39]研究发现,成骨细胞来源小细胞外囊泡不仅可以激活细胞分化相关miRNA的表达,促进骨组织再生,还可通过RANKL-RANK信号通路,影响破骨细胞的形成,可成为牙槽骨再生中骨稳态平衡的调控因素。此外,牙髓细胞来源小细胞外囊泡可促进人牙髓细胞和小鼠成骨细胞的增殖、迁移,抑制小鼠破骨细胞的形成,有效减轻牙周炎引起的骨缺失[40],牙龈间充质干细胞来源小细胞外囊泡可促进成骨细胞的迁移和成骨分化[41]。 在骨破坏方面,破骨细胞的增殖与分化在牙槽骨再生过程中同样至关重要,而破骨细胞衍生的小细胞外囊泡是调节破骨细胞生物学功能的旁分泌调节剂,来自成熟破骨细胞的小细胞外囊泡含有RANK的受体激活剂,以OPG的方式与RANKL结合,竞争性抑制破骨细胞的形成[42]。NAKAO等[43]通过结扎法建立小鼠牙周炎模型,观察牙龈间充质干细胞衍生小细胞外囊泡对炎症性骨丢失的影响,通过局部注射牙龈间充质干细胞来源小细胞外囊泡可降低牙周骨吸收和抗酒石酸酸性磷酸酶阳性破骨细胞的数量,用肿瘤坏死因子α预处理牙龈间充质干细胞可进一步增强这一效果,说明肿瘤坏死因子α预处理的牙龈间充质干细胞来源小细胞外囊泡具有调节炎症和破骨细胞生成的能力。还有研究发现,小细胞外囊泡可下调 miR-214和阻断 NF-κB 信号转导,降低破骨细胞标志物抗酒石酸酸性磷酸酶、组织蛋白酶K、基质金属蛋白酶9的表达,有效抑制骨破坏[44]。在非小细胞肺癌中,癌细胞分泌的小细胞外囊泡中含有肿瘤不良预后相关基因AREG,可在破骨前体细胞中诱导 EGFR通路激活,进而导致 RANKL表达增加,诱导破骨细胞生成标志物蛋白水解酶的表达,从而引发骨破坏和溶骨性骨转移,导致肺癌恶性循环[45],说明小细胞外囊泡来源的差异可能会造成截然不同的结果。KANG等[46]研究发现,M2型巨噬细胞来源小细胞外囊泡可促进骨组织再生,M1型巨噬细胞来源小细胞外囊泡则负调节BMP信号通路,抑制骨再生,因此小细胞外囊泡来源对于牙槽骨再生效果的影响至关重要。 (2)小细胞外囊泡促进牙槽骨的再生:在大鼠牙槽骨缺损模型中,使用人脱落乳牙干细胞分泌的小细胞外囊泡,研究其对牙槽骨再生的作用和潜在机制,发现小细胞外囊泡处理后血管生成相关基因基质细胞衍生因子1、成纤维细胞生长因子和成骨相关基因Ⅰ型胶原、人侏儒相关转录因子2、骨桥蛋白以及磷酸化的MAPK表达上调,通过Micro-CT、苏木精-伊红染色、Masson染色以及免疫荧光染色分析表明,有新生血管形成和骨再生,说明人脱落乳牙干细胞来源细胞外囊泡可能通过 MAPK 信号通路促进牙槽骨再生,有利于牙周骨缺损的治疗[47]。ZHOU等[48]将牙龈间充质干细胞来源小细胞外囊泡应用于大鼠牙周缺损模型中,可提高牙周组织的再生能力,增加骨结构的形成以及牙槽骨的改建和重塑。研究发现牙髓干细胞来源小细胞外囊泡通过下调NF-κB-p65和p38-MAPK信号通路,减轻牙周炎小鼠牙周上皮病变,促进新的牙槽骨形成[49]。LEI等[50]从牙周健康的受试者中提取牙周膜干细胞来源小细胞外囊泡,用其处理牙周炎患者的牙周膜干细胞,发现小细胞外囊泡可抑制Wnt信号的过度激活,促进牙周膜干细胞中矿化结节的形成和成骨因子表达的增加,将其结合Matrigel水凝胶用于修复大鼠牙周炎模型牙槽骨缺损,发现小细胞外囊泡能够挽救炎症环境下内源性干细胞的成骨能力,促进牙槽骨的再生,提示小细胞外囊泡是治疗牙周炎的一种有效和实用的无细胞疗法。上述结果表明,小细胞外囊泡可促进牙周支持组织中牙槽骨的再生。 不同细胞来源小细胞外囊泡在牙周组织再生中的作用,见表2。 "


龋病、牙创伤、牙髓炎以及根尖周炎都可以造成牙髓组织的不可逆损伤,牙源性干细胞成血管、成神经和成牙本质分化形成功能性神经血管化牙髓-牙本质复合体已成为治疗牙髓损伤的研究热点[51]。牙髓干细胞是牙髓再生的种子细胞,可通过旁分泌途径发挥作用,而小细胞外囊泡是旁分泌的主要介质之一[52-53]。因此牙髓干细胞介导的组织再生已经转向于探寻其旁分泌介质中小细胞外囊泡的作用,而不是直接研究牙髓干细胞本身[54-55]。 2.3.1 小细胞外囊泡可促进血管的形成 根管内空间狭小,干细胞容易缺氧坏死,影响其分化能力,而血管生成可为干细胞提供氧气和营养,是牙髓再生不可或缺的因素。研究表明,小细胞外囊泡可以增加血管内皮生长因子和缺氧诱导因子1α的表达,增强人脐静脉内皮细胞的管形成能力[56]。LI等[57]在组织坏死区域注射骨髓间充质干细胞来源小细胞外囊泡,发现有微血管的形成,为细胞提供营养,促进坏死组织再生,可作为治疗缺血性疾病的有效手段。XIAN等[58]研究表明牙髓干细胞提取的小细胞外囊泡可通过p38-MAPK信号通路刺激再生牙髓组织内小血管的形成,说明小细胞外囊泡在牙髓血管再生方面也具有较大的潜力。ZHANG等[59]用纤维蛋白水凝胶负载牙髓干细胞来源小细胞外囊泡,与牙髓干细胞和人脐静脉内皮细胞的共培养悬液混合,注射入根管内预测其可再生牙髓组织,并且迅速形成遍布新生牙髓的血管网络,在体外细胞实验中,通过免疫荧光染色发现,水凝胶支架结合小细胞外囊泡后可促进人脐静脉内皮细胞成血管,优于培养液组和单纯水凝胶组,说明牙髓干细胞来源小细胞外囊泡促进血管形成,而水凝胶只是起到支持和缓释的作用。为进一步研究小细胞外囊泡再生牙髓血管的机制,WU等[60]发现脱落乳牙牙髓干细胞来源的小细胞外囊泡能够在体外促进人脐静脉内皮细胞分化,并增强血管生成能力,植入小鼠背部皮下的异位牙齿模型中,能显著促进牙髓组织再生和血管生成,经RNA测序分析表明,小细胞外囊泡通过内部的miR-26a参与TGF-β/SMAD2/3信号通路,促进牙髓内血管再生。 2.3.2 小细胞外囊泡可促进神经的形成 牙髓内神经的形成,可使牙齿感知外界机械、温度和化学刺激,做出应答反应,保护牙髓并减少根折发生的风险。将人脱落乳牙牙髓干细胞聚集体植入年轻恒牙根管内,牙髓电活力测试阈值降低,说明牙髓感觉能力恢复,免疫荧光染色显示感冷和感热神经元标志物表达阳性,说明人脱落乳牙牙髓干细胞能够再生新的神经元[61],而有其他研究证明,人脱落乳牙牙髓干细胞再生神经的机制是通过介导旁分泌信号通路的方式实现的,其来源的小细胞外囊泡具有强大的神经保护特性[62],因此,人脱落乳牙牙髓干细胞来源的小细胞外囊泡能否再生含有神经的牙髓组织还有待研究。HUANG等[63]研究发现小细胞外囊泡中的miR-124-3p通过靶向磷酸二酯酶4B,抑制mTOR信号通路,从而抑制神经元炎症,促进轴突的生长。ZHANG等[64]发现上皮根鞘来源小细胞外囊泡可以促进牙乳头细胞中神经源性标志物髓鞘碱性蛋白101、神经丝蛋白200的表达和新神经元的再生。与上述结论矛盾的是,HU等[65]研究表明牙髓干细胞来源小细胞外囊泡可作为牙髓再生的生物工具,但并不能实现牙髓内神经元的恢复和再生。因此,小细胞外囊泡是否能够促进牙髓中神经的再生还有待进一步研究。 2.3.3 小细胞外囊泡可促进牙髓-牙本质复合体的形成 小细胞外囊泡是牙髓干细胞的诱导剂,可以触发牙髓样组织的再生,牙髓干细胞来源小细胞外囊泡可以激活MAPK途径并促进成牙本质细胞分化,ZHUANG等[66]用根尖牙乳头干细胞来源的小细胞外囊泡处理骨髓间充质干细胞,发现骨髓间充质干细胞能够摄取小细胞外囊泡,矿化结节形成的基因和蛋白质表达显著增加,植入牙根切片中,发现新形成的牙本质沉积在根管内壁上,并伴有牙髓样组织的再生。HUANG等[67]将不同培养条件下牙髓干细胞来源小细胞外囊泡和胶原蛋白膜结合植入3.0-4.0 mm长的牙本质磨片上,并将其植入裸鼠背部皮下,在牙髓干细胞成骨诱导培养条件下,可检测到成牙本质标志蛋白牙本质涎磷蛋白和牙本质基质蛋白、促血管生成因子血小板衍生因子以及成骨分化因子人侏儒相关转录因子2的表达高于普通培养组,可诱导含有神经血管的牙髓-牙本质样组织再生,进一步证明了牙髓干细胞的生长环境和分化程度会影响其小细胞外囊泡的再生功能。CHEN等[68]通过研究脂多糖预处理的人牙髓干细胞来源小细胞外囊泡对牙髓再生的影响,发现小细胞外囊泡可调节人牙髓干细胞的增殖、迁移、血管生成和分化,将小细胞外囊泡植入大鼠无髓根管模型中,在移植30 d后对根管中的再生组织进行评估,发现在脂多糖处理后,小细胞外囊泡增强了牙髓组织再生的能力,在再生组织的外层有排列整齐的成牙本质细胞,中间有大量的成纤维细胞和小血管,还可见矿化牙本质的形成,与体内正常牙髓的结构接近,说明在炎症微环境下,有利于牙髓干细胞来源小细胞外囊泡更好地发挥功能。 不同细胞来源小细胞外囊泡在牙髓组织再生中的作用,见表3 。 "

| [1] BATRAKOVA EV, KIM MS. Using exosomes, naturally-equipped nanocarriers, for drug delivery. J Control Release. 2015;219:396-405. [2] THéRY C, WITWER KW, AIKAWA E, et al. Minimal information for studies of extracellular vesicles 2018 (MISEV2018): a position statement of the International Society for Extracellular Vesicles and update of the MISEV2014 guidelines. J Extracell Vesicles. 2018;7(1):1535750. [3] DONG M, WU S, XU H, et al. FBS-Derived Exosomes as a Natural Nano-Scale Carrier for Icariin Promote Osteoblast Proliferation. Front Bioeng Biotechnol. 2021;9:615920. [4] XING X, HAN S, LI Z, et al. Emerging role of exosomes in craniofacial and dental applications. Theranostics. 2020;10(19):8648-8664. [5] GARCIA-MARTIN R, BRANDAO BB, THOMOU T, et al. Tissue differences in the exosomal/small extracellular vesicle proteome and their potential as indicators of altered tissue metabolism. Cell Rep. 2022;38(3): 110277. [6] WANG X, THOMSEN P. Mesenchymal stem cell-derived small extracellular vesicles and bone regeneration. Basic Clin Pharmacol Toxicol. 2021;128(1):18-36. [7] SUN W, ZHAO C, LI Y, et al. Osteoclast-derived microRNA-containing exosomes selectively inhibit osteoblast activity. Cell Discov. 2016;2:16015. [8] MONTEIRO LJ, VARAS-GODOY M, MONCKEBERG M, et al. Oral extracellular vesicles in early pregnancy can identify patients at risk of developing gestational diabetes mellitus. PLoS One. 2019;14(6): e0218616. [9] LAMBRECHT J, JAN POORTMANS P, VERHULST S, et al. Circulating ECV-Associated miRNAs as Potential Clinical Biomarkers in Early Stage HBV and HCV Induced Liver Fibrosis. Front Pharmacol. 2017;8:56. [10] HAN P, BARTOLD PM, SALOMON C, et al. Salivary Small Extracellular Vesicles Associated miRNAs in Periodontal Status-A Pilot Study. Int J Mol Sci. 2020;21(8):2809. [11] LUAN X, SANSANAPHONGPRICHA K, MYERS I, et al. Engineering exosomes as refined biological nanoplatforms for drug delivery. Acta Pharmacol Sin. 2017;38(6):754-763. [12] CHINNAPPAN M, SRIVASTAVA A, AMREDDY N, et al. Exosomes as drug delivery vehicle and contributor of resistance to anticancer drugs. Cancer Lett. 2020;486:18-28. [13] FAMILTSEVA A, JEREMIC N, TYAGI SC. Exosomes: cell-created drug delivery systems. Mol Cell Biochem. 2019;459(1-2):1-6. [14] LIAO W, DU Y, ZHANG C, et al. Exosomes: The next generation of endogenous nanomaterials for advanced drug delivery and therapy. Acta Biomater. 2019;86:1-14. [15] TIAN T, ZHANG HX, HE CP, et al. Surface functionalized exosomes as targeted drug delivery vehicles for cerebral ischemia therapy. Biomaterials. 2018;150:137-149. [16] LI B, YANG J, WANG R, et al. Delivery of vascular endothelial growth factor (VEGFC) via engineered exosomes improves lymphedema. Ann Transl Med. 2020;8(22):1498. [17] YU X, ODENTHAL M, FRIES JW. Exosomes as miRNA Carriers: Formation-Function-Future. Int J Mol Sci. 2016;17(12):2028. [18] QIN Y, SUN R, WU C, et al. Exosome: A Novel Approach to Stimulate Bone Regeneration through Regulation of Osteogenesis and Angiogenesis. Int J Mol Sci. 2016;17(5):712. [19] WATANABE J, SAKAI K, URATA Y, et al. Extracellular Vesicles of Stem Cells to Prevent BRONJ. J Dent Res. 2020;99(5):552-560. [20] REN S, CHEN J, DUSCHER D, et al. Microvesicles from human adipose stem cells promote wound healing by optimizing cellular functions via AKT and ERK signaling pathways. Stem Cell Res Ther. 2019;10(1):47. [21] SHI Z, WANG Q, JIANG D. Extracellular vesicles from bone marrow-derived multipotent mesenchymal stromal cells regulate inflammation and enhance tendon healing. J Transl Med. 2019;17(1):211. [22] ZHA Y, LI Y, LIN T, et al. Progenitor cell-derived exosomes endowed with VEGF plasmids enhance osteogenic induction and vascular remodeling in large segmental bone defects. Theranostics. 2021;11(1):397-409. [23] HUO JF, ZHANG ML, WANG XX, et al. Chrysin induces osteogenic differentiation of human dental pulp stem cells. Exp Cell Res. 2021; 400(2):112466. [24] SONG MK, KIM HY, CHOI BK, et al. Filifactor alocis-derived extracellular vesicles inhibit osteogenesis through TLR2 signaling. Mol Oral Microbiol. 2020;35(5):202-210. [25] CHAPARRO PADILLA A, WEBER ARACENA L, REALINI FUENTES O, et al. Molecular signatures of extracellular vesicles in oral fluids of periodontitis patients. Oral Dis. 2020. doi: 10.1111/odi.13338. Online ahead of print. [26] GEGOUT PY, STUTZ C, OLSON J, et al. Interests of Exosomes in Bone and Periodontal Regeneration: A Systematic Review. Adv Exp Med Biol. 2021;1341:67-87. [27] ČEBATARIŪNIENĖ A, KRIAUČIŪNAITĖ K, PRUNSKAITĖ J, et al. Extracellular Vesicles Suppress Basal and Lipopolysaccharide-Induced NFκB Activity in Human Periodontal Ligament Stem Cells. Stem Cells Dev. 2019;28(15):1037-1049. [28] LIU L, GUO S, SHI W, et al. Bone Marrow Mesenchymal Stem Cell-Derived Small Extracellular Vesicles Promote Periodontal Regeneration. Tissue Eng Part A. 2021;27(13-14):962-976. [29] ZHENG Y, DONG C, YANG J, et al. Exosomal microRNA-155-5p from PDLSCs regulated Th17/Treg balance by targeting sirtuin-1 in chronic periodontitis. J Cell Physiol. 2019;234(11):20662-20674. [30] BÖRGER V, BREMER M, FERRER-TUR R, et al. Mesenchymal Stem/Stromal Cell-Derived Extracellular Vesicles and Their Potential as Novel Immunomodulatory Therapeutic Agents. Int J Mol Sci. 2017;18(7):1450. [31] ZHANG Z, SHUAI Y, ZHOU F, et al. PDLSCs Regulate Angiogenesis of Periodontal Ligaments via VEGF Transferred by Exosomes in Periodontitis. Int J Med Sci. 2020;17(5):558-567. [32] CHEW JRJ, CHUAH SJ, TEO KYW, et al. Mesenchymal stem cell exosomes enhance periodontal ligament cell functions and promote periodontal regeneration. Acta Biomater. 2019;89:252-264. [33] MOHAMMED E, KHALIL E, SABRY D. Effect of Adipose-Derived Stem Cells and Their Exo as Adjunctive Therapy to Nonsurgical Periodontal Treatment: A Histologic and Histomorphometric Study in Rats. Biomolecules. 2018;8(4):167. [34] SHENG Y, GUO HM, BAI YX, et al. Dehiscence and fenestration in anterior teeth : Comparison before and after orthodontic treatment. J Orofac Orthop. 2020;81(1):1-9. [35] MI B, CHEN L, XIONG Y, et al. Osteoblast/Osteoclast and Immune Cocktail Therapy of an Exosome/Drug Delivery Multifunctional Hydrogel Accelerates Fracture Repair. ACS Nano. 2022. doi: 10.1021/acsnano.1c08284. [36] NARAYANAN R, HUANG CC, RAVINDRAN S. Hijacking the Cellular Mail: Exosome Mediated Differentiation of Mesenchymal Stem Cells. Stem Cells Int. 2016;2016:3808674. [37] YAHAO G, XINJIA W. The Role and Mechanism of Exosomes from Umbilical Cord Mesenchymal Stem Cells in Inducing Osteogenesis and Preventing Osteoporosis. Cell Transplant. 2021;30:9636897211057465. [38] NARAYANAN K, KUMAR S, PADMANABHAN P, et al. Lineage-specific exosomes could override extracellular matrix mediated human mesenchymal stem cell differentiation. Biomaterials. 2018;182: 312-322. [39] CUI Y, LUAN J, LI H, et al. Exosomes derived from mineralizing osteoblasts promote ST2 cell osteogenic differentiation by alteration of microRNA expression. FEBS Lett. 2016;590(1):185-192. [40] SHIMIZU Y, TAKEDA-KAWAGUCHI T, KURODA I, et al. Exosomes from dental pulp cells attenuate bone loss in mouse experimental periodontitis. J Periodontal Res. 2022;57(1):162-172. [41] JIANG S, XU L. Exosomes from gingival mesenchymal stem cells enhance migration and osteogenic differentiation of pre-osteoblasts. Pharmazie. 2020;75(11):576-580. [42] HUYNH N, VONMOSS L, SMITH D, et al. Characterization of Regulatory Extracellular Vesicles from Osteoclasts. J Dent Res. 2016;95(6):673-679. [43] NAKAO Y, FUKUDA T, ZHANG Q, et al. Exosomes from TNF-α-treated human gingiva-derived MSCs enhance M2 macrophage polarization and inhibit periodontal bone loss. Acta Biomater. 2021;122:306-324. [44] RAIMONDI L, DE LUCA A, AMODIO N, et al. Involvement of multiple myeloma cell-derived exosomes in osteoclast differentiation. Oncotarget. 2015;6(15):13772-13789. [45] TAVERNA S, PUCCI M, GIALLOMBARDO M, et al. Amphiregulin contained in NSCLC-exosomes induces osteoclast differentiation through the activation of EGFR pathway. Sci Rep. 2017;7(1):3170. [46] KANG M, HUANG CC, LU Y, et al. Bone regeneration is mediated by macrophage extracellular vesicles. Bone. 2020;141:115627. [47] WU J, CHEN L, WANG R, et al. Exosomes Secreted by Stem Cells from Human Exfoliated Deciduous Teeth Promote Alveolar Bone Defect Repair through the Regulation of Angiogenesis and Osteogenesis. ACS Biomater Sci Eng. 2019;5(7):3561-3571. [48] ZHOU S, YATES KE, EID K, et al. Demineralized bone promotes chondrocyte or osteoblast differentiation of human marrow stromal cells cultured in collagen sponges. Cell Tissue Bank. 2005;6(1):33-44. [49] DALEY GQ. Stem cells and the evolving notion of cellular identity. Philos Trans R Soc Lond B Biol Sci. 2015;370(1680):20140376. [50] LEI F, LI M, LIN T, et al. Treatment of inflammatory bone loss in periodontitis by stem cell-derived exosomes. Acta Biomater. 2022. doi: 10.1016/j.actbio.2021.12.035. Online ahead of print. [51] SCHMALZ G, WIDBILLER M, GALLER KM. Clinical Perspectives of Pulp Regeneration. J Endod. 2020;46(9S):S161-S174. [52] ERAMO S, NATALI A, PINNA R, et al. Dental pulp regeneration via cell homing. Int Endod J. 2018;51(4):405-419. [53] GIRAUD T, JEANNEAU C, ROMBOUTS C, et al. Pulp capping materials modulate the balance between inflammation and regeneration. Dent Mater. 2019;35(1):24-35. [54] SWANSON WB, GONG T, ZHANG Z, et al. Controlled release of odontogenic exosomes from a biodegradable vehicle mediates dentinogenesis as a novel biomimetic pulp capping therapy. J Control Release. 2020;324:679-694. [55] RAINEY K, MICHALEK SM, WEN ZT, et al. Glycosyltransferase-Mediated Biofilm Matrix Dynamics and Virulence of Streptococcus mutans. Appl Environ Microbiol. 2019;85(5):e02247. [56] ZHANG Y, HAO Z, WANG P, et al. Exosomes from human umbilical cord mesenchymal stem cells enhance fracture healing through HIF-1α-mediated promotion of angiogenesis in a rat model of stabilized fracture. Cell Prolif. 2019;52(2):e12570. [57] LI H, LIU D, LI C, et al. Exosomes secreted from mutant-HIF-1α-modified bone-marrow-derived mesenchymal stem cells attenuate early steroid-induced avascular necrosis of femoral head in rabbit. Cell Biol Int. 2017; 41(12):1379-1390. [58] XIAN X, GONG Q, LI C, et al. Exosomes with Highly Angiogenic Potential for Possible Use in Pulp Regeneration. J Endod. 2018;44(5):751-758. [59] ZHANG S, THIEBES AL, KREIMENDAHL F, et al. Extracellular Vesicles-Loaded Fibrin Gel Supports Rapid Neovascularization for Dental Pulp Regeneration. Int J Mol Sci. 2020;21(12):4226. [60] WU M, LIU X, LI Z, et al. SHED aggregate exosomes shuttled miR-26a promote angiogenesis in pulp regeneration via TGF-β/SMAD2/3 signalling. Cell Prolif. 2021;54(7):e13074. [61] XUAN K, LI B, GUO H, et al. Deciduous autologous tooth stem cells regenerate dental pulp after implantation into injured teeth. Sci Transl Med. 2018;10(455):eaaf3227. [62] JARMALAVIČIŪTĖ A, TUNAITIS V, PIVORAITĖ U, et al. Exosomes from dental pulp stem cells rescue human dopaminergic neurons from 6-hydroxy-dopamine-induced apoptosis. Cytotherapy. 2015;17(7):932-939. [63] HUANG S, GE X, YU J, et al. Increased miR-124-3p in microglial exosomes following traumatic brain injury inhibits neuronal inflammation and contributes to neurite outgrowth via their transfer into neurons. FASEB J. 2018;32(1):512-528. [64] ZHANG S, YANG Y, JIA S, et al. Exosome-like vesicles derived from Hertwig’s epithelial root sheath cells promote the regeneration of dentin-pulp tissue. Theranostics. 2020;10(13):5914-5931. [65] HU X, ZHONG Y, KONG Y, et al. Lineage-specific exosomes promote the odontogenic differentiation of human dental pulp stem cells (DPSCs) through TGFβ1/smads signaling pathway via transfer of microRNAs. Stem Cell Res Ther. 2019;10(1):170. [66] ZHUANG X, JI L, JIANG H, et al. Exosomes Derived from Stem Cells from the Apical Papilla Promote Dentine-Pulp Complex Regeneration by Inducing Specific Dentinogenesis. Stem Cells Int. 2020;2020:5816723. [67] HUANG CC, NARAYANAN R, ALAPATI S, et al. Exosomes as biomimetic tools for stem cell differentiation: Applications in dental pulp tissue regeneration. Biomaterials. 2016;111:103-115. [68] CHEN WJ, XIE J, LIN X, et al. The Role of Small Extracellular Vesicles Derived from Lipopolysaccharide-preconditioned Human Dental Pulp Stem Cells in Dental Pulp Regeneration. J Endod. 2021;47(6):961-969. [69] ZHANG C, SHANG Y, CHEN X, et al. Supramolecular Nanofibers Containing Arginine-Glycine-Aspartate (RGD) Peptides Boost Therapeutic Efficacy of Extracellular Vesicles in Kidney Repair. ACS Nano. 2020;14(9):12133-12147. [70] 罗雅馨,毕浩然,陈晓旭.间充质干细胞来源外泌体与再生医学:无细胞疗法临床应用的未来[J].中国组织工程研究,2020,24(19): 3055-3062. [71] YAN X, YANG B, CHEN Y, et al. Anti-Friction MSCs Delivery System Improves the Therapy for Severe Osteoarthritis. Adv Mater. 2021; 33(52):e2104758. |
| [1] | Liu Huan, Li Han, Ma Yunhao, Zhong Weijian, Ma Guowu. Osteogenic capacity of partially demineralized dentin particles in the maxillary sinus lift [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(3): 354-359. |
| [2] | Zhou Jie, Pei Xibo, Wan Qianbing. Advances and biological application of asymmetric dressings [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(3): 434-440. |
| [3] | Chen Jingqiao, Li Ying, Meng Maohua, Xu Xingxing, Wang Qinying, Wang Huan, Lu Jing, Shu Jiayu, Dong Qiang. Research progress in platelet-rich fibrin in stomatology [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(3): 441-446. |
| [4] | Zong Mingrui, Liu Haiyan, Li Bing, Wu Xiuping. Application of carboxymethyl chitosan in tissue engineering of stomatology [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(3): 447-452. |
| [5] | Han Tao, Hao Jianqiang, Li Wenbo, Shi Jie, Gao Qiuming. Advantages and problems of antibiotic-loaded bone cements for bone and joint infections [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(3): 470-477. |
| [6] | Lan Qian, Gu Yangcong, Xiao Xin, Bi Xueting, Li Na. Human periodontal ligament stem cells-derived exosomes interfere with the proliferation and differentiation of MC3T3-E1 cells [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(1): 54-58. |
| [7] | Xi Hualei, Xue Bing, Xu Wanqiu, Xu Xiaohang, Yao Lihong, Wang Xiumei. Neural differentiation and neural biomarker expression of dental pulp stem cells [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(1): 91-98. |
| [8] | Liu Zhuoran, Jiang Ming, Li Yourui. Extracellular vesicles in chronic periodontitis [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(1): 99-104. |
| [9] | Shi Xu, Li Ruiyu, Zhang Bing, Chen Qi, Zuo Hua. Effect of inflammatory reaction mediated by microglia polarization in spinal cord injury [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(1): 121-129. |
| [10] | Guo Yujun, Lu Wenjun, Yang Shulong, Li Zhaozhu. Effect of urine-derived stem cells and their exosomes on kidney diseases [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(1): 138-144. |
| [11] | Zhang Jinglan, Zhang Binjing, Chen Yifei, Zhang Chenyue, Hu Zhiai, Hu Haikun. Biological effects of magnetic field on osteogenesis of mesenchymal stem cells [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(1): 145-151. |
| [12] | Liu Wentao, Feng Xingchao, Yang Yi, Bai Shengbin. Effect of M2 macrophage-derived exosomes on osteogenic differentiation of bone marrow mesenchymal stem cells [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(在线): 1-6. |
| [13] | Zhu Chan, Han Xuke, Yao Chengjiao, Zhou Qian, Zhang Qiang, Chen Qiu. Human salivary components and osteoporosis/osteopenia [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1439-1444. |
| [14] | Jin Tao, Liu Lin, Zhu Xiaoyan, Shi Yucong, Niu Jianxiong, Zhang Tongtong, Wu Shujin, Yang Qingshan. Osteoarthritis and mitochondrial abnormalities [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1452-1458. |
| [15] | Zhang Lichuang, Xu Hao, Ma Yinghui, Xiong Mengting, Han Haihui, Bao Jiamin, Zhai Weitao, Liang Qianqian. Mechanism and prospects of regulating lymphatic reflux function in the treatment of rheumatoid arthritis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1459-1466. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||