Chinese Journal of Tissue Engineering Research ›› 2023, Vol. 27 ›› Issue (1): 99-104.doi: 10.12307/2022.976
Previous Articles Next Articles
Extracellular vesicles in chronic periodontitis
Liu Zhuoran1, Jiang Ming2, Li Yourui1
- 1Department of Prosthodontics, Affiliated Hospital of Binzhou Medical College, Binzhou 256600, Shandong Province, China; 2First Department of Dentistry and Endodontics, Jinan Stomatological Hospital, Jinan 250000, Shandong Province, China
-
Received:2021-12-24Accepted:2022-02-15Online:2023-01-08Published:2022-06-06 -
Contact:Jiang Ming, MD, Professor, First Department of Dentistry and Endodontics, Jinan Stomatological Hospital, Jinan 250000, Shandong Province, China -
About author:Liu Zhuoran, Master candidate, Department of Prosthodontics, Affiliated Hospital of Binzhou Medical College, Binzhou 256600, Shandong Province, China
CLC Number:
Cite this article
Liu Zhuoran, Jiang Ming, Li Yourui. Extracellular vesicles in chronic periodontitis[J]. Chinese Journal of Tissue Engineering Research, 2023, 27(1): 99-104.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
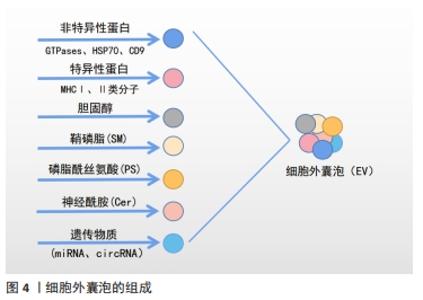
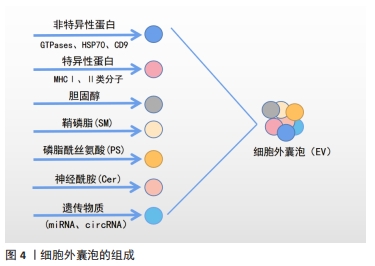
细胞外囊泡来自于不同生物体的细胞,多种研究表明,细胞外囊泡可由不同类型的哺乳动物细胞分泌(包括骨髓间充质干细胞、免疫细胞、骨细胞等)[11],也能够在多细胞生物的体液中分离出来(包括血液、尿液、唾液、母乳、精液等)[12]。原核生物(例如细菌细胞)产生的细胞外囊泡通过介导细菌-细菌和细菌-宿主间相互作用,在生理和病理功能中发挥重要作用,而来自革兰阴性菌的细胞外囊泡通常被称为外膜囊泡[13]。 细胞外囊泡的内部以及表面包含各种蛋白质、脂质、微小核糖核酸、核糖核酸和许多其他非编码核糖核酸,其中蛋白质占据细胞外囊泡内容物的大部分,主要是由非特异性蛋白以及特异性蛋白组成。非特异性蛋白在细胞外囊泡的生成和释放中发挥重要的作用,如膜融合与膜转运蛋白(如Annexin、GTPases、Rab2、Rab7)、热休克蛋白(HSP70、HSP84、HSP90)、跨膜蛋白(如CD9、CD63、CD59)、新陈代谢相关酶(如磷脂酶)等[14]。特异性蛋白主要与细胞的特异性功能相关,如B淋巴细胞表面的黏附分子(MHCⅠ、Ⅱ类分子)能够刺激CD4+细胞的抗肿瘤反应;树突细胞也能产生具有抗原呈递能力的细胞外囊泡。在不同的生理病理条件下特异性蛋白发挥不同的调节功能,因此也具有生物学标志物的潜力[15]。细胞外囊泡质膜上富含胆固醇、鞘磷脂、磷脂酰丝氨酸、神经酰胺等,而在细胞外囊泡上表达的磷脂酰丝氨酸是其特征之一[16]。除了蛋白质和脂类,细胞外囊泡还可以整合遗传物质(mRNA、miRNA、circularRNA、circRNA等),其中异常表达的circRNAs作为microRNA或蛋白质翻译的新模板在许多疾病的发生中起关键作用[17],见图4。 "

2.2 细胞外囊泡的生物学功能 近年来,各项研究发现,虽然所有细胞都通过释放细胞外囊泡来清除细胞内的代谢废物,但细胞内吞作用形成的细胞外囊泡也包含了许多重要信息分子[18]。 来自肿瘤细胞的细胞外囊泡发出细胞侵袭性的信号,并携带对以前使用的治疗方法(化疗、放疗)耐药的信息,从而成为选择个人适合疗法的标记物[19]。当肿瘤细胞来源细胞外囊泡被器官特异性细胞摄取时,重新创造生态位,为转移前做准备。在器官模型中,利用细胞外囊泡疗法可以重新定向肿瘤细胞的转移。 细胞外囊泡被宿主细胞释放后可与受体细胞合并释放内容物,在内化以后,它们可以改变基因的表达。HUANG等[20]对人牙髓干细胞来源细胞外囊泡诱导原始人牙髓干细胞和骨髓间充质干细胞向牙源性分化的潜能进行了评估,发现人牙髓干细胞和骨髓间充质干细胞都能内吞与基质蛋白(如Ⅰ型胶原)结合的细胞外囊泡,引起牙源性分化所需基因表达的增加,因此细胞外囊泡可以作为重要的诊断以及预后的标记物。 表达自杀基因酵母融合胞嘧啶脱氨酶::尿嘧啶磷酸核糖转移酶(yCD::UPRT)的间充质干细胞对于肿瘤的抑制倾向是持续性的,由自杀基因yCD::UPRT转导的人牙髓干细胞来源细胞外囊泡中含有其mRNA。这些细胞外囊泡容易穿透并整合人类肿瘤细胞,在前药5-氟胞嘧啶存在的情况下,可导致肿瘤细胞凋亡[21]。蛋白质组学分析、核酸测序分析以及胞外囊泡研究的数据库都能够让人们进一步了解以及探索细胞外囊泡所介导的生物学效应和其广泛的临床应用潜力。 2.3 细胞外囊泡与慢性牙周炎 "


2.3.1 细胞外囊泡介导慢性牙周炎的炎症反应 菌斑微生物及其产物的侵袭是慢性牙周炎的始动因子,菌斑中的细菌种类繁多,研究证实其中30余种细菌与牙周病的发生和发展相关[22],主要包括牙龈卟啉单胞菌(Porphyromonas gingivalis,Pg)、福赛斯坦纳菌(Tannerella forsythensis,Tf)、牙密螺旋体 (Treponema denticola,Td)、伴放线放线杆菌(Actinobacillus actinomycete mcomitans,Aa)等。 巨噬细胞是最早对细菌及其产物做出反应的免疫细胞之一,通过比较巨噬细胞对牙龈卟啉单胞菌及其细胞外囊泡的反应,发现牙龈卟啉单胞菌来源细胞外囊泡可显著刺激巨噬细胞产生肿瘤坏死因子α、白细胞介素12p70、白细胞介素6、白细胞介素10、干扰素β和一氧化氮[23],而牙龈卟啉单胞菌产生的这些介质水平非常低。牙龈卟啉单胞菌来源细胞外囊泡刺激诱导巨噬细胞代谢转移,增加糖酵解重要基因的表达,降低与三羧酸循环相关基因的表达。炎症小体信号转导和细胞凋亡检查发现,牙龈卟啉单胞菌并不激活巨噬细胞中的炎症小体,相比之下其细胞外囊泡诱导巨噬细胞炎症小体的激活[24]。FIMA是一种广为人知的黏附调节因子,其被认为是牙龈卟啉单胞菌黏附和侵袭宿主细胞的重要因子。来自FIMA突变株的细胞外囊泡能够穿透细胞,但在缺失牙龈卟啉单胞菌的细胞外囊泡的情况下,渗透率显著降低[25]。这些数据表明了牙龈卟啉单胞菌来源细胞外囊泡对巨噬细胞炎症表型、线粒体功能以及炎症小体激活有更为显著的影响,这提示牙龈卟啉单胞菌来源细胞外囊泡可能在慢性牙周炎的发生机制中存在潜在影响。 伴放线放线杆菌(Aa)伴发疾病与局限性侵袭性牙周炎(LAP)发生相关,伴放线放线杆菌产生许多毒力因子,包括一种白毒素(LtxA),它能特异性地杀死宿主免疫细胞,为细菌提供定植优势[26]。明确白毒素被运送到宿主细胞的机制可以帮助识别局限性侵袭性牙周炎的新治疗靶点。研究发现含白毒素的伴放线放线杆菌胞外囊泡比不含白毒素的细胞外囊泡的毒性更强,说明正是在细胞外囊泡中存在的白毒素介导了这种细胞毒性。白毒素有2种不同的分泌形式,一种是需要宿主细胞上的淋巴细胞功能相关抗原1和胆固醇的游离形式,另一种是不需要淋巴细胞功能相关抗原1和胆固醇的细胞外囊泡相关形式。细胞外囊泡结合方式为白毒素提供了与多种宿主细胞类型相互作用的能力,从而提高了白毒素的活性。这提示细胞外囊泡可以为细菌毒素提供特异性传递系统,从而加强细菌毒素的作用[27]。这一发现对于明确伴放线放线杆菌的致病机制以及设计抑制白毒素活性的药物治疗局限性牙周炎具有重要意义。 2.3.2 细胞外囊泡在慢性牙周炎的诊断、病情以及预后评估中的作用 细胞外囊泡能被选择性分泌到细胞外,其mRNA可作为慢性牙周炎早期诊断以及炎症发展导致骨吸收的生物标志物[28]。 生物信息学分析表明慢性牙周炎与炎症基因表达特征有关,程序性死亡-配体1也被称为B7-H1受体,在细胞介导的免疫反应中发挥重要作用,程序性死亡-配体1调节T细胞的激活和耐受,宿主细胞中程序性死亡-配体1的高表达可能有助于炎症疾病的慢性化[29]。牙周炎患者唾液来源细胞外囊泡中富含程序性死亡-配体1,而且其表达与炎症程度呈正相关,其程序性死亡-配体1的表达明显高于非牙周炎患者。这表明唾液来源细胞外囊泡中程序性死亡-配体1 mRNA在牙周炎不同分期之间差异有统计学意义[30],提示唾液来源细胞外囊泡中程序性死亡-配体1 mRNA的检测具有鉴别牙周炎和健康人的潜力,重度牙周炎患者牙周组织中程序性死亡-配体1的表达增加可能与机体需要更多的程序性死亡-配体1来抑制炎症组织的破坏有关。 慢性牙周炎晚期可能通过干扰肿瘤坏死因子α作为杠杆来干预成骨和破骨细胞的平衡[31],导致骨组织的吸收以及抑制成骨作用。破骨细胞分泌富含mRNA的细胞外囊泡,而破骨细胞衍生的细胞外囊泡优先将miR-214转移到成骨细胞中以抑制其活性。这些细胞外囊泡通过ephrinA2和EphA2之间的相互作用特异性识别成骨细胞。在破骨细胞特异性miR-214转基因小鼠中,细胞外囊泡分泌到血清中,miR-214和ephrinA2水平升高。因此,破骨细胞分泌富含mRNA的细胞外囊泡在成骨细胞活性中具有抑制作用[32],提示胞外囊泡在骨生成以及骨吸收过程中的有效调节作用,揭示细胞外囊泡可作为慢性牙周炎的潜在生标志物用于诊断牙槽骨的早期吸收。 2.3.3 细胞外囊泡在预防慢性牙周炎中的作用 牙周炎关系到口腔和全身的健康,因此迫切需要新的预防方法来预防该疾病,利用牙龈卟啉单胞菌的胞外囊泡开发新型疫苗已经初有成效。经鼻或经皮注射牙龈卟啉单胞菌40 kD外膜蛋白可诱导特异性抗体,从而抑制牙龈卟啉单胞菌的共聚集活性[33],这意味着这种破碎的外膜蛋白可用于慢性牙周炎的疫苗接种。 外膜囊泡是革兰阴性菌的细胞外囊泡的统称,外膜囊泡的结构和功能稳定,表现为对蛋白酶K的抗性和长期储存的能力,被认为有利于将外膜囊泡组分带入宿主免疫系统。外膜囊泡鼻腔接种小鼠可诱导外膜囊泡以剂量依赖的方式在血液和唾液中产生牙龈卟啉单胞菌特异性抗体,Toll样受体3激动剂Poly(I:C)的加入显著增强了这种抗体的产生。用外膜囊泡+Poly(I:C)佐剂免疫的小鼠血清样本检测发现不仅疫苗株和异源株的牙龈蛋白水解酶活性受到明显抑制,对小鼠牙龈菌蛋白水解酶活性也有明显的抑制作用,提示外膜囊泡+Poly(I:C)免疫血清可降低牙龈卟啉单胞菌的存活率。外膜囊泡+Poly(I:C)滴鼻免疫小鼠血清IgG(包括IgG1和IgG2a)和唾液S-IgA水平升高,免疫后至少维持28周和18周。外膜囊泡在近端器官中的积累实验和脑内注射实验同时证实了外膜囊泡的安全性[34]。外膜囊泡+Poly(I:C)鼻腔免疫在牙龈卟啉单胞菌清除和安全性方面是一种可行的疫苗策略。 2.3.4 细胞外囊泡在慢性牙周炎免疫治疗中的应用 在牙周形成炎症的过程中,一系列的微生物因子诱导了宿主的一系列反应。干细胞可以通过旁分泌机制创造最佳的微环境,以减少炎症和促进组织修复,其中细胞外囊泡及其microRNAs(miRNAs)起着关键作用[35]。 牙周炎患者外周血中辅助T细胞17(Th17)/调节性T细胞(Treg)的平衡不稳定,证明慢性牙周炎患者存在Th17/Treg功能障碍[36],通过免疫介导的组织破坏诱导Th17上调或Treg下调[37]。通过牙龈卟啉单胞菌脂多糖模拟慢性牙周炎所导致的炎症微环境,从牙周膜干细胞中提取其胞外囊泡,在正常以及炎症条件下观察其对CD4+T细胞产生的作用,结果炎症条件下胞外囊泡组辅助T细胞17表达明显低于正常条件下胞外囊泡组,调节性T细胞表达高于正常条件下胞外囊泡组,进一步研究发现miR-155-5p在两组之间显示出显著的差异,miR-155-5p被抑制,调节性T细胞下调,辅助T细胞17上调,辅助T细胞17/调节性T细胞比例上升,机体处于炎症状态。提示牙周膜干细胞来源细胞外囊泡可以将miR-155-5p转移到CD4+T细胞中,进而调节CD4+T细胞中蛋白的表达,从而影响辅助T细胞17/调节性T细胞的平衡,对炎症微环境有调节和减轻炎症的作用[38]。 在牙周病引起的先天性免疫中,巨噬细胞对牙周病原体起着至关重要的防御作用。针对不同的局部微环境,幼稚的巨噬细胞(M0)可以极化为两种不同的表型,促炎(M1)或抗炎(M2),并在不同的生理或病理条件下发挥不同的作用[39]。 在患有慢性牙周炎的患者中,M1巨噬细胞起主要作用,M1相关促炎因子肿瘤坏死因子α、白细胞介素12、白细胞介素6、白细胞介素1β、CD86水平也较高[40]。当脂多糖和干扰素γ作用于巨噬细胞时,可诱导高水平的白细胞介素12、肿瘤坏死因子α和白细胞介素1β,从而促进了巨噬细胞的炎症反应。牙龈间充质干细胞衍生细胞外囊泡作用于巨噬细胞后,白细胞介素12、肿瘤坏死因子α和白细胞介素1β的表达低于未添加细胞外囊泡的对照组,而M2巨噬细胞高表达的白细胞介素10水平高于对照组[41],提示牙龈间充质干细胞来源细胞外囊泡与巨噬细胞共同作用时能够抑制M1促炎因子的分泌,同时刺激M2抗炎因子的水平增加,促使细胞外囊泡在临床治疗巨噬细胞所致相关炎症时有了替代牙龈间充质干细胞的可能。 2.3.5 细胞外囊泡在牙周组织修复再生中的潜能 再生医学中,干细胞治疗是最主要的途径,具有自我更新以及多向分化潜能的间充质干细胞在动物研究和人类研究中应用广泛[42]。然而,干细胞体内移植存活量少,增殖、分化不可控,输送、储存困难等局限性始终难以克服。而近年来研究发现干细胞旁分泌作用中产生的细胞外囊泡能够介导新组织的宿主细胞形成,诱导细胞分化、组织再生和血管生成,它们也可以通过参与细胞间信号分泌的免疫调节作用来控制伤口的愈合和再生[8]。 利用大鼠牙周骨内缺损模型评估人骨髓间充质干细胞来源细胞外囊泡复合胶原海绵的治疗效果,结果可见成纤维样细胞浸润增强,促进了新软组织的形成,同时发现胶原海绵残留物。相反,未治疗组细胞浸润较少,牙龈软组织塌陷。而且仅有细胞外囊泡处理组在骨缺损顶端显示少量新形成的牙槽骨。而后通过对牙周膜细胞培养,证明了人骨髓间充质干细胞所分泌的胞外囊泡可被牙周膜细胞快速摄取,并且通过CD73介导的腺苷受体激活促生存的AKT和ERK信号来促进牙周膜细胞的迁移和增殖,借此来促进牙周再生。若将该技术应用于牙周组织再生[43],那么可以避免细胞移植产生免疫排斥反应以及伦理等问题,为将人骨髓间充质干细胞所分泌的胞外囊泡作为一种即用且无细胞的牙周再生疗法提供基础。 人骨髓间充质干细胞含有多种血管生长因子,如血管内皮生长因子[44],它对周围的内皮细胞有趋化因子作用,可以增加局部区域的血管数量,通过刺激血管内皮细胞来促进骨的形成与发育[45]。利用大鼠颅骨缺损模型,每周通过分析人骨髓间充质干细胞来源细胞外囊泡组、人骨髓间充质干细胞组、人骨髓间充质干细胞来源细胞外囊泡+血管生成抑制剂组样本来评估骨形成,结果表明人骨髓间充质干细胞来源细胞外囊泡组为受体细胞提供了一些与血管生成和骨再生相关的信息,从而激活了受体细胞分泌的血管内皮生长因子和成骨相关旁分泌因子。人骨髓间充质干细胞来源细胞外囊泡组培养的人骨髓间充质干细胞中血管生成相关基因如血管内皮生长因子、血管生成素1和血管生成素2的表达也显著上调[46],提示人骨髓间充质干细胞来源细胞外囊泡组具有显著的成骨潜能,人骨髓间充质干细胞中含有的细胞外囊泡可能通过促进血管生成在骨再生中发挥重要作用。 软骨修复和再生受软骨细胞和软骨细胞染色体的影响[47]。有研究在大鼠股骨远端的滑车沟上制造骨软骨缺损模型,然后分为两组,实验组术后关节内立即注射人骨髓间充质干细胞来源细胞外囊泡,另一组关节内立即注射PBS,随后每周1次采集股骨远端和滑膜组织样本进行分析,同时采集滑液样本进行细胞因子的测定,结果可见,细胞外囊泡组最早在2周就开始修复临界大小的骨软骨缺损,显著促进了新组织的形成和Ⅱ型胶原的细胞外基质沉积[48]。与此同时,细胞外囊泡组也伴随着活跃的细胞迁移和增殖,这从软骨缺损部位和滑膜上的PCNA阳性细胞数量的增加可以体现。在第6周时,细胞外囊泡处理组的CCP3阳性凋亡细胞数量明显减少,到12周时,与对照组CCP3阳性数量无明显区别[49]。人骨髓间充质干细胞来源细胞外囊泡的许多成分是有效组织再生所必需的,并进一步指出细胞外囊泡是有利于软骨修复的“无细胞”策略。见表1。 "

| [1] 王兴.第四次全国口腔健康流行病调查报告[M].北京:人民卫生出版社,2018. [2] COLOMBO M, RAPOSO G, THÉRY C. Biogenesis, secretion, and intercellular interactions of exosomes and other extracellular vesicles. Annu Rev Cell Dev Biol. 2014;30:255-289. [3] JIANG XY, YANG YZ, HU XL, et al. Research Advances on the Biological Characteristics of Hematological Malignant Cells Immunologically Regulated by Exosome--Review. Zhongguo Shi Yan Xue Ye Xue Za Zhi. 2020;28(1):339-342. [4] MOGHIMAN T, BARGHCHI B, ESMAEILI SA, et al. Therapeutic angiogenesis with exosomal microRNAs: an effectual approach for the treatment of myocardial ischemia. Heart Fail Rev. 2021;26(1):205-213. [5] TAN SHS, WONG JRY, SIM SJY, et al. Mesenchymal stem cell exosomes in bone regenerative strategies-a systematic review of preclinical studies. Mater Today Bio. 2020;7:100067. [6] XIE Y, DANG W, ZHANG S, et al. The role of exosomal noncoding RNAs in cancer. Mol Cancer. 2019;18(1):37. [7] ZABOROWSKI MP, BALAJ L, BREAKEFIELD XO, et al. Extracellular Vesicles: Composition, Biological Relevance, and Methods of Study. Bioscience. 2015;65(8):783-797. [8] COOPER LF, RAVINDRAN S, HUANG CC, et al. A Role for Exosomes in Craniofacial Tissue Engineering and Regeneration. Front Physiol. 2020; 10:1569. [9] RAPOSO G, STOORVOGEL W. Extracellular vesicles: exosomes, microvesicles, and friends. J Cell Biol. 2013;200(4):373-383. [10] TODOROVA D, SIMONCINI S, LACROIX R, et al. Extracellular Vesicles in Angiogenesis. Circ Res. 2017;120(10):1658-1673. [11] MENDT M, REZVANI K, SHPALL E. Mesenchymal stem cell-derived exosomes for clinical use. Bone Marrow Transplant. 2019;54(Suppl 2): 789-792. [12] 王琎,陈建英.细胞外囊泡研究新进展[J].中国组织工程研究,2017, 21(4):621-626. [13] TOYOFUKU M, NOMURA N, EBERL L. Types and origins of bacterial membrane vesicles. Nat Rev Microbiol. 2019;17(1):13-24. [14] MASHOURI L, YOUSEFI H, AREF AR, et al. Exosomes: composition, biogenesis, and mechanisms in cancer metastasis and drug resistance. Mol Cancer. 2019;18(1):75. [15] DENG F, MILLER J. A review on protein markers of exosome from different bio-resources and the antibodies used for characterization. J Histotechnol. 2019;42(4):226-239. [16] VERDERIO C, GABRIELLI M, GIUSSANI P. Role of sphingolipids in the biogenesis and biological activity of extracellular vesicles. J Lipid Res. 2018;59(8):1325-1340. [17] SKOTLAND T, HESSVIK NP, SANDVIG K, et al. Exosomal lipid composition and the role of ether lipids and phosphoinositides in exosome biology. J Lipid Res. 2019;60(1):9-18. [18] STANKO P, ALTANEROVA U, JAKUBECHOVA J, et al. Dental Mesenchymal Stem/Stromal Cells and Their Exosomes. Stem Cells Int. 2018;2018: 8973613. [19] HOSHINO A, COSTA-SILVA B, SHEN TL, et al. Tumour exosome integrins determine organotropic metastasis. Nature. 2015;527(7578):329-335. [20] HUANG CC, NARAYANAN R, ALAPATI S, et al. Exosomes as biomimetic tools for stem cell differentiation: Applications in dental pulp tissue regeneration. Biomaterials. 2016;111:103-115. [21] ALTANER C. Prodrug Gene Therapy for Cancer Mediated by Mesenchymal Stem/Stromal Cells Engineered to Express Yeast Cytosinedeaminase::Uracilphosphoribosyltransferase. J Stem Cell Res Ther. 2015;5(2):264. [22] NUNN ME. Understanding the etiology of periodontitis: an overview of periodontal risk factors. Periodontol 2000. 2003;32:11-23. [23] VEITH PD, CHEN YY, GORASIA DG, et al. Porphyromonas gingivalis outer membrane vesicles exclusively contain outer membrane and periplasmic proteins and carry a cargo enriched with virulence factors. J Proteome Res. 2014;13(5):2420-2432. [24] FLEETWOOD AJ, LEE MKS, SINGLETON W, et al. Metabolic Remodeling, Inflammasome Activation, and Pyroptosis in Macrophages Stimulated by Porphyromonas gingivalis and Its Outer Membrane Vesicles. Front Cell Infect Microbiol. 2017;7:351. [25] MANTRI CK, CHEN CH, DONG X, et al. Fimbriae-mediated outer membrane vesicle production and invasion of Porphyromonas gingivalis. Microbiologyopen. 2015;4(1):53-65. [26] NYGREN P, BALASHOVA N, BROWN AC, et al. Aggregatibacter actinomycetemcomitans leukotoxin causes activation of lymphocyte function-associated antigen 1. Cell Microbiol. 2019;21(3):e12967. [27] NICE JB, BALASHOVA NV, KACHLANY SC, et al. Aggregatibacter actinomycetemcomitans Leukotoxin Is Delivered to Host Cells in an LFA-1-Indepdendent Manner When Associated with Outer Membrane Vesicles. Toxins (Basel). 2018;10(10):414. [28] KIMAK A, STRYCHARZ-DUDZIAK M, BACHANEK T, et al. Lipids and lipoproteins and inflammatory markers in patients with chronic apical periodontitis. Lipids Health Dis. 2015;14:162. [29] ZAMANI MR, ASLANI S, SALMANINEJAD A, et al. PD-1/PD-L and autoimmunity: A growing relationship. Cell Immunol. 2016;310:27-41. [30] YU J, LIN Y, XIONG X, et al. Detection of Exosomal PD-L1 RNA in Saliva of Patients With Periodontitis. Front Genet. 2019;10:202. [31] ZHOU R, SHEN L, YANG C, et al. Periodontitis May Restrain the Mandibular Bone Healing via Disturbing Osteogenic and Osteoclastic Balance. Inflammation. 2018;41(3):972-983. [32] SUN W, ZHAO C, LI Y, et al. Osteoclast-derived microRNA-containing exosomes selectively inhibit osteoblast activity. Cell Discov. 2016;2: 16015. [33] MAEBA S, OTAKE S, NAMIKOSHI J, et al. Transcutaneous immunization with a 40-kDa outer membrane protein of Porphyromonas gingivalis induces specific antibodies which inhibit coaggregation by P. gingivalis. Vaccine. 2005;23(19):2513-2521. [34] NAKAO R, HASEGAWA H, DONGYING B, et al. Assessment of outer membrane vesicles of periodontopathic bacterium Porphyromonas gingivalis as possible mucosal immunogen. Vaccine. 2016;34(38):4626-4634. [35] DU YM, ZHUANSUN YX, CHEN R, et al. Mesenchymal stem cell exosomes promote immunosuppression of regulatory T cells in asthma. Exp Cell Res. 2018;363(1):114-120. [36] WANG L, WANG J, JIN Y, et al. Oral administration of all-trans retinoic acid suppresses experimental periodontitis by modulating the Th17/Treg imbalance. J Periodontol. 2014;85(5):740-750. [37] KARTHIKEYAN B, TALWAR, ARUN KV, et al. Evaluation of transcription factor that regulates T helper 17 and regulatory T cells function in periodontal health and disease. J Pharm Bioallied Sci. 2015;7(Suppl 2): S672-676. [38] ZHENG Y, DONG C, YANG J, et al. Exosomal microRNA-155-5p from PDLSCs regulated Th17/Treg balance by targeting sirtuin-1 in chronic periodontitis. J Cell Physiol. 2019;234(11):20662-20674. [39] YANG J, ZHU Y, DUAN D, et al. Enhanced activity of macrophage M1/M2 phenotypes in periodontitis. Arch Oral Biol. 2018;96:234-242. [40] RIOS FJ, TOUYZ RM, MONTEZANO AC. Isolation and Differentiation of Human Macrophages. Methods Mol Biol. 2017;1527:311-320. [41] WANG R, JI Q, MENG C, et al. Role of gingival mesenchymal stem cell exosomes in macrophage polarization under inflammatory conditions. Int Immunopharmacol. 2020;81:106030. [42] MORENO SANCHO F, LEIRA Y, ORLANDI M, et al. Cell-Based Therapies for Alveolar Bone and Periodontal Regeneration: Concise Review. Stem Cells Transl Med. 2019;8(12):1286-1295. [43] CHEW JRJ, CHUAH SJ, TEO KYW, et al. Mesenchymal stem cell exosomes enhance periodontal ligament cell functions and promote periodontal regeneration. Acta Biomater. 2019;89:252-264. [44] LEE E, KO JY, KIM J, et al. Osteogenesis and angiogenesis are simultaneously enhanced in BMP2-/VEGF-transfected adipose stem cells through activation of the YAP/TAZ signaling pathway. Biomater Sci. 2019;7(11):4588-4602. [45] DREYER CH, KJAERGAARD K, DING M, et al. Vascular endothelial growth factor for in vivo bone formation: A systematic review. J Orthop Translat. 2020;24:46-57. [46] TAKEUCHI R, KATAGIRI W, ENDO S, et al. Exosomes from conditioned media of bone marrow-derived mesenchymal stem cells promote bone regeneration by enhancing angiogenesis. PLoS One. 2019;14(11): e0225472. [47] SEKIYA I, MUNETA T, HORIE M, et al. Arthroscopic Transplantation of Synovial Stem Cells Improves Clinical Outcomes in Knees With Cartilage Defects. Clin Orthop Relat Res. 2015;473(7):2316-2326. [48] ZHANG S, CHU WC, LAI RC, et al. Exosomes derived from human embryonic mesenchymal stem cells promote osteochondral regeneration. Osteoarthritis Cartilage. 2016;24(12):2135-2140. [49] ZHANG S, CHUAH SJ, LAI RC, et al. MSC exosomes mediate cartilage repair by enhancing proliferation, attenuating apoptosis and modulating immune reactivity. Biomaterials. 2018;156:16-27. [50] 黄海宁,黄乾生.细菌胞外囊泡的研究进展[J].微生物学报, DOI: 10.13343/j.cnki.wsxb.20210582. |
| [1] | Liu Huan, Li Han, Ma Yunhao, Zhong Weijian, Ma Guowu. Osteogenic capacity of partially demineralized dentin particles in the maxillary sinus lift [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(3): 354-359. |
| [2] | Zhou Jie, Pei Xibo, Wan Qianbing. Advances and biological application of asymmetric dressings [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(3): 434-440. |
| [3] | Chen Jingqiao, Li Ying, Meng Maohua, Xu Xingxing, Wang Qinying, Wang Huan, Lu Jing, Shu Jiayu, Dong Qiang. Research progress in platelet-rich fibrin in stomatology [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(3): 441-446. |
| [4] | Zong Mingrui, Liu Haiyan, Li Bing, Wu Xiuping. Application of carboxymethyl chitosan in tissue engineering of stomatology [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(3): 447-452. |
| [5] | Han Tao, Hao Jianqiang, Li Wenbo, Shi Jie, Gao Qiuming. Advantages and problems of antibiotic-loaded bone cements for bone and joint infections [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(3): 470-477. |
| [6] | Lan Qian, Gu Yangcong, Xiao Xin, Bi Xueting, Li Na. Human periodontal ligament stem cells-derived exosomes interfere with the proliferation and differentiation of MC3T3-E1 cells [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(1): 54-58. |
| [7] | Liu Runyuan, Dong Ming, Han Wenqing, Dong Juhong, Niu Weidong. Application and progress of small extracellular vesicles in periodontal and pulp regeneration [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(1): 83-90. |
| [8] | Xi Hualei, Xue Bing, Xu Wanqiu, Xu Xiaohang, Yao Lihong, Wang Xiumei. Neural differentiation and neural biomarker expression of dental pulp stem cells [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(1): 91-98. |
| [9] | Zhu Zhenghuan, Zou Hongjun, Song Zhiwen, Liu Jinbo. Cellular microenvironment in nerve repair after spinal cord injury [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(1): 114-120. |
| [10] | Shi Xu, Li Ruiyu, Zhang Bing, Chen Qi, Zuo Hua. Effect of inflammatory reaction mediated by microglia polarization in spinal cord injury [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(1): 121-129. |
| [11] | Guo Yujun, Lu Wenjun, Yang Shulong, Li Zhaozhu. Effect of urine-derived stem cells and their exosomes on kidney diseases [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(1): 138-144. |
| [12] | Zhang Jinglan, Zhang Binjing, Chen Yifei, Zhang Chenyue, Hu Zhiai, Hu Haikun. Biological effects of magnetic field on osteogenesis of mesenchymal stem cells [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(1): 145-151. |
| [13] | Liu Wentao, Feng Xingchao, Yang Yi, Bai Shengbin. Effect of M2 macrophage-derived exosomes on osteogenic differentiation of bone marrow mesenchymal stem cells [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(在线): 1-6. |
| [14] | Zhu Chan, Han Xuke, Yao Chengjiao, Zhou Qian, Zhang Qiang, Chen Qiu. Human salivary components and osteoporosis/osteopenia [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1439-1444. |
| [15] | Jin Tao, Liu Lin, Zhu Xiaoyan, Shi Yucong, Niu Jianxiong, Zhang Tongtong, Wu Shujin, Yang Qingshan. Osteoarthritis and mitochondrial abnormalities [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1452-1458. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||