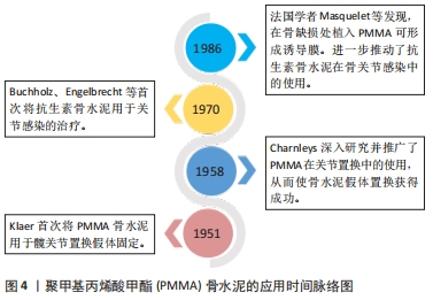
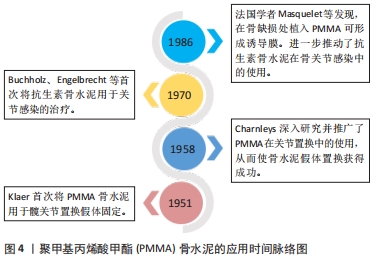
Chinese Journal of Tissue Engineering Research ›› 2023, Vol. 27 ›› Issue (3): 470-477.doi: 10.12307/2023.034
Previous Articles Next Articles
Advantages and problems of antibiotic-loaded bone cements for bone and joint infections
Han Tao1, Hao Jianqiang1, Li Wenbo2, Shi Jie2, Gao Qiuming2
- 1First Clinical Medical College of Gansu University of Traditional Chinese Medicine, Lanzhou 730000, Gansu Province, China; 2Department of Orthopedic Trauma, The 940th Hospital of Joint Logistics Support Force of Chinese People’s Liberation Army, Lanzhou 730050, Gansu Province, China
-
Received:2022-01-17Accepted:2022-03-02Online:2023-01-28Published:2022-06-01 -
Contact:Gao Qiuming, Chief physician, Professor, Master’s supervisor, Department of Orthopedic Trauma, The 940th Hospital of Joint Logistics Support Force of Chinese People’s Liberation Army, Lanzhou 730050, Gansu Province, China -
About author:Han Tao, Master candidate, First Clinical Medical College of Gansu University of Traditional Chinese Medicine, Lanzhou 730000, Gansu Province, China -
Supported by:The 940th Hospital of Joint Logistics Support Force of Chinese People’s Liberation Army Intra-Hospital Research Program - Basic and Clinical Incubation Program, No. 2021yxky037 (to GQM)
CLC Number:
Cite this article
Han Tao, Hao Jianqiang, Li Wenbo, Shi Jie, Gao Qiuming. Advantages and problems of antibiotic-loaded bone cements for bone and joint infections[J]. Chinese Journal of Tissue Engineering Research, 2023, 27(3): 470-477.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
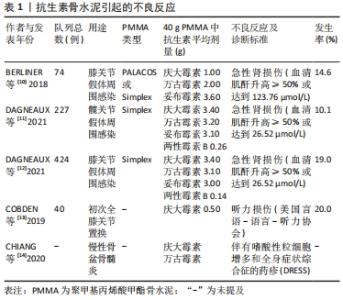
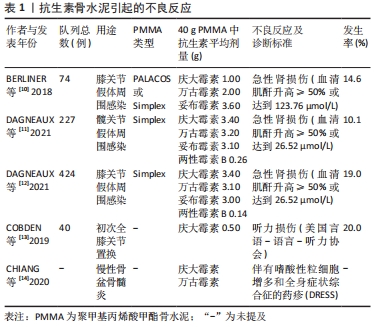
2.2 引起骨关节感染的病原微生物学 骨关节感染通常是由于开放性骨折、手术时的直接接种、邻近部位感染的蔓延或继发于其他感染源的血行播撒所致[3]。引起骨关节感染的微生物有2种不同的存在形式——浮游形式和生物膜形式,同一微生物可以在不同条件下实现两种形式之间的相互转化。浮游微生物通常自由漂浮在机体中,新陈代谢比较活跃并且可以快速复制;相比之下,生物膜是由胞外多糖包裹细胞形成的复杂多细胞结构,是微生物的稳定生长阶段,其常常定植在无活性的死骨或植入物表面上。生物膜的代谢活动比较缓慢,对宿主免疫机制和大多数抗生素有着天然的抵抗力,因此,生物膜一旦在体内形成就很难根除。有研究表明,细菌生物膜是细菌在自然界的主要生存形式,且临床上至少有65%的微生物感染与细菌生物膜有关[4]。然而,临床上的许多骨关节感染都伴有生物膜的形成,这些感染或是慢性感染、或是与植入物相关的感染、或两者兼有。 引起骨关节感染的微生物种属在不同地区和人群之间存在差异,以往最常引起骨关节感染的微生物是金黄色葡萄球菌,近年来随着针对金黄色葡萄球菌抗生素在骨科手术中的普遍使用,耐甲氧西林金黄色葡萄球菌(MRSA)引起的感染有增加的趋势[5]。一项多中心回顾性研究表明,耐甲氧西林敏感金黄色葡萄球菌仍是目前最常引起创伤性骨感染的单一致病菌,但随着临床上对革兰阳性菌的针对性预防,革兰阴性菌已经成为创伤性骨感染的主要致病菌,其中以铜绿假单胞菌为主[6]。 2.3 抗生素的选择 PMMA可以同时负载一种或多种抗生素,但并不是所有的抗生素均可与其混合使用。在制备抗生素骨水泥之前,除了要考虑抗生素的抗菌谱和安全性外,还要考虑其有效性以及是否会对PMMA的理化性质造成不利影响。因为在使用PMMA作为载体时,其聚合反应产生的高温会影响抗生素的效能,而液态抗生素会显著降低其力学强度。因此,可用于制备抗生素骨水泥的抗生素必须是粉剂形式,且要具备良好的热稳定性。 2.3.1 抗金黄色葡萄球菌药物 金黄色葡萄球菌作为引起骨关节感染的主要致病菌,仍是临床预防与治疗的主要针对对象。万古霉素、庆大霉素和妥布霉素均可用于预防和治疗金黄色葡萄球菌及其生物膜引起的感染[7],且均具有良好的热稳定性,以保证其在PMMA骨水泥固化放热的过程中不会失效。因此,万古霉素、庆大霉素和妥布霉素是最常被用于制备抗生素骨水泥的抗生素。如前所述,考虑到耐甲氧西林金黄色葡萄球菌在骨关节感染中的比重正在不断增加,而万古霉素作为耐甲氧西林金黄色葡萄球菌感染的首选抗生素,仍对耐甲氧西林金黄色葡萄球菌引起的感染有效[8]。但最近的一项研究表明,载万古霉素的PMMA骨水泥并不能有效减少耐甲氧西林金黄色葡萄球菌生物膜的形成[9]。另外,随着载万古霉素、庆大霉素和妥布霉素PMMA骨水泥在临床上的大量使用,有关其不良反应的报道也越来越多,如急性肾损伤、听力损伤、过敏等,见表1。 "

对此,寻找其他可用于制备抗生素骨水泥的抗金黄色葡萄球菌抗生素是必要的,特别是针对耐甲氧西林金黄色葡萄球菌感染的抗生素。体外研究表明,载左氧氟沙星的PMMA骨水泥对金黄色葡萄球菌的浮游和生物膜形式均具有抑制作用,且没有明显的细胞毒性和过敏性[15]。载达托霉素的PMMA骨水泥不仅可以根除葡萄球菌生物膜[7],还对耐甲氧西林金黄色葡萄球菌具有抑制作用[16],但当每40 g PMMA骨水泥中的达托霉素添加量≥0.5 g时具有细胞毒性[17]。除此之外,新一代头孢菌素类抗生素头孢洛林对耐甲氧西林金黄色葡萄球菌感染有效,当分别将头孢他洛林与万古霉素以相同的剂量添加到PMMA骨水泥中时,其对耐甲氧西林金黄色葡萄球菌的抑制能力更强,且洗脱时间更长[18]。 2.3.2 抗真菌药物 真菌感染在骨关节感染中所占比例较低,且绝大多数由白色念珠菌引起,但随着骨科手术量的增加,真菌性骨关节感染也有增加的趋势。真菌感染通常与患者的免疫功能受损(如糖尿病、类风湿性关节炎、癌症等)和生物膜的形成有关,且可能会同时合并细菌感染,因此,真菌引起的骨关节感染治疗起来更加困难。对此,一些载抗真菌药物的抗生素骨水泥已被用于真菌性骨关节感染的治疗,如两性霉素B、氟康唑等,其中使用最多的是两性霉素B[19-20]。KIM等[21]在9例被诊断为慢性真菌性假体周围关节感染患者的一期手术中使用了含两性霉素的PMMA骨水泥,并在术后进行了平均7个月的全身敏感抗真菌药物治疗,所有患者在二期关节置换术后2年的随访中没有出现真菌感染的复发。但由于目前对抗真菌药物骨水泥治疗真菌感染的报道还较少,因此其安全性尚不清楚。 2.3.3 抗结核药物 利福平和异烟肼是治疗结核杆菌感染的一线药物,但它们均无法直接用于抗生素骨水泥的制备。利福平与其他抗生素不同,其具有根除细菌生物膜的能力,但会影响PMMA骨水泥的聚合反应,导致其不能良好地固化。而异烟肼没有可用于制备抗生素骨水泥的粉末剂型[22]。因此,可直接用于制备抗生素骨水泥的抗结核药物很少。袁虎成等[23]的体外实验分别检测了载有10种常用抗结核药物PMMA骨水泥的物理性能,发现乙胺丁醇、吡嗪酰胺、链霉素、卷曲霉素、阿米卡星、莫西沙星在浓度为1.5 g、2.5 g/40 g PMMA时,抗生素骨水泥的平均面团时间、凝固时间、平均最高温度及机械强度均符合ISO标准,而含相同浓度利福平、异烟肼、利福喷丁、丙硫异烟胺抗生素骨水泥的平均面团、凝固时间均> ISO标准,但平均最高温度明显低于含其他抗生素的PMMA骨水泥,且机械强度均< ISO标准。该研究再次验证了低剂量的利福平和异烟肼即会显著影响PMMA骨水泥的物理性能,但并未对载高剂量(≥4 g/40 g PMMA)抗结核药物抗生素骨水泥的物理性能、药物洗脱及抗菌效果进行测定,还需进一步研究。因为对于抗生素骨水泥而言,抗生素的添加剂量是影响其力学性能和疗效的关键因素,这将会在下文讲到。 2.4 抗生素骨水泥的洗脱特性及力学特性 提高局部抗生素的浓度和骨的力学稳定性会在一定程度上加快对感染的控制率和骨愈合,因此,若能在不影响抗生素骨水泥力学强度的前提下保证其持续、稳定地释放高浓度抗生素,可以在很大程度上改善其对骨关节感染的疗效。但是,抗生素骨水泥中的抗生素是从其孔隙和裂缝中被动地扩散出来的,且能被洗脱的抗生素主要集中在其表面的浅层,在其被放入体内的初始阶段,位于其浅表的抗生素会爆发式的释放,而随着其在体内放置时间的延长,其释放的抗生素会大幅度减少,并维持在一个低释放状态[24]。并且,PMMA是一种稳定的有机高分子聚合物,各单体之间通过共价键连接在一起,而抗生素不会与PMMA形成化学键[25],抗生素的加入势必会改变PMMA固化后的内部结构,导致其承载横截面积净损失、应力点集中、力学强度下降。另外,抗生素骨水泥的力学强度并不是固定不变的,而是一个动态变化的过程,随着抗生素的洗脱,PMMA中的孔隙会逐渐增多,其力学强度也会逐渐降低。因此,几乎所有能影响抗生素洗脱的因素都会影响其力学强度。通过对以往文献的回顾,以下几种因素会影响抗生素骨水泥的力学强度和抗生素洗脱。 "

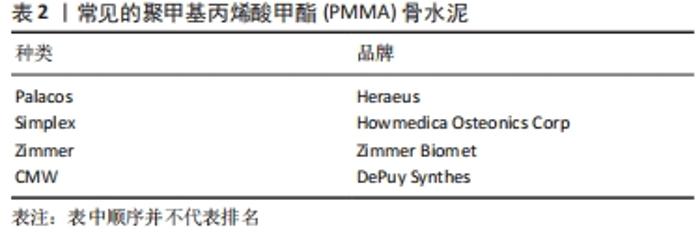
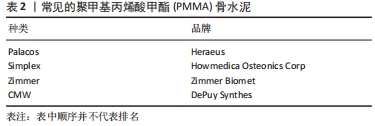
2.4.1 抗生素种类 由于抗生素是从PMMA骨水泥中的孔隙和裂缝中被动扩散到洗脱液中的,因此,抗生素的化学性质在很大程度上可以影响其在PMMA中的洗脱,从而影响PMMA的力学强度。体外实验发现,将相同剂量的万古霉素和妥布霉素加入同一种PMMA骨水泥中时,妥布霉素的总洗脱量比万古霉素的总洗脱量大得多,而将两种抗生素同时加入PMMA骨水泥中时,两种抗生素的洗脱总量均会增加,但妥布霉素的总洗脱量增加的更加明显。另外,将抗生素骨水泥在洗脱液中存放28 d后,所有抗生素骨水泥的机械强度都显著降低,且抗生素骨水泥的力学强度会随着抗生素释放量的增加而降低[26]。这可能是由于妥布霉素的分子质量(467 Da)显著小于万古霉素的分子质量(1 449 Da),而小分子质量的妥布霉素会更容易通过PMMA内部的孔隙和裂缝到达洗脱液中,从而增加了其抗生素释放量和PMMA内部的孔隙率增加,降低了其机械性能。 2.4.2 抗生素剂量 提高抗生素骨水泥中抗生素的添加剂量会增加PMMA内部的孔隙率,从而会增加抗生素的洗脱量,但会直接降低其力学强度[27]。以万古霉素为例,KIM等[28]的体外实验分别测定了载0.125,0.25,0.5,1.0,2.0 g万古霉素/ 40 g PMMA抗生素骨水泥的力学强度、抗生素洗脱率以及对耐甲氧西林金黄色葡萄球菌、金黄色葡萄球菌、表皮葡萄球菌的抗菌活性,结果发现添加了2.0 g万古霉素/40 g PMMA的抗生素骨水泥在60 d内的抗生素洗脱量最大,且只有其能够完全消灭所测试的细菌;但当万古霉素的添加剂量≥ 0.5 g 时,抗生素骨水泥的抗压强度和抗弯曲强度均会低于国际标准化组织的所有最低要求。对此,目前并未找到既能满足力学强度要求又能满足抗菌活性要求的抗生素和抗生素添加剂量,且临床上对于抗生素骨水泥中抗生素的添加剂量仍缺乏公认的规范和标准。 2.4.3 PMMA骨水泥种类 由不同种类的PMMA骨水泥制备的抗生素骨水泥,其抗生素洗脱能力和机械性能也存在差异。这可能是由于它们的生产工艺和黏度不同(见表2),从而影响了其固化后的内部孔隙大小和分布。"
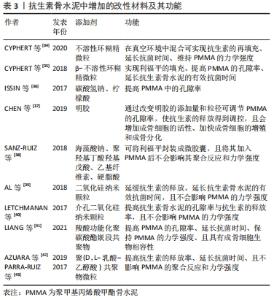
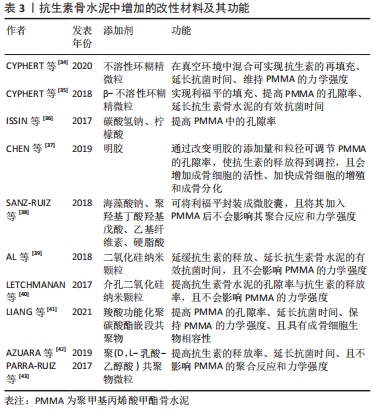
MEEKER等[29]比较了4种由不同PMMA骨水泥制备的抗生素骨水泥的抗生素洗脱能力,他们发现Palacos比Simplex表现出更强的抗生素洗脱能力,而Cobalt和Zimmer的抗生素洗脱能力介于Palacos和Simplex之间,并且Cobalt与Zimmer的抗生素洗脱能力无统计学差异。另外,有研究表明,与Simplex P相比,Zimmer Biomet品牌的PMMA骨水泥表现出更强的抗生素洗脱能力[30]。 2.4.4 混合方法 抗生素骨水泥常由固相粉剂、液相固化液和抗生素粉末3部分组成,在制备抗生素骨水泥前通常需要将PMMA固相粉剂、抗生素粉剂和固化液按一定的比例混合起来并进行充分搅拌。不同的混合方法会导致抗生素在PMMA中的分布不同,从而使得抗生素骨水泥内部的孔隙大小和分布不均。FREW等[31]比较了含有相同浓度抗生素(每40 g PMMA含0.5 g庆大霉素、2 g万古霉素)的市售和自混抗生素骨水泥的抗生素洗脱能力,他们发现在2周的时间内,自混抗生素骨水泥中的万古霉素和庆大霉素总洗脱量分别是市售抗生素骨水泥的5倍和2倍,这可能是由于市售预混的抗生素骨水泥在固化后内部的孔隙更少、大小更一致所致,因此其更适合在关节置换手术中使用。另外,手动混合会在提高抗生素释放量的同时降低抗生素骨水泥的力学性能[32]。 2.4.5 表面积和形状 由于可被释放的抗生素大部分来源于其表面的浅层,PMMA固化后的表面积越大就意味着暴露在洗脱液中可洗脱面积越大,这无疑会增加抗生素的洗脱,并且抗生素骨水泥的抗生素释放率与其固化后的几何形状有相关性。有研究表明,无论使用何种PMMA骨水泥和何种制备方法,抗生素骨水泥珠链的抗生素释放量均高于抗生素骨水泥垫片或团块[30]。 2.4.6 混合环境 不同的混合环境也会影响抗生素骨水泥中的孔隙大小和分布,从而影响抗生素的释放和机械性能。另外,较低的温度会延缓PMMA的聚合反应,导致PMMA内部的气孔增加,从而有利于PMMA中抗生素的洗脱[25]。SUNDBLAD等[33]研究了不同的混合温度对抗生素释放率的影响,结果发现相较于在21℃下制备的载妥布霉素/万古霉素抗生素骨水泥,在37 ℃和8 ℃下制备的载妥布霉素/万古霉素抗生素骨水泥的抗生素洗脱量显著增加。 2.5 抗生素骨水泥中添加的改性材料 如上所述,抗生素骨水泥具有一定的抗菌能力,但抗生素的加入使会降低PMMA骨水泥的力学强度。如何才能在提高抗生素骨水泥抗菌能力的同时尽可能减少对其力学强度的影响?对此,一些学者尝试通过在制备抗生素骨水泥的过程中加入改性材料来解决这一问题。初步研究证明,改性材料的加入使得这一问题的解决成为可能,见表3。 "

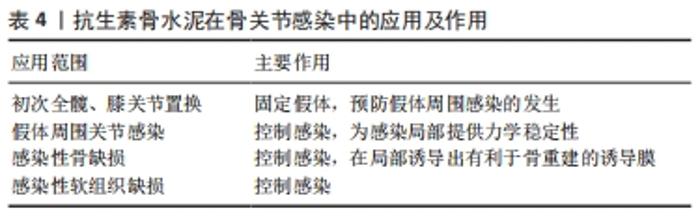
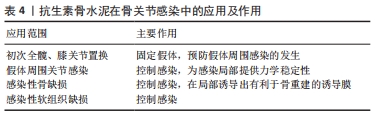
2.6.1 在初次全髋、膝关节置换中的应用 初次关节置换术中使用抗生素骨水泥的主要目的是在固定假体的同时预防假体周围感染的发生。但是,考虑到其力学特性和抗生素的洗脱特点,在初次关节置换中其是否比单纯PMMA骨水泥更有优势,目前尚有争议,特别是在初次膝关节置换术中。FARHAN-ALANIE等[44]的研究比较了抗生素骨水泥与单纯PMMA骨水泥对初次全髋和全膝关节置换术后的全因翻修率和因假体周围感染的翻修率,这项研究共纳入了371 977例初次全髋关节置换和671 246例全膝关节置换患者,统计分析表明,在全髋关节置换术中使用抗生素骨水泥的感染翻修率较单纯PMMA骨水泥低,而全因翻修率没有差异,在全膝关节置换术中,两者的全因翻修率和感染翻修率均没有差异。然而,JAMESON等[45]对在多中心接受了初次全膝关节置换术的731 214例患者的分析结果表明,相对于单纯PMMA骨水泥,在初次全膝关节置换术中使用抗生素骨水泥会降低患者的全因翻修风险、无菌翻修风险和感染翻修风险,并且术中使用了抗生素骨水泥患者的10年生存率更高。同样,BENDICH等[46]对2007-2015年期间在美国退伍军人健康管理局医院接受初次全膝关节置换术的15 972列退伍军人的回顾性分析也表明,使用抗生素骨水泥会降低初次全膝关节置换术后的全因翻修率和感染翻修率。对此,有学者认为,相较于初次全膝关节置换,抗生素骨水泥在初次全髋关节置换中似乎是有优势的,因为初次全髋关节置换术中对抗生素骨水泥的用量较初次全膝关节置换术中的用量更大,从而使抗生素的洗脱量更大、局部浓度更高;并且,初次全髋关节置换中抗生素骨水泥和假体的接触表面积更广,从而可以减少假体与骨组织的接触面积与细菌生物膜的形成[44]。但是,以往的研究表明,初次关节置换术后是否发生假体周围关节感染与患者自身状况(如种族、性别、年龄、肥胖、糖尿病、类风湿关节炎等)、地方医疗水平、手术方法、假体材质、术后护理等诸多因素有关[47-50],因此,至于是否在初次关节置换中使用抗生素骨水泥,需要临床医生在术前进行全面的评估,从而做出合理的选择。 2.6.2 在假体周围关节感染中的应用 对于假体周围感染的治疗,抗生素骨水泥的主要作用在于控制感染并消灭死腔。临床上通常会在一期手术中取出假体,并对感染灶进行彻底清创后植入抗生素骨水泥来控制感染,待感染得到控制后再择期进行二期手术植入假体,应用此方法可以有效控制关节置换术后的假体周围关节感染。有研究表明,在肩关节假体周围感染的治疗中使用抗生素骨水泥对感染的控制率高达95%[51]。另外,ORTOLA等[52]的研究表明,与含2种抗生素的PMMA骨水泥相比,含3种抗生素的PMMA骨水泥对膝关节假体周围感染的感染控制率更高,分别为1.79%和3.70%。 2.6.3 在感染性骨缺损中的应用 在治疗感染性骨缺损方面,抗生素骨水泥的使用方式比较灵活。一阶段取出植入物并彻底清创,将抗生素骨水泥填充至骨缺损处,二阶段再进行植骨或应用骨搬移技术重建骨缺损是目前治疗慢性骨髓炎和骨缺损的常用方法。应用此方法治疗感染性骨缺损时往往需要联合使用临时内固定装置或外固定架来维持局部骨的稳定性。但是,直接使用内固定物会增加感染复发和细菌生物膜形成的风险,使用外固定架有损伤周围神经、血管和针道感染的可能。对此,一些临床医生利用抗生素骨水泥对固定方法进行了改进,并取得了良好的临床效果。JIA等[53]在对183例患有下肢感染患者的治疗中使用了抗生素骨水泥被覆锁定钢板,其中股骨81例、胫骨100例、腓骨2例,治疗结果显示,95.9%的患者实现了骨愈合。WANG等[54]使用与抗生素骨水泥被覆锁定钢板相似的抗生素骨水泥板复合结构内固定对548例患有四肢骨感染的患者进行了治疗,其中包括胫骨309例、股骨207例、尺桡骨16例、肱骨13例、锁骨3例,97.6%患者的感染得到了有效控制。此类内固定最大的优势在于使用抗生素骨水泥被覆或包裹钢板可以有效避免内固定与病原菌的直接接触,从而降低了内植物感染的风险。CHO等[55]使用Ilizarov外固定系统的螺纹杆和抗生素骨水泥制备了一种可用于治疗骨髓炎的抗生素骨水泥涂层髓内铰接螺纹杆,治疗结果显示,在40例使用此内固定的骨髓炎或感染性骨不连的患者中有34例患者的感染得到了有效控制。该内固定杆可以在为患肢提供较高稳定性的同时避免因制动引起的关节僵硬的发生,并且,螺纹杆上的螺纹可以提供较高的摩擦力,从而使其在移除的过程中抗生素骨水泥涂层不会脱落。同样,RUPP等[56]的报道称,将抗生素骨水泥包裹在缠有钢丝的肱骨髓内钉上也可以用于治疗骨感染,并且也可以避免移除过程中抗生素骨水泥的脱落。除此之外,有报道称,对于患有难以重建的感染性骨缺损的低需求患者,可以考虑将抗生素骨水泥团块长期留在骨缺损处,并且这些抗生素骨水泥对患者的正常活动影响很小[57-58]。 2.6.4 在感染性软组织缺损中的应用 严重的骨关节感染常伴有软组织的感染,而严重的软组织感染局部常缺乏新生血管和血液供应,并且反复的炎症刺激会造成创面周围的纤维组织增生和瘢痕形成,会进一步阻碍血液中的抗生素到达局部感染灶。因此,全身应用抗生素对其疗效有限,而局部应用抗生素骨水泥可使抗生素直达局部感染灶,从而有效提高抗生素的利用率,使感染得到有效控制。研究表明,抗生素骨水泥的使用可显著提高四肢软组织感染的感染控制率,缩短感染性软组织创面的肉芽组织生长时间、上皮组织生长时间和二期植皮时间[59-60]。另外,抗生素骨水泥联合皮瓣技术可在有效控制四肢软组织感染的同时重建感染性软组织缺损,使的感染性创面得到一期愈合[61-62]。"

| [1] 赵行琪,余斌,胡岩君.感染性骨缺损局部抗生素载体的临床应用[J].中华创伤骨科杂志,2019,21(2):173-181. [2] SCHMITT DR, KILLEN C, MURPHY M, et al. The Impact of Antibiotic-Loaded Bone Cement on Antibiotic Resistance in Periprosthetic Knee Infections. Clin Orthop Surg. 2020;12(3):318-323. [3] ZIMMERLI W, SENDI P. Orthopaedic biofilm infections. APMIS. 2017; 125(4):353-364. [4] 斯蒂芬·L·凯特,奥利维尔·波伦斯. AO骨感染治疗原则[M].高秋明,译.上海:上海科学技术出版社.2022:3-4 [5] 徐溢明,彭慧明,翁习生.关节外科用骨水泥性能改善研究进展[J].中华骨与关节外科杂志,2020,13(7):592-597. [6] 任有亮.多中心四肢创伤性骨感染致病菌及其耐药性的流行病学研究[D].重庆:重庆医科大学,2020. [7] DALL GF, TSANG SJ, GWYNNE PJ, et al. Unexpected synergistic and antagonistic antibiotic activity against Staphylococcus biofilms. J Antimicrob Chemother. 2018;73(7):1830-1840. [8] YUENYONGVIWAT V, INGVIYA N, PATHABUREE P, et al. Inhibitory effects of vancomycin and fosfomycin on methicillin-resistant Staphylococcus aureus from antibiotic-impregnated articulating cement spacers. Bone Joint Res. 2017;6(3):132-136. [9] BALATO G, ROSCETTO E, VOLLARO A, et al. Bacterial biofilm formation is variably inhibited by different formulations of antibiotic-loaded bone cement in vitro. Knee Surg Sports Traumatol Arthrosc. 2019;27(6): 1943-1952. [10] BERLINER ZP, MO AZ, PORTER DA, et al. In-Hospital Acute Kidney Injury After TKA Revision With Placement of an Antibiotic Cement Spacer. J Arthroplasty. 2018;33(7S):S209-S212. [11] DAGNEAUX L, LIMBERG AK, OSMON DR, et al. Acute Kidney Injury When Treating Periprosthetic Joint Infections After Total Knee Arthroplasties with Antibiotic-Loaded Spacers: Incidence, Risks, and Outcomes. J Bone Joint Surg Am. 2021;103(9):754-760. [12] DAGNEAUX L, LIMBERG AK, OSMON DR, et al. Renal Toxicity Associated With Resection and Spacer Insertion for Chronic Hip PJI. J Arthroplasty. 2021;36(9):3289-3293. [13] COBDEN A, CAMURCU Y, BULUT CS, et al. Audiometric threshold shifts after total knee arthroplasty by using gentamicin-loaded bone cement. Turk J Med Sci. 2019;49(2):514-518. [14] CHIANG V, WONG J, YEUNG H, et al. DRESS syndrome induced by antibiotic-loaded bone cements and a diagnostic algorithm for related delayed-type hypersensitivity reactions. J Allergy Clin Immunol Pract. 2021;9(2):1029-1031. [15] FERREIRA M, RZHEPISHEVSKA O, GRENHO L, et al. Levofloxacin-loaded bone cement delivery system: Highly effective against intracellular bacteria and Staphylococcus aureus biofilms. Int J Pharm. 2017;532(1):241-248. [16] EICK S, HOFPETER K, SCULEAN A, et al. Activity of Fosfomycin- and Daptomycin-Containing Bone Cement on Selected Bacterial Species Being Associated with Orthopedic Infections. Biomed Res Int. 2017; 2017:2318174. [17] KILINC S, TUNC T, PAZARCI O, et al. Research into biocompatibility and cytotoxicity of daptomycin, gentamicin, vancomycin and teicoplanin antibiotics at common doses added to bone cement. Jt Dis Relat Surg. 2020;31(2):328-334. [18] HASEEB A, AJIT SV, TEH C, et al. Addition of ceftaroline fosamil or vancomycin to PMMA: An in vitro comparison of biomechanical properties and anti-MRSA efficacy. J Orthop Surg (Hong Kong). 2019; 27(2):615510612. [19] MORIMOTO Y, YO H, OHASHI H. Two-stage revision using antifungal-loaded cement beads for the treatment of Candida infection following revision total hip arthroplasty: A case report. J Orthop Sci. 2021;26(3): 505-509. [20] RELVAS-SILVA M, PINHO AR, VITAL L, et al. Azole-resistant Candida albicans Spondylodiscitis After Bariatric Surgery:A Case Report. JBJS Case Connect. 2020;10(3):e1900618. [21] KIM JK, LEE DY, KANG DW, et al. Efficacy of antifungal-impregnated cement spacer against chronic fungal periprosthetic joint infections after total knee arthroplasty. Knee. 2018;25(4):631-637. [22] ATHANS V, VEVE MP, DAVIS SL.Trowels and Tribulations:Review of Antimicrobial-Impregnated Bone Cements in Prosthetic Joint Surgery. Pharmacotherapy. 2017;37(12):1565-1577. [23] 袁虎成,马文鑫,王骞,等.载抗结核药骨水泥的筛选、制备及物理性能测定[J].中华实验外科杂志,2019,36(12):2260-2263. [24] MENSAH LM, LOVE BJ. A meta-analysis of bone cement mediated antibiotic release: Overkill, but a viable approach to eradicate osteomyelitis and other infections tied to open procedures. Mater Sci Eng C Mater Biol Appl. 2021;123:111999. [25] XU YM, PENG HM, FENG B, et al. Progress of antibiotic-loaded bone cement in joint arthroplasty. Chin Med J (Engl). 2020;133(20):2486-2494. [26] SLANE J, GIETMAN B, SQUIRE M. Antibiotic elution from acrylic bone cement loaded with high doses of tobramycin and vancomycin. J Orthop Res. 2018;36(4):1078-1085. [27] GANDOMKARZADEH M, MAHBOUBI A, MOGHIMI HR. Release behavior, mechanical properties, and antibacterial activity of ciprofloxacin-loaded acrylic bone cement: a mechanistic study. Drug Dev Ind Pharm. 2020;46(8):1209-1218. [28] KIM S, BISHOP AR, SQUIRE MW, et al. Mechanical, elution, and antibacterial properties of simplex bone cement loaded with vancomycin. J Mech Behav Biomed Mater. 2020;103:103588. [29] MEEKER DG, COOPER KB, RENARD RL, et al. Comparative Study of Antibiotic Elution Profiles From Alternative Formulations of Polymethylmethacrylate Bone Cement. J Arthroplasty. 2019;34(7): 1458-1461. [30] ATICI T, SAHIN N, CAVUN S, et al. Antibiotic release and antibacterial efficacy in cement spacers and cement beads impregnated with different techniques: In vitro study. Eklem Hastalik Cerrahisi. 2018;29(2):71-78. [31] FREW NM, CANNON T, NICHOL T, et al. Comparison of the elution properties of commercially available gentamicin and bone cement containing vancomycin with ‘home-made’ preparations. Bone Joint J. 2017;99-B(1):73-77. [32] AJIT SV, CHUN HB, HASEEB A, et al. Hand-mixed vancomycin versus commercial tobramycin cement revisited: A study on mechanical and antibacterial properties. J Orthop Surg (Hong Kong). 2019;27(2): 615499904. [33] SUNDBLAD J, NIXON M, JACKSON N, et al. Altering polymerization temperature of antibiotic-laden cement can increase porosity and subsequent antibiotic elution. Int Orthop. 2018;42(11):2627-2632. [34] CYPHERT EL, LEARN GD, MARQUES DW, et al. Antibiotic Refilling, Antimicrobial Activity, and Mechanical Strength of PMMA Bone Cement Composites Critically Depend on the Processing Technique. ACS Biomater Sci Eng. 2020;6(7):4024-4035. [35] CYPHERT EL, LEARN GD, HURLEY SK, et al. An Additive to PMMA Bone Cement Enables Postimplantation Drug Refilling, Broadens Range of Compatible Antibiotics, and Prolongs Antimicrobial Therapy. Adv Healthc Mater. 2018;7(21):e1800812. [36] ISSIN A, KOCKARA N. Simple method for increasing drug elution from polymethylmethacrylate bone cement. Eklem Hastalik Cerrahisi. 2017; 28(2):100-106. [37] CHEN L, TANG Y, ZHAO K, et al. Fabrication of the antibiotic-releasing gelatin/PMMA bone cement. Colloids Surf B Biointerfaces. 2019;183: 110448. [38] SANZ-RUIZ P, CARBO-LASO E, DEL RJ, et al. Microencapsulation of rifampicin: A technique to preserve the mechanical properties of bone cement. J Orthop Res. 2018;36(1):459-466. [39] AL TY, YANG L, JONES SA, et al. LbL-assembled gentamicin delivery system for PMMA bone cements to prolong antimicrobial activity. PLoS One. 2018;13(12):e207753. [40] LETCHMANAN K, SHEN SC, NG WK, et al. Mechanical properties and antibiotic release characteristics of poly(methyl methacrylate)-based bone cement formulated with mesoporous silica nanoparticles. J Mech Behav Biomed Mater. 2017;72:163-170. [41] LIANG ZC, YANG C, DING X, et al. Carboxylic acid-functionalized polycarbonates as bone cement additives for enhanced and sustained release of antibiotics. J Control Release. 2021;329:871-881. [42] AZUARA G, GARCIA-GARCIA J, IBARRA B, et al. Experimental study of the application of a new bone cement loaded with broad spectrum antibiotics for the treatment of bone infection. Rev Esp Cir Ortop Traumatol (Engl Ed). 2019;63(2):95-103. [43] PARRA-RUIZ FJ, GONZALEZ-GOMEZ A, FERNANDEZ-GUTIERREZ M, et al. Development of advanced biantibiotic loaded bone cement spacers for arthroplasty associated infections. Int J Pharm. 2017;522(1-2):11-20. [44] FARHAN-ALANIE MM, BURNAND HG, WHITEHOUSE MR. The effect of antibiotic-loaded bone cement on risk of revision following hip and knee arthroplasty. Bone Joint J. 2021;103-B(1):7-15. [45] JAMESON SS, ASAAD A, DIAMENT M, et al. Antibiotic-loaded bone cement is associated with a lower risk of revision following primary cemented total knee arthroplasty: an analysis of 731,214 cases using National Joint Registry data. Bone Joint J. 2019;101-B(11):1331-1347. [46] BENDICH I, ZHANG N, BARRY JJ, et al. Antibiotic-Laden Bone Cement Use and Revision Risk After Primary Total Knee Arthroplasty in U.S. Veterans. J Bone Joint Surg Am. 2020;102(22):1939-1947. [47] NAMBA RS, PRENTICE HA, PAXTON EW, et al. Commercially Prepared Antibiotic-Loaded Bone Cement and Infection Risk Following Cemented Primary Total Knee Arthroplasty.J Bone Joint Surg Am. 2020; 102(22):1930-1938. [48] LENGUERRAND E, WHITEHOUSE MR, BESWICK AD, et al. Risk factors associated with revision for prosthetic joint infection after hip replacement: a prospective observational cohort study. Lancet Infect Dis. 2018;18(9):1004-1014. [49] KONG L, CAO J, ZHANG Y, et al. Risk factors for periprosthetic joint infection following primary total hip or knee arthroplasty: a meta-analysis. Int Wound J. 2017;14(3):529-536. [50] BLANCO JF, DIAZ A, MELCHOR FR, et al. Risk factors for periprosthetic joint infection after total knee arthroplasty. Arch Orthop Trauma Surg. 2020;140(2):239-245. [51] GRUBHOFER F, IMAM M A, WIESER K, et al. Staged Revision With Antibiotic Spacers for Shoulder Prosthetic Joint Infections Yields High Infection Control. Clin Orthop Relat Res. 2018;476(1):146-152. [52] ORTOLA DJ, FENGA D, MARCELLINO S, et al. Peri-Prosthetic Knee Infection Management: Spacers Loaded with Two or Three Antibiotic Agents. Surg Infect (Larchmt). 2017;18(5):619-624. [53] JIA C, WANG X, YU S, et al. An antibiotic cement-coated locking plate as a temporary fixation for treatment of infected bone defects: a new method of stabilization. J Orthop Surg Res. 2020;15(1):44. [54] WANG X, WANG S, XU J, et al. Antibiotic cement plate composite structure internal fixation after debridement of bone infection. Sci Rep. 2021;11(1):16921. [55] CHO JW, KIM J, CHO WT, et al. Antibiotic coated hinged threaded rods in the treatment of infected nonunions and intramedullary long bone infections. Injury. 2018;49(10):1912-1921. [56] RUPP M, WALTER N, ISMAT A, et al. Polymethyl methacrylate cement coating of intramedullary implants: A new technique for revision surgery with the example of a temporary knee arthrodesis. Video article. Orthopade. 2021;50(9):758-762. [57] BEAUPRE LA, STAMPE K, MASSON E, et al. Health-related quality of life with long-term retention of the PROSthesis of Antibiotic Loaded Acrylic Cement system following infection resolution in low demand patients. J Orthop Surg (Hong Kong). 2017;25(2):613376545. [58] ELMARSAFI T, OLIVER NG, STEINBERG JS, et al. Long-Term Outcomes of Permanent Cement Spacers in the Infected Foot. J Foot Ankle Surg. 2017;56(2):287-290. [59] 张宝成,元玲,蔡贤华,等.抗生素骨水泥联合负压封闭引流术治疗软组织感染[J].中国矫形外科杂志,2020,28(23):2190-2192. [60] 叶远坚,郭子诚,刘沛辰,等.抗生素骨水泥在肢体开放性损伤伴软组织缺损创面治疗中的疗效观察[J].医学理论与实践,2021, 34(4):614-615. [61] 屈增辉,王莎.抗生素骨水泥结合股前外游离皮瓣治疗创伤性胫骨骨髓炎伴皮肤软组织缺损的效果[J].临床医学研究与实践,2021, 6(10):68-70. [62] 杨焕友,王斌,李瑞国,等.皮瓣联合抗生素骨水泥链珠在手部骨与软组织感染创面的应用研究[J].中华手外科杂志,2021,37(3): 177-179. [63] VOLEJNIKOVA A, MELICHERCIK P, NESUTA O, et al. Antimicrobial peptides prevent bacterial biofilm formation on the surface of polymethylmethacrylate bone cement. J Med Microbiol. 2019;68(6): 961-972. [64] SUTEEWONG T, WONGPREECHA J, POLPANICH D, et al. PMMA particles coated with chitosan-silver nanoparticles as a dual antibacterial modifier for natural rubber latex films. Colloids Surf B Biointerfaces. 2019;174:544-552. [65] VALENCIA ZM, MINA HJ, GRANDE TC, et al. Novel Bioactive and Antibacterial Acrylic Bone Cement Nanocomposites Modified with Graphene Oxide and Chitosan. Int J Mol Sci. 2019;20(12):2938. [66] WANG M, SA Y, LI P, et al. A versatile and injectable poly (methyl methacrylate) cement functionalized with quaternized chitosan-glycerophosphate/nanosized hydroxyapatite hydrogels. Mater Sci Eng C Mater Biol Appl. 2018;90:264-272. [67] ZHU W, LIU F, YU B, et al. Preparation of antibacterial acrylic bone cement with methacrylate derived from benzothiazole. J Mech Behav Biomed Mater. 2021;117:104403. [68] MOREJON AL, FERNANDEZ TI, ZAYAS TA, et al. Antibacterial effect of acrylic bone cements loaded with drugs of different action’s mechanism. J Infect Dev Ctries. 2019;13(6):487-495. |
| [1] | Yu Weijie, Liu Aifeng, Chen Jixin, Guo Tianci, Jia Yizhen, Feng Huichuan, Yang Jialin. Advantages and application strategies of machine learning in diagnosis and treatment of lumbar disc herniation [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(9): 1426-1435. |
| [2] | Lin Zeyu, Xu Lin. Research progress in gout-induced bone destruction mechanism [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(8): 1295-1300. |
| [3] | Ma Shuwei, He Sheng, Han Bing, Zhang Liaoyun. Exosomes derived from mesenchymal stem cells in treatment of animals with acute liver failure: a meta-analysis [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(7): 1137-1142. |
| [4] | Zhang Kefan, Shi Hui. Research status and application prospect of cytokine therapy for osteoarthritis [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(6): 961-967. |
| [5] | Xu Rong, Wang Haojie, Geng Mengxiang, Meng Kai, Wang Hui, Zhang Keqin, Zhao Huijing. Research advance in preparation and functional modification of porous polytetrafluoroethylene artificial blood vessels [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(5): 759-765. |
| [6] | Yin Kaiwen, Li Yunfeng. Application of metal-organic frameworks in implant surface modification [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(5): 783-788. |
| [7] | Chen Xiaofang, Zheng Guoshuang, Li Maoyuan, Yu Weiting. Preparation and application of injectable sodium alginate hydrogels [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(5): 789-794. |
| [8] | Liu Chuang, Shan Shuo, Yu Tengbo, Zhou Huan, Yang Lei. Advantages, discomfort and challenges of clinical application of orthopedic hemostatic materials [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(5): 795-803. |
| [9] | Li Jiaqi, Huang Yuanli, Li Yan, Wang Chunren, Han Qianqian. Mechanism and influencing factors in molecular weight degradation of non-cross-linked hyaluronic acid [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(5): 747-752. |
| [10] | Zhang Ming, Wang Bin, Jia Fan, Chen Jie, Tang Wei. Application of brain-computer interface technology based on electroencephalogram in upper limb motor function rehabilitation of stroke patients [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(4): 581-586. |
| [11] | He Yuanjie, Chen Yuheng, Zhao Yongchao, Wang Zhenglong. Progress in epigenetic regulation of vascular smooth muscle cell remodeling in the occurrence and development of aortic aneurysms [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(4): 602-608. |
| [12] | Ma Sicong, Chen Jing, Li Yunqing. Functions and roles of connective tissue growth factor in nervous systems [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(4): 615-620. |
| [13] | Yan Binghan, Li Zhichao, Su Hui, Xue Haipeng, Xu Zhanwang, Tan Guoqing. Mechanisms of traditional Chinese medicine monomers in the treatment of osteoarthritis by targeting autophagy [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(4): 627-632. |
| [14] | Zhi Liang, Wang Yulong, Zhang Qingfang, Hong Yaqing, Ke Meihua, Liu Quanquan, Long Jianjun. Propulsion deficits in hemiplegic gait of stroke patients [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(35): 5709-5715. |
| [15] | Wang Wenchi, Wu Ruiqi, Huang Jierong, Zhu Lifeng, Cui Xianqin, Li Dongzong, Chen Wenhui, Lin Chunting, Cui wei. Molecular mechanism of naringin in prevention and treatment of osteoporosis [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(34): 5528-5535. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||