Chinese Journal of Tissue Engineering Research ›› 2022, Vol. 26 ›› Issue (9): 1452-1458.doi: 10.12307/2022.445
Previous Articles Next Articles
Osteoarthritis and mitochondrial abnormalities
Jin Tao1, Liu Lin2, Zhu Xiaoyan1, Shi Yucong1, Niu Jianxiong1, Zhang Tongtong1, Wu Shujin3, Yang Qingshan2
- 1First Clinical College of Gansu University of Traditional Chinese Medicine, Lanzhou 730000, Gansu Province, China; 2Gansu Provincial People’s Hospital, Lanzhou 730000, Gansu Province, China; 3School of Pharmacy, Lanzhou University, Lanzhou 730000, Gansu Province, China
-
Received:2021-07-17Revised:2021-07-21Accepted:2021-08-12Online:2022-03-28Published:2021-12-10 -
Contact:Yang Qingshan, Associate chief physician, Gansu Provincial People’s Hospital, Lanzhou 730000, Gansu Province, China -
About author:Jin Tao, Master candidate, First Clinical College of Gansu University of Traditional Chinese Medicine, Lanzhou 730000, Gansu Province, China -
Supported by:the National Natural Science Foundation of China, No. 8176090197 (to YQS)
CLC Number:
Cite this article
Jin Tao, Liu Lin, Zhu Xiaoyan, Shi Yucong, Niu Jianxiong, Zhang Tongtong, Wu Shujin, Yang Qingshan. Osteoarthritis and mitochondrial abnormalities[J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1452-1458.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
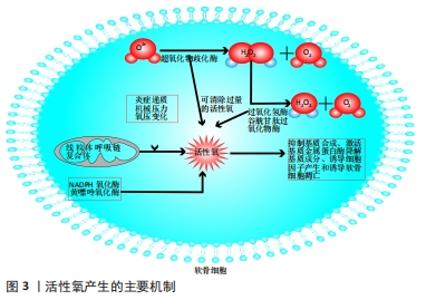
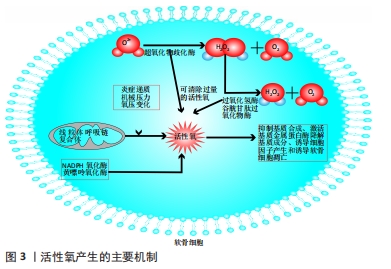
2.2 骨关节炎与线粒体氧化还原 关节软骨是一种通透性有限的无血管的致密组织,在正常生理条件下,其主要通过扩散向软骨细胞提供营养,这些营养主要来自滑液,少数来自软骨下骨髓[3]。因此,关节软骨从表层到深层的氧气和营养梯度呈不对称、递减式,并且受到如细胞密度、软骨厚度、机械负荷、细胞消耗率以及滑液中的营养浓度等诸多因素的影响[4]。在膝关节的软骨中,氧分压的水平与动脉血中的13%相比很低,氧分压从浅层的5%-7%下降到深层的不到1%[4]。在这种极度低氧类似于缺氧的情况下,软骨细胞新陈代谢的速率相对较低,无氧糖酵解便成了软骨细胞的主要能量来源,而线粒体氧化磷酸化产生ATP的量不超过总ATP产量的25%[5-6]。由于氧化磷酸化产生的ATP含量较低以及软骨细胞缓慢的新陈代谢速率,软骨细胞可以借此将氧化造成的损伤降至最低[7]。 关节软骨发生骨关节炎病变时,软骨变薄、出现微裂纹,甚至在骨关节炎中消失,深层的软骨细胞直接暴露在滑液中,而浅层的细胞很容易暴露在软骨下骨产生的各种炎症或趋化因子中。此外,软骨下骨内的微骨折和血管通道的增加可能导致软骨下骨髓中的成分渗漏到软骨中[8]。因此,健康软骨中最初建立的氧张力和分子梯度则完全被改变,在相对较高的有氧环境下,软骨细胞的有氧代谢比率会变得更高,从而产生更多的作为副产品的活性氧[9]。 活性氧是体内一类氧的单电子还原产物,包括超氧阴离子(O2?)、过氧化氢(H2O2)、羟基自由基(OH?)、次氯酸根离子(CLO?)和一氧化氮(NO)。由于未配对电子的存在,活性氧是不稳定且短暂的,通过与蛋白质及脂质等相互作用来实现稳定。活性氧主要经线粒体呼吸链产生,除线粒体途径来源外,NADPH氧化酶及黄嘌呤氧化酶也是其另一重要来源途径。其中,NADPH氧化酶是机体内氧化还原信号的关键调节剂。以往研究结果提示NADPH氧化酶4过表达可能是导致骨关节炎发病的起始原因,因为NADPH氧化酶4表达上调会导致活性氧和基质金属蛋白酶增多[10],可能为骨关节炎治疗重要靶基因。活性氧水平在正常软骨细胞中很低,但在骨关节炎病变时显著升高,较低水平的活性氧有利于维持软骨细胞的稳态,而较高水平的活性氧则可引起线粒体膜去极化,诱导线粒体途径的活性氧生成增多,从而负反馈导致活性氧的持续产生,而线粒体途径活性氧生成增多机制尚不十分清楚,可能与炎症递质、机械压力和氧压变化有关[11]。过量的活性氧可作为第二信使,抑制基质合成、激活基质金属蛋白酶降解基质成分、诱导细胞因子产生和诱导软骨细胞凋亡,进而促进软骨退行性病变[12]。大量活性氧产生,又极易诱导线粒体膜脂质化,造成线粒体功能损伤,而细胞中80%的活性氧都来自线粒体,线粒体结构和功能的完整有助于线粒体固有的活性氧防御系统发挥作用,线粒体功能损伤反过来又诱导大量活性氧产生,从而形成负反馈,导致骨关节炎病变的持续性进展。目前,越来越多的动物实验及临床试验证实减少线粒体中活性氧的生成可有效治疗骨关节炎病变。 除了活性氧的产生增加外,骨关节炎时软骨的线粒体氧化还原失衡也是由于细胞抗氧化系统水平降低所致。抗氧化系统作为一种细胞内机制,有助于消除过量的活性氧。这个抗氧化系统包括酶和非酶类抗氧化剂,如超氧化物歧化酶、过氧化氢酶和谷胱甘肽过氧化物酶。超氧化物歧化酶将O2-转化为H2O2和O2,随之过氧化氢酶和谷胱甘肽过氧化物酶催化H2O2转化为H2O和O2,最终解毒。超氧化物歧化酶有3种同工酶:胞质超氧化物歧化酶、线粒体超氧化物歧化酶和胞外超氧化物歧化酶。当发生骨关节炎时,线粒体超氧化物歧化酶的水平显著下降,从而导致软骨细胞线粒体DNA链断裂和线粒体功能障碍加剧,并显著增强创伤致骨关节炎小鼠模型的软骨退化[13]。活性氧产生的主要机制,见图3。"
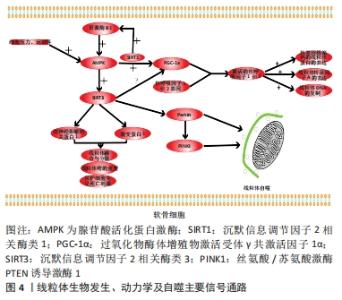
在一项使用10-30个月龄大鼠的软骨老化研究中发现随年龄增加软骨线粒体超氧化物歧化酶蛋白水平升高,但线粒体超氧化物歧化酶活性下降[14]。其活性的下降与沉默信息调节因子2相关酶类3(silent mating type information regulation 2 homolog-3,SIRT3)的减少所导致线粒体超氧化物歧化酶乙酰化的增加有关。与对照组相比,缺少SIRT3的小鼠发生了更严重的与年龄相关的骨关节炎改变,这表明与年龄相关的SIRT3的缺少可能导致了线粒体超氧化物歧化酶乙酰化的增加和线粒体超氧化物歧化酶活性的降低,进而导致了与年龄相关的骨关节炎[14]。另外,将老年软骨细胞与SIRT3及其辅因子NAD+进行孵育后线粒体超氧化物歧化酶活性升高,提示维持老化软骨细胞SIRT3的正常水平可能是维持线粒体超氧化物歧化酶活性的一种治疗策略,可显著缓解与衰老相关的骨关节炎的线粒体功能障碍和氧化还原失衡。 2.3 骨关节炎与线粒体的生物发生 线粒体的生物发生是一个复杂且具有高度可塑性的生理过程,对维持线粒体代谢和适应性反应至关重要。在这一过程中线粒体前体在核DNA和线粒体DNA的协同调控下生长分化形成新的线粒体[15]。线粒体的生物发生这一过程对各种刺激(如能量需求、生长信号和微环境变化)均能作出反应,并参与不同病理过程的调节,如肝细胞毒性、肿瘤的发生和神经变性[15]。线粒体的生物发生受到多种信号分子的调控,如腺苷酸活化蛋白激酶(adenosine 5′-monophosphate -activated protein kinase,AMPK)、SIRT、线粒体转录因子A、核呼吸因子1和2以及过氧化物酶体增殖物激活受体γ共激活因子1α(peroxlsome proliferator-activated receptor-γ coactlvator-1α,PGC-1α)。最近的研究表明,骨关节炎时软骨细胞线粒体缺乏生物合成,这种缺陷促进了软骨细胞的前分解代谢反应[15]。线粒体生物发生的减少与AMPK活性降低、PGC-1α、线粒体转录因子A及核呼吸因子1和2表达的减少密切相关,见图4。"
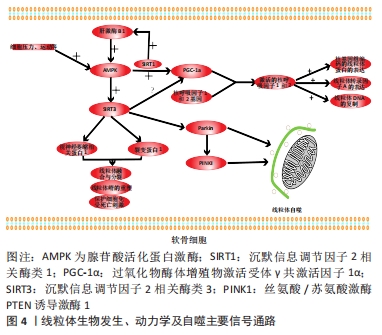
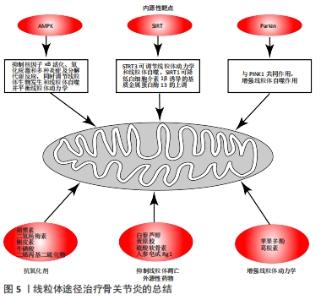
AMPK是一种高度保守的代谢调节蛋白,在细胞和生理水平上维持代谢过程中能量的动态平衡,该蛋白在不同类型的细胞中表达,并可被各种刺激如细胞压力、运动和许多影响细胞新陈代谢的物质激活。在软骨细胞内PGC-1α是 AMPKα1的下游靶分子,AMPKα1通过SIRT1简接激活PGC-1α,同时激活的SIRT1使肝激酶B1去乙酰化,进而激活肝激酶B1活性,肝激酶B1又激活AMPKα1,这样在软骨细胞内AMPKα1与SIRT1形成正反馈通路[16],一旦该通路被抑制,从而加速软骨细胞线粒体功能障碍,促进骨关节炎发生发展。 PGC-1α是一种与核呼吸因子转录共激活的因子,在软骨细胞中,PGC-1α直接与核呼吸因子基因结合并激活其转录活性。激活的核呼吸因子可以促进核基因组编码的线粒体蛋白和线粒体转录因子A的表达,从而促进线粒体DNA的复制,维持线粒体DNA的完整性和稳定性,并刺激线粒体DNA损伤的修复[17-18]。因此PGC-1α介导的AMPK活性在在阻断软骨细胞的分解代谢反应和抑制氧化应激方面是必不可少的。骨关节炎时软骨细胞线粒体的生物合成受损和PGC-1α表达的降低是可以通过在药理学上激活AMPK-PGC-1α通路完成逆转的[19],因此这是一种治疗骨关节炎的潜在策略。 在人软骨细胞中,SIRT3可以被AMPK激活,并且在降低线粒体DNA4977的减少和维持线粒体DNA的完整性和功能方面发挥作用,这表明SIRT3也参与了线粒体的生物发生。然而,SIRT3对软骨细胞PGC-1α的调控作用及其机制尚未得到证实。据报道,敲除SIRT3基因后降低了乳腺癌细胞中PGC1 miRNA和线粒体转录因子A的表达,最终抑制了线粒体的生物生成[20]。还有研究表明SIRT3-PGC-1α轴可以调节心肌细胞线粒体功能[21]。在其他细胞中的这些结果表明,SIRT3-PGC-1α轴可能也是软骨细胞线粒体生物发生的重要调控机制,但这一假说还需要进一步证实。 2.4 骨关节炎与线粒体动力学 线粒体动力学是指当环境刺激细胞时,线粒体可以通过控制融合及分裂的形态变化的过程来响应代谢变化。这些过程可以促进不同线粒体之间的内容和信号交换,促进线粒体DNA损伤的修复和线粒体活力的恢复,提高ATP合成效率,分配钙、ATP和活性氧以满足细胞的需求,并帮助细胞克服代谢和微环境造成的压力。线粒体融合包括外膜融合和内膜融合,外膜融合主要由线粒体融合蛋白1和2调节,而内膜融合主要由视神经萎缩相关蛋白1和线粒体融合蛋白1介导[22]。线粒体分裂主要由动力蛋白1、裂变蛋白1和动力蛋白2介导,这一过程可以增加线粒体数量,减少受损线粒体的细胞负荷并包裹受损分子和代谢废物,促进受损线粒体与母体线粒体的分离,从而导致前者的随后消除。 线粒体动力学对于调节线粒体功能和细胞内稳态是必不可少的。当软骨细胞发生骨关节炎病变时,若线粒体分裂在软骨细胞中变得越来越占优势,受损的线粒体会积累并经历有丝分裂。由于这些变化,线粒体不能产生足够的生物能量,调节钙并维持氧化还原状态[23]。相反,若线粒体融合占优势时可以增强线粒体的生物学功能,使软骨细胞充满活力并抑制细胞凋亡。视神经萎缩相关蛋白1是一种位于线粒体内膜中具有GTP酶活性的乙酰化蛋白,是参与线粒体动力学调节的关键蛋白之一,在线粒体融合与分裂、嵴的重塑以及保护细胞免受死亡刺激方面发挥重要作用。SIRT是一种高度保守的第三类脱乙酰酶,大多数SIRT家族成员都具有NAD+依赖的去乙酰化酶的活性。据报道,位于线粒体中的SIRT3通过发挥其去乙酰化的功能参与软骨细胞线粒体动力学的调节及骨关节炎的发生[24]。视神经萎缩相关蛋白1是SIRT3的直接靶标,SIRT3去乙酰化并激活视神经萎缩相关蛋白1会导致线粒体动力学的显著改善。此外,一项研究表明,裂变蛋白1的缺少会损害软骨细胞的溶酶体和过氧化物酶体功能[25]。在最近进行的一项研究中发现SIRT3可通过c-Jun氨基末端激酶信号通路上调裂变蛋白1的表达[26]。因此,以SIRT3为靶基因的药物可能是通过线粒体途径治疗骨关节炎的潜在方法。 此外,线粒体融合与分裂都与细胞凋亡有关。例如,线粒体分裂分子的过度表达如动力蛋白1或裂变蛋白1可诱导细胞凋亡,而抑制动力蛋白1或裂变蛋白1的表达可诱导产生一种阻碍细胞凋亡的效应。与此一致的是,减少线粒体融合蛋白的表达如线粒体融合蛋白1和2或视神经萎缩相关蛋白1,已被证明有助于细胞凋亡[27]。最近越来越多的证据表明,线粒体动力学的改变对多种疾病的炎症有很大影响,因此从线粒体动力学方面入手治疗骨关节炎是一种潜在的策略。 2.5 骨关节炎与线粒体有丝分裂 自噬是指细胞清除受损的细胞器和大分子,这一过程由分解代谢和能量压力来激活。有丝分裂是指细胞通过自噬机制选择性地分离和降解受损或功能失调的线粒体,然后合成新的线粒体成分然后将其插入剩余功能的线粒体的过程。有丝分裂这一过程对维持线粒体的动态平衡及促进细胞的存活方面有着重要的作用。 最近的报道表明自噬的活性随着年龄的增长而降低,骨关节炎的病理过程中存在与衰老相关的软骨细胞自噬功能丧失,进而导致显著的线粒体功能障碍[28]。此外,自噬的激活对保护软骨细胞有影响,这表明有丝分裂消除了受损的线粒体,这在防止氧化应激方面发挥了关键作用。还有研究表明,自噬和有丝分裂吞噬相关蛋白如自噬微管相关蛋白轻链3B和丝氨酸/苏氨酸激酶PTEN诱导激酶1(PTEN induced putative kinase 1,PINK1)在骨关节炎患者及啮齿类骨关节炎模型的软骨中高度表达,这表明有丝分裂和骨关节炎之间有很强的联系[29]。Parkin蛋白是一种细胞质E3泛素连接酶,可对线粒体膜电位的缺失做出反应,然后选择性地招募功能障碍的线粒体,其通过与PINK1的相互作用介导了吞噬过程并通过自噬小体消除标记的线粒体[30]。因此,Parkin的迁移和激活是移除受损和功能障碍线粒体的重要机制,在这些过程中的任何一个过程的异常都可能导致受损线粒体的积累。最近有研究表明,Parkin介导的对受损线粒体的清除限制了活性氧的产生并增加了骨关节炎软骨细胞的细胞存活率[31]。在ANSARI等[31]的研究中,Parkin介导的有丝分裂是在病理条件下限制软骨细胞产生活性氧以及提高骨关节炎软骨细胞生存能力的重要机制。然而,在SHIN等[32]的研究中发现PINK1/Parkin介导的有丝分裂导致了骨关节炎软骨细胞死亡;同时,在骨关节炎患者中,PINK1的表达不足与软骨的损伤和疼痛行为的减少有相关性。有丝分裂对软骨细胞的存活及功能的副作用可能与特定阶段的有丝分裂水平、软骨细胞的来源以及骨关节炎的分期和模型有关,这一方面值得进一步研究。 另外有研究表明,SIRT3介导了依赖于PINK1/Parkin通路的原代软骨细胞的有丝分裂,而二甲双胍正是通过增强SIRT3/PINK1/Parkin的信号通路从而抑制白细胞介素1β所诱导的线粒体损伤及骨关节炎样炎症改变进而来保护软骨细胞免受氧化应激的伤害[33]。植物同源结构域指蛋白23是一种在人骨关节炎软骨和滑膜中过表达的并通过促进E3连接酶降解的新型自噬抑制剂。在一项研究中表明,敲除植物同源结构域指蛋白23可以增加自噬及Ⅱ型胶原的表达并减少与骨关节炎相关蛋白的表达,从而防止白细胞介素1β诱导的骨关节炎的软骨细胞凋亡的发生,这可能使PHF23成为骨关节炎治疗的潜在靶基因[34]。 2.6 骨关节炎与线粒体遗传学 线粒体是一种独特的细胞器,它们有自己的母体遗传DNA即线粒体DNA,其中包含2个rRNA、22个tRNA和13个必需的线粒体蛋白编码基因。线粒体DNA是一个16 569 bp的环状和双链分子,该分子的突变率高于核DNA的突变率,这主要由于其接近活性氧产生的主要来源、缺乏有效的修复系统及复制率更高[35]。当人类移出非洲并使机体的能量代谢能够适应不同环境时,线粒体DNA序列通过沿辐射母系的顺序积累功能性的突变而进化,从而产生了线粒体DNA单倍群[36]。 现已证明线粒体DNA单倍群影响了骨关节炎的许多方面,如骨关节炎的发病率、患病率及进展。一项为期8年的临床研究显示,线粒体DNA单倍群J与膝关节骨关节炎的发病率相关率较低[37]。另一项研究表明,在西班牙和英国人群中线粒体DNA单倍群J和T分别降低了膝关节骨关节炎的风险[38]。此外,在一项来自中国人群的研究中线粒体DNA单倍群B似乎是膝关节骨关节炎的保护因素[39]。这些单倍群的保护作用可能是由于线粒体呼吸和糖酵解减少、自由基和促炎细胞因子(如白细胞介素33,白细胞介素6和重组人转化生长因子2)产生减少、细胞凋亡程度降低以及线粒体相关促凋亡基因Bcl-2结合元件3表达减少所致[38]。 不同的线粒体DNA单倍群的分子机制如耗氧量、ATP及活性氧的产生都会影响骨关节炎。由于这些影响,这些单倍群可能是骨关节炎诊断和预后的生物标志物且与骨关节炎的表型密切相关[40]。 因此,能够模仿线粒体DNA单倍群J的生理效应的药物可能是治疗骨关节炎的潜在策略。由于每个单倍群的反应方式都各自不同,因此需要对每个单倍群的分子机制进行精确识别,最终才能利用单倍群作为预测骨关节炎的手段。 2.7 骨关节炎时线粒体钙的调节 钙是细胞内普遍存在的第二信使并参与许多细胞过程。钙过量会导致活性氧过度产生、线粒体去极化及线粒体膜电位降低[41]。线粒体是细胞内主要的钙库之一,对维持细胞内钙的稳态极为重要。一些研究表明软骨细胞的线粒体具有转运钙的能力,对细胞外基质的钙化非常重要,这在基质小泡中已经得到证实[42]。线粒体钙的运动还诱导环氧合酶2表达和前列腺素E2产生的增加,从而导致促炎细胞因子的产生增加,如白细胞介素1β、白细胞介素33、白细胞介素8、肿瘤坏死因子α、核因子κB、环氧合酶2、前列腺素E2和基质金属蛋白酶,进而导致骨关节炎的发生。此外,细胞内钙稳态的改变是导致caspase-9激活的主要上游因素,活化的caspase-9可以通过激活caspase-3和caspase-7等执行者而导致软骨细胞的凋亡。因此,维持软骨细胞内线粒体钙的稳态代表了一种治疗骨关节炎的新策略。 2.8 通过线粒体途径治疗骨关节炎的总结 见图5。"
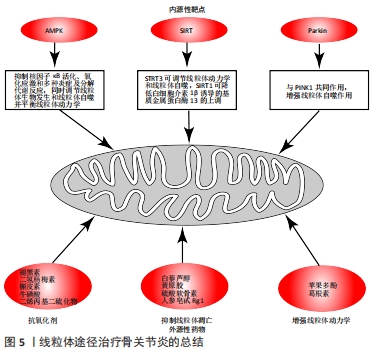

2.8.1 内源性分子靶点恢复线粒体功能 (1)AMPK:AMPK是细胞是适应能量需求变化的关键调控因子,AMPK调控异常与多种与线粒体功能障碍及细胞能量失衡相关疾病有关,如糖尿病、动脉粥样硬化、心血管疾病、癌症、神经退行性疾病和骨关节炎[43-44]。 在软骨细胞中,激活的AMPK可抑制核因子κB活化、氧化应激和多种炎症及分解代谢反应[44]。此外,AMPK也可以调节线粒体生物发生和线粒体吞噬,平衡线粒体动力学,这提示能够激活AMPK活性的药物具有限制骨关节炎进展的能力。 (2)SIRT:SIRT是高度保守的第三类脱乙酰酶,大多数SIRT家族成员都具有NAD+依赖的蛋白脱乙酰酶活性。SIRT家族由7个成员(SIRT1-SIRT7)组成,分布于整个细胞。SIRT1和STRT3是AMPK的下游活性物质,而STRT3是线粒体中主要的去乙酰化酶,激活的STRT3可以通过调节线粒体动力学和线粒体噬细胞来保护细胞。越来越多的证据表明SIRT1的活性对软骨稳态及软骨细胞线粒体自噬方面极其重要的[45-46]。若软骨细胞中SIRT1缺少会导致基质金属蛋白酶13、凋亡标志物和核因子κB的增加,从而加速骨关节炎的发展[47]。而上调SIRT1可以抑制环氧合酶2、基质金属蛋白酶13和核因子κB诱导的肿瘤坏死因子α的激活,并降低白细胞介素1β诱导的基质金属蛋白酶13的上调。因此,能够上调SIRT1或STRT3的药物可能是通过线粒体途径治疗骨关节炎的潜在方法。 (3)Parkin:在许多退行性疾病的发病机制中自噬与细胞凋亡密切相关,有研究表明自噬在骨关节炎病变中的软骨细胞中被抑制[48]。Parkin蛋白是一种细胞质E3泛素连接酶,其与PINK1共同作用,PINK1使Parkin磷酸化,使其转化为活性的磷酸化泛素非依赖性E3连接酶从而清除受损的线粒体。因此,能够介导Parkin对受损线粒体清除的药物也可能是治疗骨关节炎的潜在方法。 2.8.2 外源性药物优化线粒体功能 (1)抗氧化剂:①褪黑素:褪黑素(N-乙酰基-5-甲氧基色胺)是哺乳动物的松果体产生的一种胺激素,是一种广谱抗氧化剂和自由基清除剂[49]。褪黑素及其代谢产物可通过自由基清除作用清除活性氧并改善抗氧化酶的活性,从而调节细胞炎症、增殖、凋亡[50]。②二氢杨梅素:主要由类黄酮组成,可清除自由基并具有抗炎和抗氧化作用。其可以通过AMPK/SIRT3/PGC-1α信号通路激活SIRT3,并增强线粒体融合,维持线粒体功能和软骨细胞的稳态,提高软骨细胞的抗氧化能力及提高软骨聚集蛋白聚糖和Ⅱ型胶原的水平[51]。③槲皮素:是一种类黄酮化合物,广泛存在于蔬菜和水果中,并具有抗氧化性能。研究表明槲皮素可以用于治疗骨关节炎大鼠,并证明槲皮素可以逆转线粒体功能障碍,改善线粒体膜电位、耗氧量和ATP的产生。槲皮素通过诱导谷胱甘肽和谷胱甘肽过氧化物酶消除了过量的活性氧,从而减少甚至消除了氧化应激[52]。④牛磺酸:牛磺酸(2-氨基乙烷磺酸)是另一种在减弱自由基毒性方面非常有效的抗氧化剂,其可以改善活性氧引起的软骨细胞损伤并发挥软骨保护特性[53]。⑤二烯丙基二硫化物:是大蒜的主要成分,具有抗氧化和抗炎性质,可降低促炎性细胞因子的表达如肿瘤坏死因子α、白细胞介素1β等[54]。 (2)抑制线粒体凋亡途径:①白藜芦醇:是一种具有抗炎和抗氧化特性的非类黄酮多酚化合物,主要来源于葡萄叶、葡萄皮和各种水果。其可以通过核因子κB信号通路减轻白细胞介素1β诱导的软骨细胞凋亡[55]。②黄原胶:是由野油菜黄单胞杆菌以碳水化合物为主要原料经发酵工程生产的一种作用广泛的微生物胞外多糖。低分子量的黄原胶已用于兔骨关节炎治疗,其可以通过调节与Bcl-2相关的X蛋白/线粒体细胞色素C/Caspase信号通路抑制软骨细胞凋亡,并保护软骨细胞免于变性[56]。③硫酸软骨素:是一种从动物和鱼类的软骨中提取的糖胺聚糖,是细胞外基质的重要组成部分[57]。 一项研究表明,鲤鱼硫酸软骨素可减少线粒体裂变从而增加线粒体膜电位并抑制Caspase-3和Caspase-9的水平,进而减少软骨细胞的凋亡[58]。④人参皂甙Rg1:是人参中活性最高的成分之一。研究证明,人参皂苷Rg1可以通过增强磷脂酰肌醇3来增强Bcl-2的表达,促进基质金属蛋白酶1组织抑制剂的表达,从而抑制基质金属蛋白酶13的合成并抑制细胞色素C从线粒体释放到细胞质中[59]。 (3)增强线粒体动力学:①苹果多酚:是苹果中所含多元酚类物质的通称。研究表明苹果多酚可通过AMPK/SIRT1/PGC-1α信号通路促进线粒体DNA的完整性和线粒体融合,从而增强线粒体动力学[60]。②葛根素:是一种从中药葛根中分离得到的异黄酮衍生物,具有抗氧化、抗炎、抗癌和血管舒张作用。其可通过上调AMPK/PGC-1α活性来增加线粒体的生物发生并恢复线粒体的功能,从而减轻线粒体功能障碍和对软骨细胞的损害[61]。"

| [1] SACITHARAN PK. Ageing and Osteoarthritis. Subcell Biochem. 2019;91:123-159. [2] BLANCO FJ, REGO I, RUIZ-ROMERO C. The role of mitochondria in osteoarthritis. Nat Rev Rheumatol. 2011;7(3):161-169. [3] WANG Y, WEI L, ZENG L, et al. Nutrition and degeneration of articular cartilage. Knee Surg Sports Traumatol Arthrosc. 2013;21(8):1751-1762. [4] BEEKHUIZEN M, BASTIAANSEN-JENNISKENS YM, KOEVOET W, et al. Osteoarthritic synovial tissue inhibition of proteoglycan production in human osteoarthritic knee cartilage: establishment and characterization of a long-term cartilage-synovium coculture. Arthritis Rheum. 2011;63(7):1918-1927. [5] MORELLI AM, RAVERA S, PANFOLI I. The aerobic mitochondrial ATP synthesis from a comprehensive point of view. Open Biol. 2020;10(10):200224. [6] ZHENG L, ZHANG Z, SHENG P, et al. The role of metabolism in chondrocyte dysfunction and the progression of osteoarthritis. Ageing Res Rev. 2021;66: 101249. [7] LANE RS, FU Y, MATSUZAKI S, et al.Mitochondrial respiration and redox coupling in articular chondrocytes. Arthritis Res Ther. 2015;17(1):54. [8] AIZAH N, CHONG PP, KAMARUL T. Early Alterations of Subchondral Bone in the Rat Anterior Cruciate Ligament Transection Model of Osteoarthritis. Cartilage. 2019:1947603519878479. [9] LEPETSOS P, PAPAVASSILIOU AG. Ros/oxidative stress signaling in osteoarthritis. Biochim Biophys Acta. 2016;1862(4):576-591. [10] TEIXEIRA G, SZYNDRALEWIEZ C, MOLANGO S, et al. Therapeutic potential of NADPH oxidase 1/4 inhibitors. Br J Pharmacol. 2017;174(12):1647-1669. [11] REED KN, WILSON G, PEARSALL A, et al. The role of mitochondrial reactive oxygen species in cartilage matrix destruction. Mol Cell Biochem. 2014;397(1-2):195-201. [12] OHASHI Y, TAKAHASHI N, TERABE K, et al. Metabolic reprogramming in chondrocytes to promote mitochondrial respiration reduces downstream features of osteoarthritis. Sci Rep. 2021;11(1):15131. [13] KOIKE M, NOJIRI H, OZAWA Y,et al.Mechanical overloading causes mitochondrial superoxide and SOD2 imbalance in chondrocytes resulting in cartilage degeneration. Sci Rep. 2015;25(5):11722. [14] FU Y, KINTER M, HUDSON J, et al Aging Promotes Sirtuin 3-Dependent Cartilage Superoxide Dismutase 2 Acetylation and Osteoarthritis. Arthritis Rheumatol. 2016;68(8):1887-1898. [15] WANG Y, ZHAO X, LOTZ M, et al. Mitochondrial biogenesis is impaired in osteoarthritis chondrocytes but reversible via peroxisome proliferator-activated receptor γ coactivator 1α. Arthritis Rheumatol. 2015;67(8):2141-2153. [16] LIU Z, ZHANG H, WANG H, et al. Magnolol Alleviates IL-1β-Induced Dysfunction of Chondrocytes Through Repression of SIRT1/AMPK/PGC-1α Signaling Pathway. J Interferon Cytokine Res. 2020;40(3):145-151. [17] PICCA A, MANKOWSKI RT, BURMAN JL, et al. Mitochondrial quality control mechanisms as molecular targets in cardiac ageing. Nat Rev Cardiol. 2018;15(9): 543-554. [18] WANG Y, CHEN LY, LIU-BRYAN R. Mitochondrial Biogenesis, Activity, and DNA Isolation in Chondrocytes. Methods Mol Biol. 2021;2245:195-213. [19] ANDREUX PA, HOUTKOOPER RH, AUWERX J. Pharmacological approaches to restore mitochondrial function. Nat Rev Drug Discov. 2013;12(6):465-483. [20] CHEN LY, WANG Y, TERKELTAUB R,et al. Activation of AMPK-SIRT3 signaling is chondroprotective by preserving mitochondrial DNA integrity and function. Osteoarthritis Cartilage. 2018;26(11):1539-1550. [21] TORRENS-MAS M, PONS DG, SASTRE-SERRA J, et al. SIRT3 Silencing Sensitizes Breast Cancer Cells to Cytotoxic Treatments Through an Increment in ros Production. J Cell Biochem. 2017;118(2):397-406. [22] YANG F, LI B, YANG Y, et al. Leptin enhances glycolysis via OPA1-mediated mitochondrial fusion to promote mesenchymal stem cell survival. Int J Mol Med. 2019;44(1):301-312. [23] BLANCO FJ, FERNÁNDEZ-MORENO M. Mitochondrial biogenesis: a potential therapeutic target for osteoarthritis. Osteoarthritis Cartilage. 2020;28(8):1003-1006. [24] WANG FS, KUO CW, KO JY, et al. Irisin Mitigates Oxidative Stress, Chondrocyte Dysfunction and Osteoarthritis Development through Regulating Mitochondrial Integrity and Autophagy. Antioxidants (Basel). 2020;9(9):810. [25] KIM D, SONG J, KANG Y, et al. Fis1 depletion in osteoarthritis impairs chondrocyte survival and peroxisomal and lysosomal function. J Mol Med (Berl). 2016;94(12): 1373-1384. [26] ZHOU J, SHI M, LI M, et al. Sirtuin 3 inhibition induces mitochondrial stress in tongue cancer by targeting mitochondrial fission and the JNK-Fis1 biological axis. Cell Stress Chaperones. 2019;24(2):369-383. [27] PARK J, CHOI H, MIN JS, et al. Mitochondrial dynamics modulate the expression of pro-inflammatory mediators in microglial cells. J Neurochem. 2013;127(2):221-232. [28] LÓPEZ DE FIGUEROA P, LOTZ MK, BLANCO FJ, et al. Autophagy activation and protection from mitochondrial dysfunction in human chondrocytes. Arthritis Rheumatol. 2015;67(4):966-976. [29] WANG S, DENG Z, MA Y, et al. The Role of Autophagy and Mitophagy in Bone Metabolic Disorders. Int J Biol Sci. 2020;16(14):2675-2691. [30] ANSARI MY, HAQQI TM. Assessing Chondrocyte Status by Immunofluorescence-Mediated Localization of Parkin Relative to Mitochondria. Methods Mol Biol. 2021;2245:215-224. [31] ANSARI MY, KHAN NM, AHMAD I, et al. Parkin clearance of dysfunctional mitochondria regulates ros levels and increases survival of human chondrocytes. Osteoarthritis Cartilage. 2018;26(8):1087-1097. [32] SHIN HJ, PARK H, SHIN N, et al. Pink1-Mediated Chondrocytic Mitophagy Contributes to Cartilage Degeneration in Osteoarthritis. J Clin Med. 2019;8(11): 1849. [33] WANG C, YANG Y, ZHANG Y, et al. Protective effects of metformin against osteoarthritis through upregulation of SIRT3-mediated PINK1/Parkin-dependent mitophagy in primary chondrocytes. Biosci Trends. 2019;12(6):605-612. [34] MAIMAITIJUMA T, YU JH, REN YL, et al. PHF23 negatively regulates the autophagy of chondrocytes in osteoarthritis. Life Sci. 2020;253:117750. [35] LI H, SLONE J, FEI L, et al. Mitochondrial DNA Variants and Common Diseases: A Mathematical Model for the Diversity of Age-Related mtDNA Mutations. Cells. 2019;8(6):608. [36] WALLACE DC. Genetics: Mitochondrial DNA in evolution and disease. Nature. 2016;535(7613):498-500. [37] FERNÁNDEZ-MORENO M, SOTO-HERMIDA A, VÁZQUEZ-MOSQUERA ME, et al. Mitochondrial DNA haplogroups influence the risk of incident knee osteoarthritis in oaI and CHECK cohorts. A meta-analysis and functional study. Ann Rheum Dis. 2017;76(6):1114-1122. [38] SOTO-HERMIDA A, FERNÁNDEZ-MORENO M, OREIRO N, et al. mtDNA haplogroups and osteoarthritis in different geographic populations. Mitochondrion. 2014;15:18-23. [39] FANG H, LIU X, SHEN L, et al. Role of mtDNA haplogroups in the prevalence of knee osteoarthritis in a southern Chinese population. Int J Mol Sci. 2014;15(2): 2646-2659. [40] REGO-PÉREZ I, BLANCO FJ, ROEMER FW, et al. Mitochondrial DNA haplogroups associated with MRI-detected structural damage in early knee osteoarthritis. Osteoarthritis Cartilage. 2018;26(11):1562-1569. [41] YIN S, ZHANG L, DING L, et al. Transient receptor potential ankyrin 1 (trpa1) mediates il-1β-induced apoptosis in rat chondrocytes via calcium overload and mitochondrial dysfunction. J Inflamm (Lond). 2018;15:27. [42] NASI S, CASTELBLANCO M, CHOBAZ V, et al. Xanthine Oxidoreductase Is Involved in Chondrocyte Mineralization and Expressed in Osteoarthritic Damaged Cartilage. Front Cell Dev Biol. 2021;9:612440. [43] TERKELTAUB R, YANG B, LOTZ M, et al. Chondrocyte AMP-activated protein kinase activity suppresses matrix degradation responses to proinflammatory cytokines interleukin-1β and tumor necrosis factor α. Arthritis Rheum. 2011;63(7): 1928-1937. [44] PETURSSON F, HUSA M, JUNE R, et al. Linked decreases in liver kinase B1 and AMP-activated protein kinase activity modulate matrix catabolic responses to biomechanical injury in chondrocytes. Arthritis Res Ther. 2013;15(4):R77. [45] SCOTT JL, GABRIELIDES C, DAVIDSON RK, et al. Superoxide dismutase downregulation in osteoarthritis progression and end-stage disease. Ann Rheum Dis. 2010;69(8):1502-1510. [46] GAVRIILIDIS C, MIWA S, VON ZGLINICKI T, et al. Mitochondrial dysfunction in osteoarthritis is associated with down-regulation of superoxide dismutase 2. Arthritis Rheum. 2013;65(2):378-387. [47] MA CH, CHIUA YC, WU CH, et al. Homocysteine causes dysfunction of chondrocytes and oxidative stress through repression of SIRT1/AMPK pathway: A possible link between hyperhomocysteinemia and osteoarthritis. Redox Biol. 2018;15:504-512. [48] CETRULLO S, D’ADAMO S, GUIDOTTI S, et al. Hydroxytyrosol prevents chondrocyte death under oxidative stress by inducing autophagy through sirtuin 1-dependent and -independent mechanisms. Biochim Biophys Acta. 2016;1860(6):1181-1191. [49] HOSSEINZADEH A, KAMRAVA SK, JOGHATAEI MT, et al. Apoptosis signaling pathways in osteoarthritis and possible protective role of melatonin. J Pineal Res. 2016;61(4):411-425. [50] BORIN TF, ARBAB AS, GELALETI GB, et al. Melatonin decreases breast cancer metastasis by modulating Rho-associated kinase protein-1 expression. J Pineal Res. 2016;60(1):3-15. [51] WANG J, WANG K, HUANG C, et al. SIRT3 Activation by Dihydromyricetin Suppresses Chondrocytes Degeneration via Maintaining Mitochondrial Homeostasis. Int J Biol Sci. 2018;14(13):1873-1882. [52] QIU L, LUO Y, CHEN X. Quercetin attenuates mitochondrial dysfunction and biogenesis via upregulated AMPK/SIRT1 signaling pathway in oa rats. Biomed Pharmacother. 2018;103:1585-1591. [53] LIU C, CAO Y, YANG X, et al. Tauroursodeoxycholic acid suppresses endoplasmic reticulum stress in the chondrocytes of patients with osteoarthritis. Int J Mol Med. 2015;36(4):1081-1087. [54] SAUD SM, LI W, GRAY Z, et al. Diallyl Disulfide (DADS), a Constituent of Garlic, Inactivates NF-κB and Prevents Colitis-Induced Colorectal Cancer by Inhibiting GSK-3β. Cancer Prev Res (Phila). 2016;9(7):607-615. [55] YI H, ZHANG W, CUI ZM, et al. Resveratrol alleviates the interleukin-1β-induced chondrocytes injury through the NF-κB signaling pathway. J Orthop Surg Res. 2020;15(1):424. [56] SHAO X, CHEN Q, DOU X, et al. Lower range of molecular weight of xanthan gum inhibits cartilage matrix destruction via intrinsic bax-mitochondria cytochrome c-caspase pathway. Carbohydr Polym. 2018;98:354-363. [57] SUN Y, ZHANG G, LIU Q, et al. Chondroitin sulfate from sturgeon bone ameliorates pain of osteoarthritis induced by monosodium iodoacetate in rats. Int J Biol Macromol. 2018;117:95-101. [58] LIU Q, WANG J, SUN Y, et al. Chondroitin sulfate from sturgeon bone protects chondrocytes via inhibiting apoptosis in osteoarthritis. Int J Biol Macromol. 2019; 134:1113-1119. [59] HUANG Y, WU D, FAN W. Protection of ginsenoside Rg1 on chondrocyte from IL-1β-induced mitochondria-activated apoptosis through PI3K/Akt signaling. Mol Cell Biochem. 2014;392(1-2):249-257. [60] MASUDA I, KOIKE M, NAKASHIMA S, et al. Apple procyanidins promote mitochondrial biogenesis and proteoglycan biosynthesis in chondrocytes. Sci Rep. 2018;8(1):7229. [61] WANG L, SHAN H, WANG B, et al. Puerarin Attenuates Osteoarthritis via Upregulating AMP-Activated Protein Kinase/Proliferator-Activated Receptor-γ Coactivator-1 Signaling Pathway in Osteoarthritis Rats. Pharmacology. 2018; 102(3-4):117-125. |
| [1] | Zhang Jichao, Dong Yuefu, Mou Zhifang, Zhang Zhen, Li Bingyan, Xu Xiangjun, Li Jiayi, Ren Meng, Dong Wanpeng. Finite element analysis of biomechanical changes in the osteoarthritis knee joint in different gait flexion angles [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1357-1361. |
| [2] | Wang Baojuan, Zheng Shuguang, Zhang Qi, Li Tianyang. Miao medicine fumigation can delay extracellular matrix destruction in a rabbit model of knee osteoarthritis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1180-1186. |
| [3] | Liu Dongcheng, Zhao Jijun, Zhou Zihong, Wu Zhaofeng, Yu Yinghao, Chen Yuhao, Feng Dehong. Comparison of different reference methods for force line correction in open wedge high tibial osteotomy [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(6): 827-831. |
| [4] | Zhou Jianguo, Liu Shiwei, Yuan Changhong, Bi Shengrong, Yang Guoping, Hu Weiquan, Liu Hui, Qian Rui. Total knee arthroplasty with posterior cruciate ligament retaining prosthesis in the treatment of knee osteoarthritis with knee valgus deformity [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(6): 892-897. |
| [5] | He Junjun, Huang Zeling, Hong Zhenqiang. Interventional effect of Yanghe Decoction on synovial inflammation in a rabbit model of early knee osteoarthritis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(5): 694-699. |
| [6] | Lin Xuchen, Zhu Hainian, Wang Zengshun, Qi Tengmin, Liu Limin, Suonan Angxiu. Effect of xanthohumol on inflammatory factors and articular cartilage in a mouse mode of osteoarthritis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(5): 676-681. |
| [7] | Xu Lei, Han Xiaoqiang, Zhang Jintao, Sun Haibiao. Hyaluronic acid around articular chondrocytes: production, transformation and function characteristics [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(5): 768-773. |
| [8] | Zhang Tong, Cai Jinchi, Yuan Zhifa, Zhao Haiyan, Han Xingwen, Wang Wenji. Hyaluronic acid-based composite hydrogel in cartilage injury caused by osteoarthritis: application and mechanism [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 617-625. |
| [9] | Ma Qiaoqiao, Wu Zerui, Guo Zhuotao, Zhang Kai, Zha Guochun, Guo Kaijin. Absence of a tourniquet during total knee arthroplasty: a prospective randomized controlled trial [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(36): 5831-5836. |
| [10] | Pan Jianke, Zhao Di, Jin Xiao, Yang Weiyi, Luo Minghui, Liu Jun, Han Yanhong, Cao Houran. Implant-related errors and complications in medial open-wedge high tibial osteotomy [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(36): 5849-5856. |
| [11] | Lin Zhiyu, Han Jie, Ren Guowu, Chai Yuan, Wen Shuaibo, Wu Yukun, Xie Xiaozhong, Jin Wanqing. Active components of flemingia in regulating the signaling pathways related to knee osteoarthritis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(36): 5889-5896. |
| [12] | Song Wei, Zhang Yaxin, Jia Dazhou, Sun Yu. Adjective application of dexamethasone combined with furosemide for early pain and swelling after total knee arthroplasty [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(33): 5317-5322. |
| [13] | Qian Xiaofen, Zeng Ping, Liu Jinfu, Wang Hao, Zhou Shulong, Pan Haida. Screening key genes in synovium of osteoarthritis by a combination of differentially expressed genes and weighted co-expression network analysis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(33): 5342-5349. |
| [14] | Wang Kang, Zhi Xiaodong, Zhang Yuqiang, Gong Chao, Wang Chenliang, Wang Wei. Human amniotic epithelial cells regulate the proliferation, apoptosis and extracellular matrix synthesis of articular chondrocytes by activating the EGFR/ERK1 signaling axis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(31): 4967-4974. |
| [15] | Zhang Jian, Lin Jianping, Zhou Gang, Fang Yehan, Wang Benchao, Wu Yongchang. Semi-quantitative MRI evaluation of cartilage degeneration in early knee osteoarthritis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(3): 425-429. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||