Chinese Journal of Tissue Engineering Research ›› 2018, Vol. 22 ›› Issue (14): 2265-2271.doi: 10.3969/j.issn.2095-4344.0184
Previous Articles Next Articles
Application of nanostructured bioactive glasses in oral tissue regeneration
Xie Meng-sheng, Li Xiao-jie
- Department of Prosth odontics, Stomatology Hospital of Guangxi Medical University, Nanning 530021, Guangxi Zhuang Autonomous Region, China
-
Received:2017-12-11Online:2018-05-18Published:2018-05-18 -
Contact:Li Xiao-jie, M.D., Associate professor, Department of Prosthodontics, Stomatology Hospital of Guangxi Medical University, Nanning 530021, Guangxi Zhuang Autonomous Region, China -
About author:Xie Meng-sheng, Master candidate, Department of Prosthodontics, Stomatology Hospital of Guangxi Medical University, Nanning 530021, Guangxi Zhuang Autonomous Region, China -
Supported by:the Natural Science Foundation of Guangxi, No. 2013GXNSFBA019162; the Project for Enhancing Young Teachers’ Basic Ability in Guangxi Universities, No. 2017KY0092
CLC Number:
Cite this article
Xie Meng-sheng, Li Xiao-jie . Application of nanostructured bioactive glasses in oral tissue regeneration[J]. Chinese Journal of Tissue Engineering Research, 2018, 22(14): 2265-2271.
share this article
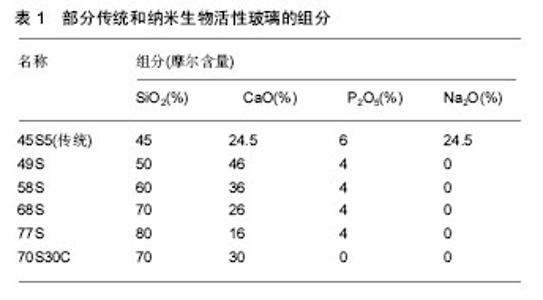
2.1 纳米生物活性玻璃材料组成 传统的生物活性玻璃是以SiO2-CaO-P2O5为主要组成成分,为了降低熔融温度,提高生物活性,常添加一些碱金属或其氧化物,最常见的45S5即是SiO2-Na2O-CaO-P2O5四元系统[4]。而纳米生物活性玻璃材料制备条件更温和,存在大量微纳米多孔结构,因此其组成可在较大范围内调整,常见的为SiO2-CaO-P2O5三元系统,2007年,又研制出SiO2-CaO二元系统的溶胶-凝胶生物活性玻璃[5],部分溶胶-凝胶法制成的纳米生物活性玻璃组成成分见 表1[2,4,6]。SiO2可提高生物活性玻璃的生物活性、力学性能和抗菌性,但传统生物活性玻璃中SiO2摩尔含量一旦超过60%,即丧失生物活性,但纳米生物活性玻璃中SiO2摩尔含量可高达80%以上,仍然可以表达生物活性。由于溶胶-凝胶法经过溶液反应步骤,材料可均匀定量地掺入一些微量元素,实现分子水平上的均匀掺杂,各类元素如镁、锶、锌、铜、银等都可以掺杂进材料中。"
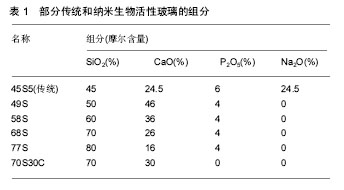

2.2 纳米生物活性玻璃的性能 2.2.1 生物活性和降解性 生物活性玻璃在体液或模拟体液中表面形成羟基磷灰石的能力是其生物活性高低的重要依据。生物活性玻璃植入体内后,材料表面生成Si-O-Si,在弱碱性条件下,其能吸附Ca2+、PO43-、CO32-在材料表面沉积,晶化形成羟基磷灰石,并通过促进成骨细胞、成牙骨质细胞等的吸附和增殖,与硬组织骨性结合,促进骨组织和牙体硬组织再生;还可通过吸附周围的细胞胶原蛋白和纤维蛋白与软组织结合并加速创面愈合。而纳米生物活性玻璃由于其高孔隙率和高比表面积[7](图1),使其更加容易诱导羟基磷灰石的沉积(图2)。通过控制纳米材料的大小,可加强纳米生物活性玻璃的生物活性,据研究一定范围内,尺寸较小的纳米生物活性玻璃[(37.6±0.81)nm]促进细胞增殖能力比较大尺寸[(74.7±0.62)nm]的纳米材料强[8],当纳米生物活性玻璃在模拟体液中浸泡,4 h就能够形成羟基磷灰石,而传统生物玻璃则需要8 h[9],另外材料表面的纳米结构还可以加强细胞的黏附和增殖,促进细胞分化,上调成骨相关基因的表达[10]。生物活性玻璃的降解速度取决于材料的结构、结晶度,尺寸大小、各组分含量等,纳米级的颗粒和孔隙使得纳米生物活性玻璃的比表面积远远大于传统生物活性玻璃,因此能够更容易地降 解[11],降解产物可释放钙、硅和磷酸根离子,促进羟基磷灰石形成及组织结合。纳米生物活性玻璃比传统生物活性玻璃具有更高的生物活性和降解性,能够促进骨组织,牙体组织及软组织的再生。 2.2.2 生物相容性 生物活性玻璃本身具有良好的生物相容性,已被证实可安全使用于口腔临床治疗。口腔组织例如牙髓干细胞、成牙本质细胞、成牙骨质细胞等,在低浓度下(≤100 mg/L)都未能观察到纳米生物玻璃的毒性作用,包括体外实验和体内实验[13-17]。而且纳米生物活性玻璃由于具有更大的比表面积,提供更多的表面吸附位点,且纳米颗粒尺寸足够小时能通过扩散作用进入细胞内,可促进细胞的增殖。但生物活性玻璃纳米颗粒由于较高的降解性,释放的Si和Ca等离子浓度如果过高可能不利于成骨细胞增殖、分化等正常行为[12]。因此纳米生物活性玻璃的生物相容性取决于纳米颗粒的大小和浓度,需要更多更详细的长期研究来确定纳米生物活性玻璃的安全使用方法。 2.2.3 载药性 传统生物活性玻璃不具备明显载药性,纳米生物活性玻璃因具有优秀的孔隙率和比表面积,比表面积能达到80.1 m2/g,远远优于传统的生物活性玻璃的1.1 m2/g。基于这些优点,其展现出理想的药物和生物活性分子基因装载的能力[18-21]。早期研究中,学者们多利用材料高比表面积特性的物理吸附作用或者用阳离子聚合物改造纳米材料表面使其载药[22-23]。2017年,Meng等[14]证明除上述特点外,纳米生物活性玻璃本身可通过形成钙离子-药物或者钙离子-基因复合体的机制来进行载药,尽管比表面积低于二氧化硅纳米颗粒,载药性能仍是后者的45倍,细胞摄取和基因转染效率明显高于商业转染试剂(聚乙烯亚胺),且细胞毒性也低于后者。纳米生物活性玻璃有望发展成为新型载药生物材料进行组织再生治疗和癌症治疗。 2.2.4 力学性能 传统生物活性玻璃的主要缺点就是其力学强度较差。断裂韧性较低,抗压强度不到 0.4 MPa,而人体松质骨的抗压强度为2-12 MPa。有学者通过提高硅离子的百分比或者晶化处理(比如A-W微晶玻璃)来提高材料的力学强度,但是这也会降低其降解性能或者生物活性。而纳米生物活性玻璃材料在提高生物活性的情况下,同时也明显增强了力学强度,抗压强度达到0.42 MPa[24]。吴成铁教授课题组使用3D打印技术制作的多孔生物活性玻璃支架由于具有均匀连续的孔隙结构,抗压强度达到了(16.10±1.53)MPa,符合理想骨再生支架材料的力学要求[25]。 2.2.5 纳米生物活性玻璃复合物的性能 为了进一步提高纳米生物活性玻璃的理化和生物特性,大量学者在材料中掺杂各类元素制成纳米生物活性玻璃复合物,以提高成骨、降解、抗菌、力学强度等性能。常见的添加元素包括镁、锌、锶、铜、银等。镁元素是骨代谢过程的重要元素,掺杂镁元素的纳米生物活性玻璃促进骨细胞的增殖和新骨形成的效果更明显。并且,镁离子掺杂的纳米生物玻璃由于网络结构的破坏,具有更快的离子释放效率。锌元素通过调节成骨相关基因如碱性磷酸酶的表达,以及蛋白合成加强纳米生物活性玻璃骨再生能力,且能提高玻璃材料与骨组织的结合性[26]。锶元素与骨组织有良好的亲和性[27],含有锶的纳米生物活性玻璃能够促进骨细胞增殖、分化,并抑制破骨细胞防止骨吸收,促进骨再生,同时材料的机械性能也有所提升[28]。锶可替换掉生物活性玻璃中的钙,材料和骨组织更好地结合,还具有促进合成代谢,抗分解代谢的作用[29]。尽管纳米生物活性玻璃本身具有一定的抗菌作用,但其本质主要是通过提高局部环境的pH值来杀灭细菌,铜离子或者银离子掺杂的纳米生物活性玻璃抗菌性明显提高[30]。其他元素,如含铕的纳米生物活性玻璃可活化骨间充质干细胞成骨分化[31],硼可提高纳米生物活性玻璃的降解性,并且对软组织创伤修复有显著提升[32]。 2.3 纳米生物活性玻璃的制作方法 传统生物活性玻璃制备方法为熔融法,是将混合原料在高温条件下 (1 300-1 500 ℃)熔融,然后在水中淬冷,最后干燥、研磨、过筛得到生物活性玻璃颗粒。但传统的熔融法能耗大、杂质掺杂成分不均匀,得到的传统生物活性玻璃呈块状且致密无孔隙,比表面积小,离子释放和降解速度较慢[1,4]。相比之下,纳米生物活性玻璃的制备方法能耗较小,无杂质掺杂,不仅能制备有着高比表面积的多孔材料,还能控制颗粒大小、形状、孔隙率等以改变其特性。现在常见的纳米生物活性玻璃制备方法有如下几种。"


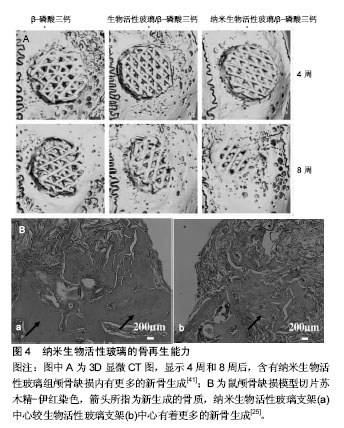
2.3.1 溶胶-凝胶法 溶胶-凝胶法是一种低能耗、反应温和、组分均匀、制备的粉体可存在大量孔隙结构的方法,由于其能简单便捷地制作纳米生物活性玻璃而被广泛地运用。溶胶-凝胶法以原硅酸四乙酯、硝酸钙和磷酸三乙酯组成为前体,在室温下进行聚合反应,形成凝胶,然后再干燥加热至600-700 ℃形成生物活性玻 璃[33]。溶胶-凝胶法制备纳米生物活性玻璃材料的组成成分、孔隙率、颗粒大小、一般形态都可通过调整制作条件和试剂的补液比等来控制,例如纳米生物活性玻璃制作过程中,加入乳酸可使材料颗粒直径在20-200 nm之间[34],而加入硅烷偶联剂的话,颗粒直径变为20- 70 nm[35];球形或者椭圆形等形状的纳米生物活性玻璃也能制造出来。但是溶胶-凝胶法制作过程比较耗时,残余的溶剂可能会导致细胞毒性,产量相对较低,并且材料结构中的大量纳米级颗粒仍然处于黏结状态,尽管进行后期处理,得到的也是形貌不规则、密度不均匀的颗粒,难以获得形貌可控、颗粒尺寸均匀的纳米生物活性玻璃。 2.3.2 模板合成法 模板合成法生物活性玻璃是近年来兴起的一类新型纳米生物活性玻璃材料,是以模板自组装技术结合溶胶-凝胶技术为基础发展而来。用表面活性剂作为结构导向剂或者形态模板剂,引入到反应体系中,表面活性剂-无机前体形成的自组装聚集体随着溶剂蒸发浓度增大,然后热处理去掉模板,得到具有特定结构的纳米生物活性玻璃材料。2004年,余承忠等[36]首次使用模板法制备出高度有序的纳米生物活性玻璃材料,相比于传统的溶胶-凝胶生物活性玻璃,介孔结构更加有序,比表面积更大,磷灰石形成活性也更快。模板合成法可以精确控制生物活性玻璃的形态和尺寸结构。陆续有学者成功制备出生物活性玻璃纳米纤维簇,还有球形、空心球形、多孔球形等不等形态的纳米生物活性玻璃材料;或用乳酸和醋酸等作为催化剂,控制颗粒表面纳米有序介孔的形成[37]。但是此种方法操作准备过程相对复杂,需要严格的控制孔隙率,颗粒大小等。更多的问题还有待探究。 2.3.3 微乳液法 微乳液是一种由水(电解质水溶液)、油(碳氢化合物)、表面活性剂、助表面活性剂以适当比例自发形成的透明或半透明的稳定体系。在微乳液中,分散着纳米尺寸的生物玻璃前体液滴,这些液滴不断地相互碰撞,可作为纳米反应器,经过加热干燥后,就得到了纳米生物活性玻璃[38]。微乳液法可通过最小的聚合生产纳米级的无机和有机复合产物,生产过程较快,另外由于表面活性剂的存在,液滴间的结合不稳定,碰撞形成的大液滴会重新变成小液滴,这种性质致使体系中液滴直径和数目不会改变,故而可以通过调整体系中的水与表面活性剂的摩尔比来实现纳米粒子尺寸控制,所得粉体粒度分布窄,不易团聚[39]。但尽管使用大量油和表面活性剂,产出也很少,技术敏感性也比较高,现在使用这种方法合成纳米生物活性玻璃的报道还比较少。 2.3.4 火焰喷雾法 火焰喷雾法是将前体溶液雾化,前体液滴在冷凝合并后形成分子核,然后1 000 ℃以上高温火焰加工诱导形成纳米颗粒,以此生产纳米生物活性玻璃。决定颗粒尺寸的关键因素是颗粒在高温区域的平均滞留时间,短暂的滞留时间(1 ms)和较高的冷却率(> 1 000 K/s)有助于纳米材料的制备[40]。火焰喷雾法产出率较高,无需额外的能量源,成分均匀性高,产物为非晶态结构故有更高的生物活性。不过操作过程需要很高的加工温度,过程中可能发生安全问题,成本也较高。 2.3.5 3D打印 近期,3D打印技术已经发展成为一种理想的制备多孔支架材料的方法,通过计算机辅助设计/计算机辅助制造(computer aided design /computer aided manufacturing,CAD/CAM)技术,可精确控制生物材料如纳米生物活性玻璃的外形,孔径大小和孔隙率(图3)。3D打印技术制造的纳米生物活性玻璃支架不仅有着可控的孔隙结构,还有着卓越的力学性能、生物活性、载药性等[25,41],今后可能成为骨组织再生治疗领域中理想的支架材料。 2.4 纳米生物活性玻璃在口腔组织再生的应用 2.4.1 颌骨组织再生 生物活性玻璃因其高生物活性,高生物相容性,以及能够促进新骨生成的能力,在过去的几十年里已经开发出多种商业产品比如固骼生、倍骼生、A-W微晶玻璃,PerioGlas等,其中倍骼生和PerioGlas(NovaBone,美国)专门应用于口腔颌骨及牙周骨组织缺损的修复再生。纳米生物活性玻璃尚未商品化,但已有学者使用恒河猴研究纳米生物玻璃,确认其在体内成骨性能良好[42]。吴成铁教授课题组比较纳米生物活性玻璃和传统生物活性玻璃材料的成骨特性,发现纳米生物活性玻璃组的新骨从支架边缘至中心大量再生,并伴随支架材料的明显降解;相反,传统生物玻璃组只在支架边缘形成新骨,材料降解也较少。可见纳米生物活性玻璃骨再生能力更加优秀,并且随着骨组织的再生,材料降解得更快更好(图4)。如今依然缺少临床人体试验确认纳米生物活性玻璃临床成骨效果的实验。 另外,许多的生物陶瓷被应用到颌骨缺损治疗中,但是生物陶瓷的生物活性较低,于是一些学者将纳米生物活性玻璃同其他生物陶瓷混合或者作为涂层涂布在后者表面,以提高后者的生物活性,使之更好地与组织的结合[43-44];某些高分子聚合物如聚乳酸和聚乙醇酸交乙酯降解物产生的局部酸性环境会有不良的组织反应,纳米生物活性玻璃的加入,不仅提高材料的生物活性,还可提高pH值来中和酸性环境[45];同时,纳米生物活性玻璃颗粒作为载体可运载药物或者基因加入各类支架材料中,以提高治疗效果。所以,纳米生物活性玻璃通过其优秀的生物活性、成骨性、载药性、生物相容性及抗菌性,无论是独立作为支架使用或者作为表面涂层、填料和药物载体同其他生物陶瓷、高分子合成材料组合使用都能发挥良好的治疗效果。 2.4.2 牙体硬组织再生 纳米生物活性玻璃在牙体硬组织再生方面的应用主要是凭借其能够促进成牙本质细胞、成牙骨质细胞的增殖,以及牙髓干细胞的增殖和牙源性分化[46],所以可作为盖髓剂进行临床运用。同时材料自身降解释放钙、硅等离子还可使牙体组织再矿化。此前已有一些实验证实在牙膏或树脂中加入生物活性玻璃对釉质再矿化有促进作用[47-49],最近有学者使用生物玻璃纳米材料再矿化釉质龋,防止釉质脱矿,电镜下观察到釉质表面由凹凸不平的蜂窝状结构变为有少量白色颗粒沉积的无空隙存在的表面平滑完整结构[50]。对于牙周炎引起的牙根吸收,因生物活性玻璃纳米材料表面可吸附相关细胞并促进其生长,故能促进牙本质及牙骨质再生,同时,Jun等[51]将Sr离子添加进生物活性玻璃纳米颗粒中,促进了与牙周韧带细胞的生物反应,可能对牙周韧带的再生有促进作用。而少量银离子的加入,可有效杀灭牙龈卟啉单胞菌和金黄葡萄球菌等,且对人类成骨细胞无毒性作用[52],其抗菌性能对于促进牙周炎症造成的牙体硬组织缺损修复再生有着辅助作 用[52-53]。"

| [1] Lee JH,Seo SJ,Kim H,et al.Bioactive glass-based nanocomposites for personalized dental tissueregeneration. Dent Mater J.2016;35(5):710-720.[2] Hench LL.The story of Bioglass.J Mater Sci Mater Med.2006; 17:967-978.[3] Wu C, Chang J. Mesoporous bioactive glasses: structure characteristics, drug/growth factor delivery and bone regeneration application.Interface Focus.2012;2(3):292.[4] 史舒雅,陈亚明.生物活性玻璃在口腔医学中的应用[J].口腔生物医学,2013,4(1):44-47.[5] Jones JR,Tsigkou O,Coates EE. Extracellular matrix formation and mineralization on a phosphate-free porous bioactive glass scaffold using primary human osteoblast (HOB) cells.Biomaterials.2007;28(9):1653-1663.[6] 雷波.新型微纳米生物活性玻璃的研制及性能研究[D].华南理工大学,2010.[7] Wu C,Ramaswamy Y,Zhu Y,et al.The effect of mesoporous bioactive glass on the physiochemical, biological and drug-release properties of poly(DL-lactide-co-glycolide) films. Biomaterials.2009; 30(12):2199.[8] Ajita J,Saravanan S,Selvamurugan N.Effect of size of bioactive glass nanoparticles on mesenchymal stem cellproliferation for dental and orthopedic applications.Mater Sci Eng C Mater Biol Appl. 2015;53:142-149. [9] Yan X,Yu C,Zhou X,et al.Highly ordered mesoporous bioactive glasses with superior in vitro bone-forming bioactivities.Angew Chem Int Ed Engl. 2004;43(44): 5980-5984.[10] Tavakolizadeh A,Ahmadian M,Fathi M,et al.Investigation of Osteoinductive Effects of Different Compositions of Bioactive Glass Nanoparticles for Bone Tissue Engineering. ASAIO J. 2017;63(4):512-517.[11] Greenspan DC,Zhong JP,Chen ZF,et al.The evaluation of degradability of melt and sol–gel derived Bioglass® in vitro. Bioceramics.1997;10:391-394.[12] Hench LL.Genetic design of bioactive glass.J Eur Ceram Soc.2009;29(7):1257-1265.[13] Warheit DB,KL Reed KL.11. Nanotoxicology: Environmental, Health and Safety (EHS) Considerations for Assessing Hazards and Risks Following Nanoparticle Exposures.John Wiley Sons Inc.2015:233-243.[14] Meng Y,Xue Y,Ma PX,et al.Intrinsic Ultrahigh Drug/miRNA Loading Capacity of Biodegradable Bioactive Glass Nanoparticles toward Highly Efficient Pharmaceutical Delivery. ACS Appl Mater Interfaces.2017;9(10):8460.[15] Jo JH,Lee EJ,Shin DS,et al.In vitro/in vivo biocompatibility and mechanical properties of bioactive glass nanofiber and poly(epsilon-caprolactone)composite materials.J Biomed Mater Res B Appl Biomater.2009;91(1):213.[16] El-Fiqi A,Kim JH,Perez R,et al.Novel bioactive nanocomposite cement formulations with potential properties: Incorporation of nanoparticle form of mesoporous bioactive glass to calcium phosphate cements.J Mater Chem B. 2015; 3(7):1321-1334.[17] Elfiqi A,Kim JH,Kim HW.Osteoinductive Fibrous Scaffolds of Biopolymer/Mesoporous Bioactive Glass Nanocarriers with Excellent Bioactivity and Long-Term Delivery of Osteogenic Drug.ACS Appl Mater Interfaces.2015;7(2):1140.[18] Sui B,Zhong G,Jiao S.Drug-loadable Mesoporous Bioactive Glass Nanospheres: Biodistribution, Clearance, BRL Cellular Location and Systemic Risk Assessment via 45Ca Labelling and Histological Analysis.Sci Rep.2016;6:33443.[19] Li X,Chen X,Miao G,et al.Synthesis of radial mesoporous bioactive glass particles to deliver osteoactivin gene.J Mater Chem B.2014;2(40):7045-7054.[20] Kim TH,Singh RK,Kang MS,et al. Gene delivery nanocarriers of bioactive glass with unique potential to load BMP2 plasmid DNA and to internalize into mesenchymal stem cells for osteogenesis and bone regeneration.Nanoscale. 2016;8(15): 8300-8311.[21] Garg S,Thakur S,Gupta A,et al.Antibacterial and anticancerous drug loading kinetics for (10-x)CuO-xZnO-20CaO-60SiO2-10P2O5 (2 ≤ x ≤ 8) mesoporous bioactive glasses.J Mater Sci Mater Med.2017; 28(1):11.[22] Wu C,Fan W,Chang J.Functional mesoporous bioactive glass nanospheres: synthesis, high loading efficiency, controllable delivery of doxorubicin and inhibitory effect on bone cancer cells.J Mater Chem B.2013;1(21):2710-2718.[23] Lin HM,Lin HY,Chan MH.Preparation, characterization, and in vitro evaluation of folate-modified mesoporous bioactive glass for targeted anticancer drug carriers.J Mater Chem B. 2013; 1(1):6147-6156.[24] Wu C,Zhang Y,Zhou Y,et al.A comparative study of mesoporous glass/silk and non-mesoporous glass/silk scaffolds: physiochemistry and in vivo osteogenesis.Acta Biomaterialia.2011;7(7):2229-2236.[25] Wu C,Luo Y,Cuniberti G,et al.Three-dimensional printing of hierarchical and tough mesoporous bioactive glass scaffolds with a controllable pore architecture, excellent mechanical strength and mineralization ability.Acta Biomaterialia. 2011; 7(6):2644-2650.[26] Murphy S,Boyd D,Moane S,et al.The effect of composition on ion release from Ca–Sr–Na–Zn–Si glass bone grafts.J Mater Sci Mater Med.2009;20(11):2207-2214.[27] Kumar KP,Arnab M,Biswanath K,et al.Influence of single and binary doping of strontium and lithium onin vivobiological properties of bioactive glass scaffolds.Sci Rep.2016;6:32964.[28] Arepalli SK,Tripathi H,Hira SK,et al.Enhanced bioactivity, biocompatibility and mechanical behavior of strontium substituted bioactive glasses.Mater Sci Eng C.2016;69:108.[29] Fredholm YC,Karpukhina N,Brauer DS,et al.Influence of strontium for calcium substitution in bioactive glasses on degradation, ion release and apatite formation.J R Soc Interface. 2012;9(70):880-889.[30] Fan W,Wu D,Ma T,et al.Ag-loaded mesoporous bioactive glasses against Enterococcus faecalis biofilm in root canal of human teeth.Dent Mater J.2015;34(1):54-60.[31] Wu C,Xia L,Han P,et al.Europium-Containing Mesoporous Bioactive Glass Scaffolds for Stimulating in Vitro and in Vivo Osteogenesis.Acs Appl Mater Interfaces.2016;8(18):11342.[32] Yang Q,Chen S,Shi H,et al.In vitro study of improved wound-healing effect of bioactive borate-based glass nano-/micro-fibers.Mater Sci Eng C Mater Biol Appl. 2015;55: 105.[33] Kaur G,Pickrell G,Sriranganathan N,et al.Review and the state of the art: Sol-gel and melt quenched bioactive glasses for tissue engineering.J Biomed Mater Res B Appl Biomater. 2016;104(6):1248.[34] Chen X,Lei B,Wang Y,et al.Morphological control and in vitro bioactivity of nanoscale bioactive glasses.J Non Cryst Solids. 2009;355:791-796.[35] Chen X,Guo C,Zhao N.Preparation and characterization of the sol–gel nano-bioactive glasses modified by the coupling agent gamma-aminopropyltriethoxysilane.Appl Surf Sci. 2008; 255:466-468.[36] 余承忠,严晓霞,赵东元.纳米介孔以及介孔-大孔复合生物玻璃及其制备方法[P].中国专利.CN1554607A.2014-12.[37] 赵娜如,雷波,陈晓峰,等.新型微纳米生物活性玻璃的模板仿生合成[J].东南大学学报医学版,2011, 30(1):215-218.[38] 杨宇霞.CaO-P<,2>O<,5>-SiO<,2>系统生物活性纳米材料的制备及其生物性能研究[D].华南理工大学, 2004.[39] Wang H,Chen X,Wang Y,et al.Preparation and characterization of the system SiO 2 -CaO-P 2 O 5 bioactive glasses by microemulsion approach.J Wuhan UnivTechnol Mater Sci Ed.2013;28(5):1053-1057.[40] Brunner TJ,Grass RN,Stark WJ.Glass and bioglass nanopowders by flame synthesis.Chem Commun (Camb). 2006;37(13):1384.[41] Zhang Y,Xia L,Zhai D,et al.Mesoporous bioactive glass nanolayer-functionalized 3D-printed scaffolds for accelerating osteogenesis and angiogenesis.Nanoscale. 2015;7(45): 19207-19221.[42] 王晶晶,施亮,徐婧,等.溶胶凝胶微纳米生物活性玻璃对恒河猴牙槽骨缺损的修复作用[J].广东医学,2016, 37(11):1610-1612.[43] Fan Z,Wang J,Liu F,et al.A new composite scaffold of bioactive glass nanoparticles/graphene: Synchronous improvements of cytocompatibility and mechanical property.Colloids Surf B Biointerfaces.2016;145:438-446.[44] Popa AC,Stan GE,Enculescu M,et al. Superior biofunctionality of dental implant fixtures uniformly coated with durable bioglass films by magnetron sputtering.J Mech Behav Biomed Mater.2015;51:313-327.[45] Qiu Z,Yang H,Wu J,et al.Ionic dissolution products of NovaBone promote osteoblastic proliferation via influences on the cell cycle.J Int Med Res.2009;37(3):737.[46] Lee JH,Kang MS,Mahapatra C,et al.Effect of Aminated Mesoporous Bioactive Glass Nanoparticles on the Differentiation of Dental Pulp Stem Cells.PloS One. 2016; 11(3):e0150727.[47] Gjorgievska E,Nicholson JW.Prevention of enamel demineralization after tooth bleaching by bioactive glass incorporated into toothpaste.Aust Dent J.2011;56(2):193-200.[48] Kohda N,Iijima M,Kawaguchi K,et al.Inhibition of enamel demineralization and bond-strength properties of bioactive glass containing 4-META/MMA-TBB-based resin adhesive. Eur J Oral Sci.2015;123(3):202.[49] Palaniswamy UK,Prashar N,Kaushik M,et al.A comparative evaluation of remineralizing ability of bioactive glass and amorphous calcium phosphate casein phosphopeptide on early enamel lesion. Dent Resh J.2016;13(4):297-302.[50] Sculean A,Nikolidakis D,Schwarz F.Regeneration of periodontal tissues: combinations of barrier membranes and grafting materials - biological foundation and preclinical evidence: a systematic review. J Clin Periodontol.2008;35(8 Suppl):106-116.[51] Jung WK,Koo HC,Kim KW,et al.Antibacterial activity and mechanism of action of the silver ion in Staphylococcus aureus and Escherichia coli.Appl Environ Microbiol.2008;74(7):2171.[52] Allan I,Newman H,Wilson M.Antibacterial activity of particulate Bioglass against supra- and subgingival bacteria. Biomaterials.2001;22(12):1683-1687.[53] 朱洁,吴大明,刘卫红.生物活性玻璃的抗菌性能及其在根管感染控制中的应用[J].口腔医学,2016, 36(6):570-572.[54] Wang X,Fang C,Liu J,et al.Biocomposites of copper-containing mesoporous bioactive glass and nanofibrillated cellulose: Biocompatibility and angiogenic promotion in chronic wound healing application.Acta Biomaterialia.2016;46:286.[55] Gupta B,Papke JB,Mohammadkhah A,et al.Effects of Chemically Doped Bioactive Borate Glass on Neuron Regrowth and Regeneration. Ann Biomed Eng.2016;44(12):1-10. |
| [1] | Pu Rui, Chen Ziyang, Yuan Lingyan. Characteristics and effects of exosomes from different cell sources in cardioprotection [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(在线): 1-. |
| [2] | Zhang Tongtong, Wang Zhonghua, Wen Jie, Song Yuxin, Liu Lin. Application of three-dimensional printing model in surgical resection and reconstruction of cervical tumor [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1335-1339. |
| [3] | Zhang Chao, Lü Xin. Heterotopic ossification after acetabular fracture fixation: risk factors, prevention and treatment progress [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1434-1439. |
| [4] | Zhou Jihui, Li Xinzhi, Zhou You, Huang Wei, Chen Wenyao. Multiple problems in the selection of implants for patellar fracture [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1440-1445. |
| [5] | Wang Debin, Bi Zhenggang. Related problems in anatomy mechanics, injury characteristics, fixed repair and three-dimensional technology application for olecranon fracture-dislocations [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1446-1451. |
| [6] | Ji Zhixiang, Lan Changgong. Polymorphism of urate transporter in gout and its correlation with gout treatment [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1290-1298. |
| [7] | Yuan Mei, Zhang Xinxin, Guo Yisha, Bi Xia. Diagnostic potential of circulating microRNA in vascular cognitive impairment [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1299-1304. |
| [8] | Wang Xianyao, Guan Yalin, Liu Zhongshan. Strategies for improving the therapeutic efficacy of mesenchymal stem cells in the treatment of nonhealing wounds [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1081-1087. |
| [9] | Wan Ran, Shi Xu, Liu Jingsong, Wang Yansong. Research progress in the treatment of spinal cord injury with mesenchymal stem cell secretome [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1088-1095. |
| [10] | Liao Chengcheng, An Jiaxing, Tan Zhangxue, Wang Qian, Liu Jianguo. Therapeutic target and application prospects of oral squamous cell carcinoma stem cells [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1096-1103. |
| [11] | Zhao Min, Feng Liuxiang, Chen Yao, Gu Xia, Wang Pingyi, Li Yimei, Li Wenhua. Exosomes as a disease marker under hypoxic conditions [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1104-1108. |
| [12] | Xie Wenjia, Xia Tianjiao, Zhou Qingyun, Liu Yujia, Gu Xiaoping. Role of microglia-mediated neuronal injury in neurodegenerative diseases [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1109-1115. |
| [13] | Li Shanshan, Guo Xiaoxiao, You Ran, Yang Xiufen, Zhao Lu, Chen Xi, Wang Yanling. Photoreceptor cell replacement therapy for retinal degeneration diseases [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1116-1121. |
| [14] | Jiao Hui, Zhang Yining, Song Yuqing, Lin Yu, Wang Xiuli. Advances in research and application of breast cancer organoids [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1122-1128. |
| [15] | Wang Shiqi, Zhang Jinsheng. Effects of Chinese medicine on proliferation, differentiation and aging of bone marrow mesenchymal stem cells regulating ischemia-hypoxia microenvironment [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1129-1134. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||