Chinese Journal of Tissue Engineering Research ›› 2018, Vol. 22 ›› Issue (14): 2251-2258.doi: 10.3969/j.issn.2095-4344.0754
Previous Articles Next Articles
Repair materials for bone defects: present status, needs and future developments
Zhou Si-jia1, Jiang Wen-xue2, You Jia2
- 1Tianjin Medical University, Tianjin 300072, China; 2Department of Orthopaedics, Tianjin First Center Hospital, Tianjin 300192, China
-
Received:2017-12-28Online:2018-05-18Published:2018-05-18 -
Contact:Jiang Wen-xue, Chief physician, Master’s supervisor, Department of Orthopaedics, Tianjin First Center Hospital, Tianjin 300192, China -
About author:Zhou Si-jia, Master candidate, TianJin Medical University, Tianjin 300072, China
CLC Number:
Cite this article
Zhou Si-jia, Jiang Wen-xue, You Jia. Repair materials for bone defects: present status, needs and future developments[J]. Chinese Journal of Tissue Engineering Research, 2018, 22(14): 2251-2258.
share this article

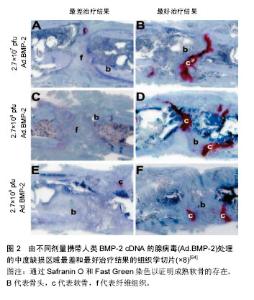
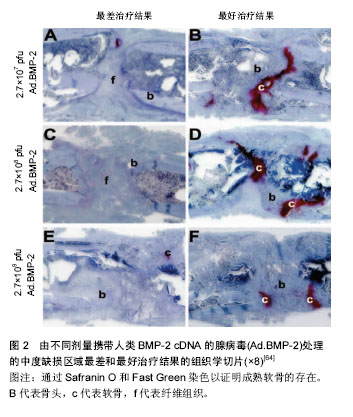
2.1 传统骨缺损修复材料 2.1.1 自体骨 自体骨由于其优异的骨传导、骨诱导及成骨性质,且拥有理想的生物相容性及三维结构,一直以来被视为骨缺损修复材料中的金标准,但骨量有限、额外的失血量和取骨区的潜在并发症等仍是限制自体骨应用不可避免的缺点[2]。目前自体骨主要包括皮质骨、松质骨及骨髓3大类,其中皮质骨分为不带血供和带血供2种形式。不带血供的操作方式相对简单,但血管的缺乏影响了愈合效果[3];带血供的操作方式可提供充分血运,促进骨愈合[4],但解剖的复杂性提高了手术的难度[5]。松质骨具备良好的骨诱导及整合能力,但缺乏一定的力学强度。此外,自体骨髓因包含间充质干细胞和骨再生相关因子,可加快血管化,促进骨修复[6]。Schmitt等[7]分别使用磷酸钙、异种骨、同种异体骨及自体骨进行骨缺损修复,在对影像学及组织学分析后发现,4种材料的骨诱导及成骨能力均不相同,其中自体骨显示出最高的成骨速率及新生骨体积比,证实了自体骨在骨修复中强大的能力。目前临床主要应用的自体骨包括髂骨、胫骨和跟骨等,近期Chiodo等[8]对髂嵴和胫骨近端的骨移植样本进行组织学研究,发现相比于胫骨,髂嵴含有更丰富的活性造血骨髓。类似的,Hyer等[9]发现髂嵴、远端胫骨和跟骨的骨髓抽吸物均含有间充质干细胞骨祖细胞,其中髂嵴的浓度更高。因此,自体骨的这些优势使其在临床治疗骨缺损方面仍占据很大的比例。 2.1.2 同种异体骨 同种异体骨是自体骨的有效替代品,无传染性、免疫性疾病,在深冻和处理后均可成为其来源[10]。异体骨具备诸多成骨性质,可被广泛应用于各种病因导致的骨缺损[11],然而具有免疫原性的同种异体骨可能会阻碍细胞黏附和分化,此外,延迟愈合和感染等并发症也相对限制了其临床使用[12]。随着制备技术的不断进步,目前同种异体骨主要以冻干异体骨的形式被广泛应用。Wei等[13]使用了2种冻干同种异体骨治疗大鼠股骨骨缺损,通过术后8周的micro-CT扫描和组织学分析,发现2者均持续形成新骨,验证了2种冻干异体骨均具备良好的骨诱导和成骨能力。近年来许多学者也通过不同实验证实了脱钙冻干异体骨拥有促进骨诱导的生长因子,能够聚集间充质干细胞并支持成骨细胞分 化[14],因此成为了目前唯一经美国食品与药品监督管理局(Food and Drug Administration,FDA)批准在北美可用于临床骨修复的生物材料[15]。 2.1.3 异种骨 异种骨来源广泛,但由于种属间抗原的差异性,必须接受人工处理而避免移植后可能发生的免疫排斥反应[16],此外,潜在的致病性和相关伦理问题也有待解决。经处理的异种骨可保留部分生物力学特性,用于骨缺损修复,但会丧失诱导间充质干细胞分化增殖的能力。最近Kubosch等[17]对10年内共232例骨缺损患者进行分析,其中116例使用异体松质骨,116例使用合成异种骨,结果发现2种材料均促进了骨愈合,但异种骨的骨诱导能力相对较差。该项病例研究也充分反映了异种骨在生物活性和骨诱导能力方面存在不足。因此,学者们提出了复合其他修复材料或相关因子的方式,包括复合骨形态发生蛋白、自体骨髓和生长因子等,已成为目前异种骨的研究热门,在避免免疫排斥的前提下,加强了骨诱导能力,进而促进骨愈合[18]。相信随着相关研究和技术的不断深入,复合异种骨会获得更大的关注。 2.1.4 脱钙骨基质 临床应用的脱钙骨基质主要取自于供体的同种异体骨,包含胶原蛋白(主要为Ⅰ型和Ⅳ型)、非胶原蛋白、生长因子、少量磷酸钙及细胞碎片等[19]。脱钙骨基质作为骨修复基质和传递生物活性剂的载体,在经过脱钙及人工处理后,暴露和释放了骨形态发生蛋白,使脱钙骨基质具有促进骨再生的骨诱导性质[20]。但脱钙骨基质的骨诱导性与其抗原性呈负相关,人工处理中过度地降低抗原会破坏过多的成骨因子,显著降低了成骨性质。此外,脱钙骨基质由于失去了大量无机成分,丧失了绝大部分的生物力学特性,并不适合用于承重部位的骨缺损修复。脱钙骨基质还具有良好的骨传导能力、组织相容性和生物孔隙结构。其中合适的生物孔隙结构能够放大骨形态发生蛋白的缓释特性,利于成骨细胞、因子附着及增长,促进骨再生[19]。控制理想的孔隙大小始终是学者们致力于解决的问题,因此Hou等[21]通过纳米自体组装肽与脱钙骨基质进行复合,减小了孔隙直径并增加了电荷相互作用,增加成骨细胞和因子的数量,同时该材料还可建立细胞黏附、增殖和分化的微环境,提高了成骨能力。目前,由于复合骨修复材料的兴起,脱钙骨基质迅速成为主流支架材料之一[22]。近期Xing等[23]创新性地使用逐层自组装技术将纳米多层重组纤维连接蛋白/钙黏蛋白嵌合体修饰脱钙骨基质,发现该复合材料通过物理拦截及化学识别,显著提高了细胞选择保留的效率,并提供有利的微环境以促进间充质干细胞的迁移、增殖和成骨分化;同时,该生物材料还具有成本效益高、储存和运输方便,以及在手术中可快速构建等优势。 2.1.5 生物陶瓷 羟基磷灰石:羟基磷灰石与人体成分具有良好的生物相容性、生物活性和骨传导性,已被广泛应用于生物医学和骨缺损修复材料[24-25]。随着纳米材料技术的飞速发展,纳米化羟基磷灰石可获得高表面活性和超微结 构[26-27],相对于传统羟基磷灰石具备更高的可吸收性和生物活性[28],此外,纳米羟基磷灰石还具有改善成骨相关细胞增殖和分化的能力。为使纳米羟基磷灰石的性质和活性获得进一步提高,目前学者们尝试使用最新的技术将纳米羟基磷灰石与其他材料进行整合[29],并得到了显著效果。国内Zhu等[30]首次采用磁性颗粒技术将磁性纳米颗粒整合至羟基磷灰石支架中,得到磁性羟基磷灰石支架,结果发现磁性羟基磷灰石支架改变了蛋白质冠状结构的组成,有助于增加与Ca2+、G蛋白偶联受体和MAPK/ERK级联相关的蛋白质浓度,从而证实磁性支架在调节细胞增殖中的作用,为设计骨组织工程的磁性支架奠定了基础。国外Jakus等[31]则利用热门的3D打印技术,使用羟基磷灰石和聚已内酯制备新型的超弹性“骨”,结果显示该材料具备良好的弹性和再吸收性,并增强了细胞活力和增殖能力。此外,超弹性“骨”的相关动物实验证明该材料不引起免疫反应和血管化,与周围组织能够快速整合,可迅速骨化并促进骨再生。因此,羟基磷灰石的纳米化技术及与其他材料和技术的整合,将会显著提高该材料的综合优势,并促进其在骨缺损方面的应用。但如何完善制备方法加强羟基磷灰石自身的机械性能,优化复合材料的生物相容性,匹配体内组织生长的降解速率,以及提高复合材料的生物安全性等,仍需要未来进一步解决。 磷酸钙:磷酸钙具有陶瓷、粉状和骨水泥多种形式,主要包括α-磷酸三钙、β-磷酸三钙、磷酸四钙等,其中以β-磷酸三钙应用最普遍。磷酸钙拥有良好的骨传导性,再吸收性和生物相容性[32],在骨修复方面具有优秀的前景。但磷酸钙本身也存在诸多不足,有限的机械强度和较高的脆性仍是该材料最突出的缺点,因此在单独应用时仅能用于非负重区域[33],其次,实现最佳的降解速率和合适的固化时间也是磷酸钙继续深入研究和突破的难点。值得一提的是,磷酸钙的多种形式在灵活应对各种类型骨缺损方面具有显著优势。国外Fukuda等[34]通过将β-磷酸三钙颗粒与酸性磷酸钙溶液混合,发现β-磷酸三钙更易凝固并形成完全互连的多孔结构,并得到理想的机械强度;随后建立的大鼠颅骨缺损模型显示β-磷酸三钙水泥和颗粒均具有较好的骨传导性,而两种形式的材料的成骨能力相当,因此β-磷酸三钙水泥和颗粒在应对各种骨缺损中具备优秀的灵活性和修复能力。此外,目前学者们已研究出磷酸钙新型可注射形式磷酸钙骨水泥,磷酸钙骨水泥由磷酸钙盐固相和血液等液相所制备,在引发沉淀反应和晶体缠结后,可实现磷酸钙骨水泥填充骨缺损后的硬化[35],因此磷酸钙骨水泥的可注射形式及可匹配各种缺损的优势,使其迅速得到了广泛关注和应用[36]。Zhao等[37]在国内首创使用磷酸钙骨水泥整合壳聚糖和聚乳糖纤维,发现该复合材料不仅具有灵活的形式,其抗弯曲强度和活力也得到了增强和提高。 2.1.6 金属材料 金属材料主要用于需要机械支撑的部位,如负重长骨(股骨,胫骨等)和椎骨的骨缺损。该类材料在应用时需要与骨骼紧密结合,从而为植入部位提供生理负荷功能。金属材料在应用中的主要问题是生理环境的腐蚀会造成材料性质的改变和体内金属离子水平的提高,从而导致材料的植入失败和潜在的毒副作用。因此理想的金属材料应具备优秀的生物相容性、安全性和耐腐蚀性[38]。目前临床应用较成熟的是钛及其合金,钛的结构近似骨组织[39],具有抗高载荷和良好的生物相容性。但钛缺乏抗腐蚀和骨结合能力,因此常需通过表面涂层增强其生物活性和抗腐蚀性[40],包括生物黏附性涂层和复合涂层。近年来,一种新型的“骨小梁金属”—多孔钽吸引了学者们的关注,它具备良好的生物相容性、理想的弹性模量、耐腐蚀性以及较高的孔隙率,钽的相关研究及临床应用已得到迅速发展,Balla等[41-42]通过体外研究,证实了钽材料具有优异的生物活性,可促进细胞黏附、生长和分化,形成丰富的细胞外基质,并增强早期的生物固定。耿丽鑫等[43]使用国产多孔钽材料进行体外实验,发现钽具有良好的三维构型和生物相容性,可促进成骨细胞的黏附、增殖及成骨基因的表达。目前钽的相关产品已应用于骨科领域中,取得了令人鼓舞的成绩,并有望成为优秀的骨缺损修复材料。 2.2 现代骨缺损修复材料 2.2.1 高分子材料 天然高分子材料:天然高分子材料种类繁多,具备良好的生物降解性和生物相容性,并可促进细胞黏附和生长,主要作为支架材料被广泛用于组织工程,成为骨缺损重要的修复材料,如壳聚糖、胶原蛋白、明胶、透明质酸、藻酸盐和丝素蛋白等[44]。然而,绝大部分天然材料的机械强度不足,过快的降解速率不适合单独作为相关成骨细胞的基质材料,以及生物学性质的不稳定和有限的制造能力,均是该类材料难以被单一设计加工和应用于骨缺损修复的主要原因。近期丝素蛋白凭借其优秀的生物相容性,高孔隙率和良好的机械性能,在骨组织工程方面表现出良好的前景[45]。目前基于丝素蛋白的支架材料得到了国内外学者的广泛关注与研究,该丝素蛋白材料不仅可作为细胞和因子的载体,具备一定的可塑性和力学强度,与此同时,在体内的降解速度与骨缺损的修复周期相匹配,因此在骨缺损材料上展现出巨大优势[46]。Perrone等[47]率先制备了新型的可再吸收型丝素蛋白螺钉,具备良好的生物相容性并能适应修复部位,且该材料的可再吸收性避免了二次移除和应力屏蔽的弊端,进一步完善了骨修复能力。此外,丝素蛋白的水凝胶形式也逐渐展现出优势,Ran等[48]利用丝素蛋白复合壳聚糖-蚕丝素蛋白/羟基磷灰石水凝胶,经体外细胞培养后发现,水凝胶可促进细胞的黏附、增殖和分化,因此该丝素蛋白复合水凝胶有望成为新一代骨缺损修复材料的理想支架。 人工高分子材料:人工高分子材料的生物相容性相对较差,亲水性和细胞黏附能力相对较弱,有可能引起无菌性炎症反应,但力学性能相对优于天然高分子材料,其固定的成分比例和易加工性同样是不可忽视的优势。该类材料主要包括聚乳酸、聚乙酸、聚乳酸聚乙酸及相关衍生复合材料,其中应用最广泛的是聚乳酸、聚乙酸和聚乳酸聚乙酸,它们主要以支架材料的形式使用,但其降解产物会引起降解速率的激增和炎性反应的发生。此外,这类材料作为骨缺损修复材料时,需要复合生长因子和相关细胞等提高生物活性和生物相容性,或复合其他材料等促进细胞的黏附和增殖[49]。目前可降解人工高分子材料和生物陶瓷组成的复合支架引起了学者们强烈兴趣,可降解高分子材料提供坚韧的结构,生物陶瓷增强骨传导性[50],该材料可在保留各自优点的基础上,灵活调整其组成和微观结构。此外,纳米技术的引入也提高了该材料的仿生化,增强了蛋白质吸附和机械性能,具有代表性的是Chen等[51]使用嵌段高分子材料矿化纳米材料,结果显示良好的机械性能和细胞相容性,为骨缺损修复材料的支架研究提供了一个新的方向。 2.2.2 复合材料 复合材料是两种及以上材料的组合,其在微观或纳米尺度上的形态或组成不同。由于单一材料在生物和理化性质方面的局限性,使得复合材料受到了广泛的重视[44]。复合生物材料可同时具备多种材料的优势,显着改善骨再生,提供良好的力学强度和改善的生物学特性。目前复合材料主要分为多种材料的复合(如生物陶瓷和高分子材料之间的复合),制备技术与材料的复合,以及组织工程技术与材料的复合等。值得关注的是现代制备技术在骨缺损材料中的应用,如静电纺丝和水凝胶等制备技术均得到了飞速发展,Ding等[52]使用静电纺丝和溶胶-凝胶法整合了聚羟基丁酸酯、聚已内酯和生物玻璃,结果发现得到的混合支架具备良好的亲水性,利于成骨细胞的黏附,并增加了细胞和碱性磷酸盐的活性。因此,这些新兴技术和不同材料的整合为下一代骨缺损修复材料的研究开辟了一个新的方向。 2.2.3 组织工程骨 种子细胞和生长因子:种子细胞是组织工程骨中生物活性的主要提供者,理想的种子细胞需来源广泛,制备难度低,具备优秀的成骨潜能和增殖能力,能够迅速分化为成骨细胞并灵活适应各种微环境[53]。目前研究和应用最广泛种子细胞的是间充质干细胞,其来源包括骨髓、脂肪组织及外周血等,但骨髓间充质干细胞仍然是首选的取材来源,间充质干细胞具备强大的增殖能力,并可分化为成骨细胞和软骨细胞等,避免了其他细胞可能引起的免疫排斥和致病性等缺陷。 生长因子指诱导成骨的生长因子,可调节细胞的增殖分化和细胞外基质的合成,这种作用主要通过早期自分泌和旁分泌的方式,提高成骨细胞的增殖速度和活性,显著增强骨组织的再生能力。目前常见的生长因子包括胰岛素样生长因子、血小板衍生生长因子和骨形态发生蛋白等,其中以骨形态发生蛋白的研究和应用最广泛,骨形态发生蛋白最早由Urist分离并发现,在经过学者们的大量研究后,证实了骨形态发生蛋白2和骨形态发生蛋白7在治疗骨缺损方面的良好效果。但如何提高和优化种子细胞和支架材料的结合效率及相应的临床效果,仍然需要未来的进一步验证和解决。 支架材料和纳米材料:支架材料是组织工程骨的中心环节,理想的支架需模拟细胞外基质的三维结构,并具备许多优势,包括:拥有支持细胞黏附、生长和迁移的多孔结构,以促进细胞-支架材料的相互作用;具备足够的弹性和机械性能;可控制的降解速率;新骨的形成均匀分布以避免骨坏死;体内最小程度的炎症和毒性反应;此外,支架还需要具备能将细胞转移到骨缺损部位的能力[54]。 理想支架材料的上述诸多特点,催生了迅速发展的纳米材料。纳米材料主要作为支架材料应用于组织工程骨中,其衍生的复合材料具备生物活性和可再吸收性,可提供良好的机械性能,促进细胞的黏附和增殖。与传统材料相比,纳米材料的复合形式可形成紧密联结,提供更好的机械性能,同时保持骨传导性和生物相容性,促进蛋白质吸附、细胞黏附和组织增殖分化。 纳米复合材料主要包括多孔支架、水凝胶和纤维支架3种形式。纳米复合多孔支架可通过不同的技术进行制备,从而获得特定的孔隙率和结晶度等特性。Yan等[55]制备了由丝素蛋白和纳米磷酸钙合成的复合支架,无细胞毒性并具有自矿化能力。纳米复合水凝胶与细胞外基质结构和组成相似,具有丰富的互连亲水网状多孔结构,为细胞附着和相互作用提供更大的空间(图1)。Nejadnik等[56]开发了一种基于磷酸钙纳米颗粒和羟基磷灰石的可注射式纳米复合水凝胶,结果表明该材料具有优秀的细胞黏附能力和可降解性,并促进了骨生长。纳米复合纤维支架模拟了天然细胞外基质的纤维结构,孔隙率高达95%,可增强细胞黏附、迁移和增殖分化的能力,目前已用于骨组织工程,常通过相分离和静电纺丝制造技术进行制备。Chae等[57]通过静电纺丝和原位合成技术成功制备了新型的羟基磷灰石/藻酸盐纳米复合纤维支架,模拟骨组织中的矿化胶原纤维,克服了机械共混/电纺复合纳米纤维的缺点。因此,结构仿生、孔隙可控和多孔网状的纳米复合材料将会成为最有前景的组织工程支架之一。 组织工程骨技术进展:尽管制备理想的组织工程骨仍然是学者们致力的目标,但此间许多研究成果促使骨组织工程得到了飞快进展。骨生物反应器技术被认为可提供种子细胞、生长因子和支架组合的理想环境,并且对骨生物反应器环境的控制已使制备离体组织工程骨成为可能,但目前仍然面临着对操作者技术过度依赖的挑战[58]。此外,近年来新一代叠加制造技术也受到大量关注,叠加制造技术以3D打印为代表,通过多层构建的制造方法,可制备具有优异机械和骨传导特性的多孔生物相容性支架[59],在结合3D图像和CT资料后可制备匹配特定骨缺损的3D骨修复材料,且可控制材料的结构、孔隙度和性质[60]。值得一提的是,目前研究最广泛和深入的仍然是纳米材料制备技术,包括制备纳米颗粒的湿化学沉淀、溶胶-凝胶合成和水热合成技术,构建孔隙可控型3D纳米纤维的分子自组装技术,以及冷冻干燥法和相分离等,均促进了纳米复合材料的发展[61]。 近年来基因工程在组织工程骨应用方面展现出不可替代的优势。基因工程可延长蛋白质的表达时间并可调控转基因的表达,刺激骨再生和骨修复[62]。目前基因载体大致分为病毒载体和非病毒载体,病毒载体包括反转录病毒、腺病毒和腺相关病毒等,非病毒载体主要是质粒,这些载体均可进行全身或局部递送。 目前基因工程在体内的运用主要包括直接注射和基因激活基质。直接注射基因载体为骨再生提供了最简单和最便捷的方法。在一系列研究中,Baltzer等[63]和Betz等[64]分别描述了在兔和大鼠骨缺损中直接注射表达骨形态发生蛋白2的腺病毒,结果显示骨修复均得到了改善(图2),但该方式受到载体剂量和注射时间的影 响[64]。此外,基因也可与基因激活基质结合递送,其允许基因载体受控地缓慢释放到周围的细胞或组织中。基因激活基质的来源包括胶原、壳聚糖、高分子材料及肌肉和脂肪组织等,而腺病毒和质粒是基因激活基质最常用的载体。近期Zhang等[65]制备了表达血小板衍生生长因子B和骨形态发生蛋白7的基因激活基质并利用腺病毒进行递送,在植入大鼠股骨骨缺损后促进了骨再生。但高度有效的递送载体和转染方法仍然是目前研究的重点,此外,安全性问题依旧是基因工程联合组织工程骨的主要障碍[66]。相信随着相关各领域技术的发展,组织工程骨必将会实现新的高度。"
| [1] Agarwal R,Garcia AJ.Biomaterial strategies for engineering implants for enhanced osseointegration and bone repair.Adv Drug Deliver Rev. 2015;94:53-62.[2] Mueller TL,Wirth AJ,van Lenthe GH,et al.Mechanical stability in a human radius fracture treated with a novel tissue-engineered bone substitute: a non-invasive, longitudinal assessment using high-resolution pQCT in combination with finite element analysis.J Tissue Eng Regen Med.2011;5(5): 415-420.[3] Patwardhan S,Shyam AK,Mody RA,et al.Reconstruction of bone defects after osteomyelitis with nonvascularized fibular graft: a retrospective study in twenty-six children.J Bone and Joint Surg Am. 2013;95(9):e56,S1.[4] 李远辉,杨运发,胡汉生,等.带血管腓骨移植修复四肢大段骨缺损:可有效促进骨愈合[J].中国组织工程研究, 2015,19(11):1641-1646.[5] Chatterjea A,Meijer G,van Blitterswijk C,et al.Clinical application of human mesenchymal stromal cells for bone tissue engineering.Stem Cells Int.2010;2010:215625.[6] Zhong WJ,Sumita Y,Ohba S,et al.In Vivo Comparison of the Bone Regeneration Capability of Human Bone Marrow Concentrates vs. Platelet-Rich Plasma.PloS One.2012;7(7):e40833.[7] Schmitt CM,Doering H,Schmidt T,et al.Histological results after maxillary sinus augmentation with Straumann(R) BoneCeramic, Bio-Oss(R), Puros(R), and autologous bone. A randomized controlled clinical trial. Clin Oral Implan Res.2013;24(5):576-585.[8] Chiodo CP,Hahne J,Wilson MG,et al.Histological Differences in Iliac and Tibial Bone Graft.Foot Ankle Int.2010;31(5):418-422.[9] Hyer CF,Berlet GC,Bussewitz BLW,et al.Quantitative Assessment of the Yield of Osteoblastic Connective Tissue Progenitors in Bone Marrow Aspirate from the Iliac Crest, Tibia, and Calcaneus.J Bone Joint Surg Am.2013;95A(14):1312-1316.[10] [10]Smith CA,Richardson SM,Eagle MJ,et al.The use of a novel bone allograft wash process to generate a biocompatible, mechanically stable and osteoinductive biological scaffold for use in bone tissue engineering.J Tissue Eng Regen Med.2015;9(5):595-604.[11] 左健,康建敏,潘乐.同种异体骨移植用于骨缺损修复的应用现状[J].中国组织工程研究,2012,16(18): 3395-3398.[12] Li J,Wang Z,Guo Z,et al.The Use of Allograft Shell With Intramedullary Vascularized Fibula Graft for Intercalary Reconstruction After Diaphyseal Resection for Lower Extremity Bony Malignancy.J Surg Oncol.2010;102(5):368-374.[13] Wei L,Miron RJ,Shi B,et al.Osteoinductive and Osteopromotive Variability among Different Demineralized Bone Allografts.Clin Implant Dent Res.2015;17(3):533-542.[14] Sbordone C,Toti P,Guidetti F,et al.Volumetric changes after sinus augmentation using blocks of autogenous iliac bone or freeze-dried allogeneic bone. A non-randomized study. J Craniomaxillofac Surg. 2014;42(2):113-118.[15] Soardi CM,Zaffe D,Motroni A,et al.Quantitative Comparison of Cone Beam Computed Tomography and Microradiography in the Evaluation of Bone Density after Maxillary Sinus Augmentation: A Preliminary Study. Clin Implant Dent Relat Res.2014;16(4):557-564.[16] Ghanaati S,Barbeck M,Booms P,et al.Potential lack of "standardized" processing techniques for production of allogeneic and xenogeneic bone blocks for application in humans.Acta Biomater.2014;10(8): 3557-3562.[17] Kubosch EJ,Bernstein A,Wolf L,et al.Clinical trial and in-vitro study comparing the efficacy of treating bony lesions with allografts versus synthetic or highly-processed xenogeneic bone grafts. BMC Musculoskel Dis.2016;17:77.[18] 张屹,陈建常,史振满.异种骨支架及其衍生材料治疗骨缺损的研究现状与进展[J].中国矫形外科杂志,2014, 22(14):1277-1279.[19] Gruskin E,Doll BA,Futrell FW,et al.Demineralized bone matrix in bone repair: history and use.Adv Drug Deliver Rev.2012;64(12):1063-1077.[20] Schubert T,Lafont S,Beaurin G,et al.Critical size bone defect reconstruction by an autologous 3D osteogenic-like tissue derived from differentiated adipose MSCs.Biomaterials.2013;34(18):4428-4438.[21] Hou T,Li Z,Luo F,et al.A composite demineralized bone matrix--self assembling peptide scaffold for enhancing cell and growth factor activity in bone marrow.Biomaterials.2014;35(22):5689-5699.[22] van Bergen CJ,Kerkhoffs GM,Ozdemir M,et al.Demineralized bone matrix and platelet-rich plasma do not improve healing of osteochondral defects of the talus: an experimental goat study. Osteoarthr Cartilag.2013;21(11):1746-1754.[23] Xing J,Mei T,Luo K,et al.A nano-scaled and multi-layered recombinant fibronectin/cadherin chimera composite selectively concentrates osteogenesis-related cells and factors to aid bone repair.Acta Biomater. 2017;53:470-482.[24] 毛克政,毛克亚,程自申,等.nHA/α-CSH复合植骨材料的研制及其固化时间和抗压强度测定[J].医用生物力学,2013,28(3):333-337.[25] Trombelli L,Simonelli A,Pramstraller M,et al.Single Flap Approach With and Without Guided Tissue Regeneration and a Hydroxyapatite Biomaterial in the Management of Intraosseous Periodontal Defects. J Periodontol.2010;81(9):1256-1263.[26] Wu XH,Wu ZY,Su JC,et al.Nano-hydroxyapatite promotes self-assembly of honeycomb pores in poly(L-lactide) films through breath-figure method and MC3T3-E1 cell functions.Rsc Adv.2015;5(9): 6607-6616.[27] 宋华,任向前,未东兴.纳米羟基磷灰石对缺损骨再生的影响[J].中国组织工程研究,2015,19(8):1155-1159.[28] Atak BH,Buyuk B,Huysal M,et al.Preparation and characterization of amine functional nano-hydroxyapatite/chitosan bionanocomposite for bone tissue engineering applications. Carbohydr Polym. 2017;164: 200-213.[29] Venkatesan J,Kim SK.Nano-hydroxyapatite composite biomaterials for bone tissue engineering--a review.J Biomed Nanotechnol. 2014;10(10): 3124-3140.[30] Zhu Y,Yang Q,Yang M,et al. Protein Corona of Magnetic Hydroxyapatite Scaffold Improves Cell Proliferation via Activation of Mitogen-Activated Protein Kinase Signaling Pathway.ACS Nano.2017; 11(4):3690-3704.[31] Jakus AE,Rutz AL,Jordan SW,et al.Hyperelastic "bone": A highly versatile, growth factor-free, osteoregenerative, scalable, and surgically friendly biomaterial.Sci Transl Med.2016;8(358): 358ra127.[32] Pina S,Oliveira JM,Reis RL.Natural-based nanocomposites for bone tissue engineering and regenerative medicine: a review.Adv Mater. 2015;27(7):1143-1169.[33] Castro AG,Polini A,Azami Z,et al.Incorporation of PLLA micro-fillers for mechanical reinforcement of calcium-phosphate cement.J Mech Behav Biomed.2017;71:286-294.[34] Fukuda N,Tsuru K,Mori Y,et al.Fabrication of self-setting beta-tricalcium phosphate granular cement.J Biomed Mater Res B Appl Biomater.2017.doi: 10.1002/jbm.b.33891. [Epub ahead of print][35] Zhang J,Liu W,Schnitzler V,et al.Calcium phosphate cements for bone substitution: chemistry, handling and mechanical properties.Acta Biomater.2014;10(3):1035-1049.[36] Zhang JT,Liu WZ,Gauthier O,et al.A simple and effective approach to prepare injectable macroporous calcium phosphate cement for bone repair: Syringe-foaming using a viscous hydrophilic polymeric solution. Acta Biomater.2016;31:326-338.[37] Zhao L,Burguera EF,Xu HH,et al.Fatigue and human umbilical cord stem cell seeding characteristics of calcium phosphate-chitosan-biodegradable fiber scaffolds.Biomaterials. 2010; 31(5):840-807. [38] 《中国组织工程研究与临床康复》杂志社学术部.医用金属材料相关产品的应用现状和发展趋势[J].中国组织工程研究与临床康复, 2010,14(51): 9621-9622.[39] Albrektsson T,Jansson T,Lekholm U.Osseointegrated dental implants. Dent Clin North Am.1986;30(1): 151-174.[40] Strakowska P,Beutner R,Gnyba M,et al.Electrochemically assisted deposition of hydroxyapatite on Ti6Al4V substrates covered by CVD diamond films - Coating characterization and first cell biological results.Mater Sci Eng C Mater Biol Appl.2016;59:624-635.[41] Balla VK,Bodhak S,Bose S,et al.Porous tantalum structures for bone implants: fabrication, mechanical and in vitro biological properties.Acta Biomater.2010;6(8):3349-3359.[42] Balla VK,Banerjee S,Bose S,et al.Direct laser processing of a tantalum coating on titanium for bone replacement structures.Acta Biomater. 2010;6(6):2329-2334.[43] 耿丽鑫,甘洪全,王茜,等.国产多孔钽对成骨细胞生物相容性及其相关成骨基因表达的影响[J].第三军医大学学报,2014,36(11):1163-1167.[44] Jahan K,Tabrizian M.Composite biopolymers for bone regeneration enhancement in bony defects. Biomater Sci-UK.2016;4(1):25-39.[45] Mottaghitalab F,Hosseinkhani H,Shokrgozar MA,et al.Silk as a potential candidate for bone tissue engineering.J Control Release. 2015;215:112-128.[46] 陈亮.丝素蛋白支架在骨组织工程中的应用进展[J].中华骨科杂志, 2016, 14(36):932-937. [47] Perrone GS, Leisk GG, Lo TJ, et al.The use of silk-based devices for fracture fixation.Nat Commun.2014;5:3385.[48] Ran J,Hu J,Sun G,et al.A novel chitosan-tussah silk fibroin/nano- hydroxyapatite composite bone scaffold platform with tunable mechanical strength in a wide range.Int J Biol Macromol. 2016;93 (Pt A):87-97.[49] Yassin MA,Mustafa K,Xing Z,et al.A Copolymer Scaffold Functionalized with Nanodiamond Particles Enhances Osteogenic Metabolic Activity and Bone Regeneration.Macromol Biosci. 2017;17(6).doi: 10.1002/mabi.201600427. Epub 2017 Jan 24. [50] Puppi D,Mota C,Gazzarri M,et al.Additive manufacturing of wet-spun polymeric scaffolds for bone tissue engineering.Biomed Microdevices. 2012;14(6):1115-1127.[51] Chen X,Gleeson SE,Yu T,et al.Hierarchically Ordered Polymer Nanofiber Shish Kebabs as a Bone Scaffold Material.J Biomed Mater Res A.2017;105(6):1786-1798.[52] Ding Y,Li W,Muller T,et al.Electrospun Polyhydroxybutyrate/Poly (epsilon-caprolactone)/58S Sol-Gel Bioactive Glass Hybrid Scaffolds with Highly Improved Osteogenic Potential for Bone Tissue Engineering.ACS Appl Mater Inter.2016;8(27):17098-17108.[53] Yousefi AM,James PF,Akbarzadeh R,et al. Prospect of Stem Cells in Bone Tissue Engineering: A Review. Stem Cells Int. 2016;2016: 6180487.[54] Bose S,Roy M,Bandyopadhyay A.Recent advances in bone tissue engineering scaffolds.Trends Biotechnol.2012;30(10):546-554.[55] Yan LP,Silva-Correia J,Correia C,et al.Bioactive macro/micro porous silk fibroin/nano-sized calcium phosphate scaffolds with potential for bone-tissue-engineering applications.Nanomedicine (Lond). 2013;8(3): 359-378.[56] Nejadnik MR,Yang X,Bongio M,et al.Self-healing hybrid nanocomposites consisting of bisphosphonated hyaluronan and calcium phosphate nanoparticles.Biomaterials. 2014;35(25): 6918-6929.[57] Chae T,Yang H,Leung V,et al.Novel biomimetic hydroxyapatite/alginate nanocomposite fibrous scaffolds for bone tissue regeneration.J Mater Sci Mater Med.2013;24(8):1885-1894.[58] Salter E,Goh B,Hung B,et al.Bone tissue engineering bioreactors: a role in the clinic?. Tissue Eng Part B Rev.2012;18(1):62-75.[59] Brunello G,Sivolella S,Meneghello R,et al.Powder-based 3D printing for bone tissue engineering. Biotechnol Adv.2016;34(5):740-753.[60] Kang HW,Lee SJ,Ko IK,et al.A 3D bioprinting system to produce human-scale tissue constructs with structural integrity.Nat Biotechnol. 2016;34(3):312-319.[61] Rezvani Z,Venugopal JR,Urbanska AM,et al.A bird's eye view on the use of electrospun nanofibrous scaffolds for bone tissue engineering: Current state-of-the-art, emerging directions and future trends. Nanomedicine.2016;12(7):2181-2200.[62] Evans CH.Gene delivery to bone.Adv Drug Deliver Rev. 2012;64(12): 1331-1340.[63] Baltzer AW,Lattermann C,Whalen JD,et al.Genetic enhancement of fracture repair: healing of an experimental segmental defect by adenoviral transfer of the BMP-2 gene.Gene Ther.2000;7(9):734-739.[64] Betz VM,Betz OB,Glatt V,et al.Healing of segmental bone defects by direct percutaneous gene delivery: effect of vector dose.Hum Gene Ther.2007;18(10):907-915.[65] Zhang Y,Cheng N,Miron R,et al.Delivery of PDGF-B and BMP-7 by mesoporous bioglass/silk fibrin scaffolds for the repair of osteoporotic defects.Biomaterials.2012;33(28):6698-6708.[66] Lu CH,Chang YH,Lin SY,et al.Recent progresses in gene delivery-based bone tissue engineering. Biotechnol Adv. 2013;31(8): 1695-1706. |
| [1] | Pu Rui, Chen Ziyang, Yuan Lingyan. Characteristics and effects of exosomes from different cell sources in cardioprotection [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(在线): 1-. |
| [2] | Zhang Tongtong, Wang Zhonghua, Wen Jie, Song Yuxin, Liu Lin. Application of three-dimensional printing model in surgical resection and reconstruction of cervical tumor [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1335-1339. |
| [3] | Zhang Chao, Lü Xin. Heterotopic ossification after acetabular fracture fixation: risk factors, prevention and treatment progress [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1434-1439. |
| [4] | Zhou Jihui, Li Xinzhi, Zhou You, Huang Wei, Chen Wenyao. Multiple problems in the selection of implants for patellar fracture [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1440-1445. |
| [5] | Wang Debin, Bi Zhenggang. Related problems in anatomy mechanics, injury characteristics, fixed repair and three-dimensional technology application for olecranon fracture-dislocations [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1446-1451. |
| [6] | Ji Zhixiang, Lan Changgong. Polymorphism of urate transporter in gout and its correlation with gout treatment [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1290-1298. |
| [7] | Yuan Mei, Zhang Xinxin, Guo Yisha, Bi Xia. Diagnostic potential of circulating microRNA in vascular cognitive impairment [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1299-1304. |
| [8] | Wang Xianyao, Guan Yalin, Liu Zhongshan. Strategies for improving the therapeutic efficacy of mesenchymal stem cells in the treatment of nonhealing wounds [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1081-1087. |
| [9] | Wan Ran, Shi Xu, Liu Jingsong, Wang Yansong. Research progress in the treatment of spinal cord injury with mesenchymal stem cell secretome [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1088-1095. |
| [10] | Liao Chengcheng, An Jiaxing, Tan Zhangxue, Wang Qian, Liu Jianguo. Therapeutic target and application prospects of oral squamous cell carcinoma stem cells [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1096-1103. |
| [11] | Zhao Min, Feng Liuxiang, Chen Yao, Gu Xia, Wang Pingyi, Li Yimei, Li Wenhua. Exosomes as a disease marker under hypoxic conditions [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1104-1108. |
| [12] | Xie Wenjia, Xia Tianjiao, Zhou Qingyun, Liu Yujia, Gu Xiaoping. Role of microglia-mediated neuronal injury in neurodegenerative diseases [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1109-1115. |
| [13] | Li Shanshan, Guo Xiaoxiao, You Ran, Yang Xiufen, Zhao Lu, Chen Xi, Wang Yanling. Photoreceptor cell replacement therapy for retinal degeneration diseases [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1116-1121. |
| [14] | Jiao Hui, Zhang Yining, Song Yuqing, Lin Yu, Wang Xiuli. Advances in research and application of breast cancer organoids [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1122-1128. |
| [15] | Wang Shiqi, Zhang Jinsheng. Effects of Chinese medicine on proliferation, differentiation and aging of bone marrow mesenchymal stem cells regulating ischemia-hypoxia microenvironment [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1129-1134. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||