Chinese Journal of Tissue Engineering Research ›› 2020, Vol. 24 ›› Issue (13): 2095-2101.doi: 10.3969/j.issn.2095-4344.1866
Previous Articles Next Articles
Research and progress in the correlation between exosomes from different sources and tumorigenesis
Cui Guoning, Liu Xiping, Hu Junrui, Li Peiqing
- Gansu University of Chinese Medicine, Lanzhou 730000, Gansu Province, China
-
Received:2019-05-20Revised:2019-05-25Accepted:2019-07-17Online:2020-05-08Published:2020-03-10 -
Contact:Liu Xiping, MD, Professor, Gansu University of Chinese Medicine, Lanzhou 730000, Gansu Province, China -
About author:Cui Guoning, MD, Gansu University of Chinese Medicine, Lanzhou 730000, Gansu Province, China -
Supported by:the National Natural Science Foundation Project, No. 81860813
CLC Number:
Cite this article
Cui Guoning, Liu Xiping, Hu Junrui, Li Peiqing. Research and progress in the correlation between exosomes from different sources and tumorigenesis[J]. Chinese Journal of Tissue Engineering Research, 2020, 24(13): 2095-2101.
share this article
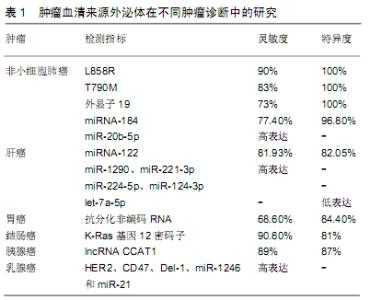
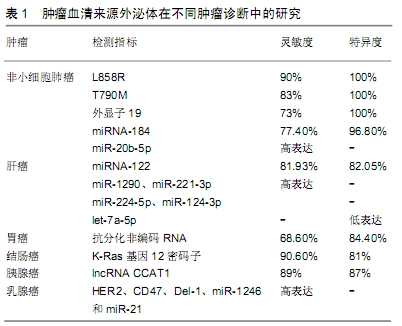
2.1 肿瘤血清来源外泌体与肿瘤诊断 外泌体广泛存在于人的体液中(血清、尿液、胸腔积液、唾液等),其中含有多种生物活性分子(miRNA、lncRNA、mRNA、蛋白和脂质等)[6],外泌体可反映细胞的病理状况,被认为是一种新型的潜在诊断标准。目前血清外泌体作为一种辅助诊断标准的研究主要集中在肿瘤标志物方面,并且取得了可观的研究成果。 2.1.1 用于非小细胞肺癌诊断的研究 非小细胞肺癌是最常见的肺癌形式,其最常见的遗传改变是表皮生长因子受体(epidermal growth factor receptor,EGFR)基因的突变,频率在10%-40%之间。基于qPCR的测试,从110名非小细胞肺癌患者的血清中提取外泌体RNA/DNA和cfDNA来探测表皮生长因子受体的突变,结果表明:L858R的总灵敏度为90%,特异性为100%;T790M的总灵敏度为83%,特异性为100%;外显子19的总灵敏度为73%,特异性为96%[7]。在血清外泌体miR-20b-5p对非小细胞肺癌的诊断价值研究中发现,血清外泌体miR-20b-5p在非小细胞肺癌中高表达,且具有较高诊断价值,可作为辅助非小细胞肺癌诊断的新型生物标志物[8];此外,刘玉山等[9]研究表明血清外泌体miRNA-184诊断非小细胞肺癌的灵敏度为77.4%,特异度为96.8%;与肺炎患者、健康体检者比,非小细胞肺癌患者血清外泌体miRNA-184的表达水平较高,可作为诊断早期非小细胞肺癌的潜在生物学标志物。 2.1.2 用于肝癌诊断的研究 在血清外泌体对肝癌细胞的诊断研究中发现,血清外泌体miR-1290在HBV相关肝细胞癌患者中升高,诊断效能较好,有望成为诊断HBV相关肝细胞癌的血清学标志物[10]。此外,血清外泌体来源的miRNA-122诊断肝癌的敏感度为81.93%、特异度为82.05%,其可作为一种新的肿瘤标志物用于原发性肝癌的早期临床诊断[11]。肝癌细胞外泌体中差异表达的miRNAs在肝细胞癌中的诊断应用价值:miR-221-3p、miR-224-5p在肝细胞癌组外泌体中的表达水平显著高于健康组、慢性乙型肝炎患者组和肝硬化患者组(P < 0.01),miR-124-3p、let-7a-5p在肝细胞癌组外泌体中的表达水平显著低于其他各组(P < 0.05)[12],提示血清外泌体中的miRNAs可能成为肝细胞癌的候选标志物。 2.1.3 用于胃癌诊断的研究 在血清外泌体对胃癌的诊断研究中发现,检测胃癌患者血清外泌体中抗分化非编码RNA(DANCR)的表达水平,其敏感性为68.6%,特异性为84.4%[13],提示胃癌患者血清外泌体中抗分化非编码RNA表达水平升高有望成为胃癌诊断的新指标。 2.1.4 用于结肠癌诊断的研究 在血清外泌体对结肠癌细胞的诊断研究中发现,结直肠癌患者血清外泌体代替肿瘤组织进行DNA中K-Ras基因12密码子突变检测的灵敏度为90.6%,一致性为81%[14],说明血清外泌体DNA可用于检测肿瘤相关突变,指导肿瘤的个体化治疗。外泌体作为一种纳米级囊泡,可通过将核酸和蛋白质转移到靶细胞和组织中,近年来研究发现MicroRNAs (miRs)在外泌体中的传递和生理、病理过程有关。肿瘤传递的miRs在肿瘤微环境中与基质细胞相互作用,调节肿瘤进展、血管生成、转移和免疫逃逸[15]。越来越多的证据表明,一些外泌体miRs(miR-150、miR-21、miR-192、let-7a、miR-223和miR-23a)在结肠癌中具有诊断和预后价值,这些新的非侵入性生物标记物,为结直肠癌患者早期检测和风险评估提供了新见解[16]。 2.1.5 用于胰腺癌诊断的研究 在血清外泌体对胰腺癌细胞的诊断研究中发现,外泌体中lncRNA CCAT1检测胰腺癌的敏感度、特异性和准确性分别为89%、87%和89%,显著高于CA19-9(P < 0.05),可作为预测胰腺癌患者不良预后的独立因素[17]。 2.1.6 用于乳腺癌诊断的研究 在血清外泌体对乳腺癌细胞的诊断研究中发现,外泌体PD-1和CTLA-4可用于乳腺癌的早期诊断,外泌体MMP9可作为一个有效的靶点应用于乳腺癌转移的早期预警和术后监测[18]。通过对921例乳腺癌患者进行研究发现,乳腺癌患者的外泌体生物标记物(HER2、CD47、Del-1、miR-1246和miR-21)明显高于健康对照组,外泌体GSTP1和trpc5与化疗耐药性有关,携带TRPC5、NANOG、NEUROD1、HTR7、KISS1R和HOXC的外泌体与总生存率、无病生存率相关,一些外泌体蛋白质(HER2、KDR、CD49d、CXCR4和CD44)以及小RNA(miR-340-5p、miR-17-5p、miR-130a-3p、miR-93-5p)与肿瘤复发或远处转移有 关[19]。 综上,检测肿瘤来源血清外泌体对肿瘤的诊断具有一定的研究价值,其有可能成为肿瘤检测的一种潜在替代诊断标志物,见表1,不同的肿瘤细胞所营造的肿瘤微环境不同,其产生的外泌体可能存在差异,进一步筛选不同肿瘤来源血清外泌体中的特异性肿瘤标志物将为肿瘤的早期诊断提供参考依据。 "
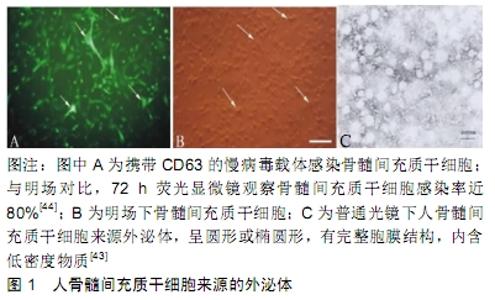
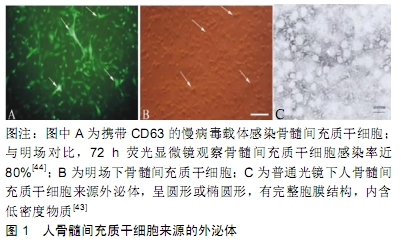
2.2 不同肿瘤细胞来源外泌体与肿瘤细胞的调控研究 外泌体具有低毒性、低免疫原性和渗透性好等优势,在介导肿瘤的发生、发展、侵袭及转移等方面发挥着重要作用[20]。从肿瘤细胞分泌的外泌体称为肿瘤来源外泌体(tumor-derived exosome,TEX),除了具备外泌体的一般特征外,更有其特殊性[21]。了解外泌体对肿瘤细胞的调控作用、可能的调控机制及肿瘤外泌体对肿瘤细胞生物学特性的影响,有助于提供新的治疗思路。近年来,国内外研究肿瘤来源外泌体与肿瘤之间的关系主要集中在其促进肿瘤发生、发展和抑制免疫系统等方面。 2.2.1 促进肿瘤细胞迁移、侵袭、增殖及生长 不同肿瘤细胞来源的外泌体对肿瘤具有一定的调控作用,在前列腺癌细胞PC-3M-2B4和PC-3M-IE8条件培养基中外泌体诱导后,巨噬细胞中CD206荧光表达显著增高,白细胞介素10、白细胞介素1β及白细胞介素12等炎症因子的表达水平与M2/TAM亚型巨噬细胞的表达谱一致,说明前列腺癌细胞来源的外泌体能诱导巨噬细胞极化为M2表型[22];前列腺癌细胞外泌体还可作用于基质细胞WPMY-1,使其高表达多种癌相关成纤维细胞相关分子,促进EGFR和ERK1/2的磷酸化,增强其迁移和侵袭能力[23]。在肝癌细胞外泌体的研究中发现,高表达ANXA2的肝癌干细胞外泌体对肝癌细胞恶性生物学特性具有调控作用,其可促进肝癌细胞系HepG2、SNU398的侵袭和转移,与肿瘤TNM分期和转移显著相关[24]。在胃癌细胞外泌体的研究中发现,胃癌来源外泌体可通过上调细胞丝氨酸/苏氨酸激酶15(STK15)的表达促进胃癌细胞增殖[25]。口腔癌患者外周血循环外泌体可促进口腔癌细胞的增殖、迁移和侵袭[26]。此外,肿瘤来源外泌体可通过调节肿瘤微环境促进肿瘤细胞生长及影响放化疗敏感性等多方式参与肿瘤的诊断和治 疗[27]。 2.2.2 调节免疫反应 肿瘤来源外泌体还涉及肿瘤的免疫逃逸过程,其可影响免疫抑制细胞的分化和激活,具有调节抗原呈递,抑制自然杀伤细胞的活性,并诱导相关效应细胞的凋亡[28]。与此同时,肝癌细胞PLC/PRF/5来源的外泌体高表达长链非编码RNA LINC ROR,巨噬细胞中LINC ROR基因沉默后,在脂多糖诱导的炎症反应下,巨噬细胞促炎症因子白细胞介素1β的表达水平明显增强,说明肝癌细胞分泌的外泌体中LINC ROR能对邻近巨噬细胞的炎症反应产生调控作用[29],此外,研究发现肝癌细胞外泌体还携带大量的肿瘤抗原甲胎蛋白和热休克蛋白70、热休克蛋白90,其冲击树突状细胞后上调其表面分子如CD83、CD80、CD86的表达可促进T淋巴细胞增殖,增加T细胞介导的肿瘤特异性和非特异性杀伤效应[30]。 2.2.3 调控基因及蛋白 胃癌来源外泌体还可促进HLA-DRnegleukocytes中Dicer1、PTEN基因的表达[31];鼻咽癌外泌体microRNA可通过抑制Bim-caspase-9- caspase-3凋亡途径的活化从而抑制鼻咽癌中肿瘤相关巨噬细胞(tumor-associated macrophages,TAM)凋 亡[32]。综上,在多种肿瘤细胞外泌体的研究中发现,肿瘤细胞来源的外泌体具有肿瘤细胞的生物学特性,其可通过调节肿瘤微环境中肿瘤相关炎性因子、细胞因子、肿瘤相关基因及肿瘤相关巨噬细胞的表达,促进肿瘤的生长、增殖,增强肿瘤的侵袭与转移能力。目前已经证实肿瘤相关巨噬细胞可通过调控肿瘤细胞中磷酸甘油酸激酶PGK1的磷酸化来调控肿瘤细胞的糖酵解,从而促进肿瘤的发展[33],这为研究肿瘤来源外泌体的生物学功能奠定了基础。研究肿瘤来源外泌体的生物学功能,不仅为肿瘤的治疗提供治疗策略,也有助于研究更有效的肿瘤诊疗方法。 2.3 干细胞来源外泌体与肿瘤的发病相关性分析 2.3.1 干细胞与肿瘤的发病 骨髓间充质干细胞是起源于中胚层的一种多能干细胞,其具有低免疫原性、多向分化性及归巢的特性[34],在组织创伤修复中发挥重要作用,因而被广泛应用于组织与器官再生治疗的研究[35]。一些细胞生物学研究表明骨髓间充质干细胞在体内具有向肿瘤区域趋化的性质,是抗癌药物的潜在载体,将这种干细胞作为一种全新的具有生物活性的肿瘤靶向细胞传递载体倍受关注[36]。有研究表明经小鼠尾静脉注射骨髓间充质干细胞后,其首先会机械堵塞于肺部,然后逐渐向肺部的肿瘤结节迁移,呈现良好的肿瘤靶向 性[37]。将骨髓间充质干细胞与肿瘤细胞共培养可改变肿瘤细胞的生物学特性,例如人骨髓间充质干细胞与乳腺癌细胞共培养,可诱导乳腺癌细胞系发生上皮间质转 化[38],促进乳腺癌细胞的迁移和侵袭[39],人骨髓间充质干细胞还可改变鼻咽癌细胞形态并下调细胞黏附蛋白及增加细胞间质蛋白水平,参与鼻咽癌上皮间质转化[40]。此外,骨髓间充质干细胞还可促进结肠癌细胞HT29的增殖与迁移[41],进一步研究发现结肠癌微环境可诱导人骨髓间充质干细胞发生恶性转化[42]。因此,骨髓间充质干细胞与肿瘤的发生发展密切相关,其具有向肿瘤细胞归巢及趋化的特性,还可促进肿瘤细胞的迁移、增殖及恶性转化,是研究肿瘤治疗首选生物载体。 2.3.2 干细胞来源外泌体的鉴定及生物功能 正常人骨髓间充质干细胞分泌的外泌体形态近似圆形,直径在40-160 nm之间,见图1,具有CD9、CD63、Alix、CD81表达,其分泌量与接种细胞数呈线性关系,可抑制单个核细胞分泌干扰素γ,内含有免疫相关microRNA (miR-301、miR-22、miR-let-7a、miR-223、miR-let-7c),且可成功构建稳定表达绿色荧光蛋白的骨髓间充质干细胞[43-45],这些研究为骨髓间充质干细胞来源外泌体的鉴定提供科学参考依据。 "

外泌体作为骨髓间充质干细胞旁分泌效应的一种分泌物,其对固有免疫、适应性免疫和抗原提呈均具有明显的抑制作用[46]。有研究发现骨髓间充质干细胞来源外泌体可促进受损子宫内膜腺体增生,抑制纤维化发展,促进子宫内膜修复[47];其还可通过调节血清中各激素含量,促进卵泡发育,降低顺铂对卵巢的损害,修复卵巢功能[48]。此外,骨髓间充质干细胞来源外泌体可减轻脊髓损伤后的病理变化,改善运动功能,促进脊髓损伤后神经功能修复[49]。骨髓间充质干细胞来源外泌体可抑制哮喘小鼠气道炎症反应,逆转哮喘小鼠Foxp3+Treg/Th17的失衡[50]。骨髓间充质干细胞分泌的外泌体作为一种新型非细胞治疗的替代疗法,在体外培养条件下可促进软骨细胞的增殖和迁移[51]。骨髓间充质干细胞来源外泌体对睾丸缺血再灌注损伤具有抗氧化(升高超氧化物歧化酶、降低丙二醛)、抗炎、抗凋亡(降低caspase-3的表达)等作用[52]。综上,骨髓间充质干细胞来源外泌体具有干细胞的生物学特性,可通过调节免疫、调节激素含量、调节炎性反应、抗氧化等途径积极参与受损组织的修复作用,其有可能是骨髓间充质干细胞发挥治疗作用的关键所在,从而作为骨髓间充质干细胞的替代品发挥生物治疗作用。 2.3.3 干细胞来源外泌体与肿瘤的发病 (1)促进肿瘤作用:肿瘤的发生与肿瘤微环境密切相关,肿瘤微环境是由肿瘤细胞和多种基质细胞(内皮细胞、免疫细胞、成纤维细胞、脂肪细胞及间充质干细胞)组成[53],肿瘤的发生发展、侵袭与转移不仅取决于自身的特征,还与肿瘤细胞和肿瘤微环境中基质细胞间的相互作用相关,各种细胞分泌的外泌体通过旁分泌或自分泌信号转导通路发挥作用[54],细胞在活化过程中或者受到外界刺激时将引发一系列复杂的细胞内分泌变化,同时向细胞外释放脂质双层结构囊泡(一种可传递信息的囊泡小体),其介导的细胞间交流广泛,参与细胞与组织的生理病理过程,是细胞信号转导的主要调节因子,其作为细胞间信息传递的中枢,通过细胞内吞作用进入细胞内,从而介导细胞与细胞之间的交流[55],骨髓间充质干细胞与肿瘤细胞均可分泌外泌体,研究发现外泌体在肿瘤的发生、发展、转移及耐药过程中起着关键作用[56]。骨髓间充质干细胞与肿瘤细胞间的交流可能是通过分泌的外泌体发挥作用。最新研究表明骨髓间充质干细胞来源外泌体能够增加小鼠乳腺癌细胞4T1的增殖、迁移和侵袭能力,可能与上调P13K/Akt信号通路的表达相 关[57];在肿瘤中,干细胞衍生的外泌体通过向邻近细胞提供独特的小RNA物种来调节肿瘤标志,促进肿瘤的发生发展[58],VALLABHANENI等[59]研究发现干细胞分泌的细胞外囊泡中存在支持肿瘤的miRNA,如miRNA-21与miRNA-34a。由此发现,骨髓间充质干细胞来源的外泌体对肿瘤具有促进作用。 (2)干细胞来源外泌体激活HH信号通路调控肿瘤:总结文献发现,骨髓间充质干细胞来源外泌体具有促进肿瘤发生发展的作用,其与肿瘤细胞间的交流可能是通过外泌体介导。肿瘤的增殖与分化与多种信号通路相关,HH信号通路在肿瘤的发生发展中扮演重要的角色。HH信号通路由HH配体、两个跨膜蛋白Patched (Patch1)、Smoh(Smoothened)及下游转录因子Gli等组成,Gli又分为Gli1、Gli2、Gli3。在哺乳动物中,HH蛋白主要由SHH(Sonic Hedgehog)、IHH(Indian hedgehog)、DHH(Desert hedgehog)等分泌蛋白组成。在胚胎发育中,SHH对细胞的增殖与分化具有重要作用,调节内皮细胞生长,促进细胞迁移并刺激新血管的形成[60-61]。为探求肿瘤治疗的靶点,人们发现调控HH信号通路可介导肿瘤的发生与发展。HH信号通路相关基因、蛋白及转录因子的表达与肿瘤的发生基本一致,其中以SHH表达关系最为密切。贾姗姗等[62]通过观察发现SHH、Ptch1、Gli1mRNA的阳性表达细胞主要分布在肝脏细胞损伤区域、癌结节增生部位及癌旁组织,其阳性表达高于对照组(P < 0.05),说明SHH信号通路可能参与肝癌细胞的发生。刘庆生等[63]通过对胃癌前病变大鼠SHH信号通路相关基因及蛋白检测,发现随着造模时间延长,模型组大鼠胃黏膜萎缩及异常增生逐渐加重,Gli1、Smo、Shh、CyclinD1、CyclinE1及c-Myc mRNA的表达不同程度升高(P < 0.05),Ptch1和SuFu表达下降(P > 0.05),说明在胃癌形成过程中存在SHH信号通路的激活,其参与胃癌前病变的发生。在胃癌干细胞研究中发现,SHH、Gli1、Wnt2及β-catenin在胃癌干细胞中的阳性表达率均显著高于癌旁组织(P < 0.05)。各细胞因子在胃癌干细胞中的表达均呈正相关(P < 0.05),说明在胃癌干细胞中SHH及Wnt/β-catenin信号通路均被激活,二者互相作用可能参与了胃癌的发生发展[64]。SHH信号通路也参与乳腺癌的调控,刘志勇等[65]通过检测334例乳腺癌组织中SHH信号通路相关蛋白的表达,发现SHH信号通路的激活与乳腺癌的侵袭相关,SHH、Ptch1、Smo、Gli1、Gli2和Gli3的表达在表型之间存在差异(P < 0.05),Gli2的表达与较差的整体生存结果相关(P=0.012),其可作为乳腺癌的预后指标。 Gli1作为SHH信号通路下游核转录因子,其高表达参与肿瘤的发生。徐又海等[66]研究采用RT-PCR对30例多发性骨髓瘤患者及20例非恶性血液病患者中SHH及Gli mRNA的表达进行检测,发现SHH与Gli1 mRNA在多发性骨髓瘤患者中高表达(P < 0.05)。许秋然等[67]研究发现肝细胞癌组织中Gli1蛋白及mRNA含量明显高于癌旁正常肝组织(P < 0.05),肝细胞癌组织中Gli1蛋白表达与SHH蛋白表达呈明显正相关(P < 0.05)。Gli1、SHH高表达可能诱导肝癌发生与侵袭、转移。人肺癌组织中的HH信号通路主要成分为SHH、Gli1和VEGF,通过免疫组化及PCR检测发现其在肺癌组织中高表达,与肿瘤发展密切相关[68]。Ptch1与Smoh作为HH信号通路中的跨膜蛋白,为探求Ptch1与SHH、Gli1等在肿瘤发生过程中的关系,徐林汇等[69]通过免疫组化对48例前列腺组织SHH、Ptch1和Gli1蛋白进行染色,用Image Pro Plus (IPP)图像分析软件定量检测蛋白表达阳性,与正常前列腺组织相比,3种信号因子在前列腺癌组织中均高表达,其表达程度与前列腺癌的临床病理特征具有一定的相关性。通过对HH信号通路中的功能性基因SHH和受体蛋白Smo基因定量检测,发现慢性粒细胞白血病中SHH、Smo表达高于正常组(P < 0.05)[70]。在临床研究中,胰腺癌组织中的SHH蛋白表达高于胰腺良性病变组织(P < 0.05)[71],食管鳞癌组织中SHH的阳性表达率为75%,明显高于癌旁组织(P < 0.05)[72],鼻咽癌HH信号通路成员SHH和Ptch1基因表达高于正常鼻咽黏膜组织(P < 0.05)[73]。 综上,SHH信号通路的激活与肿瘤的发生密切相关。SHH信号通路由分泌型信号糖蛋白SHH、膜结合受体Ptch1、跨膜蛋白Smo及下游的转录因子Gli等组成。在脊椎动物中,这一调节蛋白主要受Cos2蛋白丝氨酸/苏氨酸激酶(Fu)和Fu抑制物(SuFu)组成,SuFu可与Gli1结合抑制其活性,SHH与Ptch1结合使Ptch1与Smo脱离,Smo活化后激活Gli,Gli进入细胞核调控靶基因的转录[74]。在肿瘤过程中,SHH、Ptch1、Smo、Gli1、Gli2和Gli3参与其侵袭与转移,SHH、Ptch1、Smo、Gli1等高表达对肿瘤的形成具有促进作用,虽然有研究证明Gli1、Gli2和Gli3在肿瘤过程中存在表型差异,但其之间的关联尚不清楚。骨髓间充质干细胞来源外泌体具有促进肿瘤发生发展的作用,外泌体可能是通过激活SHH信号通路介导肿瘤的调控作用,研究骨髓间充质干细胞来源外泌体激活SHH信号通路调控肿瘤的侵袭与转移,将为揭示肿瘤的发病机制及可能的治疗途径提供参考。 2.3.4 肿瘤干细胞来源外泌体与肿瘤的发病 肿瘤干细胞是肿瘤细胞的一种亚群细胞,可从多种肿瘤细胞中分离出来[75-76],对肿瘤干细胞来源外泌体进行研究发现,肺癌干细胞来源外泌体能增强肺癌细胞增殖活性,可通过增强肺癌细胞MDR-1、ABCG2和LRR等耐药相关蛋白的表达诱导肺癌细胞对化疗药物的耐药[77];Piwil2诱导肿瘤干细胞(Piwil2-iCSC)来源外泌体能促进人脐带间充质干细胞的增殖、迁移及侵袭,但是未出现肿瘤样异质性改变[78]。胶质母细胞瘤是人类最致命的癌症之一[79],在胶质瘤微环境中,胶质瘤干细胞来源外泌体可以促进血管内皮细胞的增殖和迁移[80]。以上可见,肿瘤干细胞来源外泌体保存了肿瘤干细胞的生物学特性,通过研究肿瘤干细胞分泌外泌体与耐药基因之间的相关机制,有可能发现肿瘤治疗的潜在靶点,有待进一步深入研究。 "

| [1] COLOMBO M, RAPOSO G, THÉRY C. Biogenesis, secretion, and intercellular interactions of exosomes and other extracellular vesicles. Annu Rev Cell Dev Biol. 2014;30:255-289. [2] 刘洁,万璐,戎柯纬,等.外泌体在病毒感染中的作用[J].华中科技大学学报(医学版), 2019,48(1):104-108. [3] RAPOSO G, NIJMAN HW, STOORVOGEL W, et al. B lymphocytes secrete antigen-presenting vesicles. J Exp Med. 1996;183(3): 1161-1172. [4] CORRADO C, RAIMONDO S, CHIESI A, et al. Exosomes as intercellular signaling organelles involved in health and disease: basic science and clinical applications. Int J Mol Sci. 2013;14(3):5338-5366. [5] SHARMA A. Role of stem cell derived exosomes in tumor biology. Int J Cancer. 2018;142(6):1086-1092. [6] YU X, ODENTHAL M, FRIES JW. Exosomes as miRNA Carriers: Formation-Function-Future. Int J Mol Sci. 2016;17(12): E2028. [7] CASTELLANOS-RIZALDOS E, ZHANG X, TADIGOTLA VR, et al. Exosome-based detection of activating and resistance EGFR mutations from plasma of non-small cell lung cancer patients. Oncotarget. 2019;10(30):2911-2920. [8] 魏萍,杜鲁涛,王卿,等.血清外泌体miR-20b-5p对非小细胞肺癌的诊断价值[J].山东大学学报(医学版), 2019,57(4):91-96. [9] 刘玉山,闫红江,李春雨.血清外泌体miRNA-184在非小细胞肺癌中的表达水平及其诊断效能[J].癌症进展, 2019,17(4):411-414. [10] 高斌,熊莹晖,黄泽炳,等.乙肝相关性肝细胞癌患者血清外泌体miR-1290水平的变化及其诊断价值[J].中国普通外科杂志, 2019,28(1):31-38. [11] 张云,庹敏,刘胜武.血清外泌体来源的miRNA-122对肝癌诊断的研究[J].检验医学与临床, 2017,14(9):1260-1261. [12] 纪奇峰,祝春来,王伟,等.肝细胞癌患者血清外泌体microRNA表达鉴定[J].现代生物医学进展, 2018,18(22):4213-4218. [13] 李阳,潘磊,梁炜,等.胃癌患者血清外泌体中DANCR表达及其临床意义[J].临床检验杂志, 2017,35(3):171-174. [14] 崔琮,靳杨,谭招丽,等.结直肠癌患者血清外泌体代替肿瘤组织检测K-Ras基因突变的研究[J].临床肿瘤学杂志, 2017,22(5):395-399. [15] TOMASETTI M, LEE W, SANTARELLI L, et al. Exosome-derived microRNAs in cancer metabolism: possible implications in cancer diagnostics and therapy. Exp Mol Med. 2017;49(1):e285. [16] HOSSEINI M, KHATAMIANFAR S, HASSANIAN SM, et al. Exosome- Encapsulated microRNAs as Potential Circulating Biomarkers in Colon Cancer. Curr Pharm Des. 2017;23(11):1705-1709. [17] 任潇凡,李志花.外泌体lncRNA CCAT1在胰腺癌中的表达及其临床意义[J].岭南现代临床外科, 2019,19(1):23-27. [18] 王爱红,赵菊梅,王明全. PD-1、CTLA-4和MMP9在伴或不伴淋巴结转移乳腺癌患者外泌体中的表达[J].现代免疫学, 2019,39(2):110-114. [19] WANG M, JI S, SHAO G, et al. Effect of exosome biomarkers for diagnosis and prognosis of breast cancer patients. Clin Transl Oncol. 2018;20(7):906-911. [20] XU W C, QIAN G, LIU A Q, et al. Urinary Extracellular Vesicle: A Potential Source of Early Diagnostic and Therapeutic Biomarker in Diabetic Kidney Disease. Chin Med J (Engl), 2018,131(11): 1357-1364. [21] 陈群,吴飏,时国东,等.肿瘤来源的外泌体在肿瘤进展中的作用及其诊疗意义[J].南京医科大学学报(自然科学版), 2019,39(2): 300-305. [22] 彭一琳,倪煦东,曹帆,等.前列腺癌细胞来源的外泌体诱导巨噬细胞极化[J].中国生物化学与分子生物学报, 2019,35(2): 179-186. [23] 范维肖,雷琳,李蕊,等.前列腺癌LNCaP-AI+F细胞外泌体促进基质细胞WPMY-1功能活化[J].中国肿瘤生物治疗杂志, 2019, 26(3):293-298. [24] 潘韵芝,马赛,曹凯悦,等.高表达ANXA2肝癌干细胞外泌体对肝癌细胞恶性生物学特性的调控作用[J].中国肿瘤, 2019,28(4): 308-314. [25] 杨勇,陈霖,杨宏新,等.癌源外泌体的制备及其对胃癌细胞STK15表达的影响[J].重庆医学, 2019,48(9):1453-1456. [26] 郭怡,彭红,蹇淑娟,等.口腔癌患者循环外泌体促进舌癌细胞CAL27增殖、迁移、侵袭中的作用[J].实用口腔医学杂志, 2019,35(1):60-65. [27] LI I, NABET BY. Exosomes in the tumor microenvironment as mediators of cancer therapy resistance. Mol Cancer. 2019;18(1):32. [28] 崔雅楠,张传霞,金浩范.肿瘤细胞来源的外泌体对NK细胞活性的影响[J].中国老年学杂志, 2019,39(6):1525-1528. [29] 李雪,李楠.肝癌外泌体LINC ROR对巨噬细胞炎症反应的影响[J].四川大学学报(医学版), 2019,50(2):177-181. [30] 章菊,叶书来,张昌龙,等.HepG2细胞外泌体冲击树突状细胞介导的抗肿瘤作用[J].癌变·畸变·突变, 2019,31(1):29-34. [31] 冯慧洁,任伟宏,仝岩,等.胃癌源性外泌体对HLA-DR~(neg)leukocytes中Dicer1、PTEN基因的调控[J].免疫学杂志, 2017,33(3):203-207. [32] 吕龙辉,黄晓悫,熊小明,等.鼻咽癌外泌体miR-20a通过靶向BCL2L11基因抑制肿瘤相关巨噬细胞凋亡[J].重庆医学, 2017, 46(6):721-724. [33] ZHANG Y, YU G, CHU H, et al. Macrophage-Associated PGK1 Phosphorylation Promotes Aerobic Glycolysis and Tumorigenesis. Mol Cell. 2018;71(2):201-215.e7. [34] HE Y, CHEN D, YANG L, et al. The therapeutic potential of bone marrow mesenchymal stem cells in premature ovarian failure. Stem Cell Res Ther. 2018;9(1):263. [35] ENGLISH K, MAHON BP, WOOD KJ. Mesenchymal stromal cells; role in tissue repair, drug discovery and immune modulation. Curr Drug Deliv. 2014;11(5):561-571. [36] CHEN J, JI T, WU D, et al. Human mesenchymal stem cells promote tumor growth via MAPK pathway and metastasis by epithelial mesenchymal transition and integrin α5 in hepatocellular carcinoma. Cell Death Dis. 2019;10(6):425. [37] ZHANG TY, HUANG B, WU HB, et al. Synergistic effects of co-administration of suicide gene expressing mesenchymal stem cells and prodrug-encapsulated liposome on aggressive lung melanoma metastases in mice. J Control Release. 2015;209:260-271. [38] 许峰,金晓霞,施民新.人骨髓间充质干细胞促进乳腺癌细胞系MCF7上皮间质转化[J].基础医学与临床, 2018,38(9): 1244-1250. [39] 许鹏超,李静,赵春华.体外共培养人骨髓间充质干细胞与乳腺癌细胞可促进癌细胞的侵袭和迁移能力[J].基础医学与临床, 2016,36(5):615-620. [40] 蒋东辉,黄博,张月飞,等.人骨髓间充质干细胞诱导鼻咽癌上皮间质化的初步探讨[J].中华肿瘤防治杂志, 2014,21(23): 1851-1855. [41] 周昌宁,曹海宁,李利平.骨髓间充质干细胞促进结肠癌细胞HT29增殖和迁移[J].第三军医大学学报, 2015,37(7):649-654. [42] 赵慧巧,卢年华,张旭东,等. 结肠癌微环境对HMSC-bm形态、增殖、周期及CD34、CD90的影响[J].中国细胞生物学学报, 2018,40(5):745-751. [43] 冯影,卢士红,王昕,等.人骨髓来源间充质干细胞分泌外泌体特性研究[J].中国实验血液学杂志, 2014,22(3):595-599. [44] 任瑞,谭晓红,鲁亚成,等.一种绿色荧光蛋白标记的骨髓间充质干细胞源性外泌体的构建及鉴定[J].神经解剖学杂志, 2017,33(2): 167-171. [45] 袁林,曹依娜,杨征毅,等.人颌骨间充质干细胞的外泌体在巨噬细胞调控中的作用[J].实用口腔医学杂志,2017,33(3): 344-348. [46] 韩睿,李琳,王润清,等.间充质干细胞来源外泌体对免疫功能调控的作用与应用前景[J].中国组织工程研究, 2019,23(17): 2762-2769. [47] 王雪,刘芳.骨髓间充质干细胞来源的Exosome修复兔受损子宫内膜的研究[J].现代妇产科进展, 2018,27(3):170-174. [48] 周政,杜波,范雪,等.骨髓间充质干细胞外泌体对SD大鼠早衰卵巢的影响[J].中国科技论文, 2018,13(12):1429-1433. [49] 裴双,王琳,陈雪梅,等.骨髓间充质干细胞来源的外泌体静脉移植对脊髓损伤的修复作用[J].中国脊柱脊髓杂志, 2017,27(12):1119-1127. [50] 林颖,胡锦章,颛孙永勋,等.骨髓间充质干细胞外泌体调节哮喘小鼠Foxp3~+ Treg/Th17的平衡[J].中国组织工程研究, 2018,22(17): 2637-2643. [51] 綦惠,刘丹平,田大川,等.骨髓间充质干细胞源性外泌体对体外培养的软骨细胞增殖和迁移的调节作用[J].中国运动医学杂志, 2019,38(1):40-45. [52] 张万松,杨诚,郭文彬,等.BMSCs来源的外泌体对大鼠睾丸缺血再灌注损伤的保护作用[J].南方医科大学学报, 2018,38(8): 910-916. [53] SASAHIRA T, KIRITA T. Hallmarks of Cancer-Related Newly Prognostic Factors of Oral Squamous Cell Carcinoma. Int J Mol Sci. 2018;19(8): E2413. [54] MAO L, LI J, CHEN WX, et al. Exosomes decrease sensitivity of breast cancer cells to adriamycin by delivering microRNAs. Tumour Biol. 2016;37(4):5247-5256. [55] SHARMA A. Role of stem cell derived exosomes in tumor biology. Int J Cancer. 2018;142(6):1086-1092. [56] 张贺龙,杨俊辉,佘远岭,等.外泌体在胃癌中作用的研究进展[J].肿瘤, 2019,39(3):215-222. [57] 王丹丹,陈建中,亢春彦.BMSCs来源的外泌体对小鼠乳腺癌细胞4T1增殖、侵袭的影响及机制探讨[J].山东医药, 2015,55(35): 12-15. [58] YAN K, WU Q, YAN DH, et al. Glioma cancer stem cells secrete Gremlin1 to promote their maintenance within the tumor hierarchy. Genes Dev. 2014;28(10):1085-1100. [59] VALLABHANENI KC, PENFORNIS P, DHULE S, et al. Extracellular vesicles from bone marrow mesenchymal stem/stromal cells transport tumor regulatory microRNA, proteins, and metabolites. Oncotarget. 2015;6(7):4953-4967. [60] SALYBEKOV AA, SALYBEKOVA AK, POLA R, et al. Sonic Hedgehog Signaling Pathway in Endothelial Progenitor Cell Biology for Vascular Medicine. Int J Mol Sci. 2018;19(10): E3040. [61] CHEN G, GOTO Y, SAKAMOTO R, et al. GLI1, a crucial mediator of sonic hedgehog signaling in prostate cancer, functions as a negative modulator for androgen receptor. Biochem Biophys Res Commun. 2011;404(3):809-815. [62] 贾姗姗,李笑岩,滕菲,等.大鼠诱发型肝癌发生发展过程中Sonic Hedgehog、Ptc和Gli1表达的改变[J].中国组织化学与细胞化学杂志, 2013,22(3):207-211. [63] 刘庆生,俞建顺,蔡丹莉,等.大鼠胃癌前病变形成过程中胃黏膜Sonic Hedgehog信号通路的变化[J].中国临床药理学与治疗学, 2018,23(7): 761-769. [64] 陈浩,许浪.信号通路对胃癌干细胞及胃癌发生的影响[J].中国组织工程研究,2013,17(14):2532-2537. [65] 刘志勇,易坚,邹小明.乳腺癌组织中Hedgehog相关蛋白的表达及其临床意义[J].肿瘤防治研究, 2014,41(7):756-761. [66] 徐又海,汪兴洪.Shh、Gli1基因在多发性骨髓瘤中的表达及临床意义[J].中国临床药理学与治疗学, 2015,20(3):309-313. [67] 许秋然,郑鑫,昝献峰,等.胶质瘤相关癌基因1在肝细胞癌中的表达及其与Shh、Vimentin、E-cad-herin蛋白的相关性研究[J].细胞与分子免疫学杂志, 2012,28(5):536-539. [68] 郑晓文,陈一强,孔晋亮,等. Hedgehog信号通路成分SHH和Gli-1及血管内皮生长因子在人肺癌中的表达[J].中国全科医学, 2014,17(18): 2096-2102. [69] 徐林汇,尹青青,张咪,等.组织芯片检测Hh信号通路相关蛋白在前列腺癌中的表达及临床意义[J].基因组学与应用生物学, 2018,37(6):2726-2730. [70] 朱华民,李扬秋.实时定量PCR检测慢性粒细胞白血病患者Shh、Smo基因的表达水平[J].第三军医大学学报, 2014,36(3): 267-269. [71] 林松挺,陈正义,钟文洲.SHH蛋白在胰腺癌组织中的表达及其临床意义[J].中国普通外科杂志, 2016,25(9):1266-1270. [72] 赵志龙,张丽芳,张佳,等.Shh与MMP2在人食管鳞癌组织中的表达及意义[J].南方医科大学学报, 2013,33(7):1008-1011. [73] 沈冰,夏含笑,朱凌霄,等.鼻咽癌中Shh和Ptch1基因的表达及其临床意义[J].临床与实验病理学杂志, 2016,32(7):761-765. [74] VAN DEN BRINK GR. Hedgehog signaling in development and homeostasis of the gastrointestinal tract. Physiol Rev. 2007;87(4): 1343-1375. [75] LIN TC, WANG KH, CHUANG KH, et al. Modulation of tumor stem cell characteristics by 17β-estradiol in human mesenchymal stem cells derived from ovarian endometrioma. Taiwan J Obstet Gynecol. 2019; 58(3):338-344. [76] PREUSSNER J, ZHONG J, LOOSO M, et al. Connect-four: genomic analyses of regenerating stem cells identifies zygotic Dux factors as tumor initiators. Mol Cell Oncol. 2019;6(2):1565469. [77] 刘铁娥,于艳,戴广海.肺癌干细胞分泌外泌体增强肺癌细胞对化疗敏感性的研究[J].现代中西医结合杂志, 2019,28(15): 1622-1625. [78] 张丹,何大维,李典,等.肿瘤样干细胞来源的外泌体促进人脐带间充质干细胞的增殖和侵袭[J].南方医科大学学报, 2018,38(12): 1440-1447. [79] GIMPLE RC, BHARGAVA S, DIXIT D, et al. Glioblastoma stem cells: lessons from the tumor hierarchy in a lethal cancer. Genes Dev. 2019; 33(11-12):591-609. [80] 徐峰,牛万祥,谢时帅,等.胶质瘤干细胞来源的外泌体对血管内皮细胞增殖和迁移的影响[J].国际神经病学神经外科学杂志, 2018, 45(5):443-447. |
| [1] | Pu Rui, Chen Ziyang, Yuan Lingyan. Characteristics and effects of exosomes from different cell sources in cardioprotection [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(在线): 1-. |
| [2] | Zhao Min, Feng Liuxiang, Chen Yao, Gu Xia, Wang Pingyi, Li Yimei, Li Wenhua. Exosomes as a disease marker under hypoxic conditions [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1104-1108. |
| [3] | Chen Ziyang, Pu Rui, Deng Shuang, Yuan Lingyan. Regulatory effect of exosomes on exercise-mediated insulin resistance diseases [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(25): 4089-4094. |
| [4] | Gao Kun, Chen Dayu, Zhang Yong, Liu Weidong, Sun Shufen, Lai Wenqiang, Ma Dujun, Wu Yihong, Lin Zhanpeng, Jiang Yinglu, Yu Weiji. Achyranthes bidentata alcohol extract inhibits extracellular matrix degradation of the cartilage by regulating synovial fibroblast exosomes [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(23): 3636-3640. |
| [5] | Wang Kang, Zhi Xiaodong, Wang Wei. Effect of stem cell derived exosomes on repairing peripheral nerve injury [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(19): 3083-3089. |
| [6] | Zhao Shuangdan, Zheng Jiahua, Qi Wenbo, Huang Xianghua. Role and mechanism of exosomes derived from mesenchymal stem cells in reproductive system diseases [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(19): 3097-3102. |
| [7] | Liu Feng, Zhang Yu, Wang Yanli, Luo Wei, Han Chaoshan, Li Yangxin. Application of temperature-sensitive chitosan hydrogel encapsulated exosomes in ischemic diseases [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(16): 2479-2487. |
| [8] | Cai Yuan, Deng Chengliang. Therapeutic application of adipose stem cell-free liquid extracts: skin aging, wound healing, scar recovery and nerve regeneration [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(13): 2097-2102. |
| [9] | Liu Tao, Zhang Nini, Huang Guilin . Relationship between extracellular vesicles and radiation-induced tissue injury [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(13): 2121-2126. |
| [10] |
Xie Fei, Li Yanle, Lin Xinxiao, Hu Haiwei, Sang Zhicheng, Sun Yongsheng, Jiang Kewei, Cheng Ying, Wen Guannan, Wen Jianmin, Sun Weidong.
Mechanism underlying mechanical stress regulating fibroblasts-derived
exosomes at the osteotomized end following hallux valgus correction |
| [11] | Xu Huijun, Zhang Mi, Shi Dongmei, Wu Saixuan, Lu Ying, Dong Ming, Niu Weidong. Fetal bovine serum exosomes promote the proliferation of osteoblasts [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(31): 4961-4965. |
| [12] | Gu Yubo, Zhang Dongliang, Yuan Wei, , Song Lujie. Exosomes from adipose-derived stem cells can promote cavernous nerve regeneration in rats [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(31): 4979-4985. |
| [13] | Li Zhenxiang, Jiang Xiaokui, Shen Fangfang, Li Shaoshan. Immuoregulatory effects of colorectal cancer cell-derived exosomes on CD8+ T cells [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(31): 5002-5006. |
| [14] | Yuan Yiming, Wang Yan, Chen Chengcheng, Zhao Mingyue, Pei Fei. Efficacy of exosomes in peripheral nerve injury [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(31): 5079-5084. |
| [15] | Lai Yu, Han Jie. Mechanism and progress of exosomes in the treatment of nonunion [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(27): 4349-4355. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||