Chinese Journal of Tissue Engineering Research ›› 2020, Vol. 24 ›› Issue (13): 2087-2094.doi: 10.3969/j.issn.2095-4344.2063
Previous Articles Next Articles
Detection methods of mesenchymal stem cells-derived exosomes
Yang Qinxin, Wang Dali, Wei Xue
- Department of Burn and Plastic Surgery, Affiliated Hospital of Zunyi Medical University, Zunyi 563000, Guizhou Province, China
-
Received:2019-10-15Revised:2019-10-17Accepted:2019-11-19Online:2020-05-08Published:2020-03-10 -
About author:Yang Qinxin, Master candidate, Department of Burn and Plastic Surgery, Affiliated Hospital of Zunyi Medical University, Zunyi 563000, Guizhou Province, China -
Supported by:the National Natural Science Foundation of China, No. 81871570
CLC Number:
Cite this article
Yang Qinxin, Wang Dali, Wei Xue. Detection methods of mesenchymal stem cells-derived exosomes [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(13): 2087-2094.
share this article
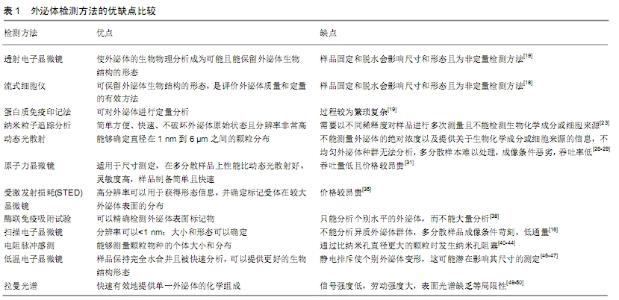
外泌体作为细胞间信息交流的重要介质,在组织修复、免疫等领域发挥独特的生物学功能,具有广阔的研究和应用前景。如何高效、高纯度地分离外泌体是实现其组学分析和功能研究的关键。实际上除了不同来源细胞分泌的外泌体存在异质性之外,同种细胞来源的外泌体也有可能大小形态各异。外泌体的体积小、密度低、分离难度大,而且不同分离方法得到的外泌体理化性质不同,这导致了外泌体研究存在大量不可控性和难重复 性[19]。如今已经开发了许多基于外泌体物理及生物化学性质的分离技术,如超速离心法、密度梯度离心法、超滤法以及目前比较成熟的商用化试剂盒等。 超速离心法是目前外泌体分离的“金标准”,也是使用最广泛的方法。超速离心法工作原理:基于外泌体的大小,大的较早沉淀在管底,而小的需更大的离心力才能沉淀。可溶性组分不受离心影响,但是非外泌体颗粒如脂蛋白和蛋白质聚集体可能会一同沉淀[20]。超速离心法的缺点在于仪器昂贵、耗时费力、产量低且重复离心操作可能对外泌体造成破坏。密度梯度离心法分离原理:基于外泌体的密度,可从不同密度的颗粒分离出外泌体,外泌体移动至其平衡密度,而高密度的可溶性组分将在管底沉淀[20]。密度梯度离心法获得的外泌体纯度较高,但是步骤繁琐且耗时。超滤法则是利用不同截留相对分子质量的超滤膜对样品进行选择性分离,可溶性蛋白质和小于临界值(约105 kD)的颗粒被推向过滤膜,然后在过滤膜处收集外泌体[20]。虽然超滤法简单高效,但超滤过膜时加压可引起外泌体变形或破坏且可能受蛋白污染。目前用得较多的商用化试剂盒是Exo Quick试剂盒和Isolation试剂盒,这2种试剂盒都是基于沉淀法原理来分离外泌体。Exo Quick试剂盒是通过一种螯合物对外泌体进行捕捉,Isolation试剂盒是通过将水分子聚合到一起,强行减少可溶性成分,使其从溶液中析出,之后经过低速离心即可收集外泌体[21]。虽然商用化试剂盒分离外泌体速度快、产量高,但是价格较昂贵且有一定的细胞毒性。目前分离外泌体的方法众多,但是还没有同时满足外泌体高浓度及高产量的方法,这将影响后续准确高效地检测外泌体的物理及生物化学性质。 为获得外泌体形态、大小、密度及蛋白质组成等信息,可以通过透射电子显微镜、纳米粒子追踪、流式细胞仪、蛋白质印记和酶联免疫吸附法等对外泌体进行检测,分述如下。 2.1 透射电子显微镜 透射电子显微镜,简称透射电镜,是把经加速和聚集的电子束投射到非常薄的样品上,电子与样品中的原子碰撞而改变方向,从而产生立体角散射。散射角的大小与样品的密度、厚度相关,因此可以形成明暗不同的影像,影像放大、聚焦后在成像器件(如荧光屏、胶片以及感光耦合组件)上显示出来,可以看到在光学显微镜下无法看清的小于0.2 μm的细微结构,这些结构称为亚显微结构或超微结构。目前透射电镜的分辨力可达0.2 nm。这是目前检测外泌体方法中用到最多的方法之一,此法目前也相对成熟。它的检测效果也与外泌体的提取方法相关。研究发现在透射电镜下差速超速离心法获得的外泌体直径多分布于30-100 nm,较为均一;Exo Quick试剂盒法获得的外泌体不够均匀;Isolation试剂盒法获得的外泌体背景污染较严重, 可能存在蛋白质污染[21]。透射电镜的优点在于使外泌体的生物物理分析成为可能且能保留外泌体生物结构的形态;缺点在于样品固定和脱水会影响尺寸和形态且为非定量检测方法。 透射电镜检测脐带间充质干细胞源性外泌体[18]:将2 mL PBS加入分离外泌体的离心管中混匀,按照1∶50倍稀释后取外泌体稀释液10 μL,滴加于2 mm的含碳载样铜网上,在室温下静置5 min后用滤纸将多余液体轻轻吸去,3%磷钨酸钠溶液(pH 6.8)室温负染5 min,双蒸水轻轻洗1遍后室温晾干,透射电镜观察到外泌体呈圆形或椭圆形,大小不均匀,直径30-100 nm,有完整的膜结构,内含低密度物质。 2.2 流式细胞仪 流式细胞仪是对细胞进行自动分析和分选的装置。它可以快速测量、存贮、显示一系列重要的生物物理、生物化学方面的特征参量,并根据预选的参量范围把指定的细胞亚群从中分选出来。多数流式细胞仪只能测量一个细胞的诸如总核酸量、总蛋白量等指标,而不能鉴别和测出某一特定部位的核酸或蛋白的多少。也就是说,它的细节分辨率为零。此法现在也相对成熟,能较准确检测出外泌体及其来源细胞的表面标记物,但外泌体粒径太小,折射率低,低于常规流式细胞仪分析的阈值,因此不能准确区分粒子与噪声。采用常规的流式细胞仪进行检测时往往需要将外泌体与微珠连接以增大表面积、增强反射,或者加入纳米金颗粒来增加外泌体粒径之后再检测。目前已有学者搭建了一种高灵敏的流式细胞仪(HSFCM),将可检测的外泌体粒径降至40 nm,能够在不连接微珠的情况下实现每分钟 10 000个外泌体的检测,并能够结合免疫荧光的方法进行外泌体标志蛋白质的定量检测,目前该仪器已商品 化[22]。流式细胞仪的优点在于可保留外泌体生物结构的形态,是评价外泌体质量和定量的有效方法;缺点在于干燥过程中外泌体可能会坍塌而形成杯状形态。 普通流式细胞仪检测脐带间充质干细胞源性外泌体表面标志物的方法:首先单独加入CD63-PE/ CD9-FITC/CD81-PE/CD83-PE不同类型的流式抗体 5 μL,室温避光孵育15 min。由于外泌体的粒径太小,很难用普通流式细胞仪检测,采用纳米金颗粒增加外泌体的粒径。方法如下:染色后的外泌体溶液加入分支聚乙烯亚胺37 ℃孵育15 min,之后超速离心去除分支聚乙烯亚胺,加入纳米金颗粒轻柔重悬后置于培养箱中 60 min,加入APC-DNA染料室温孵育15 min,上流式细胞仪检测,APC阳性颗粒即为所需要检测的外泌体。脐带间充质干细胞源性外泌体CD9、CD63、CD81和CD83呈阳性表达[18]。流式细胞仪检测人脐血间充质干细胞外泌体表面标志物,其表达外泌体共性标志CD63、CD81以及间充质干细胞表面黏附分子CD90、CD73、CD105、CD166、CD29[23];流式细胞仪检测骨髓间充质干细胞外泌体表面标志物,其表达CD9、CD81、CD63蛋白以及其来源细胞的特异性蛋白CD44 [24]。 2.3 蛋白质免疫印记法 蛋白质印迹法(免疫印迹试验)即Western blot,其基本原理是通过特异性抗体对凝胶电泳处理过的细胞或生物组织样品进行着色。通过分析着色的位置和着色深度获得特定蛋白质在所分析的细胞或组织中表达的信息。不同方法提取出的外泌体用此法检测的结果也略有差异。研究发现,差速超速离心法提取到的外泌体特异性标志物CD9与CD63在表达强度上远高于Exo Quick试剂盒法和Isolation试剂盒法;其次,Exo Quick试剂盒法和Isolation试剂盒法提取到的外泌体特异性标志物仅在CD81的表达上略高于差速超速离心法[21]。此法的优点在于可对外泌体进行定量分析;缺点则是过程较为繁琐复杂。 骨髓间充质干细胞来源外泌体特异性蛋白的分析:配置15%分离胶和5%浓缩胶,取外泌体悬液40 μL与5×SDS上样缓冲液10 μL混合煮沸5 min,加于凝胶上样孔内,浓缩胶恒压80 V,分离胶恒压120 V,200 mA恒流1 h。将凝胶中的蛋白质通过湿转法移至硝酸纤维素膜上,室温下用含5%脱脂牛奶的封闭液处理1 h,经1×TBST缓冲液洗脱后加入CD9、CD63单克隆抗体于4 ℃条件下反应过夜,再次洗脱后加入辣根过氧化物酶标记的羊抗兔二抗,于室温下平缓摇动1 h,经1×TBST缓冲液洗膜3次,加入化学发光底物,骨髓间充质干细胞来源外泌体表达CD9、CD63蛋白[25]。 2.4 纳米粒子追踪分析 纳米颗粒跟踪分析技术是一种光学粒子跟踪方法,用于获取外泌体的浓度和尺寸分布,能够检测直径小于50 nm的单个粒子,是近年来新兴的纳米级别测量技术之一。纳米颗粒在其悬浊液中受到周边溶液分子的撞击而做无规则的布朗运动,然后通过斯托克斯-爱因斯坦方程,这些颗粒在单位时间内(ts)的移动速度与其本身的粒度(dh)、溶液的黏度(?)和温度(T)存在数量上的关系。因此通过观察溶液中的颗粒运动轨迹,得出与之相关的颗粒粒径数据,同时通过仪器内置的高速相机和软件,对观察到的每一个颗粒进行跟踪分析,最终提供与常规粒度仪所不同的粒径数量分布以及颗粒物浓度的分析结果。马尔文纳米颗粒跟踪分析仪(NanoSight)所具备的溶液状态(原位测试)下的测试,为外泌体颗粒提供了非常好的结构与功能上的保护,并且能够让外泌体颗粒在更接近其原始状态下进行测量,保证了数据的真实性和有效性。另外,独一无二的浓度测量技术,直接为研究人员提供可靠的外泌体浓度数据。 使用NanoSight LM10(NanoSight Ltd.,Minton Park,UK)进行外泌体的绝对尺寸分布分析,粒子会根据布朗运动和扩散系数自动跟踪和确定尺寸。将外泌体稀释在1 mL过滤的PBS中,测量条件:温度(23.75±0.5) ℃,黏度(0.91±0.03) cP,每秒帧数25,测量时间60 s。对每个样品进行3次记录,结果显示外泌体的大小在90-150 nm之间[26]。此法的优点在于简单方便、快速、不破坏外泌体原始状态且分辨率非常高;缺点在于需要以不同稀释度对样品进行多次测量且不能检测生物化学成分或细胞来源。 2.5 动态光散射 动态光散射也称为光子相关光谱或准弹性光散射。它可以检测粒径介于1 nm和6 μm之间的粒子相对尺寸分布[27-28]。由于与溶剂分子的连续碰撞,流体中的粒子会随机移动,这称为布朗运动粒子的随机运动。颗粒的速度取决于温度、黏度和(流体动力学)颗粒直径,粒子越小,布朗运动就越快。经历布朗运动的粒子引起散射光的光强波动,其通常在30 s内完成测量。通过应用光散射理论中的数学算法,从光强波动中获得相对尺寸分布。光散射理论需要溶剂和外泌体之间的折射率差,这是目前未知的。动态光散射在单分散样品(即含有一种特定尺寸的颗粒样品)的大小测定中表现良好,并监测样品变化例如聚集[29-31],检测多分散样品(即含有不同大小的颗粒的样品)的尺寸大小是不太准确的,因为测量的尺寸大小受到少量较大颗粒的影响。此外,结果取决于应用的数学算法[29-30],只有粒径相差至少2倍才能计算出不同大小外泌体的尺寸[29,32]。该方法的优点是能够确定直径在1 nm到6 μm之间的颗粒分布;缺点在于动态光散射不能测量外泌体的绝对浓度以及提供关于生物化学成分或细胞来源的信息,且不均匀的外泌体种群无法分析,多分散样本难以处理,成像条件恶劣。 2.6 原子力显微镜 原子力显微镜是1986年由BINNIG等[33]开发的,并提供亚纳米分辨率地形成像。原子力显微镜由末端具有尖锐尖端的悬臂梁组成,与其扫描样品表面没有物理接触,测量尖端的运动,并通过软件创建三维图像。 由于横向分辨率为3 nm,垂直分辨率<0.1 nm [34],原子力显微镜适用于尺寸大小的检测,在多分散样品上的性能比动态光散射好[31]。SIEDLECKI等[34]和YUANA等[35]表明原子力显微镜可以用来测量外泌体在生理状态下的相对尺寸大小。由于原子力显微镜的分辨率高,外泌体必须结合到非常平坦的表面,例如云母,抗体可与外泌体表面结合,从而获得生物化学信息[34]。因为用抗体结合外泌体的表面效率是未知的,所以不能确定外泌体的浓度。此外,表面结合可能影响外泌体的形态,可能会影响实际直径。此方法的优点在于适用于尺寸测定,在多分散样品上性能比动态光散射好,灵敏度高,样品制备简单且快速;缺点在于吞吐量低且价格较昂贵。 2.7 受激发射损耗荧光显微镜 受激发射损耗荧光显微镜是一种高分辨率荧光显微镜。它成功地检测出了直径为16 nm的颗粒,这对于外泌体的大小来说足够小[36-37]。受激发射损耗荧光显微镜不仅有望用于确定荧光标记的外泌体的大小和位置,而且高分辨率可以用于获得形态信息,并确定标记受体在较大外泌体表面的分布[38]。如果检测体积已知,则可以确定浓度,并且用于探测 10 000个颗粒的测量时间是数小时[39]。 2.8 酶联免疫吸附试验 酶联免疫吸附试验已被用于外泌体的检测,但没有广泛使用[40]。使用膜联蛋白或表面抗原抗体捕获外泌体,随后使用抗表面抗原(检测抗体)的独特抗体检测外泌体。这种技术的优点在于可以精确检测外泌体表面标记物;缺点是只能分析个别水平的外泌体,而不能大量分析[41]。 2.9 扫描电子显微镜 扫描电镜是介于透射电镜和光学显微镜之间的一种微观形态观察手段,主要是利用二次电子信号成像来观察样品的表面形态,即用极狭窄的电子束去扫描样品,通过电子束与样品的相互作用产生各种效应,其中主要是样品的二次电子发射。它可直接利用样品表面材料的物质性能进行微观成像。此法的优点是分辨率可以<1 nm;大小和形态可以确定。缺点是不能分析异质外泌体群体,多分散样品成像条件苛刻,且通量低。 用扫描电镜检测外泌体时,将外泌体用3.7%戊二醛固定15 min,PBS洗涤2次,用梯度浓度乙醇(体积分数分别为40%,60%,80%,96%-98%)进行脱水,乙醇蒸发后将样品在玻璃基板上室温静置24 h,在金-钯溅射后通过扫描电镜分析,检测结果显示:所有外泌体都为一个直径30-50 nm的球形[16]。 2.10 电阻脉冲感测 电阻脉冲感测是用Coulter原理表征悬浮液中外泌体大小的另一种方法[42]。电阻脉冲感测基于用导电液体填充的纳米孔,所述导电液体在通过球形纳米粒子(例如外泌体)时被置换或移出,随后计算出的电阻变化随颗粒尺寸成比例增加,并在每次颗粒通过孔时记录下来。因此,电阻脉冲感测能够测量颗粒物种的个体大小和分布[43-45]。在电阻脉冲感测中,可以检测到的尺寸范围由上限处的孔径大小和下限的最小可检测电阻变化所决定,后者约为孔径的20%。例如,直径为400 nm的孔可以将直径为80-400 nm的囊泡分级。电阻脉冲感测方法的主要限制之一是通过比纳米孔直径更大的颗粒时发生纳米孔阻塞[46-47]。因此,为了检测高度异质性的样品(例如含有凋亡小体、微囊、外泌体),电阻脉冲感测不是合适的方法。有趣的是,如果使用电阻脉冲感测,则来自生物学和细胞培养物的外泌体样品可能包含异质外泌体种类,并且在外泌体检测期间可能构成影响[17]。 2.11 低温电子显微镜 低温电子显微镜是显微镜的一种形式,其在低温下分析样品。在传统的显微镜中,样品在成像之前被脱水,在干燥过程中外泌体可能会崩溃形成杯状形态[48]。然而,在冷冻电镜中,由于样品保持完全水合并且被快速分析,所以外泌体被显示为圆形颗粒[49]。低温电子显微镜的优点之一是样品在冷冻条件下进行分析,无需预先染色或阳离子化。因此,低温电子显微镜可以提供更好的生物结构形态。在一项关于血浆来源外泌体的研究中,YUANA等[50]显示了低温电子显微镜在检测外泌体的结构和形态异质性方面的有用性。有趣的是,低温电子显微镜也显示静电排斥使个别的外泌体变形,这可能潜在影响其尺寸的测定[51]。 2.12 拉曼光谱 拉曼光谱使用单色激光光源照射样品。由于样品中分子振动过程中的波长漂移,拉曼光谱中的光散射产生了分子的特征光谱,例如核酸、蛋白质。因此,拉曼光谱提供样品化学成分的无标记测定。与通常进行批量分析的其他外泌体检测技术相反,拉曼光谱在几分钟内即使提供单一外泌体的化学组成也非常有效[52]。由于已知的生物大分子光谱的可用性,例如核酸、蛋白质和脂质(外泌体的主要成分),拉曼光谱能够检测封装在外泌体内的分子信息。尽管拉曼光谱在分析外泌体方面具有独特的特点,但其具有信号强度低、劳动强度大、表面光谱缺乏等局限性。为了提高信号强度和信号的均匀性,LEE等[53]设计了一种基于聚二甲基硅氧烷的等离子体纳米级平台,使拉曼光谱对外泌体进行更加有效地捕获和化学分析。 2.13 外泌体检测方法的研究进展 外泌体是通过形态、尺寸和蛋白质组成这3个层面来检测的。以上介绍了众多不同检测外泌体各个特征的方法,它们亦有各自的优点与不足,见表1。目前,没有一种方法可以精确地检测以及规模化整个外泌体。因为它们的检测结果受其提取方法的影响。此外,检测外泌体更严格的特征可能需要流式细胞仪、电子显微镜和完整的RNA、脂质和蛋白质分析。这将有助于更好地探索外泌体的生物学特性及其与疾病的动态平衡关系[41]。 "


最近有研究发现另一种高通量外泌体检测系统是纳米等离子体分析。纳米等离子体分析是一种用于制作纳米孔阵列的薄金薄膜,薄膜的光照引起强烈的电磁场或表面等离子体[54]。表面等离子体允许独特的光学传输,并由于其阻力而产生纳米孔阵列的独特光谱。当外泌体结合到其特异性抗体功能化的纳米孔时,观察到光谱的变化且直接与外泌体的相对分子质量相关。同样,新兴的方法之一是色谱技术,例如尺寸排阻色谱法。在NORDIN等[55]的一项比较研究中,作者指出与传统的超速离心法相比,尺寸排阻色谱法获得的外泌体更纯净且无聚集。虽然尺寸排阻色谱法是一种分离技术[56],但是将其与基于抗体的捕获方法结合,例如固定在琼脂糖凝胶珠上的抗体可以使其成为外泌体分离和检测方法的新技术。 目前,需要一种快速有效、灵敏、低成本的用于检测外泌体的方法,不仅考虑它们的尺寸大小,还要考虑它们的起源细胞。在临床上,一个根本的问题是外泌体量化的技术挑战。虽然精确测量外泌体颗粒数量和蛋白质含量方面取得了很大进展,但仍然迫切需要在实验室之间对外泌体检测程序进行标准化。这对用于临床试验目的的外泌体剂量是特别重要的。外泌体检测技术的进步表明了选择合适的生物物理和/或分子方法用于外泌体检测的重要性。外泌体检测程序已经从光谱(例如动态光散射)方法发展到基于纳米技术的高通量技术(例如电阻脉冲感测、流式细胞术)。由于没有任何一种技术满足外泌体的所有特性,推测在不久的将来,多种技术联合可用于外泌体生物物理学和分子学同时表征[15]。对外泌体更好的理解以及用于外泌体定量、分离和储存,建立效价测定的标准化方法将提高未来对基于外泌体的诊断和治疗应用[47]。 "

| [1] REN N, ZHANG S, LI Y, et al. Bone mesenchymal stem cell functions on the hierarchical micro/nanotopographies of the Ti-6Al-7Nb alloy. Br J Oral Maxillofac Surg. 2014;52(10):907-912. [2] SUN L, FAN X, ZHANG L, et al. Bone mesenchymal stem cell transplantation via four routes for the treatment of acute liver failure in rats. Int J Mol Med. 2014;34(4):987-996. [3] FRIEDENSTEIN AJ, DERIGLASOVA UF, KULAGINA NN, et al. Precursors for fibroblasts in different populations of hematopoietic cells as detected by the in vitro colony assay method. Exp Hematol. 1974; 2(2):83-92. [4] LAFLAMME MA, MURRY CE. Heart regeneration. Nature. 2011;473 (7347):326-335. [5] DENZER K, KLEIJMEER MJ, HEIJNEN HF, et al. Exosome: from internal vesicle of the multivesicular body to intercellular signaling device. J Cell Sci. 2000;113 Pt 19:3365-3374. [6] RAPOSO G, NIJMAN HW, STOORVOGEL W, et al. B lymphocytes secrete antigen-presenting vesicles. J Exp Med. 1996;183(3): 1161-1172. [7] THÉRY C, AMIGORENA S, RAPOSO G, et al. Isolation and characterization of exosomes from cell culture supernatants and biological fluids. Curr Protoc Cell Biol. 2006;Chapter 3:Unit 3.22. [8] 许文荣,孙瑶湘.外泌体内分子标志物检测及其临床应用[J].临床检验杂志,2017,35(3):161-164. [9] LI T, YAN Y, WANG B, et al. Exosomes derived from human umbilical cord mesenchymal stem cells alleviate liver fibrosis. Stem Cells Dev. 2013;22(6):845-854. [10] BRUNO S, GRANGE C, DEREGIBUS MC, et al. Mesenchymal stem cell-derived microvesicles protect against acute tubular injury. J Am Soc Nephrol. 2009;20(5):1053-1067. [11] GATTI S, BRUNO S, DEREGIBUS MC, et al. Microvesicles derived from human adult mesenchymal stem cells protect against ischaemia-reperfusion-induced acute and chronic kidney injury. Nephrol Dial Transplant. 2011;26(5):1474-1483. [12] 李梦芸,刘德伍,毛远桂.干细胞源性外泌体在创面修复中的作用研究进展[J].中华烧伤杂志,2017,33(3):180-184. [13] 杨前,刁波.间充质干细胞源性外泌体研究进展[J].华南国防医学杂志, 2018,32(2):137-141. [14] 刘青武,陈佳,蒙玉娇,等.间充质干细胞源性外泌体及其在创面修复中的研究进展[J].中国临床药理学与治疗学, 2019,24(7):826-832. [15] KHATUN Z, BHAT A, SHARMA S, et al. Elucidating diversity of exosomes: biophysical and molecular characterization methods. Nanomedicine (Lond). 2016;11(17):2359-2377. [16] SOKOLOVA V, LUDWIG AK, HORNUNG S, et al. Characterisation of exosomes derived from human cells by nanoparticle tracking analysis and scanning electron microscopy. Colloids Surf B Biointerfaces. 2011; 87(1):146-150. [17] MOKARIZADEH A, DELIREZH N, MORSHEDI A, et al. Microvesicles derived from mesenchymal stem cells: potent organelles for induction of tolerogenic signaling. Immunol Lett. 2012;147(1-2):47-54. [18] 肖漓,白剑,陈文,等.脐带间充质干细胞外泌体的分离和鉴定[J].中华细胞与干细胞杂志(电子版),2016,6(4):236-239. [19] PAOLINI L, ZENDRINI A, DI NOTO G, et al. Residual matrix from different separation techniques impacts exosome biological activity. Sci Rep. 2016;6:23550. [20] 边素艳,刘宏斌.细胞外囊泡的分离及鉴定方法[J].新医学, 2019,50(9): 658-662. [21] 郭莹,王秀伟,牛玉虎,等.人脐带间充质干细胞来源外泌体提取方法的比较[J].中国组织工程研究,2018,22(9):1382-1388. [22] TIAN Y, MA L, GONG M, et al. Protein Profiling and Sizing of Extracellular Vesicles from Colorectal Cancer Patients via Flow Cytometry. ACS Nano. 2018;12(1):671-680. [23] 张娟,刘峰,张薇,等.人脐血间充质干细胞来源的外泌体:分离鉴定及生物学特性[J].中国组织工程研究, 2014,18(37):5955-5960. [24] 梁亚会,郭子宽,王芳,等.PEG 6000快速提取间充质干细胞外泌体[J].空军医学杂志,2017,33(3):176-179. [25] 胡国文,李青,牛鑫,等.旋转超滤:一种提取细胞外泌体的新方法[J].第二军医大学学报,2014,35(6):598-602. [26] FRANQUESA M, HOOGDUIJN MJ, RIPOLL E, et al. Update on controls for isolation and quantification methodology of extracellular vesicles derived from adipose tissue mesenchymal stem cells. Front Immunol. 2014;5:525. [27] CLARK NA, LUNACEK JH, BENEDEK GB. A Study of Brownian Motion Using Light Scattering. Amer J Phys. 1970;38(6):575-585. [28] DIECKMANN Y, CÖLFEN H, HOFMANN H, et al. Particle size distribution measurements of manganese-doped ZnS nanoparticles. Anal Chem. 2009;81(10):3889-3895. [29] BRYANT G, THOMAS JC. Improved Particle Size Distribution Measurements Using Multiangle Dynamic Light Scattering. Langmuir. 1995;11(7):2480-2485. [30] FILELLA M, JINGWU Z, NEWMAN ME, et al. Analytical applications of photon correlation spectroscopy for size distribution measurements of natural colloidal suspensions: capabilities and limitations. Colloids & Surfaces A Physicochemical & Engineering Aspects. 1997; 120(1-3): 27-46. [31] HOO CM, STAROSTIN N, WEST P, et al. A comparison of atomic force microscopy (AFM) and dynamic light scattering (DLS) methods to characterize nanoparticle size distributions. Journal of Nanoparticle Research. 2008;10(1 Supplement): 89-96. [32] HOEKSTRA AG, SLOOT PMA. Biophysical and Biomedical Applications of Nonspherical Scattering. London: Academic Press, 2000:585-602. [33] BINNIG G, QUATE CF, GERBER C. Atomic force microscope. Phys Rev Lett. 1986;56(9):930-933. [34] SIEDLECKI CA, WANG IW, HIGASHI JM, et al. Platelet-derived microparticles on synthetic surfaces observed by atomic force microscopy and fluorescence microscopy. Biomaterials. 1999;20(16): 1521-1529. [35] YUANA Y, OOSTERKAMP TH, BAHATYROVA S, et al. Atomic force microscopy: a novel approach to the detection of nanosized blood microparticles. J Thromb Haemost. 2010;8(2):315-323. [36] WESTPHAL V, HELL SW. Nanoscale resolution in the focal plane of an optical microscope. Phys Rev Lett. 2005;94(14):143903. [37] WILLIG KI, RIZZOLI SO, WESTPHAL V, et al. STED microscopy reveals that synaptotagmin remains clustered after synaptic vesicle exocytosis. Nature. 2006;440(7086):935-939. [38] HEIN B, WILLIG KI, HELL SW. Stimulated emission depletion (STED) nanoscopy of a fluorescent protein-labeled organelle inside a living cell. Proc Natl Acad Sci U S A. 2008;105(38):14271-14276. [39] VAN DER POL E, HOEKSTRA AG, STURK A, et al. Optical and non-optical methods for detection and characterization of microparticles and exosomes. J Thromb Haemost. 2010;8(12): 2596-2607. [40] OSUMI K, OZEKI Y, SAITO S, et al. Development and assessment of enzyme immunoassay for platelet-derived microparticles. Thromb Haemost. 2001;85(2):326-330. [41] ERDBRÜGGER U, LANNIGAN J. Analytical challenges of extracellular vesicle detection: A comparison of different techniques. Cytometry A. 2016;89(2):123-134. [42] GRAHAM MD. The Coulter principle: Imaginary origins. Cytometry A. 2013;83(12):1057-1061. [43] ANDERSON W, KOZAK D, COLEMAN VA, et al. A comparative study of submicron particle sizing platforms: accuracy, precision and resolution analysis of polydisperse particle size distributions. J Colloid Interface Sci. 2013;405:322-330. [44] LANE RE, KORBIE D, ANDERSON W, et al. Analysis of exosome purification methods using a model liposome system and tunable-resistive pulse sensing. Sci Rep. 2015;5:7639. [45] KO J, CARPENTER E, ISSADORE D. Detection and isolation of circulating exosomes and microvesicles for cancer monitoring and diagnostics using micro-/nano-based devices. Analyst. 2016;141(2): 450-460. [46] MAAS SL, DE VRIJ J, BROEKMAN ML. Quantification and size-profiling of extracellular vesicles using tunable resistive pulse sensing. J Vis Exp. 2014;(92):e51623. [47] XU R, GREENING DW, ZHU HJ, et al. Extracellular vesicle isolation and characterization: toward clinical application. J Clin Invest. 2016; 126(4):1152-1162. [48] POSPICHALOVA V, SVOBODA J, DAVE Z, et al. Simplified protocol for flow cytometry analysis of fluorescently labeled exosomes and microvesicles using dedicated flow cytometer. J Extracell Vesicles. 2015;4:25530. [49] PETERSEN KE, MANANGON E, HOOD JL, et al. A review of exosome separation techniques and characterization of B16-F10 mouse melanoma exosomes with AF4-UV-MALS-DLS-TEM. Anal Bioanal Chem. 2014;406(30):7855-7866. [50] YUANA Y, KONING RI, KUIL ME, et al. Cryo-electron microscopy of extracellular vesicles in fresh plasma. J Extracell Vesicles. 2013;2(1): 21494. [51] GREY M, DUNNING CJ, GASPAR R, et al. Acceleration of α-synuclein aggregation by exosomes. J Biol Chem. 2015;290(5):2969-2982. [52] SMITH ZJ, LEE C, ROJALIN T, et al. Single exosome study reveals subpopulations distributed among cell lines with variability related to membrane content. J Extracell Vesicles. 2015;4:28533. [53] LEE C, CARNEY RP, HAZARI S, et al. 3D plasmonic nanobowl platform for the study of exosomes in solution. Nanoscale. 2015;7(20): 9290-9297. [54] BARNES WL, DEREUX A, EBBESEN TW. Surface plasmon subwavelength optics. Nature. 2003;424(6950):824-830. [55] NORDIN JZ, LEE Y, VADER P, et al. Ultrafiltration with size-exclusion liquid chromatography for high yield isolation of extracellular vesicles preserving intact biophysical and functional properties. Nanomedicine. 2015;11(4):879-883. [56] BÖING AN, VAN DER POL E, GROOTEMAAT AE, et al. Single-step isolation of extracellular vesicles by size-exclusion chromatography. J Extracell Vesicles. 2014;3. [57] LAI RC, YEO RW, TAN KH, et al. Exosomes for drug delivery - a novel application for the mesenchymal stem cell. Biotechnol Adv. 2013;31(5): 543-551. [58] YEO RW, LAI RC, ZHANG B, et al. Mesenchymal stem cell: an efficient mass producer of exosomes for drug delivery. Adv Drug Deliv Rev. 2013;65(3):336-341. [59] PAOLINI L, ZENDRINI A, DI NOTO G, et al. Residual matrix from different separation techniques impacts exosome biological activity. Sci Rep. 2016;6:23550. [60] SÓDAR BW, KITTEL Á, PÁLÓCZI K, et al. Low-density lipoprotein mimics blood plasma-derived exosomes and microvesicles during isolation and detection. Sci Rep. 2016;6:24316. |
| [1] | Pu Rui, Chen Ziyang, Yuan Lingyan. Characteristics and effects of exosomes from different cell sources in cardioprotection [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(在线): 1-. |
| [2] | Lin Qingfan, Xie Yixin, Chen Wanqing, Ye Zhenzhong, Chen Youfang. Human placenta-derived mesenchymal stem cell conditioned medium can upregulate BeWo cell viability and zonula occludens expression under hypoxia [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(在线): 4970-4975. |
| [3] | Wang Xianyao, Guan Yalin, Liu Zhongshan. Strategies for improving the therapeutic efficacy of mesenchymal stem cells in the treatment of nonhealing wounds [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1081-1087. |
| [4] | Zhao Min, Feng Liuxiang, Chen Yao, Gu Xia, Wang Pingyi, Li Yimei, Li Wenhua. Exosomes as a disease marker under hypoxic conditions [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1104-1108. |
| [5] | Wang Shiqi, Zhang Jinsheng. Effects of Chinese medicine on proliferation, differentiation and aging of bone marrow mesenchymal stem cells regulating ischemia-hypoxia microenvironment [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1129-1134. |
| [6] | Kong Desheng, He Jingjing, Feng Baofeng, Guo Ruiyun, Asiamah Ernest Amponsah, Lü Fei, Zhang Shuhan, Zhang Xiaolin, Ma Jun, Cui Huixian. Efficacy of mesenchymal stem cells in the spinal cord injury of large animal models: a meta-analysis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1142-1148. |
| [7] | Hou Jingying, Yu Menglei, Guo Tianzhu, Long Huibao, Wu Hao. Hypoxia preconditioning promotes bone marrow mesenchymal stem cells survival and vascularization through the activation of HIF-1α/MALAT1/VEGFA pathway [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 985-990. |
| [8] | Shi Yangyang, Qin Yingfei, Wu Fuling, He Xiao, Zhang Xuejing. Pretreatment of placental mesenchymal stem cells to prevent bronchiolitis in mice [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 991-995. |
| [9] | Liang Xueqi, Guo Lijiao, Chen Hejie, Wu Jie, Sun Yaqi, Xing Zhikun, Zou Hailiang, Chen Xueling, Wu Xiangwei. Alveolar echinococcosis protoscolices inhibits the differentiation of bone marrow mesenchymal stem cells into fibroblasts [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 996-1001. |
| [10] | Fan Quanbao, Luo Huina, Wang Bingyun, Chen Shengfeng, Cui Lianxu, Jiang Wenkang, Zhao Mingming, Wang Jingjing, Luo Dongzhang, Chen Zhisheng, Bai Yinshan, Liu Canying, Zhang Hui. Biological characteristics of canine adipose-derived mesenchymal stem cells cultured in hypoxia [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1002-1007. |
| [11] | Geng Yao, Yin Zhiliang, Li Xingping, Xiao Dongqin, Hou Weiguang. Role of hsa-miRNA-223-3p in regulating osteogenic differentiation of human bone marrow mesenchymal stem cells [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1008-1013. |
| [12] | Lun Zhigang, Jin Jing, Wang Tianyan, Li Aimin. Effect of peroxiredoxin 6 on proliferation and differentiation of bone marrow mesenchymal stem cells into neural lineage in vitro [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1014-1018. |
| [13] | Zhu Xuefen, Huang Cheng, Ding Jian, Dai Yongping, Liu Yuanbing, Le Lixiang, Wang Liangliang, Yang Jiandong. Mechanism of bone marrow mesenchymal stem cells differentiation into functional neurons induced by glial cell line derived neurotrophic factor [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1019-1025. |
| [14] | Duan Liyun, Cao Xiaocang. Human placenta mesenchymal stem cells-derived extracellular vesicles regulate collagen deposition in intestinal mucosa of mice with colitis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1026-1031. |
| [15] | Pei Lili, Sun Guicai, Wang Di. Salvianolic acid B inhibits oxidative damage of bone marrow mesenchymal stem cells and promotes differentiation into cardiomyocytes [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1032-1036. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||